ELANE基因突变致重型先天性中性粒细胞缺乏症伴牙周损害1例
2020-08-06陈炀王艳张琼张越茗邹静
陈炀 王艳 张琼 张越茗 邹静
口腔疾病研究国家重点实验室 国家口腔疾病临床医学研究中心四川大学华西口腔医院儿童口腔科,成都 610041
重型先天性中性粒细胞缺乏症(severe congenital neutropenia,SCN)是一种以外周血和骨髓成熟中性粒细胞缺乏为特点的异质性疾病,其主要表现包括外周血中性粒细胞的绝对计数减少(<0.5×109·L-1),早发性细菌感染和早幼粒细胞/中幼粒细胞阶段骨髓腔内骨髓形成、成熟障碍等[1]。近年来,研究表明SCN与ELANE等多种基因突变有关[1],其发病率为1/100万~2/100万,发病率与性别无关[2]。
SCN患者口腔局部可表现为复发性、疼痛性口腔溃疡及广泛性牙周破坏。牙周病损主要为快速进展性牙周炎,临床表现为牙龈红肿、探诊出血、牙龈退缩、牙周附着丧失、牙周袋形成、牙槽骨广泛吸收、牙齿松动,可累及乳牙列及恒牙列,最终导致乳牙和恒牙早失[3-4]。四川大学华西口腔医院儿童口腔科接诊1例ELANE基因突变导致的SCN伴牙周损害,现报道如下。
1 病例报告
患者,女,4岁,汉族,2010年1月因全口牙齿松动就诊。患儿自2岁以来出现全口牙龈红肿、出血,3岁自觉牙齿松动,近2月来松动加重,影响咀嚼。家长述患儿频繁感冒和反复肺炎。患儿全身发育未见明显异常,智力正常。患儿有一同胞妹妹,身体健康;家族内无类似患者。
1.1 检查
颌面部及口腔专科检查:颜面部左右对称,颈部可触及颌下淋巴结肿大;口腔卫生差,牙面软垢覆盖面积占牙面1/3以下,简化软垢指数(debris indexsimplified,DI-S)为1,全口牙龈红肿,探诊出血(+),51、62、74、84牙龋齿,全口牙牙根暴露,松Ⅱ~Ⅲ度(图1)。患儿口角糜烂伴有皲裂,表面覆盖血痂。家长诉患儿下唇内侧、舌尖等有反复发作的溃疡,直径1~3 mm不等,具有“黄、红、凹、痛”的特征。患儿面容未见明显异常改变(图2)。

图1 治疗前口内相Fig 1 Image of oral cavity before treatment

图2 治疗前正面相Fig 2 Facial image of patient before treatment
影像学检查:全口牙牙槽嵴吸收破坏严重(图3)。

图3 治疗前全景片Fig 3 The panoramic radiograph before treatment
基因检测:ELANE基因有1个杂合突变(c.661G>T)。初诊血常规:白细胞计数4.6×109·L-1,红细胞计数5×1012·L-1,中性粒细胞计数0.26×109·L-1,静脉血铅600 μg·L-1。
骨髓涂片:粒红细胞比例倒置,早幼粒细胞比例增高,中性晚幼粒细胞以下阶段细胞少见,粒细胞成熟障碍(图4)。

图4 治疗前骨髓涂片 × 1 000Fig 4 Bone marrow aspirate smears before treatment × 1 000
根据患者的临床表现、血液学检查及基因检测结果,诊断为:1)SCN;2)铅中毒;3)慢性牙周炎。
1.2 治疗
局部口腔治疗:定期行全口龈上、龈下洁刮治,过氧化氢及生理盐水冲洗,上碘甘油;51、62、74牙拔除术;口腔卫生宣教,嘱患儿加强口腔卫生。1月后复诊检查牙周基础治疗情况,并嘱患儿3~6月定期复查。
全身系统性疾病治疗:患儿于四川大学华西第二医院小儿血液肿瘤科治疗粒细胞缺乏症,遵医嘱口服地榆升白片0.2 g,每日3次,螺旋藻胶囊350 mg,每日3次,定期随访;口服二巯丁二酸进行驱铅治疗,剂量为每次350 mg·m-2体表面积,每日3次,连续5 d,继而改为每日2次,每次剂量不变,连续14 d。每个疗程共计19 d,停药4~6周后复查血铅。以上治疗均取得患儿监护人的知情同意。
1.3 治疗效果
口腔局部:牙周基础治疗后1月复查,牙齿松动未见明显加重,但口腔卫生较差。6月复查,全口卫生较差,牙面沉积大量软垢,牙龈稍红;全景片示后牙区牙槽骨较初诊时稍有进一步吸收(图5)。嘱患儿继续定期行牙周治疗,加强口腔卫生。1年复查,患儿无不适主诉,口腔卫生差,牙龈红肿、探诊出血未见明显改善,混合牙列期,11、16、21、26、31、32、36、41、42、46牙已萌出;全景片示16、26、36、46牙槽嵴顶位于根中1/3,前磨牙区牙胚无骨质覆盖(图6)。3年复查,早期恒牙列,口腔卫生差,牙龈红肿,探诊出血(+)未见明显改善,26、36、46牙松Ⅰ度,15、25牙松Ⅱ度,余牙松(-);全景片示双侧下后牙区牙槽骨广泛性吸收,牙槽嵴低平,26、36、46牙槽骨吸收至根尖1/3(图7)。

图5 6个月复查全景片Fig 5 Image of the panoramic radiograph six month later
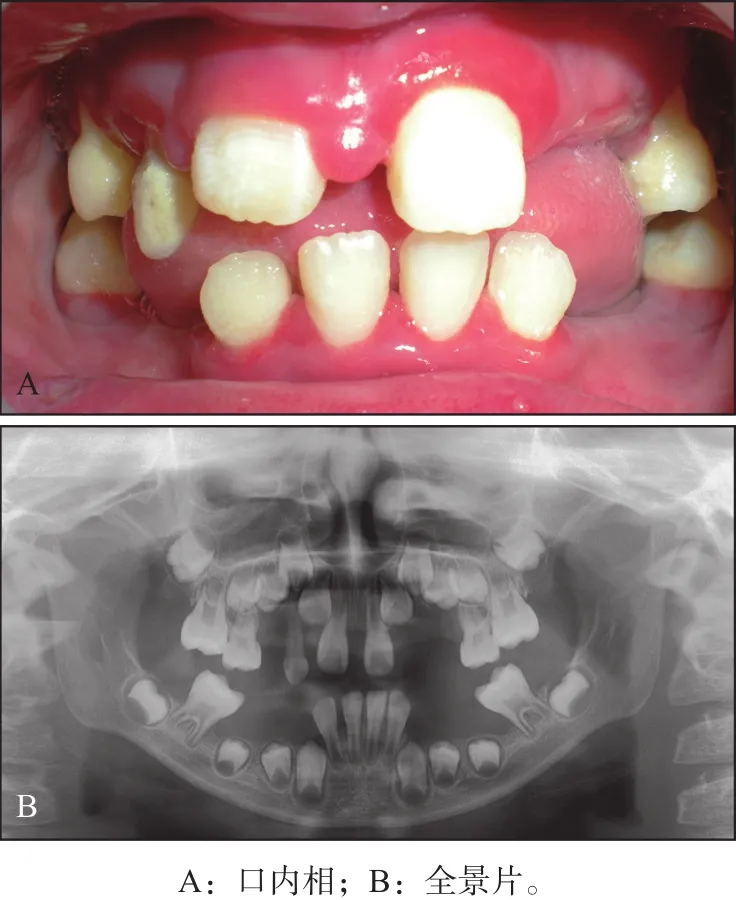
图6 患儿1年复查口内相及全景片Fig 6 Image of oral cavity and the panoramic radiograph one year later

图7 患儿3年复查口内相及全景片Fig 7 The image of oral cavity and the panoramic radiograph three years later
全身系统性疾病:患儿口服地榆升白片、螺旋藻胶囊后中性粒细胞计数仍低于参考值(表1),但随访期间全身健康状况良好,未出现全身感染。经驱铅治疗后,患儿血铅浓度有所降低,为288 μg·L-1,继续行驱铅治疗。

表1 患儿血常规检查结果Tab 1 Blood routine examination of patient
2 讨论
重型慢性粒细胞减少症国际登记处(Severe Chronic Neutropenia International Registry,SCNIR)对于SCN的临床诊断标准为:1)出生至少3个月后,至少3次外周血细胞计数重复均显示中性粒细胞计数低于500·μL-1或0.5×109·L-1;2)患者出现反复发热、慢性牙龈炎、不规则间隔感染等临床表现;3)骨髓涂片显示粒系细胞成熟障碍,多停滞在早幼粒细胞阶段;4)骨髓细胞染色体核型分析为正常核型[5]。本例患儿自出生反复出现“肺炎”、慢性牙周炎等感染性疾病;多次血常规检查示外周血细胞计数均小于0.5×109·L-1,没有周期性波动;骨髓涂片示粒系细胞成熟障碍;除外免疫缺陷、自身免疫性疾病及肿瘤,诊断为SCN。
目前国内SCN伴发牙周炎症的报道较少。刘永红等[6]曾报道1例,患儿女性,2岁6个月,因反复间断发热入院,血常规检查示中性粒细胞绝对值为0.41×109·L-1,基因检测后发现ELANE基因有1个杂合突变(c.640G>A),确诊为先天性中性粒细胞缺乏症;患儿全口牙龈重度萎缩,牙根暴露。X线片示牙槽骨呈广泛性吸收达根中及根尖1/3。虽经过常规口腔护理,但效果欠佳,3个月随访时51、61、71、81牙已缺失。该患儿与本例患儿临床表现相似,但二者影像学表现略有不同,该患儿牙槽骨广泛性均匀吸收,而本例患儿为后牙区较前牙区牙槽骨吸收更严重,基因检测结果同为ELANE基因突变,但突变位点不同。国外关于SCN伴牙周损害的报道[7-9]中,患儿口腔表现均有探诊出血、探及深牙周袋等慢性牙周炎的表现,全口牙进行性松动,影像学表现为严重牙槽骨吸收。An tonio等[7]报道了1例HAX-1基因突变相关的SCN患者,女,4岁,口腔专科检查见双侧颌下淋巴结肿胀,口腔卫生状况较差,牙龈红肿,探诊出血,可探及深牙周袋,全口牙松动。Hastürk等[8]报道的病例中患儿口腔表现为牙齿松动,大部分牙齿严重龋坏,釉质发育不全明显,牙龈红肿,探诊出血,可探及深牙周袋。Antonio等[7]及Hastürk等[8]报道的病例与本例患儿相似,影像学检查可见牙槽骨吸收后牙区较前牙区严重,但牙槽骨吸收速度不同步的原因有待研究。Fernandes等[10]报道了1例5岁女性患者,口腔检查见牙龈出血,牙齿进行性松动1年,可探及深牙周袋,影像学检查示广泛性牙槽骨水平吸收,10年随访见患儿口腔健康状况良好,牙周炎得到控制。可能原因是长期严格口腔检查,有效口腔卫生状况的维护。另外,Gonzalez等[9]报道1例SCN患者,女,16岁,口腔检查见探诊出血,可探及深牙周袋,46牙Ⅰ度根分叉病变,基因检测发现HAX-1基因突变,经过1年定期牙周基础治疗,患儿牙周炎症得到控制及改善,46牙探诊深度及根分叉病变位点减少。定期牙周治疗及有效的自身口腔清洁在一定程度上可以改善SCN患者牙周炎症。
对于SCN伴牙周损害的治疗,目前均采用常规定期牙周治疗,但治疗效果不一。刘永红等[6]报道的患儿经过3个月的常规牙周治疗,效果不佳,作者认为可能与缺乏中性粒细胞导致抵抗力低下有关。而另一些报道[7,9-10]认为,定期牙周治疗及有效的自身口腔清洁可以在一定程度上改善SCN患者牙周炎症。本例患儿经过定期牙周治疗及清洁,牙龈红肿有所改善,牙槽骨吸收未见明显进展,牙周炎症得到一定的控制,但总体效果欠佳,患儿牙周病损仍处于活跃状态。其原因可能为SCN对牙周组织造成了病理性破坏,同时患儿年龄较小,口腔黏膜及牙龈红肿、疼痛,未能配合进行有效的自我口腔卫生维护,导致其口腔卫生状况差,造成了患儿牙周炎症控制不佳。
SCN是一种罕见的单基因遗传性疾病,可为X连锁或常染色体隐性或显性遗传。ELANE、HAX-1、GFI1、G6PC3、SBDS、WAS、TCIRG1、JAGN11以及CSF3R等基因突变均可能导致SCN,其中ELANE基因突变最常见(占55.6%),HAX-1、GFI1、SBDS、WAS、G6PC3等约占4.9%,但仍有40%以上的患者基因突变位点不明[11-13]。ELANE基因位于染色体19p13.3,由5个外显子组成,编码318个氨基酸的中性粒细胞弹性蛋白酶(neutrophil elastase,NE)。NE是一种丝氨酸蛋白酶,在粒细胞分化的早幼粒细胞阶段高度表达,相比于HAX-1基因突变和其他基因突变,ELANE基因编码NE位点变异的患者患有更严重的牙周疾病[1]。其病理机制可能是ELANE基因发生突变导致错误折叠NE蛋白的产生并在中性粒细胞内质网中聚集,从而激活“未折叠蛋白反应”,最终导致中性粒细胞凋亡[14]。本例患儿基因检测发现ELANE基因有1个杂合突变(c.661G>T),目前未见关于该突变位点报道,其具体致病机制有待进一步研究。
本例中患儿牙周红肿,全景片示双后牙区牙槽骨广泛性吸收,尽管经过常规的牙周治疗,患者炎症没有得到明显的缓解,除了自身口腔卫生维护不佳外,可能与中性粒细胞减少或缺乏有关。中性粒细胞是维护口腔健康的关键免疫细胞,中性粒细胞的减少或缺乏导致抗菌肽LL-37缺乏,常引起牙周炎症。Pütsep等[15]研究表明抗菌肽LL-37与患者口腔健康之间存在相关性。LL-37是一种抗菌肽,是在骨髓中性粒细胞成熟过程中产生的天然杀菌成分,效力上与传统抗生素相似,并作为促肽储存在中性粒细胞颗粒中,中性粒细胞在牙周组织中聚集并释放LL-37,与其他抗菌成分一起控制着龈下微生物群,维持牙周组织健康。但SCN患者中性粒细胞发育受损,血浆LL-37前体水平较低,SCN患者唾液或中性粒细胞中抗菌肽缺乏[1,15]。
SCN的治疗旨在预防及积极控制感染,一旦出现发热和感染的症状应及时就医并积极治疗。应用造血生长因子(如粒细胞集落刺激因子,granulo-cyte colony stimulating factor,G-CSF)可以改善SCN症状并降低患者对感染的易感性。但使用G-CSF治疗的SCN患者,骨质丢失的发生率较高。长期持续使用高剂量G-CSF可能诱发白血病。对于高剂量GCSF治疗无效的患儿应该考虑行造血干细胞移植以期根治SCN。尽管近年来移植技术提高,但对SCN患者进行的造血干细胞移植可能存在移植物抗宿主病,或发生向骨髓增生异常综合征/急性髓系白血病转变等并发症,且仍有较高致死率及罹患率[16]。相关报道[6-7]中,虽经G-CSF治疗以及定期牙周基础治疗,但因患儿自身口腔卫生维护不佳,牙周病损未得到有效的控制。而Gonzalez等[9]报道,患儿未使用G-CSF治疗SCN,但在定期牙周基础治疗及患者良好的个人口腔卫生护理下,牙周病损亦得到一定控制。本例患儿临床表征为慢性牙周感染,无全身严重感染症状。经小儿血液肿瘤科会诊,综合评估治疗风险与获益后,建议暂不行造血生长因子治疗及造血干细胞移植术,定期复查,对症治疗慢性牙周感染。经3年随访,患儿中性粒细胞计数虽低于参考值,但全身健康状况尚可。但因SCN是一类先天性免疫缺陷疾病,中性粒细胞缺乏,仅对症治疗这类疾病引起的牙周炎症效果欠佳。在G-CSF等药物治疗全身系统性疾病及牙周定期基础治疗、患者自身有效口腔卫生维护情况下,SCN的牙周病损可得以改善。
本例患儿同时伴有铅中毒病史,患儿家属否认患儿饮食、居住地空气、饮水等因素导致铅中毒,中毒具体原因不明。儿童高铅血症和铅中毒要依据儿童静脉血铅水平进行诊断,连续2次静脉血铅水平为100~199 mg·L-1为高铅血症,高于等于200 mg·L-1为铅中毒。铅中毒对儿童的危害是一个剂量—效应连续的过程,可累及神经、血液、消化、泌尿、免疫、内分泌等全身多系统并影响生长发育[17]。儿童主诉症状包括消化系统症状(如便秘、腹泻、腹痛、厌食、恶心、呕吐)、神经系统症状(如多动、注意力不集中、脾气暴躁、攻击性行为)、血液系统症状(如面色苍白),其中神经系统症状较常见[18];口腔表现主要为龈缘黑色铅线。目前关于铅中毒是否会影响口腔健康的报道较少。El-Said等[19]报道,长期暴露于铅环境的工人牙周炎发病率及龋病易感性增加,但其生物学机制尚不明确。患儿服用二巯丁二酸进行驱铅治疗,目前该药物对口腔健康的影响未见报道。本例患儿牙周炎症是否受铅中毒或其治疗药物的影响尚不明确,有待进一步研究。
本例患儿因全口牙齿松动、牙龈红肿、出血等口腔表现就诊,经多学科会诊,确诊为SCN。这提示口腔医师在临床工作中,对于牙周炎患儿,应引起足够的重视,进行必要的全身检查,排查可能的疾病。一经确诊,应根据疾病的发生发展特点及其对口腔健康的影响,为患儿制定个性化治疗计划。ELANE基因突变致NE蛋白错误折叠及LL-37缺乏可能是SCN患儿牙周损害的发病机制。定期牙周治疗及有效的自身口腔清洁可在一定程度上缓解SCN患儿牙周炎症,为其远期修复提供一定的条件。
利益冲突声明:作者声明本文无利益冲突。
