水溶性大豆多糖对马铃薯淀粉理化性能的影响
2020-07-29焦昆鹏马丽苹张晓宇罗磊向进乐樊金玲杜琳
焦昆鹏,马丽苹,张晓宇,罗磊,向进乐,2,樊金玲,杜琳
1(河南科技大学 食品与生物工程学院,河南 洛阳,471023) 2(河南省食品绿色加工与质量安全控制国际联合实验室,河南 洛阳,471023)3(食品加工与安全国家级实验教学示范中心,河南 洛阳,471023)
马铃薯淀粉是一种重要的植物淀粉,其生产量和商品量仅次于玉米淀粉[1-2]。马铃薯淀粉具有颗粒大、易膨胀、黏度高、糊化透明度高等独特特性,因此常被用作稳定剂、增稠剂和黏结剂广泛地应用于香肠、面包和膨化食品等淀粉基食品中[3]。水溶性大豆多糖是指从大豆或豆浆、豆腐、发酵豆等大豆制品加工的副产物豆渣中分离提取出的一种高度支化的天然聚阴离子多糖[4],水溶性大豆多糖除具有膳食纤维所具有的功能特性以外,还具有诸如乳化性、酸性条件下对蛋白颗粒的稳定作用、抗黏结性、抗氧化性、成膜性能及泡沫稳定性等特性,是一种应用广泛的功能性食品添加剂[5]。
大量研究表明,茶多糖、普鲁兰多糖、亚麻多糖、黄原胶、瓜尔胶、果胶、菊糖以及葡聚糖等非淀粉多糖能影响淀粉的热力学和流变学特性,改变和控制淀粉基食品的质构,改善保水性和冻融稳定性,抑制贮藏期间淀粉的老化以及保持贮藏期间产品质量等功能特性[6-11]。有研究表明β-葡聚糖可显著降低燕麦淀粉的消化速度和程度[12],瓜尔胶能显著降低蜡质玉米淀粉的消化速度和程度[13]。此外,针对普鲁兰多糖、果胶、黄原胶、菊糖、果胶、海藻酸钠及阿拉伯木聚糖等开展的相关研究也发现这些非淀粉多糖均具有一定程度的抑制淀粉消化性的特点[14-20]。
目前,有关水溶性大豆多糖对马铃薯淀粉性质如淀粉糊化、溶解性和膨胀力、透明度和消化性的影响尚未见报道,本实验研究水溶性大豆多糖对马铃薯淀粉理化性能的影响,以期为水溶性大豆多糖在马铃薯淀粉加工工业中的应用提供一些理论依据和技术参数。
1 材料与方法
1.1 材料与仪器
马铃薯淀粉,山东金城股份有限公司;水溶性大豆多糖(纯度为80 %),安徽中旭生物科技有限公司;高温α-淀粉酶(40 000 U/g)、糖化酶(100 000 U/g),江苏锐阳生物科技有限公司。
差示扫描量热仪(DSC1型),瑞士Mettler-Toledo公司;黏度仪(Viscograph-E 803 302型),德国Brabender公司;紫外可见分光光度计(722N型),上海精密科学仪器有限公司;分析天平(FA1 004型),上屏仪器公司;高速台式离心机(TGL-18C型),上海安亭科学仪器厂;数显恒温水浴锅(HH-4型),常州普天仪器制造有限公司。
1.2 实验方法
1.2.1 水溶性大豆多糖-淀粉混合物的制备
用去离子水将水溶性大豆多糖配制成一定浓度的胶体溶液(以干基计,水溶性大豆多糖的质量分数分别为0%、0.5%、1.0%、3.0%、5.0%、7.0%),用磁力搅拌器使之充分溶解分散。再称取适量的马铃薯淀粉加入到上述配制好的胶体溶液中以制成质量分数5.0%的马铃薯淀粉胶体混合物(干基),搅拌至均匀,备用。
1.2.2 淀粉理化性质的测定
1.2.2.1 糊化特性测定
称取一定量1.2.1中不同含量的水溶性大豆多糖与马铃薯淀粉混合物,置于Brabender黏度仪的测量杯中对马铃薯淀粉的糊化特性进行测定。设置测量盒扭矩为700 cmg,测量转速为75 r/min,从30 ℃开始升温,升温速率为1.5 ℃/min,升温到95 ℃后保温30 min,再以1.5 ℃/min的降温速率降至50 ℃,保温30 min,得到黏度随时间和温度变化的Brabender黏度曲线[21]。
1.2.2.2 差示扫描量热仪分析
称取一定量1.2.1中不同含量的水溶性大豆多糖-淀粉-混合物,用差示扫描量热仪专用塑料移液管从搅拌的样品中取出适量样品,放置差示扫描量热仪专用的铝高压坩埚中,然后用精密天平(精度d=0.01 mg)称量坩埚中的样品质量,用坩埚盖子将样品压紧并制成片状,最后将压好的样品进行热扫描并记录糊化焓值。测定温度为25~100 ℃,加热速度为10 ℃/min。记录初始糊化温度,峰值糊化温度,最终糊化温度和糊化焓。用空白作为参照,每个样品重复3次。糊化焓值以样品中的干基淀粉计。重复实验2次,取平均值。
1.2.2.3 透明度测定
取上述制备的50 mL混合样品于100 mL的烧杯中,并在95 ℃的磁力搅拌水锅锅中搅拌糊化20 min。为了减少误差,用热蒸馏水将淀粉调至原来的体积,然后冷却至室温。取适量样品置于1 cm比色皿中,在650 nm处用分光光度计测定样品透明度[8],重复3次,结果取平均值。
1.2.2.4 溶解度和膨胀力测定
取适量上述制备的样品,在90 ℃水浴中搅拌15 min,冷却至室温,将糊状物置于100 mL离心管中, 在3 000 r/min离心20 min,除去上清液,称取管中剩余物质质量(P)及管中剩余物烘干后质量(C),分别按公式(1)和公式(2)计算溶解度(S)和膨胀度(B),结果取3次的平均值。
(1)
(2)
式(1)、(2)中:W为淀粉干基质量,g;P为离心后沉淀物质量,g;C为离心后沉淀物干基质量,g。
1.2.2.5 体外消化率测定
参考汪名春等[20]的体外消化酶解法测定水溶性大豆多糖-淀粉混合物的体外消化特性。称取200 mg的马铃薯淀粉(干基)和一定质量的水溶性大豆多糖(水溶性大豆多糖分别占马铃薯淀粉干重的0、5%、10%、15%、20%),置于装有转子的50 mL 烧杯中,然后加入制备好的5 mL 0.2 mol/L醋酸钠缓冲溶液(pH 5.2),在95 ℃的水浴中振荡15 min,取出至冷却至室温,再置于37 ℃恒温振荡浴中10 min,然后加入在37 ℃下预热的20 mL α-淀粉酶和葡糖淀粉酶混合物(用醋酸钠缓冲溶液配制酶溶液,α -淀粉酶和葡糖淀粉酶用量分别为2 290 U和150 U),然后置于37 ℃恒温振荡水浴锅中水解,反应溶液分别经过不同时间(0、20、40、90、120、180 min)水解后从中取出1 mL,然后加入5 mL无水乙醇使之停止反应。样品在4 000 r/min离心15 min后,取上清液,通过DNS比色法[22]测定样品中还原糖的含量,按公式(3)计算其水解率,结果取2次的平均值。
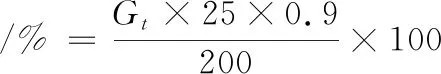
(3)
式中:Gt为水溶性大豆多糖-淀粉混和物在酶水解t时间后产生的葡萄糖质量,mg。
1.3 数据处理
实验数据均重复3次,用Excel整理数据,用SPSS 19.0软件进行实验数据方差分析,数据以X±s表示,差异显著性水平为0.05。
2 结果与分析
2.1 水溶性大豆多糖对马铃薯淀粉糊化特性的影响
不同添加量的水溶性大豆多糖(水溶性大豆多糖添加量是指水溶性大豆多糖占干马铃薯淀粉质量百分比)对马铃薯淀粉糊化特性的影响见图1,其特征值变化如表1所示。。由图1可以看出,在糊化起始阶段,淀粉颗粒不溶于水,所有样品体系黏度值均很低。而随着体系温度的升高,淀粉颗粒受热吸水膨胀,其分子间和分子内的氢键强度减弱,淀粉颗粒大量吸水膨胀,体系黏度逐渐升高并达到最大值,继续受热,引起氢键断裂,颗粒破裂,直链淀粉析出,黏度下降,而在随后的冷却降温过程中,直链淀粉分子重排,重新形成氢键,黏度上升[23],马铃薯淀粉和水溶性大豆多糖/马铃薯淀粉混合体系均表现出上述类似的黏度曲线,但水溶性大豆多糖/马铃薯淀粉混合体系的黏度曲线整体下移,且水溶性大豆多糖添加量越高,曲线下移幅度越大。表1数据也表明,一定量水溶性大豆多糖的添加(当添加量大于3%时)使水溶性大豆多糖/马铃薯淀粉混合体系的峰值黏度显著下降(P<0.05),类似结果也出现在FUNAMI等[24]、LIU等[25]和SHENG等[26]的研究中。水溶性大豆多糖属于阴离子多糖,在其半乳糖醛酸主链上分布着阿拉伯糖等中性糖侧链,具有毛刷状一样网络支架结构,这一特点使其能够对淀粉颗粒进行不同程度的包被,从而抑制了淀粉颗粒的吸水膨胀,造成了峰值黏度的下降[27]。
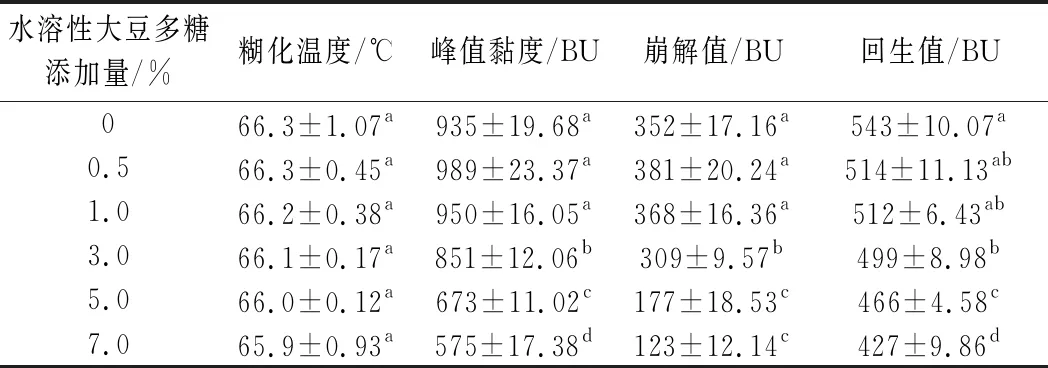
表1 水溶性大豆多糖对马铃薯淀粉糊化特性曲线特征值的影响Table 1 The effect of soluble soybean polysaccharides on the characteristic value of potato starch gelatinization curves
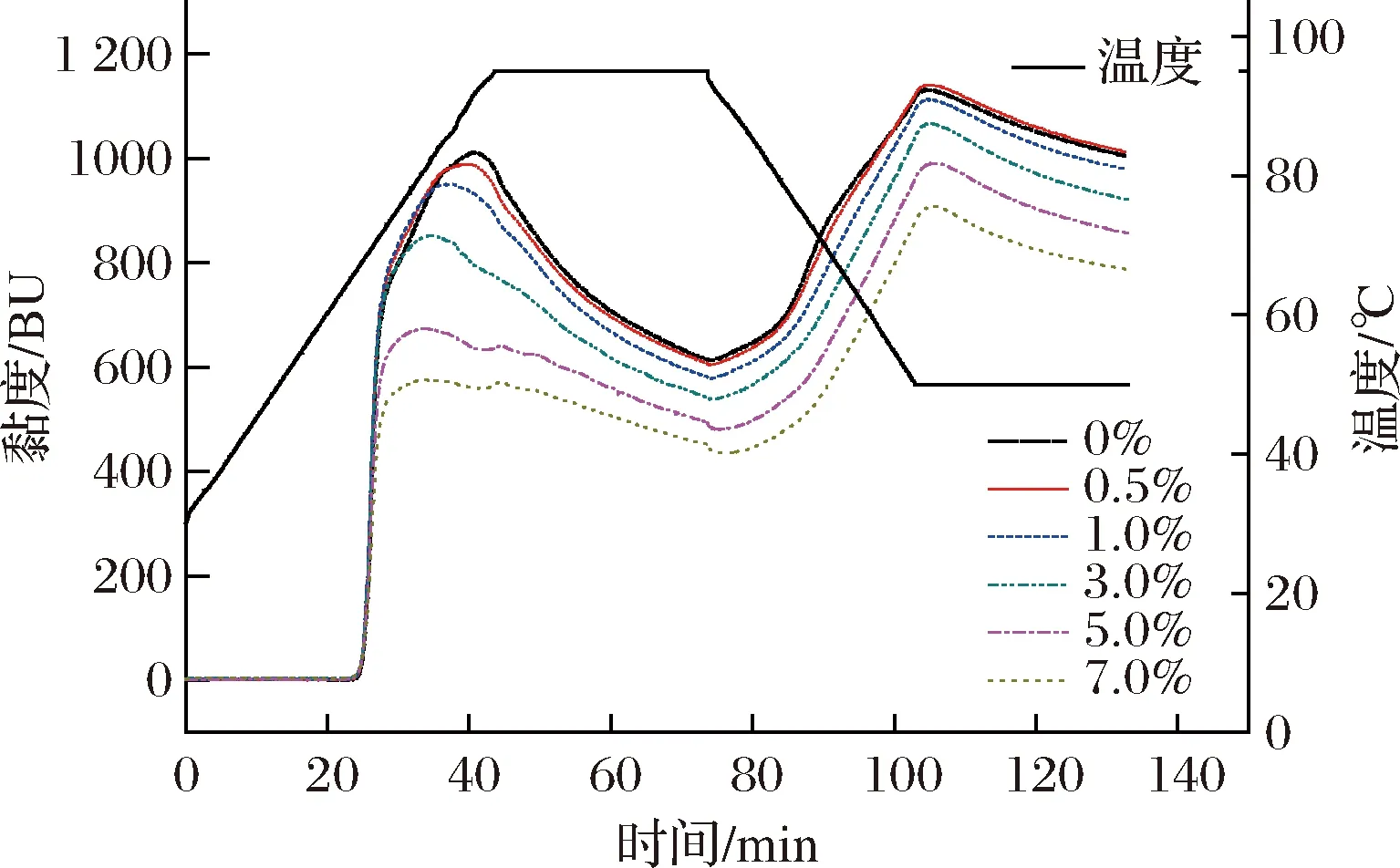
图1 添加水溶性大豆多糖对马铃薯淀粉糊化特性的影响Fig.1 Effect of adding soluble soybean polysaccharides on gelatinization characteristics of potato starch
由表1可知,水溶性大豆多糖对马铃薯淀粉糊化初始温度影响不大,这与王思远等[28]和谭永辉等[29]研究结果相一致。另外,不同添加量的水溶性大豆多糖对马铃薯淀粉糊的崩解值和回生值影响程度不同。回生值反映了淀粉糊化后分子链的迁移重排能力和短期老化程度[30]。回生值越低代表淀粉短期老化程度越低[31]。当水溶性大豆多糖添加量从3%增加到7%,马铃薯淀粉回生值显著下降(P<0.05),降幅最大达到21%。这可能是水溶性大豆多糖与渗透出的直链淀粉以氢键结合,抑制淀粉分子移动重排造成的[30]。崩解值反映了淀粉颗粒在加热过程中的稳定性[21]。崩解值越低,淀粉水合作用和膨胀能力越低,其耐剪切能力则越强[31]。当水溶性大豆多糖添加量为3%时,复合体系的崩解值下降了12%,之后随着水溶性大豆多糖添加量继续增加,崩解值不断下降,水溶性大豆多糖添加量为7%时,下降幅度最大,为65%。水溶性大豆多糖的添加致使水溶性大豆多糖/马铃薯淀粉复合体系崩解值和回生值的下降,说明水溶性大豆多糖能够使得马铃薯淀粉糊热稳定性增加,并且抑制了马铃薯淀粉凝胶的短期老化,这与LIU等[25]和王思远等[28]的研究结果一致。
2.2 水溶性大豆多糖对马铃薯淀粉差示扫描量热曲线特征参数的影响
淀粉糊化时,淀粉颗粒高温受热吸水膨胀,致使其分子间和分子内的氢键断裂,过程中伴有能量变化。因此,可以通过差示量热扫描测定[32]。糊化焓变与断裂淀粉颗粒结构所需的能量相关;糊化温度反映了淀粉有序结构消失的温度范围[28]。表2为水溶性大豆多糖添加对马铃薯淀粉糊化起始温度、峰值温度、终止温度和焓变的影响。
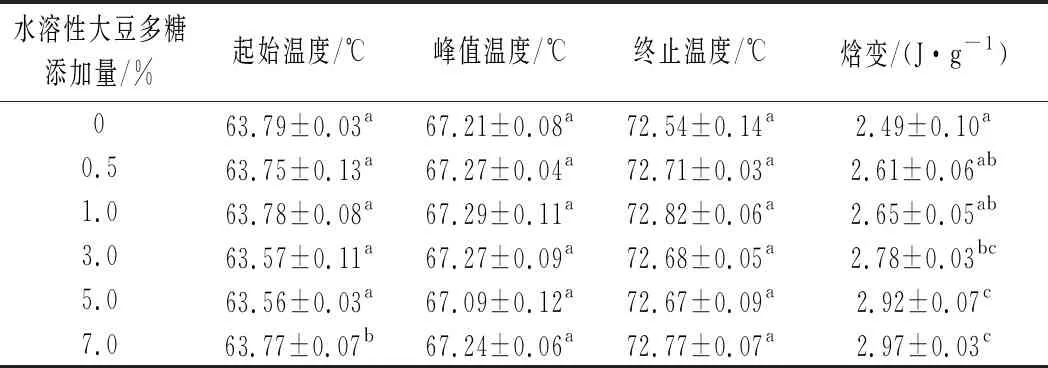
表2 水溶性大豆多糖对马铃薯淀粉差示扫描热量曲线特征参数的影响Table 2 Effect of soluble soybean polysaccharides on characteristic parameters of differential sanning calorimetry curves of potato starch
由表2可以得出,随着水溶性大豆多糖添加量的增加,马铃薯淀粉的糊化起始温度、峰值温度以及终止温度基本保持不变,这与布拉班德黏度仪测定的起始糊化温度不变相一致。差示扫描量热法所测得的糊化起始温度低于黏度仪所测的混合体系的糊化起始温度,说明不同比例混合体系的熔融进程早于黏度增加的开始进程[33]。水溶性大豆多糖添加量在3%以下时,对马铃薯淀粉吸热焓没有明显影响(P>0.05),而当水溶性大豆多糖添加量继续增加,马铃薯淀粉焓变也缓慢增加,这可能由于马铃薯淀粉颗粒在升温过程中受热吸水膨胀,淀粉分子扩散,氢键断裂,而足够量的水溶性大豆多糖在淀粉表面形成水化层,使得淀粉外层得到保护,要使氢键断裂则需要更多热量,具体表现为焓变增加[34]。研究发现不同水胶体的添加会提高淀粉糊化终值温度,而糊化起始温度、糊化峰值温度或者升高,或者不变,在多数情况下,糊化焓值下降。同时也有研究表明,水胶体对淀粉糊化温度及焓值没有影响[35],而李远等[33]和BILIADERIS等[36]却发现水胶体能增加淀粉糊化焓值。这可能是因为胶体结构导致淀粉与水胶体之间的相互作用不同所造成,比如不同支化度、分子质量、分子柔性、阴离子电荷的存在和类型等[35]。总之,水胶体对淀粉糊化的影响规律不一。本研究结果与王思远等[28]研究大豆多糖对大米淀粉糊化影响时的结果类似。
2.3 水溶性大豆多糖对马铃薯淀粉糊透明度的影响
马铃薯淀粉糊透明度非常高,这一特点有利于食品加工过程中形成更好的色泽。淀粉糊化后,其分子重新排列、相互缔合的程度是影响淀粉糊透明度的重要因素。如果淀粉颗粒在吸水和受热时能够完全膨胀,并且糊化后淀粉分子也不发生相互缔合,则淀粉糊中无残存的淀粉颗粒,也无回生后形成的凝胶束,淀粉糊非常透明[37]。而淀粉糊的透明度通常也会受到淀粉本身的成分以及外来添加物等因素的影响。图2为水溶性大豆多糖对马铃薯淀粉糊透明度的影响。由图2可知,0.5%~1%水溶性大豆多糖对马铃薯淀粉糊的透光率没有显著影响(P>0.05),3%水溶性大豆多糖使马铃薯淀粉糊的透光率显著下降了21.22%(P<0.05),之后随着水溶性大豆多糖的增加,马铃薯淀粉糊的透光率趋于平缓。这可能因为水溶性大豆多糖附着在马铃薯淀粉颗粒表面,阻碍淀粉颗粒完全膨胀糊化,导致淀粉糊中存在残存淀粉颗粒,从而造成淀粉糊透明度下降[38]。
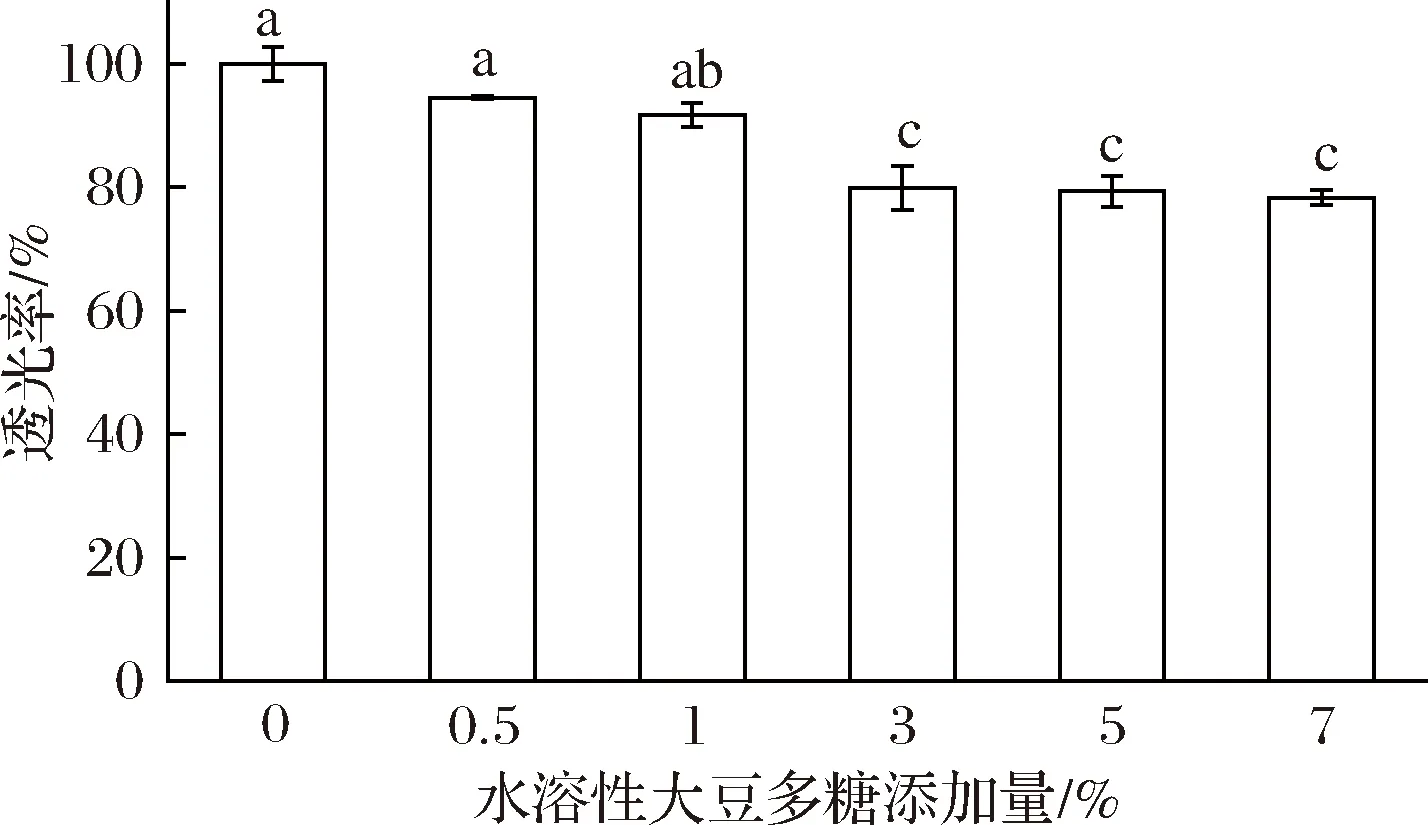
图2 添加水溶性大豆多糖对马铃薯淀粉糊透明度的影响Fig.2 Effect of adding soluble soybean polysaccharides on the transparency of potato starch paste
2.4 水溶性大豆多糖对马铃薯淀粉膨胀力的影响
淀粉颗粒的膨胀力反映了淀粉样品的水合能力,与支链淀粉含量和淀粉颗粒大小相关[39]。马铃薯淀粉在糊化过程中,其分子被切割,晶体结构被破坏,然后游离水进入淀粉分子内部,使淀粉颗粒的体积膨胀。图3为添加水溶性大豆多糖对马铃薯淀粉膨胀力的影响。由图3可以看出,0.5%~1%水溶性大豆多糖对马铃薯淀粉膨胀力没有明显的影响(P>0.05)。而3%~5%水溶性大豆多糖能够显著抑制马铃薯淀粉的膨胀(P<0.05),但没有明显的浓度效应(P>0.05)。多糖如魔芋葡聚糖、瓜尔豆胶和刺槐豆胶的存在能延缓淀粉颗粒膨胀,这是由于多糖能够使连续相增厚或与水结合以限制水的有效性或流动性,从而防止颗粒膨胀[40]。水溶性大豆多糖溶液黏度较低,因此不大可能通过使连续相增厚而限制淀粉的水分供应。一个可能的解释就是水溶性大豆多糖在淀粉颗粒周围形成多糖层,与淀粉竞争自由水,降低淀粉颗粒与水相互作用的机会,从而抑制淀粉膨胀。
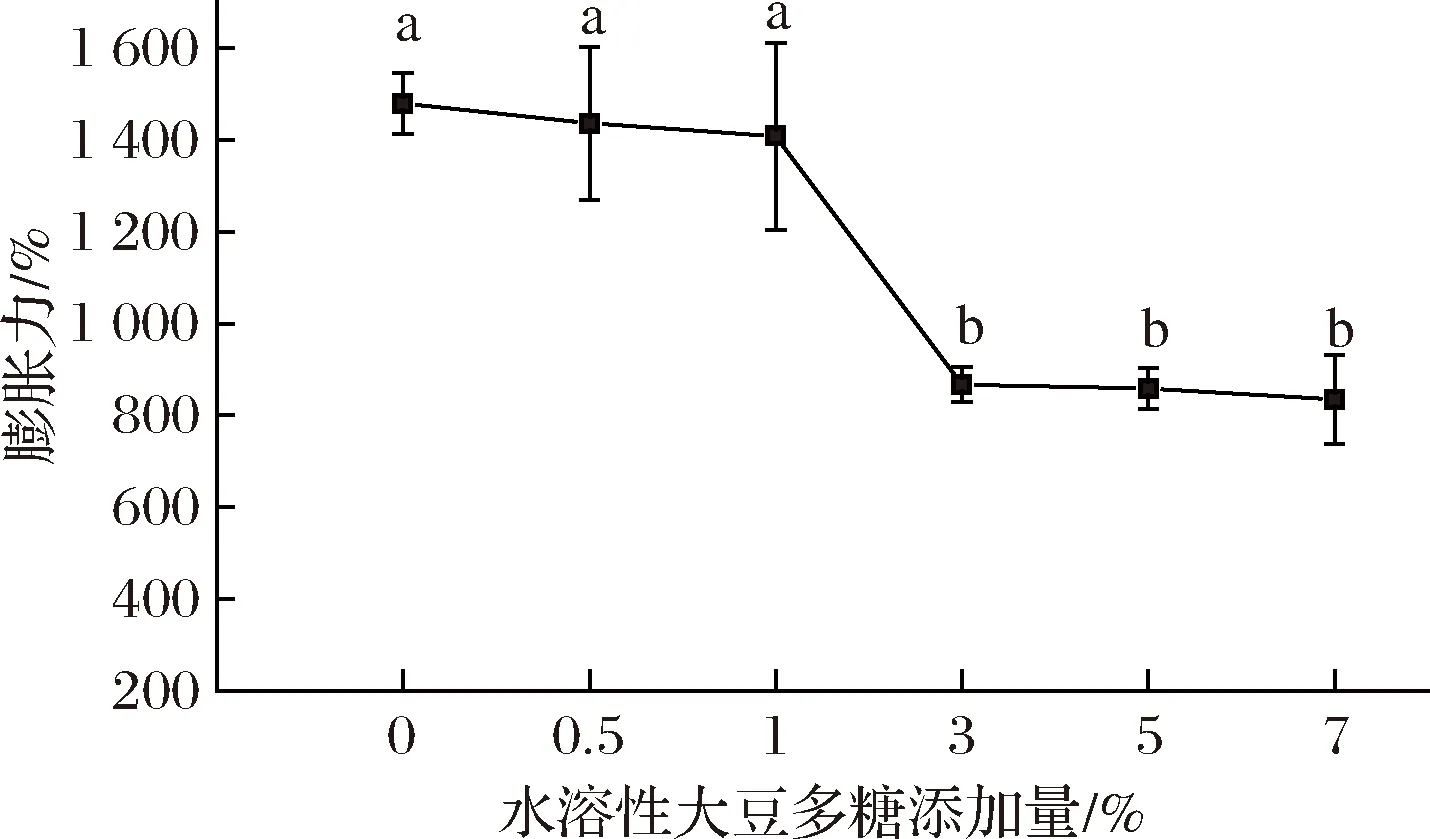
图3 添加水溶性大豆多糖对马铃薯淀粉膨胀力的影响Fig.3 Effect of adding soluble soybean polysaccharides on swelling power of potato starch
2.5 水溶性大豆多糖对马铃薯淀粉溶解度的影响
当淀粉与水共热时,氢键发生断裂,晶体结构被破坏,水分子通过氢键与直链淀粉和支链淀粉的羟基相连,导致颗粒膨胀和溶解度增加[41]。图4为添加水溶性大豆多糖对马铃薯淀粉溶解度的影响。
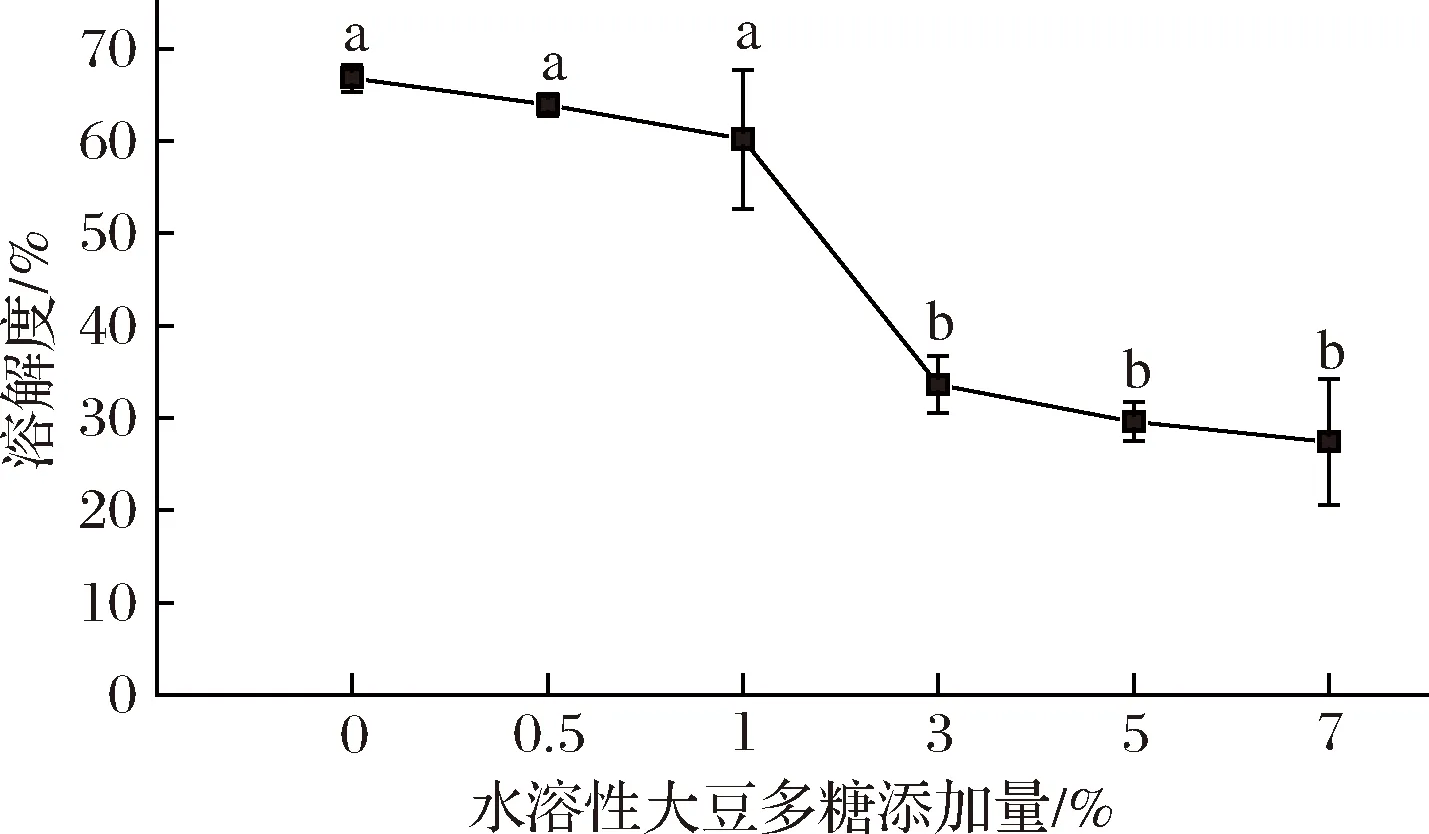
图4 添加水溶性大豆多糖对马铃薯淀粉溶解度的影响Fig.4 Effect of adding soluble soybean polysaccharides on solubility of potato starch
由图4可以看出,0.5%~1%水溶性大豆多糖对马铃薯淀粉的溶解度没有显著影响(P>0.05),而当多糖添加量从1.0%增加到3.0%,马铃薯淀粉溶解度下降非常显著(P<0.05),之后淀粉溶解度趋于恒定。淀粉的溶解主要是直链淀粉和小的支链淀粉从膨胀的颗粒中溢出[42]。水溶性大豆多糖的添加致使马铃薯淀粉膨胀力下降(图3),再加上水溶性大豆多糖可能对马铃薯淀粉的物理包裹作用,而使淀粉颗粒中直链淀粉和小的支链淀粉溶出率下降,表现为溶解度下降。
2.6 水溶性大豆多糖对马铃薯淀粉消化特性的影响
水溶性大豆多糖对马铃薯淀粉消化特性的影响如图5所示。由图5可知,0~20 min淀粉的水解速度快速升高,20~180 min内淀粉的水解速度相对缓慢。在相同水解时间内,与原淀粉相比,加入水溶性大豆多糖后淀粉的水解率显著下降(P<0.05),且水解速率随着水溶性大豆多糖添加量的增加而逐渐降低。水解180 min后,水溶性大豆多糖占马铃薯淀粉干基的20%时淀粉反应体系的水解率由原淀粉的20.18%下降至16.24%。说明水溶性大豆多糖可以在一定程度上抑制淀粉的水解速度,且这种抑制作用随着水溶性大豆多糖添加量的增加而增加,这与汪名春等[20]研究的菊糖可以减少马铃薯淀粉的体外消化率和消化程度的结果一致。淀粉颗粒受热膨胀后会发生糊化,且糊化程度与淀粉消化性成正比[43]。水溶性大豆多糖的添加导致马铃薯淀粉消化性下降,可能是水溶性大豆多糖抑制马铃薯淀粉的膨胀,从而导致其糊化程度下降所造成的。另外,水溶性大豆多糖还可能与马铃薯淀粉相互作用,形成空间位阻,阻碍消化酶与底物的接触,从而降低酶解效率。有研究表明,非淀粉多糖具有抑制淀粉消化酶酶活的作用[44-45],这也可能是其导致淀粉消化率下降的原因之一。而水溶性大豆多糖导致马铃薯淀粉消化性下降的具体原因则有待进一步研究。
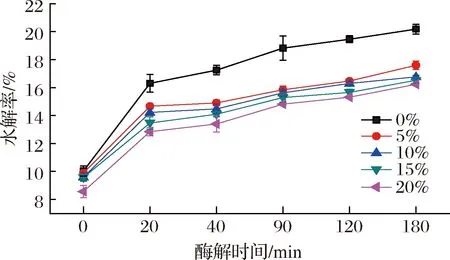
图5 添加水溶性大豆多糖对马铃薯淀粉水解率的影响Fig.5 Effect of adding soluble soybean polysaccharides on hydrolysis rate of potato starch
3 结论
当水溶性大豆多糖添加量大于1%时,能降低马铃薯淀粉糊黏度,提高马铃薯淀粉黏度热稳定性,抑制马铃薯淀粉的老化,且能导致马铃薯淀粉的透明度、溶解度和膨胀力降低。水溶性大豆多糖还能在一定程度上可以延缓马铃薯淀粉的消化,而其对马铃薯淀粉的糊化温度基本无影响。
