γ-干扰素释放试验在活动性肺结核诊断中的价值
2020-07-25黄德东刘庭贵韩湉湉庄建文魏西飞
黄德东 刘庭贵 张 云 施 洁 韩湉湉 庄建文 魏西飞 顾 兴
结核分枝杆菌(Mycobacteriumtuberculosis, MTB)感染严重危害人类健康。据世界卫生组织报道,全球有1/3的人感染过MTB,而我国结核感染水平高达44.5%,MTB患者数高居全球第2位[1-3]。结核病的早诊断、早治疗成为防治结核病的关键。MTB分离培养鉴定、痰抗酸染色(antiacid stains smear, AAS)是诊断结核病的金标准,但由于MTB培养耗时较长;AAS敏感性不高,在结核感染早期诊断中受限[4]。AAS、结核菌素皮肤实验(tuberculin skin test, TST)、结核分枝杆菌抗体(tuberculosis antibody, TBAb)或结核分枝杆菌免疫球蛋白(tuberculosis Immunoglobulin,TB-Ig),在灵敏度及特异性上都有局限性[5]。结核γ-干扰素释放试验(tuberculosis interferonγ release assay TB-IGRA)在临床中被运用于活动肺结核的诊断[6-9]。TB-IGRA的原理为:加入结核分枝杆菌早期分泌抗原靶6(early-secreted antigenic target-6, ESAT-6)和培养基滤过蛋白-10(culture filtrate protein-10, CFP-10),经过全血中的抗原递呈细胞刺激结核分枝杆菌致敏的效应T细胞产生γ-干扰素(interferonγ IFN-γ)。释放的IFN-γ可通过酶联免疫吸附实验(enzyme-linked-immunosorbent assay, ELISA)定量检测,来判断效应T细胞是否被结核致敏,判断是否诊断结核感染。这种方法操作方便、成本相对较低[10]。我国部分结核病高负担地区,特别是我国西南部医疗资源不充足地区开展TB-IGRA,有利于控制结核病。使用TB-IGRA、TST、TB-Ig在贵州省织金县人民医院疑似肺结核患者中检出活动性肺结核,评价TB-IGRA、TST、TB-Ig检测的检验效能。本项目获得织金人民医院伦理委员会的批准,所有观察对象都签署了知情同意书。
资料与方法
一、项目对象
2018年12月20日至2019年12月20日间在织金县人民医院结核病门诊或感染科结核病区住院的患者,根据《中华人民共和国卫生行业标准-肺结核诊断(WS 288-2017)》诊断标准筛查[11],疑似肺结核患者1 627例,年龄范围男性904例,女性723例,平均年龄(37.6±21.3)岁。其中活动性肺结核1 373例,年龄范围男性768例,女性605例,平均年龄(36.8±20.0)岁;非活动肺结核患者254例,男性145例,女性109性,平均年龄(37.9±21.9)岁。组间的年龄、性别比例均无统计学意义。
纳入标准: ①根据肺结核诊断标准诊断为疑似肺结核;②自愿参加,并签署知情同意书;③年龄:18~65岁。排除标准:①合并除结核外的其它感染性疾病,如病毒性肝炎、肺孢子菌肺炎、艾滋病等;②心、脑、肝、肾等重要器官的严重病变或功能衰竭;③吸毒、酗酒、精神病患者;④有恶性肿瘤或恶性肿瘤病史;⑤抗结核治疗超过3个月;⑥已经妊娠或半年内准备妊娠者。患者入组后除进行TB-IGRA、TST、TB-Ig检测外,同时进行常规临床实验室检验、微生物检验及病理和影像学方面的检测。活动性肺结核病的标准包括: ①病理标本中出现干酪样肉芽肿并确诊为结核者;②通过临床病征诊断的活动性肺结核者;③予以抗结核治疗有效者。
二、主要仪器设备及试剂
酶标仪(Bio Tek Elx800),电热恒温水浴槽(上海始恒仪器 CU-420),细胞培养箱(Thermo Scientific 8000)。γ-干扰素体外释放试验诊断试剂盒购自北京万泰生物技术有限公司。结核分枝杆菌抗体IgG诊断试剂盒购自康华技术有限公司。
三、研究方法
1.IGRA-ELISA实验: 采集5 ml静脉血置于肝素锂抗凝管中,轻轻摇匀后尽快分装到本底对照管(N)、特异性刺激管(T)、阳性对照管(P)中,每种管分装1.5 ml新鲜全血,颠倒混匀后置于含5%二氧化碳、37 ℃恒温细胞培养箱中培养20~24 h。按照试剂盒说明书用 ELISA定量检测释放的IFN-γ水平。根据酶标仪测量结果,计算T、N、P管中血浆相应的IFN-γ 含量,按试剂说明书要求判断结果。
2.TST试验方法: 据文献及诊断标准进行,试剂为结核菌素纯化蛋白衍生物(purified protein derivative, PPD)[11-12]。所有受试对象于左前臂背侧上1/3处,皮内注射0.1 ml(含5 IU),72 h后按照肺结核诊断(WS 288-2017)标准判断结果[11]。由于织金县是结核病高发地区、潜伏感染率高,中度阳性及以上结果判定为结核病感染TST实验阳性。
3.TBAb检测方法: 主要检测结核分枝杆菌免疫球蛋白G(TB-IgG),按参考文献[13]及严格参照试剂说明书进行操作与结果判读。
四、统计学方法
结 果
一、一般资料结果
本项目纳入疑似肺结核患者共有1 627例,活动性肺结核患者1 373例,非活动肺结核患者254例,组间的年龄、性别比例均无统计学意义。卡介苗(Bacillus Calmette-Guérin, BCG)接种情况,主要通过询问接种史和检查上臂的卡痕判断是否有BCG接种史,组间比例无统计学意义,见表1。
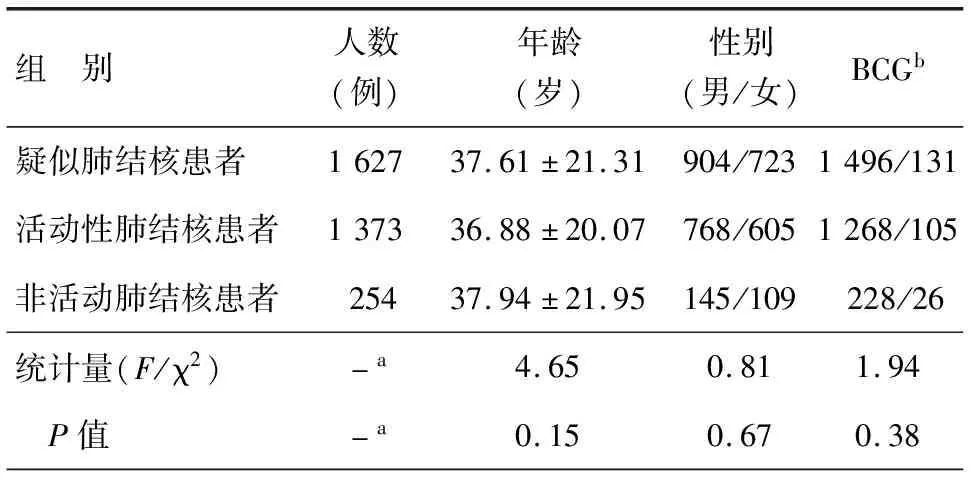
表1 对象人口学资料及卡介苗接种史
二、IGRA、TST与TB-IgG检测结果
纳入的疑似结核患者中被诊断为活动性肺结核的1 373例,非活动性肺结核的254例。IGA诊断活动性肺结核的敏感性达91.26%,在非活动性肺结核组中诊断的阴性病例的特异性达到79.13%,见表2。
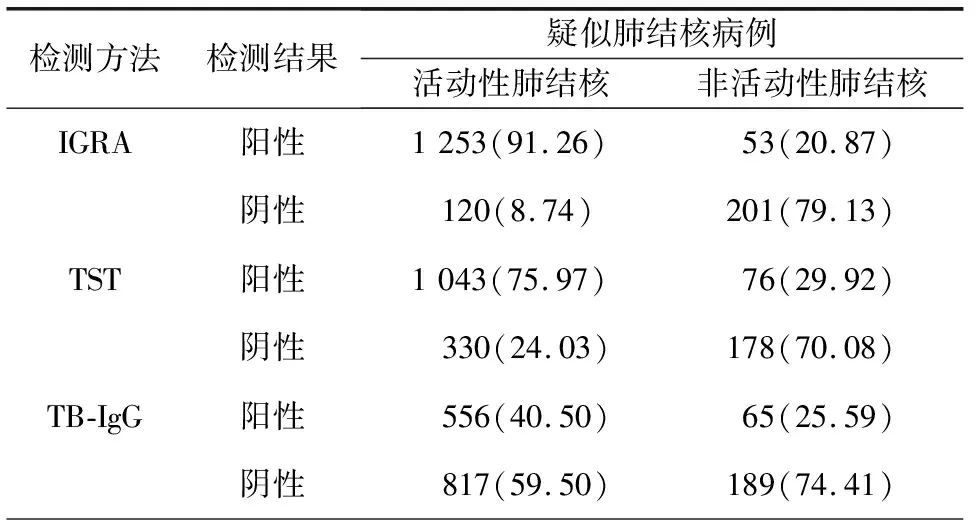
表2 疑似肺结核IGRA、TST、TB-IgG检测结果[n(%)]
三、检测效能比较结果
IGRA、TST、TB-IgG在疑似肺结核患者中诊断活动性肺结核的比较,见表3。IGRA的敏感性、特异性、阳性预测值、阴性预测值和准确性分别为91.2%、80.1%、95.9%,62.6%和89.4%,均高于TST、TB-IgG。
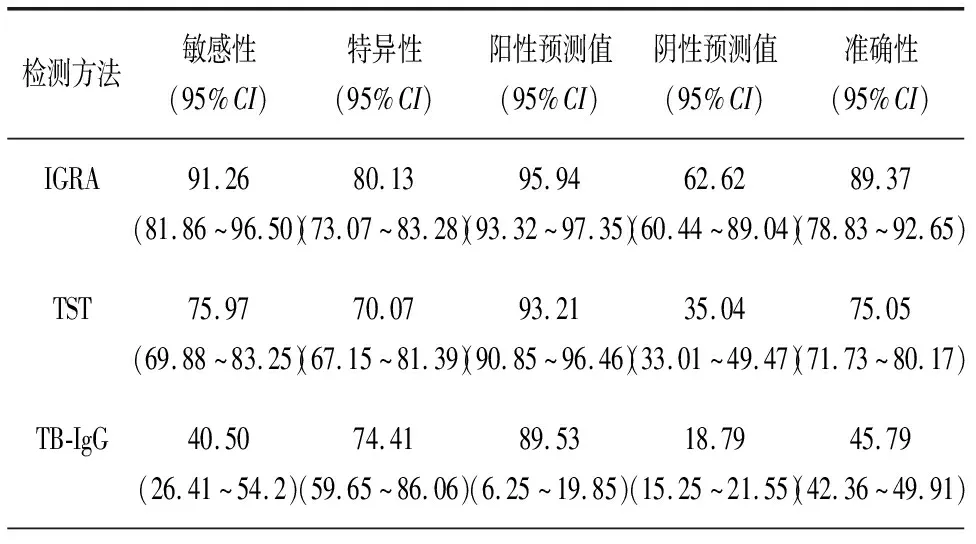
表3 IGRA、TST与TB-IgG检测结果效能比较(%)
四、BCG接种IGRA、TST、TB-IgG检测结果
活动性肺结核患者中,IGRA在有BCG接种史患者中阳性率为91.48%;在无BCG接种史的患者中阳性率为88.57%。BCG接种对IGRA诊断疑似肺结核患者中的活动性肺结核影响无统计学意义,(χ2=1.03,P=0.31)。TST诊断疑似肺结核中的活动性肺结核的阳性率为75.9%,而诊断有BCG接种的活动性肺结核中的阳性率为79.4%,明显高于无BCG接种史的患者中的阳性率(34.2%),有统计学意义(χ2=108.17,P<0.001)。BCG接种史对TB-IgG检测影响也不明显,无统计学意义(χ2=0.53,P=0.47),BCG疫苗接种对IGRA、TST与TB-IgG诊断活动性肺结核的结果,见表4。

表4 BCG疫苗接种对IGRA、TST与TB-IgG诊断活动性肺结核的结果[n(%)]
非活动性肺结核患者中,228例有BCG接种史,IGRA的阳性率为26.6%,而在无BCG接种史中的阳性率为23.8%,相差不明显,无统计学意义(χ2=0.05,P=0.83)。TST诊断疑似肺结核中的非活动性肺结核的阳性率为29.9%,而在有BCG接种史中的阳性率为31.4%,高于无BCG接种史的阳性率23.8%,但无统计学意义(χ2=1.58,P=0.21)。BCG接种史对TB-IgG检测影响无统计学意义(χ2=1.58,P=0.28),见表5。

表5 BCG疫苗接种对IGRA、TST与TB-IgG诊断非活动性肺结核的结果[n(%)]
讨 论
IGRA能区分结核分枝杆菌感染和BCG接种引起的免疫应答,对于BCG广泛接种、结核病高发的我国西南部地区有特别意义[14]。本项目在贵州织金县人民医院的疑似肺结核患者中评价了IGRA分析方法早期诊断活动性肺结核的价值。
IGRA 是利用结核分枝杆菌感染者外周血中存在结核分枝杆菌致敏的T淋巴细胞,这些T淋巴细胞再次接触结核分枝杆菌特异性抗原时可发生克隆增殖分化并释放 IFN-γ 的原理进行检测[15]。采用 ELISA检测方法,简便、设备要求不高、价格相对便宜,适宜在我国西南部医疗资源不充足地区使用。国外研究表明IGRA的敏感性在80%以上,特异性在90%以上[7-8,13,16-17]。我国学者也报道了IGRA在新兵结核筛查、潜伏性结核调查、诊断肺结核及肺外结核、调查结核密切接触者的结核感染中的运用,也都显示敏感性、特异性、准确性很高[12,14,18-19]。本文结果中,IGRA是在疑似肺结核中诊断活动性肺结核,敏感性、特异性、阳性预测值、准确性,分别是91.26%、80.13%、95.94%、89.37%,与国内外研究基本一致[5-6,8,12,14,19-20]。但本文结果中的阴性预测值只有62.62%,较其它研究低[6,10,21],这可能与我们纳入研究对象的总体有差别。本文纳入的是肺结核疑似患者,故活动性肺结核可能性大,阳性预测值及敏感性稍高,阴性预测值较低。
TST,采用的是人型结核分枝杆菌制成的PPD-C及从卡介苗制成BCG-PPD。PPD试验通过激活中心记忆性T淋巴细胞反应,它检测的不仅包含活动性结核,也包含陈旧的、休眠的结核分枝杆菌感染[22]。本文结果中TST的敏感性、特异性、阳性预测值、准确性,分别是75.9%、70.0%、93.2%、75.0%,与国内外研究结果基本一致。但阴性预测值较低,仅有35.0%。可能与我们纳入研究的样本是疑似肺结核患者有关。PPD试剂很难标准化,不同的PPD试剂可能也会导致结果的偏差,特别在阳性患者占主要的样本中阴性预测值可能会受到更多影响[6]。
结核分枝杆菌抗体测定,TB-IgG检测,由于此次检测的试剂盒测定的IgG,仅讨论TB-IgG的测定。国外研究者使用结核分枝杆菌早期表达的蛋白 ESAT6, CFP10、antigen 85A 和结核分枝杆菌DNA结合蛋白1(MDP-1)及α-晶体样蛋白作为抗原(α-CLP),测定TB-IgG诊断活动结核及结核潜伏感染都显示很好的准确性(P<0.05)[22-23]。Tobias Broger团队使用三种结核分枝杆菌蛋白抗原推定结核感染的敏感性、特异性分别为85.0%、34.0%。本文测定TB-IgG诊断活动性肺结核,敏感性、特异性及准确性较国外研究低[23-24]。可能主要是因为国外在抗原试剂中抗原的选择及优化上有区别。与国内学者比较,TB-IgG诊断活动性肺结核的敏感性、特异性、准确性相差不大[7,22,25]。
本文结果发现IGRA诊断疑似肺结核人群中的活动性肺结核的敏感性、特异性、准确性比TST、TB-IgG均高,与国内外研究结果一致[6-8,12,17-19,24]。结核分枝杆菌感染的免疫反应主要是细胞免疫反应[22]。IGRA检测的就是结核特异性T细胞释放的IFN-γ,理论上应该比通过抗原抗体反应原理的TB-IgG有更好的检验效能[22]。TST为体内试验,是受到患者当时机体各种因素的影响,不如体外实验IGRA易于标准化[17]。机体的致敏T淋巴细胞再次受到结核特异性抗原刺激后产生IFN-γ可能也增加,但是并不一定使巨噬细胞集聚、浸润的反应程度也能成比例的增强,即TST阳性也不一定就增加。一部分结核分枝杆菌感染者巨噬细胞可能对IFN-γ反应低或不反应,而出现PPD试验假阴性;BCG接种者会导致PPD试验假阳性[14,19]。
在评价BCG接种对IGRA、TST、TB-IgG检测的影响中发现:受影响最大是TST,而对IGRA、TB-IgG的影响不大。有BCG接种人群中,活动性肺结核的敏感性达到79.42%,而特异性将为34.29%。尽管本实验采用的是人型结核分枝杆菌制成的PPD-C,但与BCG有部分共同抗原,导致PPD假阳性[17]。而IGRA采用的CFPl0和ESAT6,是通过比较基因组学筛选的仅存在于结核分枝杆菌和牛结核分枝杆菌基因组中,而BCG的基因组中缺失[10]。
综上所述,IGRA在疑似肺结核患者中诊断活动性肺结核有很好的敏感性、特异性、准确性。开展IGRA,并联合TST、TB-IgG将能显著提高我国医疗资源不充足的西南结核病高发区结核病的诊治水平。
