输尿管镜钬激光碎石术后肾包膜下血肿相关危险因素探讨
2020-07-24李勋钢张文圣
李勋钢,张文圣
(江西省九江市第一人民医院泌尿外科,九江 332000)
输尿管镜碎石术是治疗泌尿系结石最常用的微创技术,研究表明处理尿路结石是有效、相对安全的[1-3],但仍会出现输尿管穿孔、假道、输尿管撕脱、出血及脓毒败血症等严重并发症。肾包膜下血肿是体外冲击波碎石术 (extracorporeal shock wave lithotripsy,ESWL)比较常见的并发症,输尿管镜碎石术后出现肾包膜下血肿比较少见,目前偶有报道[4-6]。肾包膜下血肿会影响患者术后康复,严重可导致休克甚至死亡。本研究拟通过分析我院行输尿管镜钬激光碎石术患者的临床资料,旨在探讨术后发生肾包膜下血肿的相关危险因素。
1 资料与方法
1.1 临床资料 2013年9月-2019年9月我院行输尿管镜钬激光碎石术1428例,男827例,女601例,年龄 21-83 岁,平均(53.6±12.7)岁。 患者术前进行泌尿系超声、静脉肾盂造影、CT或者肾小球滤过率和肾动态明确诊断,均采用输尿管镜钬激光碎石术治疗,平均手术时间(39.1±12.6)min。其中单纯右侧输尿管结石785例,单纯左侧输尿管结石515例,双侧结石128例;输尿管下段685例,中段514例、上段229例;肾积水分为无、轻度、中度、重度:其中无肾积水86例,轻度328例,中度473例,重度541例;结石长径平均(10.8±4.5)mm;术前放置输尿管支架管97例,其中双侧21例;平均液体灌注压(13.2±2.6)mmHg;尿培养阳性157例,主要为大肠杆菌;合并高血压及糖尿病129例;孤立肾43例。
1.2 手术方法 采用德国WOLF牌输尿管硬镜,cook公司生产的超滑导丝及输尿管支架管 (双J管),科医人大功率钬激光。麻醉成功后,患者取截石位,常规消毒铺巾,F8/9.8输尿管硬镜,如果输尿管狭窄进镜困难,换用F6/7.5输尿管细镜,国产灌注压力泵压力设置为11-20mmHg,流量为120-200ml/min,在cook超滑导丝引导下直视进入输尿管,找到输尿管结石后,采用钬激光碎石机(550um激光纤维)碎石,能量设为0.6-1.0 J,频率10-20Hz。将结石击碎为2mm大小。碎石成功后,在超滑导丝引导下放置F5双J管内引流,退出输尿管镜,留置双腔气囊导尿管,手术结束。
1.3 统计学方法 采用SPSS22.0软件进行统计分析,计数资料比较采用χ2检验或者Fisher’s精确检验,计量资料采用(±s)表示,比较采用t检验。单因素分析对变量因素采用Logistic回归分析,P<0.05为差异有统计学意义。
2 结果
2.1 SRH(subcapsular renal hematoma)患者的一般临床结果 患者术后出现肾包膜下血肿(SRH)23例,其中男15例,女8例,均经B超及CT确诊。3例出现明显腰痛伴发热。SRH直径>4 cm较大血肿5例,其中1例双肾包膜下血肿并失血性休克;SRH直径<4 cm 18例;当SRH症状较轻,采取卧床休息、止血、加强抗感染等保守治疗,15例采取保守治疗好转。当SRH所致症状较重、血肿较大,大于4 cm或者血红蛋白下降明显,需行肾血管造影检查,必要时行肾动脉栓塞,需输血和肾血管造影检查3例。2例肾包膜下血肿形成脓肿或者未吸收,采取经皮肾穿刺引流治愈。
2.2 危险因素分析 将SRH组与无SRH组进行单因素分析,结果如下:两组间液体灌注压(P=0.028)、手术时间(P=0.019)、结石大小(P=0.043)、合并肾积水(P=0.016)、是否合并泌尿道感染(P=0.011)、是否合并高血压、糖尿病(P=0.040)及是否为孤立肾(P=0.023)等统计学上存在明显差异性;而年龄(P=0.052)、性别(P=0.285)、结石位置(P=0.178)、结石侧别(P=0.623)及术前是否留置输尿管支架管(P=0.733)无明显统计学差异(表1)。并将7种危险因素作为自变量进行Logistic回归分析表明:液体灌注压(0R=3.26 ,P=0.003)、手术时间(0R=2.87 ,P=0.002)、结石大小(0R=2.68,P=0.035),合并肾积水(0R=5.73,P=0.005),是否合并泌尿道感染 (0R=2.01,P=0.022)及是否为孤立肾(0R=3.30,P=0.015)是输尿管镜钬激光碎石术后发生肾包膜下血肿的独立危险因素(表 2)。
3 讨论
肾包膜下血肿(SRH)是输尿管镜钬激光碎石术后比较严重的并发症,发生率不超过1%,Bai等对2848例输尿管钬激光碎石术后出现肾包膜下血肿的患者总结发现,其发生率为0.4%[7,8]。国内王洛夫等[9]也报告了518例输尿管镜碎石术后出现肾包膜下血肿的患者发生率为0.6%,一般在术后1周以内发生。本组SRH总发生率为1.61%,高于以往的研究报道,我们的研究统计了所有输尿管镜钬激光术后发生包膜下血肿的患者,均采用B超及CT检查发现,包括无症状及有症状的SRH。患者无症状未进行检查可能漏诊,有研究认为URL术后SRH发生率降低的偏见会导致产生研究偏差[10]。因此,如果仅对有症状的SRH患者进行统计研究,可能存在研究偏差。
肾包膜下血肿是由于肾包膜下的血管破裂,使血液集聚在肾包膜和肾实质之间而形成血肿,其可能与肾内血管畸形、肾盂内持续高压灌注及输尿管梗阻解除后突然出现的积水肾减压效应等有关,还可能与体内毒素蓄积,使血小板的聚积、黏附功能降低及术前肾功能损害等相关[11,12]。王洛夫等[9]研究 认为高血压、糖尿病、高龄、感染是SRH发生的危险因素。而肾盂内压变化是SRH发生的诱因。本研究采用单因素分析表明液体灌注压、手术时间、结石大小、合并肾积水、是否合并泌尿道感染、是否合并高血压、糖尿病及是否为孤立肾可能为SRH发生的危险因素,研究发现SRH组与无SRH组比较,液体灌注压更大、结石更大、手术时间更长,常合并肾积水、泌尿道感染及高血压和糖尿病,孤立肾的比例明显高于无SRH组(27.8%,2.8%)。我们进一步采用Logistic回归多因素分析,结果表明液体灌注压、手术时间、结石大小、合并肾积水、是否合并泌尿道感染及是否为孤立肾为SRH发生的独立危险因素。高血压和糖尿病与SRH的发生存在相关性。高血压、糖尿病可引起全身血管病变,更容易产生动脉粥样硬化,会增加出血风险。但本组研究结果提示其并不是SRH的独立危险因素。液体灌注压、手术时间、结石大小及是否合并尿道感染为SRH发生的独立危险因素,与桂志明等[13]研究报道的结果一致,认为大的结石意味着更长的手术时间增加了组织及血管的通透性,从而导致SRH的发生。灌注液速度过快、压力过大使肾盂内压升高、肾血管内压增加,导致肾组织血管破裂形成SRH。这要求在手术操作过程采取必要措施尽量避免肾盂内压导致SRH,我们的体会是不严重影响手术术野操作情况下,尽量低灌注速度、低灌注压;要注意输尿管镜三通开关间断排水减压,也可以同时插入10号单腔导尿管至膀胱排尿减压或者拔除输尿管镜排水减压。肾积水尤其是重度积水,肾皮质变薄,如果肾盂压过高,更容易导致SRH发生。本组研究也显示肾积水是SRH发生的独立危险因素,与大多数研究报道一致。
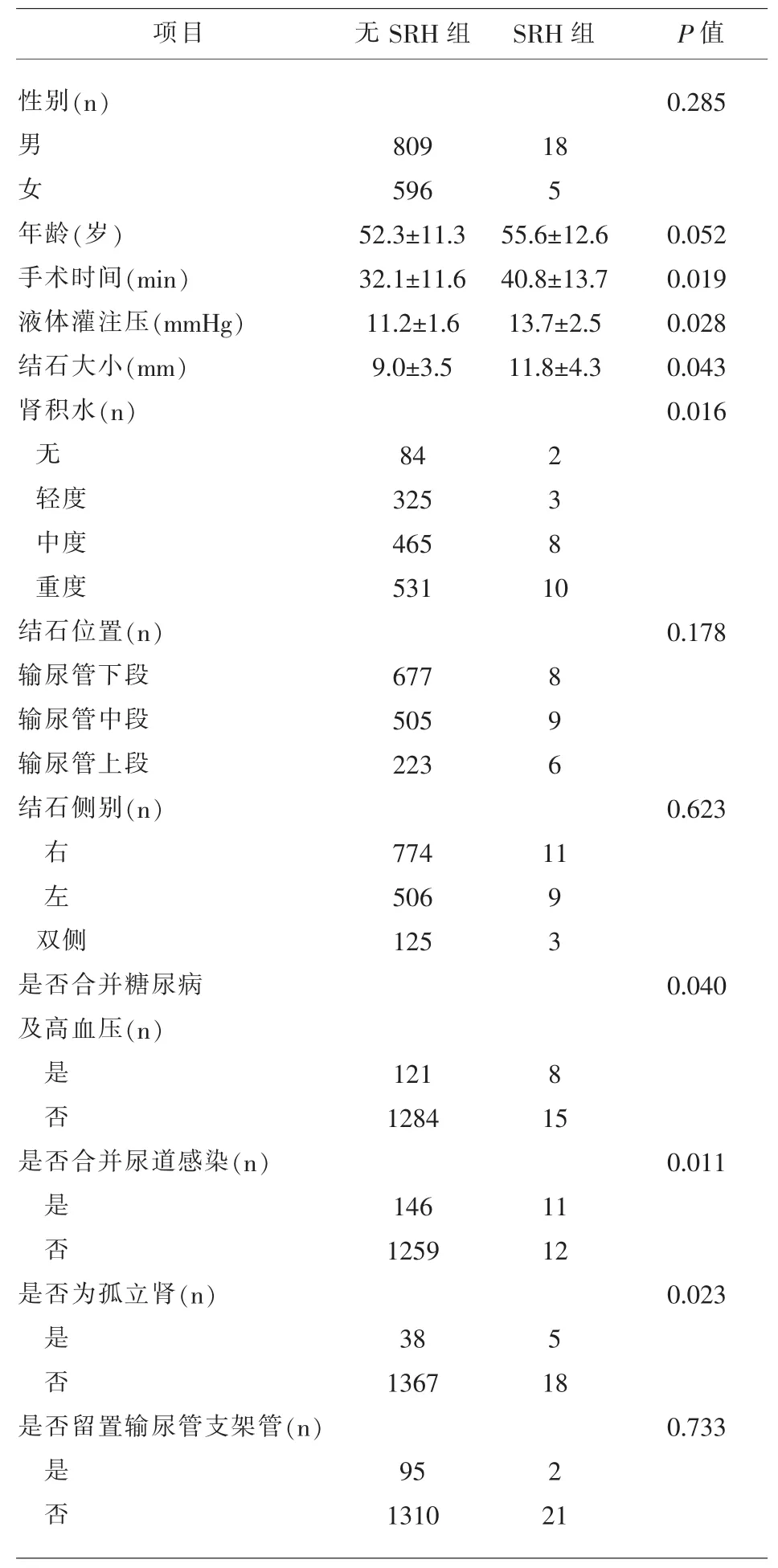
表1 SRH组与无SRH组单因素分析结果比较
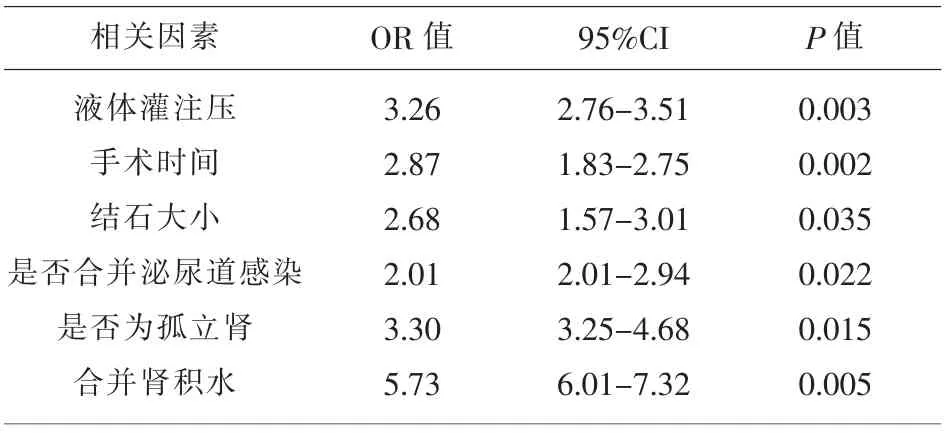
表2 术后SRH的多因素Logistic回归分析结果
本研究将是否为孤立肾纳入单因素相关性及多因素Logistic回归分析,结果显示是否为孤立肾也为SRH发生的独立危险因素。孤立肾患者,肾实质代偿性增大,孤立肾肾结石的治疗具有较高的出血风险,有研究报道采用PCNL等治疗孤立肾肾结石,与普通肾结石患者比较,具有更高的术后输血率,最高达10%[14]。本研究结果提示孤立肾为SRH发生的独立危险因素,目前未见相关研究报道。
我们的研究还通过对患者年龄、性别、结石位置、结石侧别及术前是否留置输尿管支架管进行单因素分析,结果表明均与SRH的发生无明显相关性。术前留置输尿管支架管虽然有利于肾积水的缓解和减轻泌尿道感染,可以降低SRH的发生率,但本研究结果SRH组与无SRH组比较无明显差异性。
肾包膜下血肿(SRH)的治疗以休息、止痛、止血、抗感染等保守治疗为主。如果患者出现血压不稳定,血红蛋白持续下降,应考虑并发失血性休克可能,及时输血、积极抗休克。并需行肾血管造影检查明确出血部位,必要时选择性动脉栓塞止血,避免无法止血切除肾脏可能。本研究15例采取保守治疗好转,进行输血和肾血管造影检查3例,无1例出现肾脏切除。如果SRH合并感染形成脓肿或者巨大血肿无法吸收,可以采取B超引导经皮穿刺置管引流治疗。本研究2例因形成脓肿,采取经皮肾穿刺引流治愈。
输尿管镜钬激光碎石术后发生肾包膜下血肿(SRH)比较少见,但是引起的后果比较严重。本研究评估其发生的危险因素,旨在引起泌尿外科医师的高度重视,术前充分评估其风险,减少SRH的发生。
