加氢催化剂对模拟生物油轻质组分与甲醇加氢共裂化制备芳香烃的影响
2020-07-23蔡勤杰张素平
孟 欣, 蔡勤杰, 张素平
(华东理工大学 煤气化及能源化工教育部重点实验室, 上海 200237)
0 引言
生物油提质被认为是实现生物油高品位利用的有效途径[1],[2]。以分子筛等固体酸材料为催化剂的生物油催化裂化技术是一种有前景的生物油提质技术, 其可以对生物油脱氧并发生芳构化等反应得到富芳香烃的液体燃料。但是,由于生物油的氢含量偏低, 导致裂化过程中易形成低氢碳比的焦炭。有研究表明,两段式的加氢共裂化过程是一种有效的生物油裂化改进方式, 该过程首先通过加氢预处理提高生物油原料的氢含量(饱和度),再通过裂化阶段的富氢化合物的协同转化进行二次供氢,从而抑制焦炭形成。由于生物油中的酚类化合物易导致裂化催化剂的结焦失活, 并且相对于醛酮类等其他生物油组分, 酚类化合物的加氢反应活性较低,因此,通过加氢催化剂的优化来实现酚类化合物的高效加氢并形成醇类等饱和化合物,从而减少进入裂化阶段的酚类化合物的量,对于提高加氢共裂化过程的稳定性具有重要意义。在生物油组分的加氢研究中,Ni 是最具代表性的廉价活性金属[3],[4]。有研究表明,以Ni 为基础添加第二种金属(Cu 和Fe 等),添加的金属可与Ni 发生协同作用,形成双功能加氢催化剂,从而在醛类和酚类等加氢反应过程中产生积极作用[5]~[8]。 此外,具有催化活性的载体,如酸性的ZrO2和Al2O3等[9],[10],也能与Ni 等金属发生协同催化效应而促进酚类等生物油组分的转化。
本文以富酚的模拟生物油轻质组分为原料,考察了两种类型的载体 (惰性的SiO2和酸性的ZrO2)负载的单金属Ni 和双金属Ni-Cu 和Ni-Fe催化剂在模拟轻质组分与甲醇加氢共裂化制备芳香烃过程中的催化效果, 以此来优选适宜生物油轻质组分(如水相和蒸出馏分)与甲醇加氢共裂化的加氢催化剂, 并深入理解不同加氢催化剂对生物油轻质组分化合物(特别是酚类)加氢行为以及后续裂化行为的影响。
1 实验与方法
1.1 实验原料与仪器
模拟生物油轻质组分的有机物成分包括乙酸、羟基丙酮、苯酚、邻苯二酚和愈创木酚[11],其质量分数分别为20%,20%,3%,3%和3%,其余为水,质量分数为51%。 为了模拟低甲醇掺混的反应过程, 选用较高的模拟生物油与甲醇比例(2∶1)。
采用自行搭建的固定床反应系统、Agilent 6820 型气相色谱仪(安捷伦科技有限公司)、华爱9560 型气相色谱仪(上海华爱色谱分析技术有限公司)和Clarus 500 型气相色谱质谱联用仪(GCMS)(珀金埃尔默有限公司)进行实验与分析。
1.2 催化剂
加氢催化剂Ni/SiO2,Ni-Cu/SiO2,Ni-Fe/SiO2,Ni/ZrO2,Ni-Cu/ZrO2和Ni-Fe/ZrO2均通过等体积浸渍法制备而成, 其中,SiO2和ZrO2购买于阿拉丁试剂公司,Ni,Cu 和Fe 的负载量均为5%。
加氢催化剂的制备: 以Ni-Fe/ZrO2为例,称取一定量的Ni(NO3)2·6H2O 和Fe(NO3)3·9H2O 溶于一定体积的去离子水中;将计算称量好的ZrO2浸 渍 在 按 比 例 配 制 好 的Ni(NO3)2·6H2O 和Fe(NO3)3·9H2O 水溶液中,室温下静置12 h,然后置于110 ℃的烘箱中干燥过夜; 最后将催化剂前驱体放入马弗炉中以5 ℃/min 的升温速率升温至500 ℃,保持2 h;实验前,将催化剂在500 ℃的H2气氛下还原2 h。
裂化催化剂采用商用分子筛催化剂ZSM-5(Si/Al=25),购买于南开大学分子筛厂,在使用前置于马弗炉中500 ℃焙烧2 h 使其活化。
1.3 实验装置及流程
加氢裂化反应装置如图1 所示。 加氢反应和裂化反应均在固定床反应器中进行,其中,加氢段反应管内径为10 mm, 裂化段反应管内径为14 mm,当进行加氢共裂化反应时,两个固定床反应器采用串联形式连接。实验气氛为H2,流量为100 mL/min,反应过程中系统压力维持在4.0 MPa。 原料通过给料泵进入反应系统, 雾化后依次通过加氢和裂化反应段, 加氢反应段的温度控制在250℃,裂化反应段的温度控制在400 ℃,加氢催化剂和裂化催化剂的用量均为2 g,反应物的质量空速(WHSV)恒为2 h-1,反应时间为6 h,该反应工况的选择是基于文献[11]。 反应结束后,产生的气体首先经过冷凝器冷凝, 冷凝之后的产物再通过气液分离器将气体与液体分离, 分别收集并进行分析。

图1 加氢裂化反应装置示意图Fig.1 Schematic diagram of the hydrogenation-cocracking reactor
1.4 产物分析
实验过程中获得的气体产物由集气袋采样,通过华爱9560 型气相色谱仪 (毛细管柱型号为HP-AL/KCL,检测器采用热导检测器)进行定量分析;加氢反应获得的液体产物为均一相,裂化后得到的液体产物由明显分层的水相和油相组成;加氢反应获得的液体产物和加氢裂化所得的油相液体产物通过Clarus 500 型气相色谱与质谱联用仪(色谱柱型号为DB-WAX)进行定性分析,并通过峰面积归一法进行定量分析; 加氢过程中固体产物的生成量很少,可忽略,加氢裂化过程中裂化催化剂表面的焦炭生成量通过热重分析仪进行分析; 加氢过程得到的液体产物通过Agilent 6820型气相色谱仪(色谱柱型号为HP-5,检测器为氢火焰离子检测器)进行定性分析,并通过外标法进行定量分析, 以计算加氢反应后反应物的残余量以及对应加氢产物的生成量,产物收率Yi的计算式为

式中:mi为加氢产物的生成量,g;i 为液体、 气体或焦炭;mLR为反应物进料量,g。
2 结果与讨论
2.1 催化反应结果
为了理解不同加氢催化剂对整体加氢共裂化过程的影响, 首先研究了不同加氢催化剂对模拟生物油轻质组分和甲醇加氢过程的影响, 随后开展不同加氢催化剂下模拟生物油轻质组分与甲醇的加氢共裂化研究。
2.1.1 加氢催化剂对加氢过程的影响
不同加氢催化剂作用下, 加氢产物的产率如图2 所示。从图2 可以看出:不同催化剂对加氢反应的液体产物的产率影响较小, 液体产率均为90%左右;当加氢催化剂为Ni-Fe/SiO2时,液体产物的产率最高,为95.8%,当加氢催化剂为Ni/ZrO2时, 液体产物的产率最低, 为87.2%;以SiO2为载体的催化剂加氢得到的液体产物的产率要略高于以ZrO2为载体的催化剂加氢得到的液体产物的产率,气体产物的产率则与之相反,且气体产物主要为甲烷等轻质烷烃以及少量的COx。

图2 不同加氢催化剂作用下,加氢产物的产率Fig.2 Yield of hydrogenation products with different hydrogenation catalysts
为了了解模拟的轻质组分中各化合物的加氢转化行为, 对不同加氢催化剂作用下的各组分反应前、 后的含量进行了检测, 检测结果如表1 所示。

表1 不同加氢催化剂作用下,生物油组分及其典型加氢产物的含量Table 1 The contents of bio-oil components and typical hydrogenation products with different hydrogenation catalysts mmol
将加氢反应获得的液体产物采用GC-MS 进行分析,其中各族类化合物的相对含量如图3 所示。

图3 不同加氢催化剂作用下,加氢产物各族类化合物的相对含量Fig.3 The relative contents of different kinds of hydrogenation products with different hydrogenation catalysts
由表1 和图3 可以看出:在不同加氢催化剂作用下,酮类(羟基丙酮)和酸类(乙酸)的转化行为相近,酚类的转化行为差异较明显;羟基丙酮主要发生羰基的加氢反应得到丙二醇; 尽管乙酸的转化率有所不同,但对应的加氢产物(乙醇)的产量始终较低, 乙酸主要和甲醇及丙二醇等醇类发生酯化反应得到酯类,在加氢产物中检测出9%~29.1%的酯类(包括乙酸甲酯、丙二醇乙酸酯等);在Ni/ZrO2的催化作用下, 酚类的加氢效果最好,而在Ni-Fe/SiO2的催化作用下, 酚类的加氢效果最差。
2.1.2 加氢催化剂对加氢共裂化过程的影响

图4 不同加氢催化剂作用下,加氢共裂化产物的产率Fig.4 Yield of hydrogenation-cocracking products with different hydrogenation catalysts
不同加氢催化剂作用下, 加氢共裂化产物的产率如图4 所示。 由图4 可以看出:当Ni/ZrO2为加氢催化剂时, 加氢共裂化的油相产率最高,为24.8%;其余工况下,油相产物的产率均为12.2%~19.8%;当Ni-Fe/SiO2为加氢催化剂时,加氢共裂化的油相产率最低,仅为12.2%。分析气体产物时发现,与以Ni/ZrO2为加氢催化剂的工况相比,其他工况的C2H4,C3H6和C4H8等轻质烯烃的生成量更多,总产率为1.7%~2.9%。从催化剂表面的积炭产率也可以看出:以Ni/ZrO2为加氢催化剂时,在裂化阶段,HZSM-5 催化剂的表面积炭量最少;而以Ni-Fe/SiO2为加氢催化剂时, 在裂化阶段,HZSM-5 催化剂的表面积炭量最大。
分析水相产物时发现, 各工况的水相产物中均存在一定量未转化的乙酸和甲醇, 根据它们在水相产物中的残余量计算得到的甲醇和乙酸的转化率如表2 所示。 从表2 中可以看出,以Ni/ZrO2为加氢催化剂时, 加氢共裂化过程的乙酸转化率接近95%,同时,甲醇转化率在99%以上;而对于其他工况, 乙酸和甲醇转化率均存在不同程度的下降。
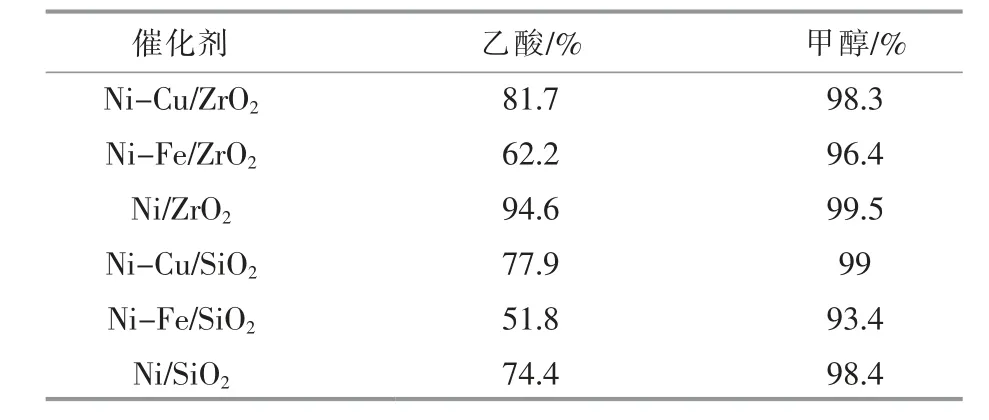
表2 不同加氢催化剂作用下,乙酸和甲醇的转化率Table 2 Conversion rates of acetic acid and methanol with different hydrogenation catalysts
不同加氢催化剂作用下, 加氢裂化油相产物各组分的相对含量如图5 所示。从图5 可以看出,以Ni/ZrO2为加氢催化剂时, 芳香烃的相对含量最高, 为99.2%, 同时含氧副产物的相对含量较低;在其他工况下,含氧副产物的相对含量均有一定程度的提升,其中,以Ni-Fe/SiO2为加氢催化剂时,油相产物中含氧副产物的相对含量最高(主要是酚类),为9.41%。

图5 不同加氢催化剂作用下,加氢裂化油相产物各组分的相对含量Fig.5 Component contents of hydrogenation-cocracking products with different hydrogenation catalysts
2.2 分析与讨论
上述实验结果表明, 不同的加氢催化剂对模拟生物油轻质组分与甲醇的加氢乃至加氢共裂化行为会产生显著影响。
在加氢阶段,以惰性SiO2为载体的3 种加氢催化剂(Ni/SiO2,Ni-Cu/SiO2和Ni-Fe/SiO2),在酮类加氢方面有良好的催化效果, 使其转化为对应的醇类(丙二醇)。但是,这3 种催化剂在酚类的加氢转化上催化效果较差, 尽管有部分邻苯二酚和甲氧基苯酚通过脱羟基和脱甲氧基作用生成了苯酚,但苯环的加氢效率很低,导致加氢产物中存在大量的苯酚(包括未转化的和其他酚类形成的)。这表明在惰性载体无催化活性的情况下,金属Ni,Cu 和Fe 对酚类加氢的催化作用有限。 在以惰性SiO2为载体的3 种催化剂中,Ni-Cu/SiO2对酚类加氢效果要略优于Ni/SiO2, 这是因为Cu 也能作为活性中心对酚类的转化产生一定的促进作用[14]; 但是,Ni-Fe/SiO2对酚类加氢的催化效果反而不如Ni/SiO2,这可能是因为Ni 和Fe 会在SiO2载体上形成Ni-Fe 合金[6],在这种情况下,Fe 对酚类的加氢没有催化作用,反而会阻碍酚类在Ni 上的吸附,从而削弱了作为唯一活性中心的Ni 对酚类的加氢作用。
当以Ni/ZrO2为催化剂时, 不仅酮类的加氢效率较高,酚类也得到了高效的转化,这与Ni/SiO2的催化行为显著不同。 根据所得加氢产物可知,苯酚主要发生苯环加氢反应得到环己醇;邻苯二酚发生苯环加氢反应生成环己二醇, 也可能发生脱羟基和苯环加氢反应生成环己醇; 愈创木酚主要发生脱甲氧基和苯环加氢反应生成环己醇。 Foster A J[15]认为,苯酚能够在ZrO2的酸性位上发生分段吸附活化,从而与Ni 上解离吸附的氢发生相互作用最终实现加氢反应, 即Ni 与ZrO2存在协同作用。 但是,当以Ni-Cu/ZrO2和Ni-Fe/ZrO2为催化剂时, 酚类的加氢效率显著下降。Huynh T M 发现,Cu 会在一定程度上阻碍Ni 与酸性位的直接协同作用, 同时Cu 和酸性位并不能通过相互作用促进苯酚转化,因此,加入Cu 之后,苯酚的加氢效率显著降低[16]。 基于这一观点,我们分别测试了原料在Cu/ZrO2和Fe/ZrO2(Cu 和Fe 的负载量均为5%)作用下的的加氢效率,结果如表3 所示。 由表3 可知, 在Cu/ZrO2和Fe/ZrO2的催化作用下,酚类的加氢效率均较低,这是因为Cu 和Fe 的存在削弱了Ni 与ZrO2酸性位之间的相互作用,同时自身也难以通过与ZrO2相互作用来对酚类进行加氢。

表3 在Cu/ZrO2 和Fe/ZrO2 的催化作用下,酚类加氢反应前后的含量Table 3 Contents of phenols with Cu/ZrO2 and Fe/ZrOm2mol
当以Ni/ZrO2为加氢催化剂时, 酚类的加氢效率最高, 相应的整体加氢共裂化的油相产物的产率也最高,同时,油相中目标产物芳香烃的含量也最高。 相比而言,使用其他加氢催化剂的工况,加氢共裂化过程的油相品质和产率均有不同程度的下降,其中,以Ni-Fe/SiO2为催化剂时,酚类的加氢效率最低, 其对应的加氢共裂化过程的油相产物的产率和品质均为最低。 同时还发现,以Ni/ZrO2为加氢催化剂时,甲醇等反应物在加氢共裂化过程中的转化效果最好, 而且气体产物中烯烃的生成量以及裂化阶段催化剂表面的积炭生成量均最少。
以上结果表明,以Ni/ZrO2为加氢催化剂的加氢共裂化过程具有最好的反应稳定性, 而使用其他加氢催化剂的工况, 由于裂化阶段催化剂表面的积炭生成量较多,会导致催化剂活性下降。有研究表明,对于含氧化合物的裂化过程,首先发生脱氧反应生成轻质烯烃, 随后轻质烯烃再进一步发生芳构化反应得到芳香烃[17]。在本文中,对于使用其他加氢催化剂进行加氢共裂化的工况, 随着裂化催化剂活性的下降,一方面,初步脱氧反应的效率下降, 导致甲醇和乙酸等反应物的转化率降低以及油相中含氧副产物的产生,另一方面,芳构化能力的减弱,导致轻质烯烃的释放。这些负面影响最终使得目标产物芳香烃的产率降低。 结合前面加氢研究的讨论, 未在加氢阶段转化的酚类是导致裂化催化剂失活加快的主要原因。 这些酚类易发生缩合形成焦炭沉积在催化剂表面, 导致催化剂的失活。 由于Ni/ZrO2使得酚类高效加氢转化为环己醇和环己二醇等醇类化合物, 不仅避免了酚类存在导致的裂化催化剂的快速失活, 同时这些醇类可直接通过脱羟基和脱氢反应高效转化为芳香烃。
我们注意到, 即使以Ni/ZrO2作为加氢催化剂,乙酸并不能有效加氢生成乙醇,这是因为乙酸主要和醇类发生酯化反应生成酯类, 乙酸加氢生成乙醇的效率较低,因此,加氢产物中还有较多的乙酸和酯类。 文献[18]发现,乙酸单独裂化的能力较差,由于其富氧的特性,当其以脱水的形式脱氧后,易形成低氢碳比的焦炭。 而本文中以Ni/ZrO2为加氢催化剂的加氢共裂化过程的稳定性较好,说明甲醇的存在起到了积极作用而且是必需的。有研究表明, 富氢的甲醇在裂化过程中会首先脱氧生成乙烯等轻质烯烃,在轻质烯烃(H/C=2)芳构化生成芳香烃 (H/C<2) 的过程中会产生富余氢。 这些富余氢能够参与到乙酸及酯类的脱氧反应中,生成轻质烯烃类中间产物并进一步芳构化生成芳香烃, 从而抑制焦炭和含氧化合物的生成[19]。此外,以Ni/ZrO2作为加氢催化剂时,加氢产物中还有少量未转化的酚类, 这表明甲醇对酚类的转化也能起到促进作用[17]。 但从其他加氢共裂化过程的结果来看,由于本文所采用的油/甲醇比例较高(2∶1),在酚类加氢效果不佳而导致进入裂化阶段的酚类较多时, 原料中所掺混的甲醇不足以使这些酚类都得到高效转化。 这也体现了Ni/ZrO2作为加氢催化剂在加氢共裂化过程中的优势,即通过加氢阶段对酚类的高效加氢,使得共裂化过程中对甲醇供氢的需求量减少, 从而能够减少原料中的甲醇掺混量,提高工艺经济性。
文献[11]的研究结果表明,甲醇单独裂化的油相产率约为22%,而本文优化工况下的油相产物产率可达24.8%,且芳香烃类含量在99%以上,表明模拟生物油轻质组分在甲醇的促进下确实高效转化为了液体芳香烃。
3 结论
本文主要开展了不同加氢催化剂对生物油模拟轻质组分与甲醇加氢共裂化制备芳香烃的影响研究,考察的加氢催化剂分别为以SiO2和ZrO2载体负载的Ni,Ni-Cu 和Ni-Fe 催化剂。 研究结果表明: 所有加氢催化剂对于酮类加氢都有良好的催化效果而对酸类加氢的催化效果较差, 且在酚类加氢的催化效果上有所差别;Ni/ZrO2具有最好的酚类加氢催化效果, 这得益于金属Ni 和ZrO2酸性位的协同作用;Ni-Cu/ZrO2和Ni-Fe/ZrO2对酚类加氢的催化效果不如Ni/ZrO2,因为Cu 和Fe与Ni 形成合金后阻碍了Ni 和ZrO2的协同作用;以SiO2为载体的加氢催化剂缺乏载体的酸性位,其对酚类加氢的催化效果均不高。 由于酚类的高效加氢, 以Ni/ZrO2为加氢催化剂的加氢共裂化过程借助协同反应物甲醇在裂化阶段的二次供氢作用,实现了整体反应物的高效转化,油相产率达到24.8%,其中芳香烃的相对含量在99%以上;而使用其他加氢催化剂的工况, 由于裂化阶段的酚类进料量较大,加速了裂化催化剂的失活,导致油相产率和品质都显著下降。因此,在较少甲醇掺混的加氢共裂化过程中, 以Ni/ZrO2为加氢催化剂更有利于芳香烃的生成,从而提高生物油的品质。
