莲黄颗粒治疗鸡大肠杆菌病的试验研究
2020-07-21杨俊芸刘起军
杨俊芸,刘起军
(1.四川省内江市食品药品检验检测中心,四川内江641000;2.四川恒通动保生物科技有限公司研究院,四川内江 641000)
莲黄颗粒收载于 《兽药质量标准·中药卷》(2017版),是由穿心莲、黄芩等8味中药组方,经提取加工制成的颗粒剂,具有清热燥湿,凉血止痢功效,用于治疗鸡的热毒下痢[1]。该制剂尽管在我国有多家兽药企业申报文号,产品也具有较广泛的临床应用基础且积累了诸多经验,然而我们却很少见到关于该制剂的相关研究论文。为了更好地确定该产品的临床定位,我们采用实验临床试验方法,采用致病性大肠杆菌造模,观察了莲黄颗粒治疗鸡大肠杆菌病的有效性与安全性。
1 材料与方法
1.1 材料
1.1.1 试验药品
莲黄颗粒,由四川恒通动保生物科技有限公司中试生产,批号为20190701。每1g相当于原生药1.26g。规格:100g/袋。
氟苯尼考粉,河南省天亿源动物药业有限公司生产,规格100g,批号19062401。
1.1.2 菌株及标准血清
大肠杆菌O78株与大肠杆菌“O”抗原定型血清,购自中国兽药品监察所。
1.1.3 其它试剂及主要仪器
普通肉汤培养基 (产品批号:20190614)、营养琼脂培养基(产品批号:20190708),购自青岛高科园海博生物技术有限公司。
DHP-9162型电热恒温培养箱,上海恒科学仪器有限公司;超净工作台,苏州安泰空气技术有限公司;TGL-16B型高速台式离心机,上海安亭科学仪器厂;分析天平,赛多利斯科学仪器(北京)有限责任公司;智能蒸汽灭菌器,长春市百奥生物仪器有限责任公司;HZQ-C02型空气浴振荡器,哈尔滨市东联电子技术开发有限公司。全自动细菌鉴定药敏检测仪:BDPhoenixTMSystem,型号 :PhoenixTM100,BD (Becton and Dickinson Company)公司。
1.1.4 试验动物
未经鸡大肠杆菌疫苗免疫的1日龄健康海兰褐公雏,从长春市农科院饲养场购买。饲养至12日龄时随机抽取30只,分别采血并从泄殖腔取排泄物进行细菌分离培养,用抗大肠杆菌O78的标准血清作玻片凝集反应,确认试验鸡群中不存在鸡大肠杆菌O78感染。并且每天观察记录鸡群健康状况,确认无疫病发生。
1.1.5 饲料及试验鸡饲养管理
雏鸡无抗生素添加的全价饲料,四川简阳佳旺饲料有限公司生产。试验鸡饲养在本研究院动物中心鸡舍,自由采食与饮水。
1.2 方法
1.2.1 大肠杆菌O78株复壮
选4日龄健康海兰褐鸡3只,胸肌注射0.2 ml菌液方式进行 (平板计数确定为1010cfu/ml)。隔离饲养,待典型症状出现后,无菌采集病鸡的肝、脾组织或心包内分泌物,分别接种于营养肉汤琼脂、麦康凯琼脂和伊红美兰琼脂上,经37℃培养,观察培养的细菌菌落形态,进行革兰氏染色、镜检、观察结果。
1.2.2 病原分离与鉴定
无菌操作采取濒死鸡肝脏、脾脏、心脏及心包液等,做病料触片及染色镜检。
将病料接种在营养肉汤中进行增殖培养,37℃,24h后观察肉汤变化。
采用全自动细菌鉴定药敏检测仪进行细菌鉴定。取1个或几个菌落于0.85%NaCl基物安培管,用ATB麦氏比浊管制备混浊度相当于0.5 McFarland(1McFarland相当于含细菌3×108个/ml)的菌悬液,用定量连续ATB接种器于ID32E试验条每孔接种55μl菌悬液。在ADH、LDC、URE、LARL、GAT、5KG孔中滴2滴矿物油, 盖上盖子,37℃好氧培养18~24h后,在吲哚反应孔中加1滴James试剂,用ATB分析仪读取结果并用相应软件分析。
血清型鉴定按中国兽医药品监察所《大肠埃希氏菌“O”抗原定型血清使用说明书》进行。
1.2.3 大肠杆菌计数及感染液制备
挑取斜面保存的大肠杆菌O78,接种于营养肉汤培养基37℃培养24h,将菌液5000r/min离心15min,弃上清液,沉淀用0.05mol/L的PBS(pH7.2)洗涤两次,按照倍比稀释法,依次配制稀释度为10-2~10-9的菌悬液。采用10-4~10-9稀释度的菌液进行计数。分别移取不同稀释度的菌液0.1mL,均匀涂布在营养肉汤琼脂平板上,静置20~30min,使菌液渗透于培养基内,然后将培养皿倒转,37℃培养16h后计数,每个浓度重复4次。用PBS液调整至1×1010cfu/ml,4℃冰箱保存备用。
1.2.4 试验鸡分组与处置
将供试鸡随机分为7组,每组80只,如表3-1所示。9日龄时,中药预防组开始给药,到12日龄时,除健康对照组外每只鸡胸肌注射大肠杆菌培养液攻毒0.2ml(攻毒浓度为3.5×109cfu/ml)。各组动物按表3-1进行处置,为准确把握给药剂量,采用灌胃方式给药,各组不同剂量的药物溶解成同体积灌胃。
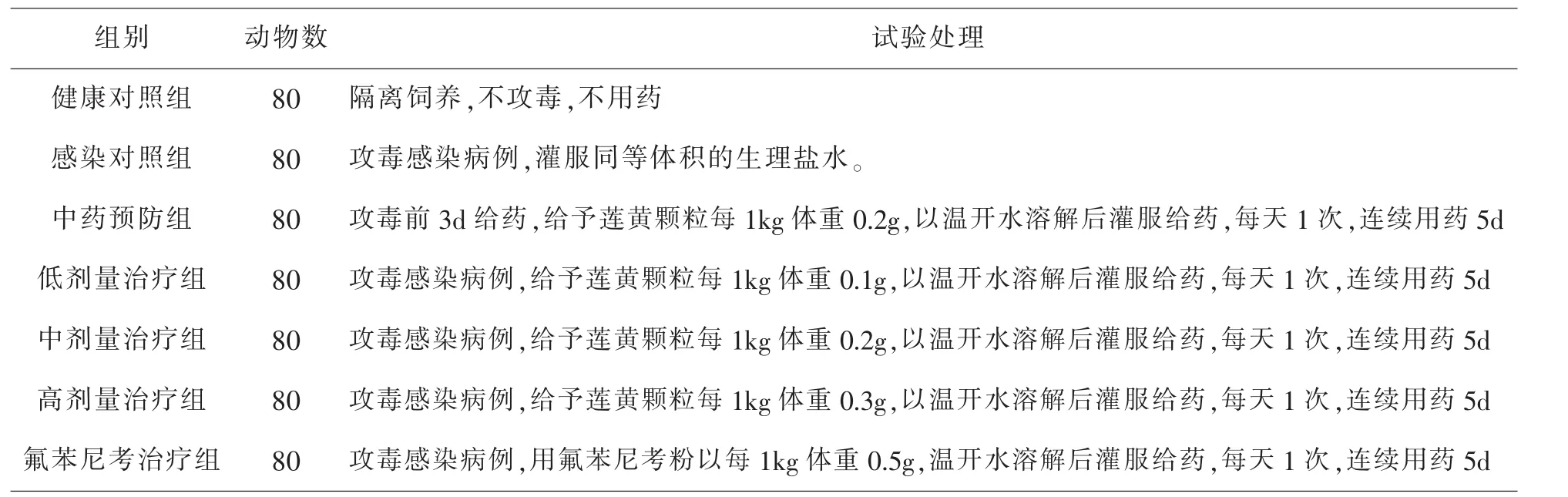
表3-1试验鸡分组与处置
1.2.5 临床判定标准
1.2.5.1 感染发病 健康对照组精神活泼,行为、饮食欲正常。与此相对应,雏鸡接种大肠杆菌后呈现精神沉郁,蹲伏扎堆,不欲饮食等明显临床症状;无菌采集心血、肝脏或气囊等,能分离到大量与攻毒菌株相同血清型大肠杆菌者判定为感染发病。
发病率(%)=组内发病数(只)/该组试验鸡数(只)×100%
保护率(%)=(攻毒对照组发病率-给药组发病率)/攻毒对照组发病率×100%。
1.2.5.2 感染死亡 试验期间,鸡在接种大肠杆菌后突然死亡或出现明显大肠杆菌病临床症状后死亡,剖检可见多数具有大肠杆菌病内脏器官病变,并从肝脏、心血或气囊等分离等到与接种菌相同的大肠杆菌者判定为感染死亡。
感染死亡率(%)=组内死亡数(只)/该组试验鸡数(只)×100%
1.2.5.3 治愈 发病鸡经治疗后精神状态、饮食欲、粪便恢复正常,其它临床症状消失,抽查剖检内脏器官正常,从肝脏、心血或气囊等分离不到与接种菌相同的大肠杆菌者判定为治愈。治愈率(%)=组内治愈数(只)/该组试验鸡发病数(只)×100%
1.2.5.4 增重 称量试验开始时及试验结束时鸡的体重,观察试验鸡体重变化情况,为尽量减少试验鸡抓捕应激,仅称量各组平均体重。
增重率 (%)=组内最终平均体重-初始平均体重/初始平均体重×100%
1.2.6 统计分析 利用SPSS19.0软件对莲黄颗粒用于人工感染鸡大肠杆菌病各组鸡的发病率、病死率、治愈率采用χ2检验进行统计分析;对莲黄颗粒对各组试验鸡增重的影响结果进行单因素方差分析,采用Duncan法进行多重比较,结果以均值±标准差(x±SD)表示,P<0.05表示差异显著,P<0.01表示差异极显著。
2 结果
2.1 人工感染发病情况
按照预备临床试验的攻菌剂量和造模条件,给12日龄鸡胸肌注射大肠杆菌培养液0.2ml攻毒(攻毒浓度为3.5×109cfu/ml),成功造成了鸡大肠杆菌病模型。试验鸡攻菌3h后,各组鸡开始陆续发病,最初出现精神沉郁,食欲减损,活动减少,蹲伏或拥挤扎堆。试验鸡攻菌4h后,除中药预防组仅有少数鸡只发病外,其余各组全部发病。此后病鸡精神萎靡,闭目呆立,或扎堆而卧,羽毛蓬乱,饮、食欲大减,排污黄色或黄绿色稀便;部分鸡呼吸困难,张口伸颈,气促喘粗;有的鸡站立不稳,腿翅无力,或瘫软卧地。攻菌6h后开始有鸡死亡,10h死亡数增加,24-48h达死亡高峰,72h后死亡明显减少。各组鸡发病和死亡情况见表 3-3、3-4。
2.2 病理变化
病死鸡肛门及其周围羽毛粘附粪污,早期死亡鸡仅见急性败血症病变,中后期死亡病鸡出现典型的心包炎、肝周炎、气囊炎,少数可见关节炎病变。心包腔积有淡黄色浑浊渗出液,心包壁增厚,不透明,附着纤维素性渗出物,少数鸡只甚至可见黄色干酪样物质,心脏肿大,心肌有坏死灶;肝脏肿大,肝脏表面覆盖灰白色纤维素性渗出物,容易剥离,肝实质偶有灰色坏死区;肾脏肿大充血;气囊壁混浊,不均匀增厚,呼吸面被覆干酪样渗出物;嗉囊内容物充实,酸臭气味浓烈;腺胃、肌胃内容物有酸臭气味,腺胃黏膜糜烂,肌胃角质层溃疡,有斑点状出血;十二指肠、空肠、回肠、盲肠等黏膜出血、脱落,肠系膜充血出血。
2.3 细菌分离与鉴定
将所采集病料,用无菌生理盐水洗脱、稀释,划线接种于麦康凯和伊红美兰培养基中,37℃培养24h,挑取麦康凯平板上的粉红色菌落、伊红美兰平板上的黑色泛金属光泽的菌落,镜检呈革兰氏染色阴性中等大小杆菌。对照组样品未分离到致病性大肠杆菌。
采用全自动细菌鉴定药敏检测仪进行细菌鉴定,确定致病病原为大肠杆菌。
按中国兽医药品监察所 《大肠埃希氏菌“O”抗原定型血清使用说明书》进行血清型鉴定,确定各人工感染组样品均为O78菌株。
2.4 莲黄颗粒对人工感染鸡大肠杆菌病的预防作用
攻毒前3天给药,给予中剂量莲黄颗粒每1kg体重0.2g,以温开水溶解后灌服给药,每天1次,连续用药5d,对人工感染鸡大肠杆菌病有明显的预防作用,攻菌后发病率仅为12.5%,其保护率达87.5%,与感染对照组相比,发病率和病死率均有显著差异(P<0.01)。预防组发病鸡经继续服用莲黄颗粒后全部康复,结果见表3-2。
2.5 莲黄颗粒对人工感染鸡大肠杆菌病的治疗作用

表3-2莲黄颗粒对人工感染鸡大肠杆菌病的治疗作用
鸡接种大肠杆菌发病后,莲黄颗粒治疗组分别按每 1kg体重 0.1g、0.2g、0.3g的剂量溶解成同体积灌胃给药,病情很快得到控制。12h后精神、饮食欲明显好转;36h-48h后病鸡临床症状基本消失,活动增加,饮食欲基本恢复正常。莲黄颗粒高中低剂量组治疗效果均极显著优于感染对照组(P<0.01)。其中,高、中剂量治疗组与氟苯尼考治疗组的治疗效果相当(P>0.05),且显著高于低剂量治疗组(P<0.01或P<0.05,表3-3)

表3-3 莲黄颗粒对人工感染鸡大肠杆菌病治疗作用
2.6 莲黄颗粒对试验鸡增重的影响
各组鸡在12日龄时平均体重差异不显著(P>0.05)。在17日龄各组鸡停药后,感染对照组体重极显著低于其他各组(P<0.01),预防组体重与正常对照组体重相仿,且极显著高于其他各组(P<0.01);低剂量组与健康对照组、预防组、中、高剂量治疗组以及氟苯尼考治疗组相比,也存在极显著性差异(P<0.01);中、高剂量组和氟苯尼考组之间无显著性差异(P>0.05)。详见表3-4。
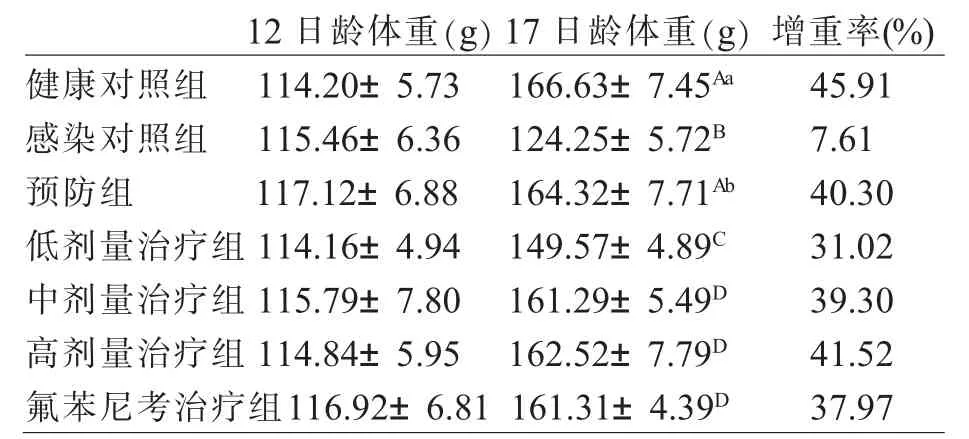
表3-4 莲黄颗粒对试验鸡增重的影响
3 讨论
莲黄颗粒收载于 《兽药质量标准·中药卷》(2017版),是由穿心莲、黄芩、白头翁、地榆、马齿苋、诃子、秦皮、甘草等8味中药组方,经提取加工制成的颗粒剂,具有清热燥湿,凉血止痢功效,用于治疗鸡的热毒下痢[1]。莲黄颗粒组方药物中,穿心莲味苦性寒,具有清热解毒、消肿止痛功效,主治感冒发热,湿热下痢,蛇虫咬伤,疮痈疔毒等病证;黄芩味苦性寒,具有清热燥湿、泻火解毒、止血、安胎功效,主治肺热咳嗽,胃肠湿热,泻痢,黄疸,高热贪饮,便血,衄血,目赤肿痛,痈肿疮毒,胎动不安等病证。二药共为君药。白头翁味苦性寒,具有清热解毒,凉血止痢功效,主治热毒血痢,湿热肠黄等病证;地榆味苦酸涩,性微寒,具有凉血解毒,止血敛疮功效,主治血痢,衄血,子宫出血,疮黄疔毒,烫伤等病证;马齿苋味酸、性寒,具有清热解毒、凉血止痢功效,主治热毒下痢,疮黄肿毒,热淋血尿,便血,蛇虫咬伤等病证。三药共为臣药。诃子味苦酸涩、性平,具有涩肠、敛肺功效,主治久泻久痢,便血,脱肛,肺虚咳喘等病证;秦皮味苦涩、性寒,具有清热燥湿、收涩止痢和明目等功效,主治湿热下痢、目赤肿痛、云翳等病证。二药共为佐药。甘草味甘性平,具有补脾益气、祛痰止咳、和中缓急、解毒、调和诸药、缓解药物毒性烈性等功效,主治脾胃虚弱、倦怠无力、咳喘、咽喉肿痛、中毒和疮疡等病证,为使药。尽管《兽药质量标准》中药卷标明莲黄颗粒的主治是鸡热毒下痢,但众多研究文献表明,组成莲黄颗粒的中药及其成分对抑制大肠杆菌或防治鸡大肠杆菌病有效[3-8]。王娜通过研究证实黄芩提取物黄芩苷能在体外有效抑制大肠杆菌的生长,MIC为1.56mg/ml。赵银丽等研究表明,黄芩水煎液药物浓度为5g/ml时可使7日龄雏鸡获得90%以上的攻毒保护;药物浓度为10g/ml时可使100%雏鸡获得攻毒保护,说明黄芩可以对抗鸡大肠杆菌,用于防治鸡的大肠杆菌病。梁英等研究发现黄芩提取物(黄芩黄酮)对鸡大肠杆菌具有明显的体内抑菌作用,并对人工诱发的鸡大肠杆菌病有明显的防治效果,预防组有效率达80%,治疗组有效率达70%。
本试验结果表明,给药组鸡的发病症状较感染对照组轻;剖检观察表明,给药组鸡脏器的病理变化较感染对照组轻;给药组的病死率均极显著低于感染对照组(P<0.01),治愈率、试验鸡增重均极显著高于感染对照组(P<0.01),表明莲黄颗粒对人工诱发的鸡大肠杆菌病有较好的防治作用。
4 结论
4.1 采用12日龄海兰褐公雏,每只鸡胸肌注射0.2ml浓度为3.5×109cfu/ml的大肠杆菌O78株,成功造成了鸡大肠杆菌病模型,发病率100%,致死率78.8%,发病鸡具有较稳定的鸡大肠杆菌病临床症状和病理剖检特征,并从病死鸡脏器分离到鸡致病性大肠杆菌。
4.2 攻毒前3d,按每1kg体重0.2g莲黄颗粒的剂量,灌胃给药,对人工感染鸡致病性大肠杆菌具有明显的保护作用,其保护率达87.5%,表明该浓度的莲黄颗粒可用于鸡大肠杆菌病的预防。
4.3 按每1kg体重0.1g、0.2g、0.3g莲黄颗粒的剂量,灌胃给药,对人工感染鸡大肠杆菌病有较好的治疗作用,各组治愈率分别为73.75%、88.75%和91.25%,中、高剂量组的疗效与氟苯尼考(92.50%)治疗效果相当。
4.4 推荐莲黄颗粒用于预防和治疗鸡大肠杆菌病的剂量为每1kg体重0.2~0.3g,内服给药,每日1次,连用5d。
