炎症性肠病与慢性肝脏疾病的关系及其管理策略
2020-07-21王江滨
王江滨
吉林大学白求恩第三医院/中日联谊医院 消化内科,长春 130033
近年来,由于炎症性肠病(inflammatory bowel disease,IBD)发生率的增加,其已成为国内外消化系统疾病中的常见病,而且也在国内外消化病领域内引起广泛重视。相关研究以及治疗药物的发展不仅大大推动了人们对IBD更深入认识,而且也推动了临床诊断治疗的进步。由于本病临床特征的复杂性,以及对药物治疗应答的个体化差异,所以如何科学管理IBD患者已经成为国内外普遍关注的问题。
IBD合并慢性肝脏疾病的现象在临床上并不少见,其病因受多方面因素影响:(1)IBD与自身免疫性肝病具有共同发病机制,包括原发性硬化性胆管炎(PSC)、原发性胆汁性胆管炎(PBC)、自身免疫性肝炎(AIH)在内的自身免疫性肝病在发病机制上与IBD有重叠的共同因素,尤其是PSC,其合并IBD的几率在80%以上。IBD患者合并PSC的几率为1.4%~7.5%[1];(2)IBD合并病毒性肝炎以及免疫抑制剂治疗诱导的肝炎病毒再激活。国内外的调查数据[2-4]普遍显示IBD合并病毒性肝炎的几率与当地一般人群病毒性肝炎的发生率一致,但是也有IBD患者HBV/HCV感染率高于本地一般人群感染率的报道[5]。当IBD患者接受免疫抑制剂治疗,而预先又忽略了对慢性HBV感染的筛查时,则存在慢性HBV感染加重或再激活的发生风险。应用免疫抑制剂之前忽略了对慢性HCV感染的筛查,尤其是对隐匿性慢性丙型肝炎的筛查,也同样存在HCV再激活的发生风险。(3)IBD合并药物性肝损伤。IBD患者一旦被确诊后常常需要长期药物维持治疗,而且在病情反复的发作过程中,免不了要应用多种药物。抗生素、激素类药物、免疫抑制剂均在我国《药物性肝损伤诊治指南》[6]中被列在诱导药物性肝损伤常见药物前7位序列之中。如果患者应用了传统中药,而又未得到严密观察时,其诱导肝损伤的几率被列在第1位。(4)IBD合并非酒精性脂肪性肝病(NAFLD)。尽管IBD由于腹泻、吸收障碍等原因常有消瘦等现象,但是近年来很多研究均表明IBD患者合并脂肪肝的几率明显高于当地一般人群[7]。IBD的炎症活动度,病程,肠道手术病史,激素、免疫抑制剂、抗生素应用史可能都与IBD合并脂肪肝的发生密切相关[8]。
1 IBD与自身免疫性肝病
1.1 IBD与PSC 在自身免疫性肝病中,PSC与IBD的关系最为密切。80%以上的PSC患者可合并IBD[9],其中以溃疡性结肠炎(ulcerative colitis,UC)最为常见,少数PSC也可合并克罗恩病(Crohn’s disease, CD)。鉴于IBD患者合并PSC的几率是1.4%~7.5%[1],因此对中年发病的男性IBD患者,当存在血清生化异常时,一定要高度警惕合并PSC的可能。
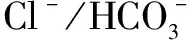
大多数PSC患者是因难治性UC伴ALP和GGT升高而被诊断。肠道表现以全结肠或右半结肠为主,不累及直肠,炎症反应通常轻微,但癌变的概率高。IBD的诊断常早于PSC 6~7年。少数PSC患者也可合并CD。除IBD外,PSC还常合并胰腺炎、糖尿病、自身免疫性甲状腺炎等。PSC有3个变异类型,即:小胆管PSC、PSC/AIH重叠综合征、IgG4相关性胆管炎[11]。小胆管PSC更易合并IBD,PSC/AIH也可合并IBD,但发生率低,而IgG4相关性胆管炎一般不合并IBD。50%以上PSC患者可检测到抗核抗体、平滑肌抗体、核周型抗中性粒细胞胞质抗体等抗体[13],但抗体水平低并无特殊诊断价值。核周型抗中性粒细胞胞质抗体更常见于PSC合并UC患者。
近年来认为之前报道PSC合并IBD几率高达80%的数据被低估了。与单纯IBD相比,PSC合并IBD患者结肠癌的发生率增加4~5倍。因此,对已经诊断PSC的患者,无论是否有IBD的临床表现,均应进行内镜筛查。对已合并IBD患者,每年都要进行内镜或结合染色内镜进行筛查。对不合并IBD者,至少每3~5年复查1次内镜。
对确诊PSC的患者可应用常规剂量的熊去氧胆酸(UDCA),不推荐应用高剂量UDCA。PSC合并IBD时可以联合应用糖皮质激素, 疗效仍不理想时也可试用抗-TNFα。近年来已经有多项临床研究[14]报道了抗-TNFα对PSC合并IBD患者的临床疗效, 虽然结果不完全一致,但总体上可明显改善PSC的临床表现。目前认为抗-TNFα改善PSC的作用是直接机制,而对所合并IBD的治疗作用是间接机制。新近还有关于整合素α4β7、黏附蛋白-1以及赖氨酸氧化酶-2位点的治疗研究[12],初步研究结果显示其既对PSC有效,也对合并的IBD有效,相关机制尚需进一步探讨。
1.2 IBD与PBC PBC与IBD共存的现象较其他肝病与IBD共存时相对比较容易诊断,因为90%~95% PBC患者血清抗线粒体抗体(AMA)阳性。一旦M2型AMA阳性并存在胆汁淤积的临床和实验室表现时则可诊断为PBC。与单纯PBC易发生于女性的现象不同,合并IBD的PBC更易出现于男性,通常更年轻[15]。PBC在IBD患者中的发生率高于普通人群,虽然PBC合并UC和CD的概率大致相仿,但还是UC略常见。UC的病变多半不重,也很少是全结肠型。一般PBC的诊断是在IBD之后,也有同时被诊断的病例,但很少有先诊断PBC再发现其合并IBD的报道。当IBD患者合并有乏力、皮肤瘙痒以及ALP、GGT上升时一定要进行AMA自身抗体的检测。
IBD合并PBC的病因可能是由分子模拟机制所诱导。具有抗原表位的肠道微生物与诱导PBC的某种抗原具有分子结构上的相似性,在诱导IBD同时诱导了PBC。有研究[16]表明IBD继发肠道细菌感染是诱导PBC的重要原因。另外,PBC的某些主要组织相容性复合体易感基因与IBD重叠,其是PBC合并IBD的主要遗传易感机制。一旦确诊为IBD与PBC并存,应立即应用UDCA进行治疗,UDCA不仅是被国际公认对PBC最有效的药物,而且也有助于合并IBD的恢复和预防IBD的复发。
有临床研究[17]对151例PBC患者中6例合并IBD的患者进行长达10年的随访,结果表明3例合并UC、3例合并CD,6例患者均有AMA阳性和胆汁淤积的表现,对UDCA治疗均表现出完全应答的临床疗效。
1.3 IBD与AIH AIH/PSC重叠综合征合并IBD的报道多于单纯AIH患者,为数不多的病例主要见于UC。AIH/PSC重叠综合征是否合并UC与疾病严重程度并不相关,而且2种疾病的活动度也没有关联。类固醇激素、UDCA、6-巯基嘌呤(6-MP)联合治疗的应答率好[18]。
一项关于单纯AIH合并IBD的报道[19]显示,在98例AIH患者中,39例(39.8%)合并肠道炎症,其中10例(10.2%)合并UC,3例(3.1%)合并CD,4例合并非特异性结肠炎(4.1%)。
2 IBD与病毒性肝炎
2.1 IBD与病毒性肝炎 国内外有多项研究先后调查了IBD患者的HBV/HCV感染率问题。虽然各项研究所示IBD合并HBV/HCV的感染率不同,但多数研究表明两者同时存在的情况与本地HBV/HCV感染率相近。我国是HBV慢性感染率较高的国家,2006年全国HBV感染率调查[20]显示在1~19岁人群中HBsAg携带率为7.18%。近年来政府先后通过加强乙型肝炎疫苗的免费接种,加强对血源、输血以及医源性传播的管理,HBV的人群感染率已明显下降,但是2004年的调查数据[21]显示在15~29岁人群中,HBsAg的阳性率仍达4.38%。一项来自上海对714例IBD患者的调查[22]表明,HBsAg阳性率为5.46%,与当地一般人群相比无显著性差异,其中UC和CD分别为5.68%和5.29%。北京多达1259例IBD患者的调查[4]表明,HBsAg的阳性率为4.29%,与我国一般人群的感染率也相接近,但是其调查数据表明CD患者的HBsAg阳性率略高于UC患者。广州的一项调查[23]表明,CD、UC患者HBsAg的阳性率分别为13.6%、16.8%,与一般人群13.8%感染率无明显差异,CD和UC的差异也不具有统计学意义。来自韩国关于513例IBD患者的调查[24]也得到相类似的结果。然而关于IBD患者慢性HBV/HCV感染率是否与当地一致的问题,也有来自国际上不同的调查意见。巴西的一项调查[25]表明IBD患者HBcAb、HBsAg阳性率明显高于本地普通人群;法国的一项研究[26]表明,本地域HCV感染率仅为0.86%,而IBD患者血清HCV抗体阳性率高达5.98%。另一项来自意大利的研究[27]同时检测了HCV RNA及HCV抗体,结果表明,CD患者HCV感染率明显高于当地普通人群,且CD患者的HCV慢性感染率高于UC患者。
2.2 免疫抑制剂治疗过程中的肝炎病毒再激活 近年来抗病毒治疗的进步已经改变了慢性乙型肝炎和慢性丙型肝炎的预后,而且抗病毒治疗慢性HCV感染完全可以达到病毒不再复发的目的。但是由于病毒生物学活性的不同,当合并HBV感染,甚至是在病毒已经被控制的情况下,若应用免疫抑制剂时,则存在HBV再激活的发生风险。一旦发生HBV再激活,疾病进展的风险明显增加,甚至死亡或不得不接受肝移植。无论自发性病毒清除,还是正在接受抗病毒治疗,只要接受免疫抑制剂治疗,HBV再激活的发生风险相同。
免疫抑制剂治疗中HBV再激活的定义:(1)HBV DNA阴性患者再现HBV DNA;(2)HBV DNA较基线水平增加10倍及以上;(3)HBV DNA水平上升至>109拷贝/ml。应用1个免疫抑制剂时HBV再激活的风险为20%,应用1个以上免疫抑制剂时HBV再激活的发生风险是80%。判断是否发生了HBV的再激活需要进行动态观察,免疫抑制剂应用状态下ALT的升高常明显晚于HBV DNA的升高,有时不易被早期发现[28]。
HBsAg阳性/HBcAb阳性患者当接受中等剂量(10~20 mg/d强的松或等量类固醇激素)或高剂量(>20 mg/d强的松或等量类固醇激素)类固醇激素,疗程≥4周时,HBV再激活的风险>10%。美国胃肠病学会(AGA)共识意见[29]推荐在应用类固醇激素前要进行预防性抗病毒治疗,至少维持至免疫抑制剂治疗结束后6个月。HBsAg阳性/HBcAb阳性、HBsAg阴性/HBcAb阳性者,当接受TNFα抑制剂(英夫利昔单抗、阿达木单抗、赛妥珠单抗等)治疗时,HBV再激活的风险为1%~10%。HBsAg阳性/HBcAb阳性者使用≥4周低剂量类固醇激素(<10 mg/d强的松或等量类固醇激素),HBsAg阴性/HBcAb阳性者使用≥4周中、高剂量类固醇激素时,HBV再激活的风险也为1%~10%。AGA共识意见对HBV再激活风险在1%~10%的患者,也推荐抗病毒治疗至免疫抑制剂结束后6个月,以预防HBV再激活,但AGA共识意见同时也强调应综合抗病毒获益及耐药发生可能决定是否选择预防性抗病毒治疗,尤其是对HBsAg阴性的患者。对于HBV再激活风险<1%的患者,目前AGA共识意见不推荐常规预防性抗病毒治疗,其见于下述情况:HBsAg阳性/HBcAb阳性、HBsAg阴性/HBcAb阳性使用传统免疫抑制剂如硫唑嘌呤(AZA)、6-MP、甲氨蝶呤或口服≤1周任何剂量类固醇激素,或HBsAg阴性/HBcAb阳性者使用≥4周低剂量类固醇激素(<10 mg/d强的松或等量类固醇激素)。
3 IBD合并药物性肝损伤
目前在全球范围内报道具有潜在肝毒性的药物达1100多种,而IBD患者常用的抗感染药、激素类药物、免疫抑制剂等均被我国列在可诱导肝损伤药物中的前7位。如果同时使用中草药,而且并未被严格观察,其导致药物性肝损伤的几率更大。药物代谢异常、药物介导的免疫反应、遗传因素、药物介导胆汁酸转运系统的损伤都是药物性肝损伤的主要发病机制。在诱导药物性肝损伤的常见药物中抗感染药被列在第2位,激素类药物被列在第4位[6]。
虽然临床普遍应用的美沙拉嗪较过去常用含有磺胺成分的柳氮磺胺吡啶安全,但也有其诱导药物性肝损伤的报道,所以在最初用药的5~90 d尚需进行严密观察。如果仍然选用传统柳氮磺胺吡啶,应更加警惕肝损伤。嘌呤类药物包括AZA和6-MP,均是诱导药物性肝损伤的常见药物,其诱导IBD患者发生肝损伤的几率约为3%,但也有前瞻性研究[30]结果显示其诱导肝损伤的概率可高达10%。既可诱导慢性,也可诱导急性肝损伤。AZA和6-MP的血药浓度不影响其对IBD的临床疗效,但是与其诱导的药物不良反应密切相关。除骨髓抑制外也包括对肝脏的毒性。AZA和6-MP在硫嘌呤甲基转移酶(thiopurine methyltransferase,TPMT)的作用下生成有效代谢产物6-巯基嘌呤核苷酸。AGA共识推荐当IBD患者应用嘌呤类药物时,可对TPMT基因型进行分析,存在基因突变时,其嘌呤类药物血药浓度升高,不仅骨髓抑制的发生率高,肝损伤的发生率也可能会增加。TPMT在我国汉人中的变异率并不高,因此,我国专家共识意见[31]并不推荐常规检测。突变型TPMT检出率在日本人群中也不高,但在野生型TPMT日本IBD患者中AZA诱导的肝损伤发生率并不低[31]。应用AZA导致肝损伤后可改用6-MP治疗,改用6-MP后很少发生进一步的肝损伤。AZA是6-MP和咪唑类药物的复合衍生物, AZA导致的肝损伤应该是其中咪唑类药物的作用。另外,AZA是在谷胱甘肽转移酶的作用下才能生成6-MP,当机体相对缺乏该酶活性时则易发生药物性肝损伤。虽然我国专家共识意见[31]将甲氨蝶呤列在治疗IBD所推荐药物之中,但在国际范围都很少应用甲氨蝶呤治疗IBD。虽然甲氨蝶呤诱导药物性肝损伤的发生概率并不低,但病情多半比较轻微,停药后可自行恢复。
TNFα拮抗剂英夫利昔单抗、阿达木单抗、赛妥珠单抗近年来已被广泛应用于临床治疗IBD患者,其不仅疗效好,而且也比较安全,但有关英夫利昔诱导肝损伤的报道并不少见。英夫利昔诱导的肝损伤在临床上常不易被确定诊断,因为活动性IBD患者本身就容易并发肠外自身免疫现象,包括肝功能的异常。另外IBD合并PSC、NAFLD的几率也相对较高,同时应用的其他药物也都有诱导药物性肝损伤的可能。
近来澳大利亚研究组[32]报道了一项关于175例接受英夫利昔治疗IBD患者合并肝损伤的调查结果。其中CD 149例,UC 29例,在英夫利昔用药后发生肝损伤者57例,但其中RUCAM评分<3分(可能)者只有11例,3~8分(很可能)者10例,>8分(确定)者仅1例。患者很少伴有发热和皮疹,多见于男性,预先存在NAFLD者更易出现药物性肝损伤。之前也有关于IBD患者应用英夫利昔诱导肝损伤的报道[33],研究结果也表明其发生率并不高,临床表现类似于自身免疫性肝炎,部分患者伴有发热和皮疹。肝损伤通常发生在应用英夫利昔14~18周后[32]。
4 IBD合并NAFLD
IBD患者常因腹泻、营养吸收障碍以及全身炎症反应等,表现为体质下降,甚至严重消瘦,按传统认识一般不会关注IBD患者的脂肪肝问题, 但是近年来已有多项研究[6]表明与本地一般人群相比,IBD患者脂肪肝的发生率不但不低,反而升高。近期脂肪肝的诊断方法多是超声影像结合血清生化学检查,之前也有结合活组织检查的研究,更早期研究(1952年-1970年)还有根据人体解剖学结果的报道。Gizard 等[34]团队文章采用超声影像结合血清生化学检查的方法确诊脂肪肝,研究共纳入13项涉及1471例UC患者的研究,结果表明,UC患者脂肪肝的发生率平均为23%(1.5%~55%)。其中一项来自意大利的研究[35]以超声影像作为诊断方法,在317例UC患者中合并脂肪肝的发生率为13.6%,高于当地一般人群7.3%的发生率。Gizard 团队的研究中还纳入了4项涉及604例CD患者的研究,结果表明,脂肪肝的合并率为1.5%~39.5%,其中涉及311例CD患者的最大规模研究[36]表明其合并脂肪肝的发生率是39.5%,高于当地普通人群20%的发生率。IBD患者合并脂肪肝的病因比较多,多因素分析[37]表明肠道炎症病变的活动度、病程、是否行小肠手术、类固醇激素用药史都与NAFLD的发生密切相关。虽然到目前为止,多数研究表明IBD患者合并脂肪肝的发生率高,但也有来自美国的调查[37]表明IBD合并脂肪肝的几率是8.2%,低于美国普通人群33.6%的报道。由此可见,并不能单纯通过与当地人群脂肪肝发生率进行对比的数据而做出简单结论。存在腹泻、吸收障碍、食欲减退、消瘦等因素情况下IBD合并NAFLD的机制尚需进一步探讨。
有研究组[38]通过肝脏瞬时弹性成像技术对380例IBD患者进行分析,结果有33%的患者合并脂肪肝,12.2%的患者合并不同程度的肝纤维化。患者血清中TNFα蛋白水平和mRNA水平均升高,提示抗TNFα的应用不仅能治疗IBD,也有助于治疗IBD合并的脂肪性肝病[39]。
除上述PSC、病毒性肝炎、药物性肝损伤和NAFLD外,IBD患者还可合并肝淀粉样变性、门静脉血栓,并发肝脓肿的几率也高于一般人群[34]。
5 小结
综上所述,由于IBD的复杂病因和需要进行长期管理的特点,必须警惕其可能同时存在或在IBD病因和用药基础上并发的肝脏问题,以真正实现对IBD患者的科学管理。
