白藜芦醇清除DPPH自由基反应的动力学
2020-07-18周巾英欧阳玲花王丽祝水兰潘润天冯健雄
周巾英,欧阳玲花,王丽,祝水兰,潘润天,冯健雄*
江西省农业科学院农产品加工研究所(南昌 330200)
自由基造成了一些疾病如动脉粥样化、神经变性、慢性抑郁症、癌症和生理学衰老等[1-2]而引起人们的关注。研究发现抗氧化剂具有清除自由基能力,具有抗病、抗菌、抗逆及延缓衰老等作用[3],已被广泛用于食品工业中。抗氧化剂分为合成抗氧化剂和天然抗氧化剂,合成抗氧化剂因对人体健康存在一定的危害,许多国家已禁用有些合成抗氧化剂[4]。天然抗氧化剂在自然界广泛存在,种类繁多,有很大的潜力取代合成抗氧化剂,也是今后食品工业的发展趋势。因此,从天然植物中寻找高效、安全的天然抗氧化剂,及研究各种天然抗氧化成分的作用机理,都是值得深入研究的课题。
白藜芦醇(Resveratrol,Res)是一种生物活性很强的天然多酚类化合物,具有抗衰老[5]、降低血小板聚集[6]、预防和治疗心血脑管疾病[7]、抗菌[8]、抗致癌作用[9],广泛存在于葡萄、花生、虎杖等植物中[10]。大量研究报道是致力于从葡萄、虎杖、花生等植物中提取白藜芦醇的工艺[5]、白藜芦醇定量测定方法建立[11-12]以及体外抗氧化活性研究[7],但是花生红衣中白藜芦醇的体外抗氧化活性及反应动力学尚未见报道。此次试验在超声波辅助提取花生红衣中白藜芦醇[12]的基础上,采用体外抗氧化活性评价方法测定白藜芦醇的抗氧化活性,及DPPH自由基消除法研究白藜芦醇与自由基的反应动力学,以期为白藜芦醇在食品等领域的应用提供科学指导。
1 材料与方法
1.1 材料
二苯基苦味酰基苯肼(1, 1-Diphenyl-2-picryhydrazyl,DPPH)、白藜芦醇(Resveratrol,Res,98%)、2, 6-二叔丁基-4-甲基苯酚(Butylated hydroxytoluene,BHT),购于百灵威公司;无水乙醇、磷酸、高硫酸钾、磷酸钠、钼酸铵、硫酸、铁氰化钾、三氯乙酸等均为分析纯,购于陇西化工股份有限公司。
1.2 主要仪器和设备
TP-214型电子天平(北京赛多利斯仪器系统有限公司);B-260型恒温水浴锅(上海亚荣生化仪器厂);电热恒温干燥箱(上海精宏实验设备有限公司);UV-3100PC紫外-可见分光光度计(上海美普达有限公司);LXJ-IIB型离心机(上海安亭科学仪器厂)。
1.3 方法
1.3.1 DPPH·清除率的测定
DPPH·清除试验根据Hatano等[13]提出的方法制定。在样品管中加入一定量的样品和DPPH·溶液,摇匀并在30 ℃放置30 min。在515 nm处测定不同浓度样品与DPPH·反应后的吸光度、样品在无水乙醇溶剂中的吸光度、DPPH·在无水乙醇溶剂中的吸光度,以无水乙醇溶剂为空白样品,BHT为参照物,每次处理重复3次。

式中:D空白为DPPH·与溶剂混合液的吸光度;D样品表示DPPH·与样品反应后的吸光度;D对照为样品与溶剂混合的吸光度。
1.3.2 总抗氧化能力的测定[14]
分别取1.0 mL不同样品溶液加入10 mL离心管中,再加入3.0 mL磷钼试剂溶液(磷钼试剂溶液中包括0.6 mol/L硫酸、28 mmol/L磷酸钠和4 mmol/L钼酸铵),混合均匀,混合液在95 ℃水浴锅中分别水浴30,60,90,120,150和180 min,放置冷至室温,在695 nm处检测样品的吸光度,以蒸馏水为空白,BHT为对照,将试验重复3次,求平均值。
1.3.3 还原性能力的测定[15]
在10 mL离心管中分别加入2.5 mL 0.2 mol/L pH 6.6的磷酸缓冲液和1 mL不同浓度的样品液,加入2.5 mL 1%铁氰化钾,混合均匀后放置50 ℃反应20 min,取出冷却至室温后,加入2.5 mL 10%三氯乙酸,以4 000 r/min离心10 min,取2.5 mL上清液,加入2.5 mL蒸馏水和0.5 mL FeCl3,混匀后静置10 min,在700 nm处检测样品的吸光度,BHT作为对照。
1.3.4 DPPH·标准曲线的建立
精确称取9.06 mg DPPH标准品,用无水乙醇在烧杯中溶解后转移到100 mL的容量瓶中,再用无水乙醇定容至100 mL,配制成质量浓度为90.6 μg/mL的标准溶液,置于4 ℃冰箱中保存备用。分别取0,2,4,6,8和10 mL标准溶液至10 mL容量瓶中,并用无水乙醇定容,在517 nm处测定其吸光度,以浓度C为横坐标,吸光度D为纵坐标,绘制标准曲线,得到回归方程D=0.010 13C-0.017 81,R2=0.998。
1.3.5 DPPH·法[16]
在DPPH·溶液(浓度为60 μmol/L)中加入不同体积的白藜芦醇溶液(浓度为0.01 mol/L),在517 nm处测定DPPH·吸光度随时间的变化情况,直到DPPH·的吸光度达到稳定。溶液中DPPH·的剩余率可由式(2)计算得出:

式中:Df为稳定态时DPPH·的吸光度;D0为初始时DPPH·的吸光度。
2 结果与分析
2.1 白藜芦醇体外抗氧化活性研究
2.1.1 DPPH·清除率
DPPH·是一种以氮为中心的稳定自由基,其乙醇溶液为紫红色,在波长515 nm处有最大吸光度。此方法是基于抗氧化剂给自由基提供氢原子或电子引起紫红色消褪来检测样品的抗氧化活性大小。自由基分为羟基自由基、烷基自由基和过氧自由基。若提取物能够降低DPPH·的最大吸光度,则表示它含有降低羟基自由基、烷基自由基和过氧自由基有效浓度的能力,可以有效防止脂质过氧化反应,从而抑制氧化过程。抗氧化剂清除DPPH·的清除率越高,其抗氧化能力越强。图1表明白藜芦醇和BHT对DPPH·都有较高的清除能力,清除率与抗氧化剂的含量呈正相关性,随着抗氧化剂含量的增加,其对DPPH·的清除力也逐渐增强。白藜芦醇对DPPH·的清除率明显高于BHT对DPPH·的清除率。

图1 不同样品清除DPPH·的量效关系图
2.1.2 总抗氧化能力
磷钼络合物法通常用于一些酚类、VE和类胡萝卜素等抗氧化物的抗氧化活性测定,其原理是抗氧化物质中的氢或电子转移到Mo(Ⅵ),将其还原生成绿色的Mo(Ⅴ)络合物,最大吸收波长为695 nm,吸光度越大,表示抗氧化剂的活性越强。图2表明随着反应时间增加,白藜芦醇和BHT溶液的吸光度增大,即抗氧化剂的抗氧化活性也逐渐增强。白藜芦醇和BHT具有较高的抗氧化活性,但白藜芦醇的抗氧化活性高于BHT。
2.1.3 还原性能力
还原能力的测定是为了检验样品是否是一个良好的电子供给体,还原能力强说明样品是个良好的电子供给体,供给电子除把Fe3+还原成Fe2+外,还可与自由基反应,生成稳定的物质。一般情况下,样品的还原能力与其抗氧化活性存在一定的相关性,样品还原能力的高低可间接反映其抗氧化能力的强弱。白藜芦醇和BHT的还原能力如图3所示。在所检测的浓度范围内,随着加入抗氧化剂浓度的增加,溶液吸光度也逐渐升高,则表明样品的还原能力逐渐增强。当检测样品质量浓度为0.1 mg/mL时,白藜芦醇和BHT在700 nm处对应的吸光度分别为0.884和0.788,表明在相同浓度下白藜芦醇的还原能力强于BHT的还原能力,这一结果与2.1.2的试验结果相一致。

图2 不同样品的总抗氧化能力
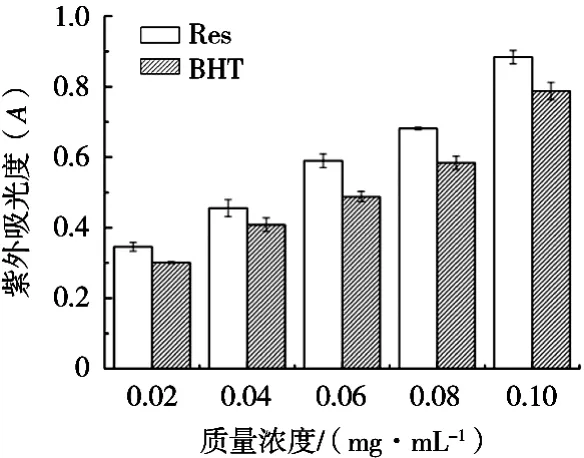
图3 不同样品还原能力的量效关系图
2.2 白藜芦醇与DPPH自由基的反应动力学研究
2.2.1 反应时间影响
不同浓度的白藜芦醇对DPPH的消除反应如图4所示。随着反应时间的延长,溶液中DPPH·的吸光度逐渐减弱,即白藜芦醇对DPPH·的消除率逐渐增大,当反应超过6 h后体系趋于平衡,即体系中DPPH·的浓度基本保持不变,此反应被称为一个慢反应[16]。
2.2.2 白藜芦醇浓度影响
图5显示白藜芦醇浓度对DPPH·清除能力的影响,反应时间固定30 min。由图4和图5可知,白藜芦醇抗氧化剂对DPPH·的消除能力随自身浓度的增加而升高。当白藜芦醇浓度较低时,其对DPPH·的消除率增幅较大;随白藜芦醇浓度的继续增加,其对DPPH·的消除率增幅相对变小。这是由于反应初始,体系中DPPH·的浓度较大,反应向正方向反应移动,随着体系中DPPH·的浓度降低,反应向正反应进行的速度减慢,即白藜芦醇抗氧化剂对DPPH·的消除率增幅变小[16]。由图4和图5曲线拟合计算得到白藜芦醇的半消除率浓度EC50为0.047±0.004 μmol antioxidant/μmol DPPH·,反应化学计量数为0.094±0.07,抗自由基能力(Antiradical power,ARP)为21.28±0.27。

图4 DPPH·加入不同浓度的白藜芦醇后随时间变化情况

图5 反应时间为30 min,白藜芦醇浓度对清除DPPH·能力的影响
2.2.3 反应级数及反应速率常数
白藜芦醇与DPPH·的消除反应可由式(3)表示:

反应速度方程应遵守:

式中:k为反应速度常数;c为反应物浓度,μmol/L。
由式(3)可得出:

当[AH]≫[DPPH·]时,反应可假设为一级反应,则:
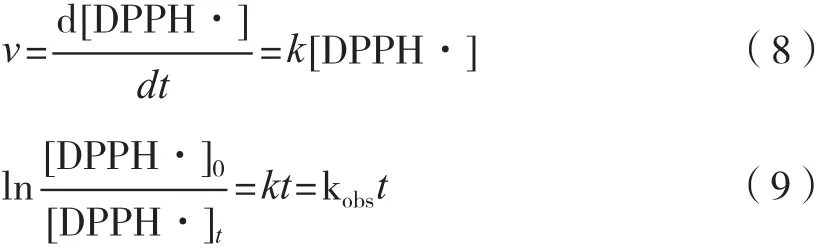
式中:[DPPH·]0为DPPH·的初始浓度,μmol/L;[DPPH·]t为反应时间t时的DPPH·浓度,μmol/L;kobs为一级反应速率常数;t表示反应时间,h。
以ln[DPPH·]0/[DPPH·]t对t作图,如图6所示。可知,ln[DPPH·]0/[DPPH·]t与t基本呈线性关系,得出反应速率常数kobs为5.85×10-3±0.04 μmol/L-1·s-1,R2为0.994,因此该反应符合一级反应动力学模式。

图6 白藜芦醇对清除DPPH·反应的ln[DPPH·]0/[DPPH·]t-t图
2.3 白藜芦醇清除DPPH·反应机理推测

图7 白藜芦醇与DPPH·反应机理推测
白藜芦醇属于酚类化合物,其抗氧化机理分为两类,即抽氢反应机理和单电子质子转移机理。抽氢反应机理是先将抗氧化剂与自由基反应,通过OH键上的H转移到自由基上,抗氧化剂清除自由基的能力取决于羟基提供氢的能力,这主要与羟基的羟基键解离能、反应的活化能和反应标准摩尔反应热数据有关[17]。单电子质子转移机理是在溶剂体系中,溶剂分子尤其是极性溶剂分子与抗氧化剂分子之间形成分子间氢键,阻碍了抽氢反应发生,故反应转向电子转移反应[18],但DPPH·与酚类化合物主要是通过抽氢反应机理来进行反应的。裴玲等[19]、徐顺等[20]、曹曼等[21]都通过理论计算得出白藜芦醇中4'位羟基的活性高于3, 5位羟基的活性。结合试验和理论研究结果,对白藜芦醇与DPPH·反应进行了以下推测,分为三个步骤(图7):首先,白藜芦醇上的一个酚羟基失去一个质子,DPPH·接受这个质子形成DPPH-H,此反应为速率决定反应(反应a);然后失去一个质子的白藜芦醇结构重排,即烯键上的碳失去质子,再跟一个DPPH·分子发生反应,即反应b;最后发生结构重排的白藜芦醇分子相互反应形成一个多酚化合物,这个反应可能由于空间位阻较大,反应很慢甚至不会发生反应。此推论还需其他更多的检测结果来支持这个结论;另外,失去一个质子的白藜芦醇发生结构重排生成一个单醌结构的化合物。
3 结论
综合分析各项试验结果得出花生红衣中白藜芦醇的抗氧化活性强于BHT,白藜芦醇和DPPH自由基的消除反应是一级反应。从试验与机理角度探讨了白藜芦醇与DPPH自由基的消除反应机理,推测4'位羟基的活性大于其他位的羟基,更容易与自由基发生反应,但其仍是个相对复杂的过程。今后将更深入地研究白藜芦醇与DPPH自由基的作用机制,从而更清楚地阐明其工作机制,为改造和开发富含白藜芦醇的产品开发应用提供更有利的理论基础。
