靶向PGRMC1基因sh RNA真核表达载体的构建和鉴定
2020-07-16程艳余晓红
程艳 余晓红
郑州大学第一附属医院妇科 郑州 450052
靶向基因治疗是使正常基因通过分子生物工程或治疗在肿瘤细胞中借Yinte远程作用的手段,抑制致瘤基因或修复有缺陷的基因,使肿瘤细胞的生长受到抑制,而不影响正常细胞。国内外研究表明,孕酮受体膜成分(PGRMC1)和恶性肿瘤关系密切,在卵巢癌、乳腺癌、结肠癌、肺癌、子宫颈癌和其他恶性肿瘤中呈高表达,但确切的作用机制尚不清楚[1-3]。我们通过构建靶向PGRMC1基因shRNA 真核表达载体,以期抑制PGRMC1基因表达而使PGRMC1基因表达下调,为PGRMC1开展卵巢癌基因治疗奠定基础和提供实验工具。
1 材料与方法
1.1材料与试剂人卵巢癌细胞株SKOV3细胞系购自上海研究所。RPMI1640培养基,新生小牛血清,逆转录(RT)-PCR试剂盒购自美国Gibco公司。限制性内切酶, DNA连接酶购自上海生工有限公司。脂质体Lipofectamine2000 , TRIzol试剂的产品,空载体pcDNA3.1A购自美国Introvigen公司 。四氮唑蓝(MTT),氨基糖苷类抗生素G418购自Sigma公司。
1.2PGRMC1基因的设计和合成从GenBank获取PGRMC1 mRNA 的完整序列。根据Tuschl设计原则[4],设计3条shRNA (short hairp in RNA),特异性干扰PGRMC1基因3段不同序列。设计另1条shRNA 干扰选中的shRNA 中的碱基序列作为阴性对照,经BLAST检索确定且与PGRMC1 mRNA 及其他基因编码序列无同源性。按照该试剂盒的使用说明,用TRIzoL 试剂提取RNA。其中1μg总RNA 在SuperScrip tTM Ⅱ逆转录酶的作用下反转录产生cDNA。PCR 引物用于扩增靶向和对照序列产物(引物序列PGRMC1正义链5'-GCTCTGGCTTTGCATTTGATGCA-3 ' ,反义链5'- AGGAGCAGAAGTTTGAAC -3')。转染48 h后,收集细胞,漂洗2次,用冷PBS后,将细胞裂解,提取总蛋白。该产品12%的SDS-PAGE ,以蛋白质电泳转移仪将产物转至硝酸纤维素膜上,加入孕酮受体膜成分的抗体(1∶ 1000~1200),4℃反应过夜,PBST洗膜,和1∶ 4000山羊抗兔IgG / HRP室温下搅拌12 h,用化学发光试剂反应5 min,用发光成像仪成像。

2 结果
2.1PCR扩增PGRMC1基因的开放阅读框结果RT-PCR扩增的PGRMC1产物经琼脂糖凝胶电泳分析, 发现所扩增的条带特异性强, 大小为2000 bp, 与预期的大小一致。见图1。
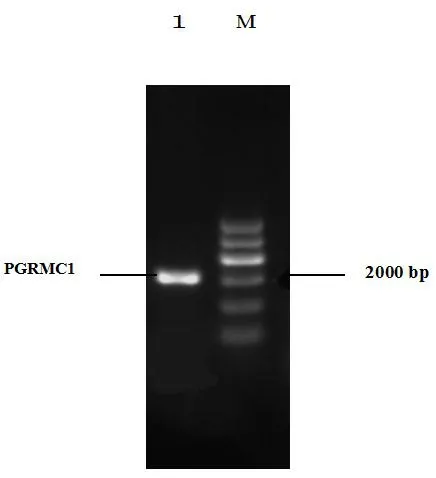
1. PGRMC1 PCR 产物 M: DNA Marker
图1 PGRMC1基因的PCR扩增结果
2.2组件的构建和鉴定重组质粒pcDNA3.1 (-)/PGRMC1 PRGMC1测序克隆pcDNA3.1 (-)/PGRMC1的表达载体,所述重组质粒pcDNA3.1 (-)/PGRMC1。PCR实验阳性的菌落提取质粒DNA,用限制性酶MsqI酶切位点的酶和Smo I双重消化,结果显示,PGRMC1成功地建立到pcDNA3.1 (-)的真核表达载体中。
2.3筛选的细胞系和鉴定稳定转染将pcDNA3.1 (-)/孕酮受体膜成分质粒转染卵巢癌细胞系SKOV3,培养4周后,将孕酮受体膜成分阳性细胞稳定表达株。通过RT-PCR和转染的pcDNA3.1的Western印迹分析(-)/孕酮受体膜成分SKOV3细胞与SKOV3细胞转染空载体相比,表达的两个内部基准电平基本上是相同的;而前者孕酮受体膜成分-基因表达水平显著增加,表明重组质粒已经成功传递到表达(图3,图4)和SKOV3细胞系。

1: 未酶切的pcDNA3.1(-)/PGRMC1
Undigestion of pcDNA3.1(-)/PGRMC1
2: MspI 和SmoI双酶切后的pcDNA3.1(-)/PGRMC1
MspI and SmoI digestion of pcDNA3.1(-)/PGRMC1
3: PGRMC1 PCR 产物product M: DNA marker
图2 pcDNA3.1(-)/PGRMC1 双酶切鉴定结果

图3 通过RT-PCR检测在PGRMC1的表达 稳定转染SKOV3细胞系
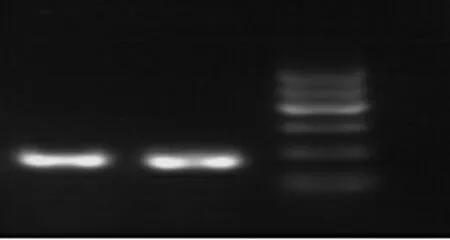
图4 免疫印迹检测稳定转染前,后SKOV3细胞系中的PGRMC1基因表达
3 讨论
PGRMC1是一类小分子蛋白,含有194个氨基酸,包括1个N端跨膜结构域,1个细胞色素b5样或亚铁血红/类固醇结合域。PGRMC1主要分布在后期卵黄的卵巢、肝脏和头肾。研究发现,PGRMC1在乳腺癌、结肠癌、肺癌、宫颈癌等恶性肿瘤组织中呈过度表达,动物实验发现PGRMC1在卵巢中含量比较大[4-5]。且PGRMC1在卵巢癌组织中普遍呈过度表达,可促进卵巢癌细胞的增殖。PGRMC1不仅与孕激素结合,还可以与其他甾体和非甾体类物质结合。有研究发现,PGRMC1可以促进卵巢癌的发生,敲除此基因后,卵巢癌细胞的增殖受到抑制,顺铂的敏感性会增加。提出削弱PGRMC1的作用,有望作为卵巢癌靶向治疗及辅助化疗的一部分[6-8]。
在此研究中,我们成功构建PGRMC1到真核表达载体pcDNA3.1(-)中,通过限制性内切酶鉴定,测序,证实了靶基因的PRGMC1的正确序列,成功地建立了稳定整合在基因组中的DNA染pcDNA3.1(-)/PGRMC1-SKOV3细胞克隆时,细胞克隆的细胞进行培养,用RT-PCR和Western blot检测PRGMC1高表达的稳定转染卵巢癌细胞。
本实验构建的载体经PCR电泳图谱和测序证实了克隆RNAi打靶序列完全正确, 合成的寡核苷酸已成功载入载体。通过构建shRNA真核表达载体,成功地阻抑了PGRMC1基因在人卵巢癌细胞SKOV3中的表达,成功构建的pcDNA3.1(-) / PGRMC1 质粒 SKOV3细胞系为研究PGRMC1调节卵巢癌的分子机制及下游基因奠定了基础,为进一步研究PGRMC1基因在肿瘤细胞发生和恶性进展的作用及探讨卵巢癌基因治疗新方法提供了可能。
