3D打印技术在肾门部肾肿瘤肾部切中的应用研究
2020-07-09张向民褚健曲发军叶剑青干思舜储传敏王磊杨炜潘秀武崔心刚
张向民 褚健 曲发军 叶剑青 干思舜 储传敏 王磊 杨炜 潘秀武 崔心刚
摘要: 目的 总结探讨3D打印技术在肾门部肾肿瘤行腹腔镜肾脏部分切除术中的应用经验。方法 回顾2016年5月至2018年7月,本科收治的10例肾门部肾肿瘤患者,10例患者术前均采用CT三维重建,并应用3D打印机进行肾脏3D模型打印。其中男7例,女3例,年龄43~71岁,平均年龄51岁;肿瘤直径1.6~4.3cm,左侧4例,右侧6例。10例患者均经后腹腔行腹腔镜下肾部分切除术。结果 通过3D打印技术,成功构建10例肾脏肾肿瘤模型,手术均顺利完成,无一例中转开放,术中、术后无明显并发症。手术时间60~110min,热缺血时间15~26min,术中出血量小于50ml。住院时间5~7天,术后病理提示切缘阴性,病理均为透明细胞癌。随访10~34个月,所有患者恢复良好,未见肿瘤复发转移及其他异常表现。结论 肾门部肾肿瘤对于大部分泌尿外科医生是一难题,3D打印技术的引进,把这一难题简易化。通过肾脏3D模型的建立,肾门肿瘤的大小、毗邻、浸润深度及与肾血管、集合系统的关系变得一目了然,也进一步帮助手术医生拟定更为合适的方案,减少术中肾血管和集合系统的损伤概率,更大程度的确保切缘阴性和保留肾功能。3D打印技术在肾门部肾肿瘤中的应用精准、安全、有效、可行,是一项值得泌尿外科医生推广应用的辅助技术。
关键词: 肾门部肾肿瘤;腹腔镜手术;3D打印
【中图分类号】R322.6 【文献标识码】A 【文章编号】2107-2306(2020)02-174-02
我科自2016年5月至2018年7月,运用3D打印技术,我科对收治的10例肾门部肾肿瘤患者进行了肾脏3D模型构建,10例均经腹膜后入路行腹腔镜下肾部分切除术,手术效果良好,现报告如下:
1资料与方法
1.1临床资料
本10例肾脏肿瘤患者,男性7例,女性3例,平均年龄51岁;10例患者均为常规体检发现,其中2例合并高血压病,口服药物血压控制情况良好;术前CT、MRI提示10例肿瘤长径在1.6~4.3cm之间,其中左侧4例,右侧6例,肿瘤均位于肾门部、边界尚清楚,术前检查排除手术禁忌证;术前CT三维重建明确肿瘤均位于肾门处,距离肾盂<1cm,紧贴肾脏动静脉;10例均经腹膜后入路行腹腔镜下肾部分切除术。
1.2 3D模板建立
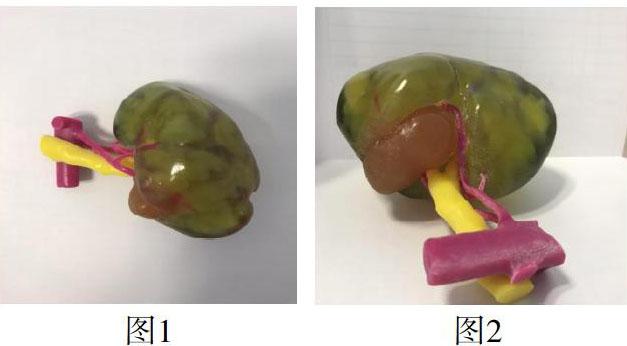
术前行双肾CT三维,包括肾动脉、静脉期影像。将采集的患者CT影像资料采用Philips IntelliSpace Portal V5.0.1软件进行3D重建,然后使用Formlab Forml+3D打印机对肾脏模型进行分色打印。模型选用4种颜色:动脉为粉红色,静脉黄色,肾实质淡绿色半透明,肾门肿瘤以淡褐色/肉色实体表示(图1、2)。3D打印模型能清晰显示肿瘤与集合系统肾门血管的毗邻关系,通过该模型可对肿瘤血供、毗邻关系、切除范围路径进行分析。
1.3手术方法
全身麻醉成功后,常规留置导尿,患者健侧卧位,凸出患侧腰部。在腋后线12肋缘下、腋前线肋弓缘下及腋中线髂嵴上2指位置分别置入3个 Trocar,常规气囊扩张后腹膜间隙, 建立气腹。清除腹膜外脂肪,靠近腰大肌纵行切开肾周筋膜,沿腰大肌表面向肾门分离出肾动、静脉,注意肾动脉分支及变异,充分游离肿瘤周围的肾周脂肪, 完整暴露肾肿瘤及周围部分正常腎组织,将肾动脉游离出一段。在阻断肾血供前,根据术前3D打印模型比对找到肿瘤的大致位置,行肾动脉完全阻断,冷刀沿肿瘤边界剪开肾包膜,并沿剪开的肾包膜边界向下仔细分离,寻找肿瘤假包膜边界,吸引器沿该界面外缘钝性游离肿瘤纵深面,充分游离肿瘤。确认肿瘤假包膜无破损后,离断肿瘤底面。观察肾脏创面情况,免调针缝合法依次进行肾集合系统修复,关闭深层肾组织及破损的肾盂,继续缝合外层肾组织。为减少热缺血时间,在完成第深层缝合后可开放肾血供,观察肾脏表面渗血情况,再次加固缝合外层肾组织(“2+1”缝合法)。腋后线切口取出标本,髂嵴上切口放置负压引流管,逐层关闭切口。标本送病理。
2 结果
10例手术均顺利完成,无中转开放,围手术期无严重并发症。手术时间60~110min,热缺血时间15~26min,术中出血量小于50ml。术后切开肿瘤,见标本内部为实性组织,其内可见少许坏死灶,切面淡黄色,病理均提示为均为透明细胞癌。术后平均住院时间6d,二类切口常规抗炎对症处理。该组随访10~34个月,所有患者恢复良好,未见肿瘤复发转移及其他异常表现。
3讨论
医学3D打印技术近几年迅猛发展,由于其低成本及定制的外科特点,3D 模型应用于术前设计、医学教育、导板辅助手术、结合生物材料植入领域,尤其是颌面外科、口腔科等整形手术,泌尿外科领域也有报道1-4。传统CT、MRI 甚至特定格式的彩超数据都可以用来数字建模后 3D 打印。根据应用目的不同,3D 打印的材料可以是塑料、陶瓷、蜡、聚合树脂、金属等。一些生物材料及细胞组织的打印也有研究报道。研究结果显示,应用3D模型提高患者对疾病的认知是一个增强医患沟通、提高患者总体满意度的有效手段。3D 打印模型能够精确显示肾肿瘤患者肿瘤大小、深度及其与周围组织和血管毗邻情况11,利于术前规划手术切除范围、预判应该规避的血管、输尿管及手术的难点,更加直观,满意度较高。
对于肾门部肾肿瘤5,要达到肾部分切手术精确切除的要求,首先必须确定肿瘤大小、周围血管、输尿管毗邻及切除范围等信息,才能在限定的热缺血时间内保证手术效果并最大限度地保存肾功能。现阶段运用CT三维重建对肿瘤进行评估,虽然可以明确肿瘤与周围组织的关系,但仅限于平面图像观察,对集合系统、动静脉血管及可行的手术路径显示不够直观立体。而基于CT三维重建的3D打印模型能很好地克服上述不足:3D模型能够精准再现肿瘤与周围组织的结构关系,特别是对于高度复杂肿瘤,术前和术中可直接利用3D模型进行手术过程的分析模拟,初步判定手术路径、肿瘤切除范围及术中需要注意规避的血管、输尿管等难点问题,提高手术安全性。术中根据体位、手术视野的变化,可将3D打印模型固定至相应角度和方位,与手术视野比对,大致定位肿瘤12。随后阻断肾血供,避开并保护输尿管,距离肿瘤边缘1cm利用冷刀切开正常肾实质、沿肿瘤假包膜锐性分离、底面离断等操作将肿瘤完整切除。缝合采用“2+1”方式13,即集合系统修补时采用双向倒刺线免打结缝合深部肾创面,并在完成外层肾组织第1次缝合后开放肾血供以缩短热缺血时间,再根据肾脏表面渗血情况,加固缝合外层肾组织,最大化地减少对肾功能的损害。对于较大的肾门部肿瘤,完整切除肿瘤后,缝合可能成为主要困难,故对于部分肿瘤较大、创面大的肾门部肿瘤,采取锁边缝合也是一种选择6-10,13。
总之,肾门部肾肿瘤对于大部分泌尿外科医生是一难题,3D打印技术的引进,把这一难题简易化。通过肾脏3D模型的建立,肾门肿瘤的大小、毗邻、浸润深度及与肾血管、输尿管、集合系统的关系变得一目了然,也进一步帮助手术医生拟定更为合适的方案,减少术中肾血管和集合系统的损伤概率,更大程度的确保切缘阴性和保留肾功能。3D打印技术在肾门部肾肿瘤中的应用精准、安全、有效、可行,是一项值得泌尿外科医生推广应用的辅助技术。
参考文献
[1]Michalski M H, Ross J S. The shape of things to come: 3D printing in medicine [J] . JAMA, 2014, 312(21): 2213-2214.
[2]Kyung YS, Kim N, Hong JH. Application of 3-D Printed Kidney Model in Partial Nephrectomy for Predicting Surgical Outcomes: A Feasibility Study [J]. Clinical Genitourinary Cancer, 2019, 17(5): 878-884.
[3]Kim MG, Chi BH, Yoo JJ. Structure establishment of three-dimensional (3D) cell culture printing model for bladder cancer [J]. PLOS ONE, 2019, 14(10): 00223689.
[4]Zhang Y, Ge HW, Li NC, et al. Evaluation of three-dimensional printing for laparoscopic partial nephrectomy of renal tumors: a preliminary report [J]. World J Uorl, 2016, 34: 533-7.
[5]Thompson RH, Lane BR, Lohse CM, et al. Every minute counts when the renal hilum is clamped during partial nephrectomy [J]. Eur Urol, 2010, 58: 340-5.
[6]Lane B R, Fergany A F, Linehan W M. Should preservable parenchyma, and not tumor size, be the main determinant of the feasibility of partial nephrectomy? [J]. Urology, 2010, 76:608-609.
[7]Laryngakis N A, Guzzo T J. Tumor enucleation for small renal masses [J]. Curr Ooin Urol, 2012, 22: 365-371.
[8]Dong W, Lin T, et al. Laparoscopic partial nephrectomy for T1 renal cell carcinoma : comparison of two resection technique in a multi-institutional propensity score-matching analysis [J]. Ann Surg Oncol, 2016, 23: 1395-1402
[9]Hung A J, Cai J. “Trifecta” in partial nephrectomy [J]. J Urol, 2013, 189: 36-42.
[10]Chung B I, Lee U J. Laparoscopic partial nephrectomy for completely intraparenchymal tumors [J]. J Uorl, 2011, 186: 2182-2187.
[11]Chen y, Li H. Surgical planning and manual image fusion based on 3D model facilitate laparoscopic partial nephrectomy for intrarenal tumors [J]. World J Uorl 2014,32: 1493-1499.
[12]陳雷,林宁殊,殷民,许建挺,张鹏.腔内超声引导下腹腔镜肾部分切除术治疗完全肾内型肾肿瘤5例报告[J].临床泌尿外科杂志,2015,30:231-234.
[13]刘溪,潘秀武,杨启维,李霖,黄海,吕建敏,等.后腹腔镜下肾部分切除术治疗中度复杂性肾癌的方法改进及疗效分析(附84例报道)[J].临床泌尿外科杂志,2016,31:533-537.
作者简介:张向民,硕士,住院医师.
通讯作者:崔心刚,博士后,主任医师,E-mail: cuixingang@smmu.edu.cn
基金项目:上海市浦东新区公利医院青年英才(项目编号 GLRq2019-03)
