高分子量外消旋聚乳酸的合成、表征及工艺优化
2020-07-07王雅琪王柳迪李玉林刘昌胜
王雅琪, 杨 洋, 王柳迪, 李玉林, 刘昌胜
(华东理工大学材料科学与工程学院,教育部医用生物材料工程研究中心,上海 200237)
近年来,自然灾害、交通事故、工业污染及人口老龄化等原因造成的骨组织缺损和损伤已成为日益困扰和影响人类健康的一项重要医学课题[1]。传统的金属骨修复材料具有较高的力学性能,已被用来制作内固定器械,然而金属材料的模量远高于骨组织的模量,这往往引起应力遮挡效应,进而导致并发症的产生[2];同时大多数金属材料在使用过程中易释放出毒性金属离子,对人体产生毒副作用。此外,医用金属材料普遍缺乏生物降解性能,常常需要二次手术取出[3]。因此,现在多将可降解的高分子材料用于骨修复,其中聚乳酸(PLA)作为一种生物基可降解聚合物[4,5],具有良好的生物相容性[6]和生物可吸收性[7],在体内的降解可通过高分子链中酯键的水解断裂实现,其降解产物乳酸为人体正常代谢产物,因此对人体无毒副作用[8],已被广泛用于临床和医药领域,其应用主要包括药物输送[9]、手术缝合线[10]、骨固定材料[11]、防黏连膜[12]和可吸收骨修复支架等[13]。然而,临床使用的PLA 由于分子量较低,力学强度较差,限制了它在组织修复领域的进一步应用,因此需要开发高分子量PLA 的合成技术。
现有的PLA 合成路线包括乳酸直接缩合聚合、丙交酯开环聚合(ROP)和乳酸共沸脱水缩合聚合3 种制备方法[14]。乳酸直接缩合聚合是由乳酸经本体缩合聚合反应生成聚乳酸的方法,但乳酸缩合聚合过程中会生成水,而水的存在不利于反应正向进行,因此所得到的产物分子链较短[15]。乳酸共沸脱水缩合聚合是将乳酸和催化剂在减压条件下于回流的高沸点非质子溶剂中共沸脱水以制备分子量较高的PLA 的一种方法,但该反应条件苛刻,生产成本高且工艺复杂[16,17]。与前面两种合成方法相比,ROP 反应过程中没有副产物产生,可以获得分子量较高的PLA[18];但该反应需要在无水、无氧条件下进行,这一严苛条件增加了反应设备的设计难度,使得高分子量PLA 的大规模可控制备技术难以实现,限制了我国PLA 产业的发展。此外,传统的丙交酯开环聚合反应通常要使用有机溶剂如甲苯[19,20],不仅增加了成本,而且有毒副作用。
鉴于此,本研究报道了一种绿色环保的丙交酯开环聚合技术,反应过程中不引入任何有机溶剂,在无水、无氧操作系统及熔融状态下进行,操作简便,实验规模易于放大。通过研究丙交酯开环聚合影响因素(反应时间、反应温度、催化剂与单体的物质的量之比)对所制备外消旋聚乳酸(PDLLA)分子量的作用规律,并结合正交实验设计优化开环聚合反应条件,制备了高分子量PDLLA,并对其力学性能、降解性能及生物相容性进行了研究。
1 实验部分
1.1 原料和试剂
外消旋-丙交酯(D, L-LA):分析纯,济南岱罡生物工程有限公司;辛酸亚锡(Sn(Oct)2):分析纯,西格玛奥德里奇(上海)贸易有限公司;二氯甲烷:分析纯、上海凌峰化学试剂有限公司;磷酸二氢钾、磷酸氢二钠、氯化钠、氯化钾、无水乙醇、二甲基亚砜(DMSO):分析纯,上海泰坦科技股份有限公司;超纯水:华东理工大学生物材料所。
1.2 测试与表征
采用傅里叶变换红外光谱仪(美国Thermo Fisher 公司Nicolet 6700 型)测定聚合物的红外光谱,将聚合物在液氮中冷冻后置于粉碎机粉碎为粉末,取适量粉末与KBr 充分混合研磨后采取压片制样,扫描范围4 000~500 cm-1;采用凝胶渗透色谱(GPC)仪(美国WATERS 公司Waters1515 型)测定聚合物的数均分子量,流动相为四氢呋喃(THF),流速1 mL/min,测试温度35 ℃,标样为聚苯乙烯(PS);采用差示扫描量热仪(TA 仪器公司DSC 2910 型)测定聚合物的玻璃化转变温度,从25 ℃以10 ℃/min 的速率升温至120 ℃(一次升温),保持1 min;以10 ℃/min 的速率从120 ℃降至-20 ℃,保持5 min;以10 ℃/min 的速率由-20 ℃升温至120 ℃(二次升温)后结束测试;采用核磁共振仪(德国BRUKER 公司AVANCE-III 型,400 MHz)分析聚合物的结构,氘代氯仿(CD3Cl)为溶剂;采用综合热分析仪(德国NETZSCH 公司STA409PC 型)测定聚合物的分解温度,使用真空干燥的聚合物样品,升温区间为25~600 ℃,氮气氛围,升温速率为10 ℃/min。
1.3 实验步骤
1.3.1 PDLLA 的制备 实验在无水、无氧条件下进行。在手套箱称取一定质量的D, L-LA 于三口烧瓶,加入适量催化剂Sn(Oct)2,反应容器在真空条件下于室温预干燥1 h 后,通入氩气,然后快速升温至130~170 ℃的某一温度,在该温度反应一段时间,全程保证装置处于氩气氛围。反应结束后,先停止加热,但整个反应装置仍处于氩气氛围保护,当反应瓶降至室温后再停止氩气保护。产物经二氯甲烷溶解后,加入无水乙醇沉淀,得到的沉淀物在60 ℃经真空干燥24 h 后得到PDLLA 样品,并存放到-20 ℃的冰箱中。
1.3.2 反应条件对PDLLA 分子量的影响 (1)催化剂与单体的物质的量之比对PDLLA 数均分子量的影响。控制反应时间为7.0 h,分别研究在反应温度130、140、150 ℃时,不同的催化剂与单体的物质的量之比(1.15∶5 000、2.04∶5 000、2.66∶5 000、3.02∶5 000、3.38∶5 000、4.44∶5 000)对产物的数均分子量的影响。(2)反应时间对PDLLA 数均分子量的影响。控制催化剂与单体物质的量之比为2.66∶5 000,分别研究在反应温度为130、140 ℃时,不同反应时间(1、3、6、9、12、15 h)得到的产物的数均分子量及单体转化率。(3)反应温度对PDLLA 数均分子量的影响。控制反应时间为6.0 h,分别研究在催化剂与单体的物质的量之比为1.15∶5 000、2.04∶5 000、2.66∶5 000 时,不同反应温度(130、140、150、160、170 ℃)对产物数均分子量的影响。(4)正交实验。通过设计正交实验对PDLLA 的合成工艺进行优化。正交实验各因素水平见表1。
1.3.3 力学性能测试 首先将聚合物用平板硫化机在180 ℃、10 MPa 经热压制得聚合物薄膜(120 mm×150 mm×0.5 mm),然后将薄膜裁剪成哑铃型,最后采用电子万能试验机(美特斯工业系统(中国)有限公司CMT-2503)测试薄膜的力学性能。测试标准为GB/T 1040—2006,样条拉伸速率10 mm/min,温度25 ℃,湿度50%,每组5 个平行样品。

表1 正交实验设计及结果Table 1 Design and results of orthogonal test
1.3.4 降解性能测试 使用平板硫化机在180 ℃、10 MPa 经热压制得120 mm×150 mm×0.5 mm 的聚合物薄膜,然后将其裁剪成10 mm×10 mm×0.5 mm 的样品。将薄片置于10 mL pH=7.4 的PBS 缓冲液中,于37 ℃恒温振荡箱进行材料降解实验。在到达预先设置的取样时间后,取出聚乳酸样品并用大量去离子水冲洗,经滤纸除去样品表面水分后,测得其湿态质量,经真空干燥48 h 至样品达到恒重后测得此时的质量即为样品的干态质量,并记录此时溶液的pH。每个时间点、每组样品取3 个平行样,记录每个样品的初始质量。通过公式(1)计算样品的吸水率( rH2O):
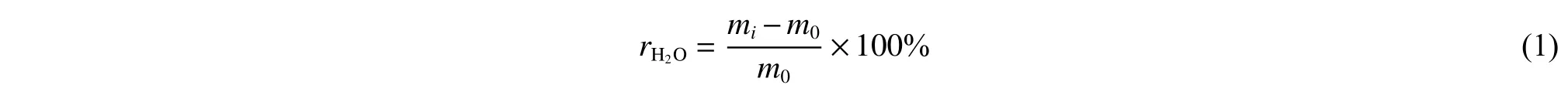
其中,mi为第i 天样品的湿态质量,m0为样品降解前的初始质量。
1.3.5 细胞活性测试 将热压得到的纯聚乳酸膜裁剪成10 mm×10 mm×0.5 mm 的样品,将聚合物膜放置于24 孔板内(每孔1 个样品),每个组分取3 个样品,在超净台紫外辐照24 h 灭菌。每个孔板接种2×104个小鼠成纤维(L929)细胞后于37 ℃培养箱孵育1,3 d 和7 d。在各培养时间点,每孔加入100 μL 3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT)溶液(5 mg/mL),继续在37 ℃恒温箱孵育4 h 后,移去每孔的培养基。将薄膜移至新的孔板内,每孔用500 μL 二甲基亚砜(DMSO)在37 ℃恒温振荡箱溶解所得的甲瓒晶体。15 min 后,每孔取100 μL 液体于96 孔板中,测定492 nm 处的吸光度(OD)值。
2 结果与讨论
2.1 PDLLA 的合成工艺优化
2.1.1 催化剂与单体的物质的量之比 图1 示出了催化剂与单体的物质的量之比对PDLLA 数均分子量的影响。当反应温度为130 ℃和140 ℃时,PDLLA 的数均分子量随催化剂含量增加呈现先上升再下降的趋势,这是由于当催化剂含量较少时,随着催化剂含量的增加,反应速率加快,使得聚合物分子链快速增长;而当催化剂含量超出某一值时,链增长中心过多,从而使聚合物数均分子量反而下降。当反应温度为150 ℃时,聚乳酸数均分子量则随催化剂含量增加直接呈下降趋势,这是由于高温会导致一些副反应如解聚反应[21,22]发生,从而使产物链长变短。
2.1.2 反应时间 图2 示出了反应时间对PDLLA 数均分子量及单体转化率的影响。在所选取的反应温度下,当反应时间为3~6 h时,数均分子量最高;继续增加反应时间,数均分子量反而呈下降趋势,这可能是由于长时间高温条件造成了酯交换等副反应的发生,导致PDLLA 分子链变短[23]。实验结果表明反应6.0 h 时单体转化率达到最大值,再继续延长反应时间,单体转化率基本维持不变。因此,控制反应时间为6.0 h 可以获得较大的单体转化率及高分子量的PDLLA。
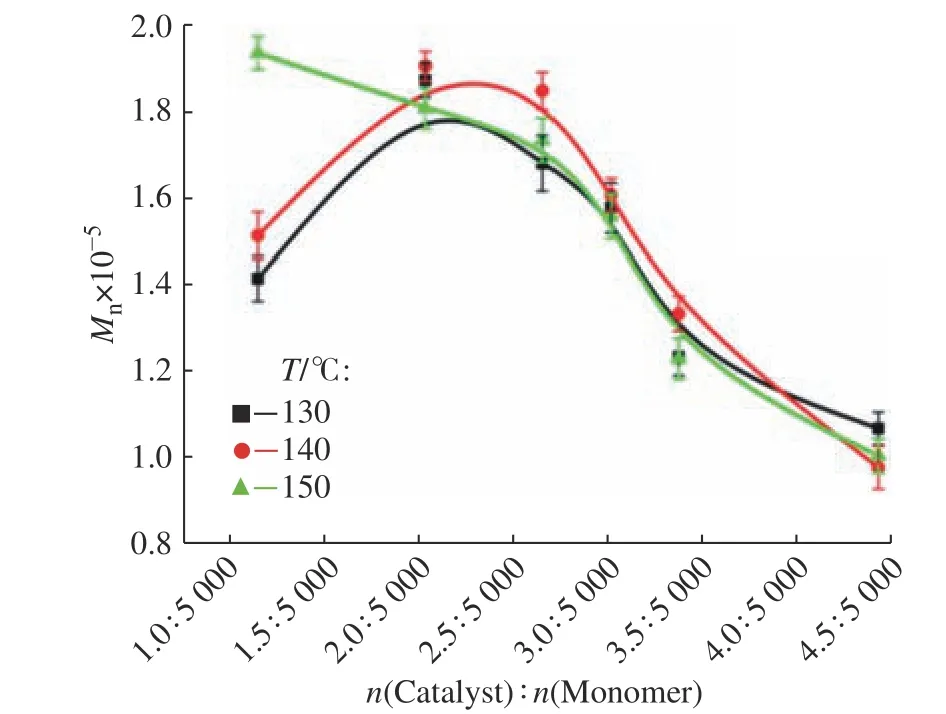
图1 催化剂与单体的物质的量之比对PDLLA 数均分子量的影响Fig. 1 Effect of molar ratio of catalyst to monomer on the numberaverage molecular weight of PDLLA

图2 反应时间对PDLLA 数均分子量及单体转化率的影响Fig. 2 Effect of reaction time on the number-average molecular weight and monomer conversion rate of PDLLA
2.1.3 反应温度 图3 示出了PDLLA 数均分子量与反应温度的关系。当催化剂与单体的物质的量之比为1.15∶5 000时,聚合物数均分子量随温度增加呈先上升后下降的趋势,在150 ℃有一极值。当催化剂与单体的物质的量之比为2.04∶5 000 时,数均分子量变化趋势也是先上升后下降,但数均分子量的极大值出现在较低的温度(140 ℃),且数均分子量要高于物质的量之比为1.15∶5 000 的数均分子量。这可能是由于在一定范围内升高反应温度可增加分子的运动速率,使得数均分子量增加。丙交酯经开环聚合得到聚乳酸的过程还伴随着聚乳酸分子链解聚的过程,反应温度的继续升高导致了解聚反应速率要快于开环聚合的速率,最终引起了数均分子量的下降[24]。当催化剂与单体的物质的量之比增加至2.66∶5 000 时,数均分子量随反应温度的增加而下降,这是由于引发剂过多导致引发位点增加,则在相同单体加入量下,平均到每一引发点的单体量减少,因此聚合产物的数均分子量降低。
2.1.4 合成工艺优化 从正交实验结果(表1)及极差分析图(图4)可得PDLLA 的最优合成工艺为A1B2C1,即温度选取135 ℃,催化剂与单体物质的量之比为2.04∶5 000,反应时间选取4.5 h。如果综合考虑单体转化率,则反应时间可选为6.0 h。
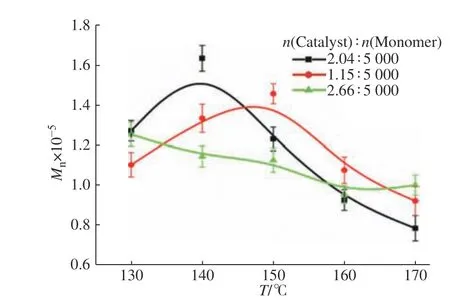
图3 反应温度对PDLLA 数均分子量影响Fig. 3 Effect of reaction temperature on the number-average molecular mass of PDLLA
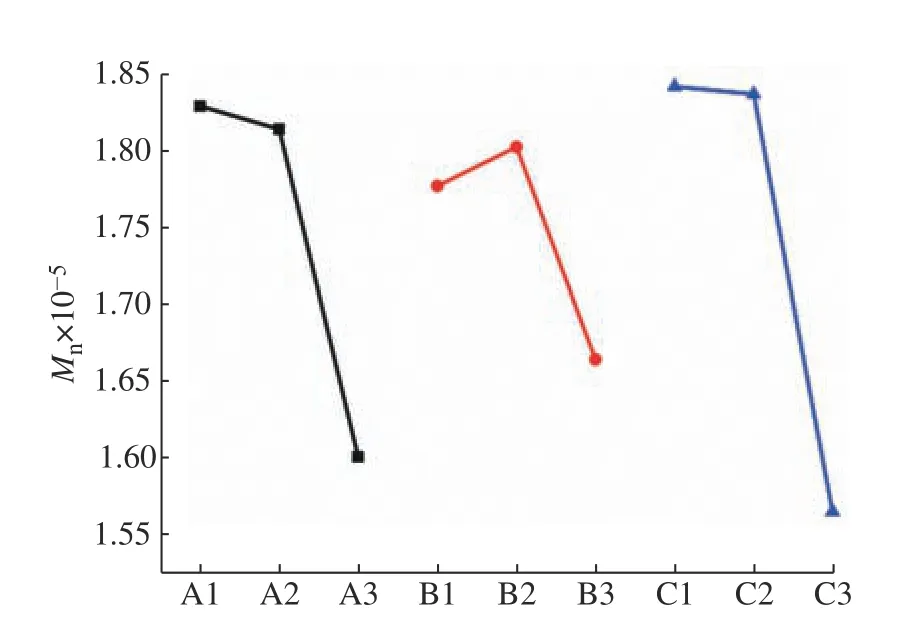
图4 正交实验极差分析图Fig. 4 Range analysis of orthogonal experiment
2.2 材料表征
2.2.1 PDLLA 数均分子量及热性能 在上述优化合成条件下制备PDLLA,并对样品的数均分子量及热性能进行表征。图5(a)为通过GPC 测定的淋洗时间与信号强度之间的关系,PDLLA 的峰值分子量(Mp)为3.81×105,数均分子量为2.01×105,分子量分布(PDI)为2.12。图5(b)为PDLLA 的DSC 曲线,可以看出所得PDLLA 为无定型聚合物,其玻璃化转变温度(Tg)为49.9 ℃。图5(c)为PDLLA 的热重曲线,所得PDLLA 的热分解温度(Td)为271.1 ℃,证明所制备的PDLLA 具有较好的热稳定性。
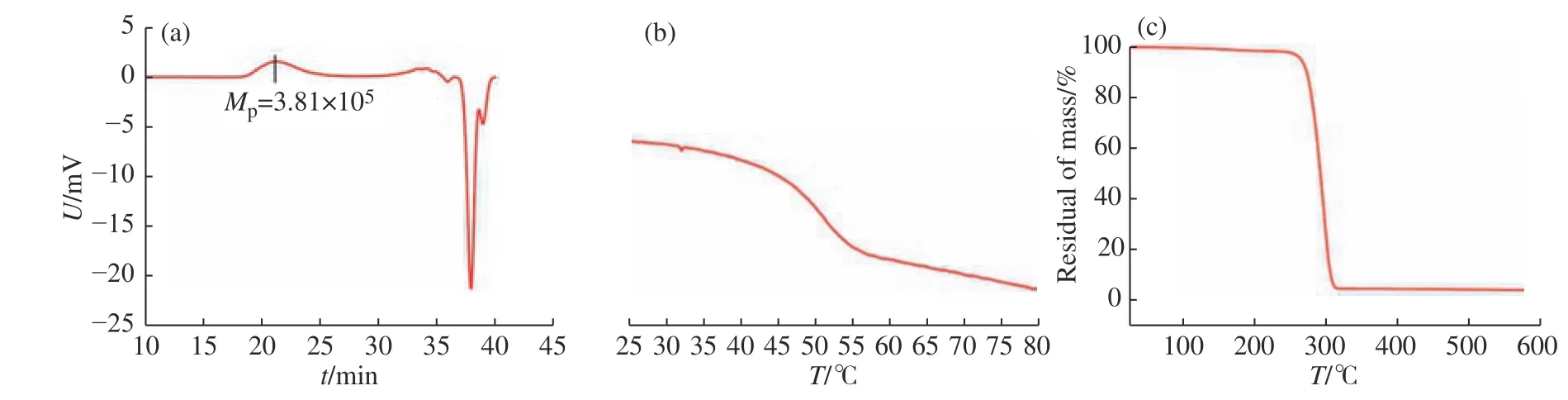
图5 聚合物的(a)GPC、(b)DSC 与(c)热重曲线Fig. 5 (a) GPC, (b) DSC and (c) TG curves of PDLLA
2.2.2 PDLLA 的结构表征 从图6(A)的1H-NMR 谱图中可以看出:δ=1.56 处是PDLLA 分子链上―CH3中的H 原子,δ=5.16 处为PDLLA 骨架上面的―CH2―中的H 原子。从图6(B) 的红外光谱图可以看出:1 743 cm-1处的峰为PDLLA 重复单元酯键中C=O的伸缩振动峰,1 034 cm-1处的吸收峰对应于C―O―C 的伸缩振动,2 970~2 872 cm-1的峰与―CH3和―CH2―的C―H 键的伸缩振动相对应,因此,样品的所有峰都与PDLLA的特征峰一致[25]。
2.2.3 力学性能 通过上述优化的合成工艺制备的PDLLA 的应力-应变曲线见图7,PDLLA 的拉伸强度为(39.01±1.34) MPa,断裂伸长率为3.94%±0.54%,弹性模量为(1.68±0.34) GPa。聚乳酸的力学强度对其在生物医学领域的应用极其重要,高分子量聚乳酸能展现更好的强度和韧性,适合开发骨组织修复支架材料或非承重骨组织的固定材料。
2.2.4 PDLLA 的降解性能 图8(a)为PDLLA 在PBS 溶液中的吸水率及质量变化曲线,图8(b)为PDLLA 降解过程中溶液pH 的变化曲线。初始100 d 内PDLLA 的质量变化不明显,在100~220 d 出现较明显的质量减少,220 d 后则出现急速的质量减少。PDLLA 的吸水率变化趋势则与之相反:初始100 d 吸水率较小,100~220 d 吸水率显著上升,220 d 后吸水率迅速上升。PDLLA 的降解速率与其吸水率有关,降解前期PDLLA 材料致密性较高,能降低体液溶胀侵蚀的速率,从而能减缓材料降解速率并维持较高的强度。随着降解时间延长,材料结构变得疏松,水分对PDLLA 的侵蚀速率加快,因此材料的降解速率加快,从而导致了材料的破裂(图9)[26]。溶液pH 在初期变化不大,可能是前期降解速率较慢的原因,随时间的延长,降解速率加快,乳酸的积累增多,这些因素使得PDLLA 降解速率明显加速,导致pH 显著降低[27]。进一步观察PDLLA 膜膜在降解过程的微观变化(图10),可以看出材料在降解前的表面及断面较为平滑,经过240 d 降解后,材料表面粗糙,伴随有大量微孔和颗粒产生。材料降解后断面内产生的孔明显大于表面,这一现象进一步证明PDLLA 内部降解要快于外部。这可能是因为PDLLA 材料首先吸水溶胀接着发生水解反应,此过程会释放出酸度较高的乳酸,通常材料表面的乳酸降解产物比较容易被缓冲溶液中和或淋洗带走,而内部降解产生的乳酸不易排出,因此易造成内部乳酸的过多积蓄,导致内部降解速率较快,而表面降解速率反而较慢[28]。

图7 PDLLA 的应力-应变曲线Fig. 7 Stress-strain curve of PDLLA
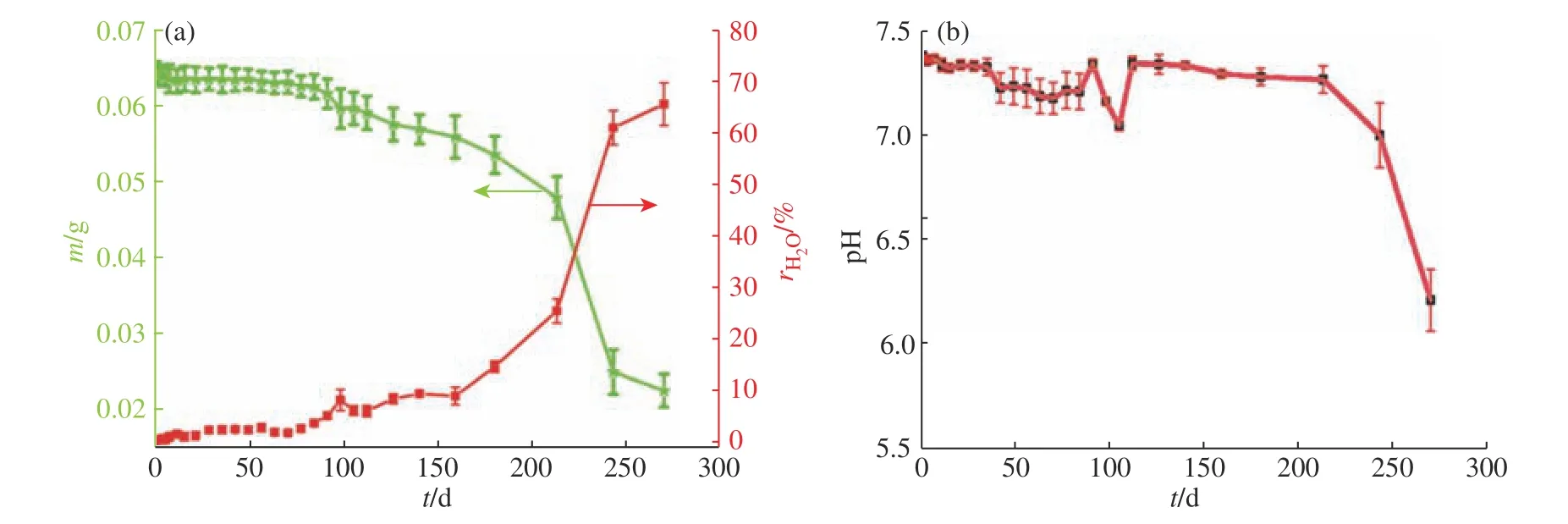
图8 PDLLA 降解曲线:(a)吸水率及质量变化曲线;(b)pH 变化曲线Fig. 8 Degradation profile of PDLLA: (a) water absorption rate and mass variation; (b) pH variation

图9 PDLLA 的外观照片:(a)降解前;(b)降解28 d;(c)降解240 dFig. 9 Digitalphotos of PDLLA: (a) before degradation; degraded after (b) 28 d and (c) 240 d

图10 PDLLA 降解前后的扫描电镜照片Fig. 10 SEM images of PDLLA before and after degradation
2.2.5 细胞活性 选择L929 为模型细胞,采用MTT 法评估了其在PDLLA 膜上1,3,7 d 的细胞活性,结果如图11 所示。结果表明,PDLLA 薄膜表面的细胞增殖量要高于空白对照组,表明PDLLA 对细胞无毒性,且有助于细胞的增殖。
3 结 论
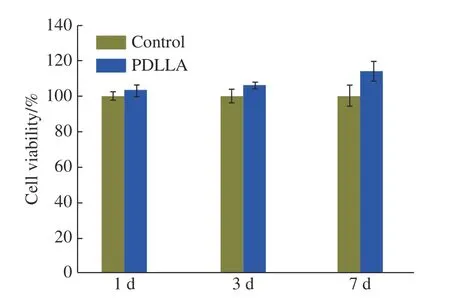
图11 L929 细胞在PDLLA 膜表面的细胞活性Fig. 11 Cell vaibility of L929 cells cultured on the surface of PDLLA membranes
(1)D, L-LA 开环聚合生成PDLLA 的最佳合成条件:反应温度为135 ℃,催化剂与单体物质的量之比为2.04∶5 000,反应时间选取4.5 h,如果综合考虑单体转化率的话,反应时间可选为6.0 h。根据正交实验优化的条件所得聚乳酸的数均分子量为2.01×105,拉伸强度为(39.91±1.34) MPa,断裂伸长率为3.94%±0.54%,弹性模量为(1.68±0.34) GPa。
(2)PDLLA 薄膜可促进小鼠成纤维细胞的增殖。
