阻塞性睡眠呼吸暂停低通气综合征对患者超声骨密度的影响及与跌倒风险的相关性
2020-07-07黄占强曹亚文曹俊杰巴春贺丁华杰
黄占强,王 娜,曹亚文,赵 翠,曹俊杰,巴春贺,丁华杰
(承德医学院附属医院1.老年病科,2.超声科,河北 承德 067000)
阻塞性睡眠呼吸暂停低通气综合征(OSAHS)是多种原因导致睡眠状态下反复出现低通气和(或)睡眠中断,引起慢性间歇性低氧血症伴高碳酸血症以及睡眠结构紊乱,进而使机体发生一系列病理生理改变的临床综合征,主要表现为睡眠打鼾伴呼吸暂停及日间嗜睡、疲劳、记忆力下降等。由于呼吸暂停引起反复发作的夜间低氧和高碳酸血症,可导致高血压、冠心病和脑血管疾病等并发症及交通事故,甚至出现夜间猝死。研究显示,OSAHS与骨密度之间存在关联,OSAHS患者与非OSAHS患者骨密度之间存在显著差异[1]。通过超声骨密度T值可评估患者骨质疏松情况,骨质疏松性骨折的发生率随着年龄的增长而增加,跌倒后骨折与老年骨质疏松有直接关系,跌倒风险增加和骨密度降低是导致骨质疏松性骨折的重要因素[2],而老年患者由于其他慢性疾病而常常忽视骨质疏松症。目前针对OSAHS的研究较多,但大部分研究主要是针对心脑血管,针对OSAHS与跌倒风险的研究较少。本研究的目的是明确OSAHS对老年患者超声骨密度影响,通过睡眠呼吸暂停低通气指数(apnea hypopnea index,AHI)评估OSAHS与跌倒风险之间的相关性。
1 资料与方法
1.1 研究对象
选取2016年3月至2018年12月于承德医学院附属医院老年病科住院,根据《睡眠呼吸暂停低通气综合征诊治指南》[3]行多导睡眠监测(PSG)确诊为OSAHS的患者65例。依据AHI(指在睡眠过程中每小时低通气加呼吸暂停发生次数总和)分为轻中度和重度组。其中,轻中度组(5次/h≤AHI<30次/h)44例,重度组(AHI≥30次/h)21例。选择同期住院行PSG排除OSAHS的患者31例为对照组(AHI<5次/h)。
OSAHS组与对照组间年龄、性别、基础疾病、血Ca、血P、25羟基维生素D[25(OHD)]、甲状旁腺激素(PTH)差异均无统计学意义(P>0.05)。轻中度组、重度组与对照组体重指数两两比较差异有统计学意义(P<0.05),见表1。
排除标准:慢性肾病、慢性阻塞性肺疾病、风湿性疾病,既往有导致代谢障碍的疾病:如甲状腺功能亢进,神经性厌食症,恶性肿瘤等疾病,接受骨质疏松治疗或药物治疗可能影响骨代谢(非甾体类抗炎药,噻嗪类、华法林,肝素,激素替代治疗)及接受过持续气道正压通气治疗的患者。本研究经过承德医学院附属医院伦理委员会同意。

表1 3组患者一般情况比较
1)与对照组比较,P<0.05;2)与轻中度组比较,P<0.05
1.2 骨密度检测
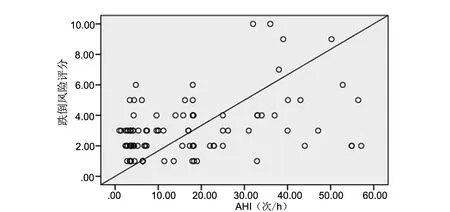
采用超声骨密度仪应用定量超声法(QUS)测量T值,QUS检查由经培训的专人采用韩国OsteoSys公司的ONOST-3000超声骨密度检查仪测定受试者右侧跟骨骨密度T值,根据超声骨密度数值评估患者是否存在骨质疏松。低骨量和骨质疏松症的诊断:依据世界卫生组织(WHO)给出的标准: 依据世界卫生组织(WHO)给出的标准:T>-1.0 SD为正常骨密度,在-2.5 SD 依据卫生部《老年人跌倒干预技术指南》中的老年人跌倒风险评估量表(FRASE)作为测评工具。该量表包括运动、跌倒史、睡眠状况、自控能力、精神不稳定状态、感觉障碍、用药史、相关病史8个项目的35个子条目,每个子条目得分分别设定为1、2和3分。最终各项子条目累计得分,总得分为0~53分。跌倒风险程度判定:低危:1~2分;中危:3~9分;高危:10分及以上。 对照组与轻中度及重度组间骨密度T值比较差异无统计学意义,三组患者骨质疏松发生率的比较差异无统计学意义,P>0.05。见表2。 表2 三组患者骨密度检测情况比较 通过Pearson相关性分析显示,血Ca、BMI与AHI呈正相关(P<0.05),T值与AHI呈负相关(P<0.05),血P、PTH、25(OHD)与AHI无相关性(P>0.05)。见表3。 表3 AHI与各组骨代谢标志物指标的相关性分析 Tab 3 Correlation analysis between AHI and bone metabolism markers in each group 指标AHIrPCa 0.308 0.002P-0.117 0.25825(OHD) 0.139 0.178PTH 0.222 0.030BMI 0.520<0.05T值-0.349<0.05 对照组与轻中度OSAHS组跌倒风险比较差异无统计学意义(P>0.05),对照组、轻中度组与重度组OSAHS组跌倒风险比较差异有统计学意义(P<0.05)。 见表4。 所有患者AHI与跌倒风险呈正相关(r=0.399 ,P<0.01)。见图1。 本研究骨密度的测量是通过超声骨密度仪应用跟骨定量超声法测量T值。胡一顺等[4]研究显示QUS测定骨强度指数(stifiness index,STI)与DXA测定骨密度(bone mass densitometry,BMD)有较好的相关性和一致性,虽然QUS诊断骨质疏松的检出率要明显低于DXA,但骨量异常(包括骨量减少和骨质疏松)的检出率则明显高于DXA。国外Hartl等[5]认为定量超声独立于BMD有预测骨折风险的价值,且定量超声以其非创伤性、无辐射及操作简单等优点弥补了DXA或骨活检的缺陷。本研究跌倒风险应用卫生部老年人跌倒风险评估量表,该量表具有良好的信度和效度,且易于操作,敏感度高,对跌倒风险区分效度好,跌倒风险预警效果好。 表4 三组患者AHI及跌倒风险评分 1)与对照组比较,P<0.05;2)与轻中度组比较,P<0.05 图1 AHI与跌倒相关性分析Fig 1 Correlation analysis of AHI and fall risk 研究显示OSAHS患者的间歇缺氧对骨代谢产生负性作用。缺氧增加动物模型和人类破骨细胞的体积和数量,通过增加白介素-6(IL-6)、血管内皮生长因子(vascular endothelial growth factor,VEGF)的表达提升破骨细胞的作用,减少破骨细胞成熟和分化[6]。缺氧能直接导致骨细胞功能的异常和缺氧相关性疾病,如贫血和慢性呼吸紊乱,他们和骨质减少相关联,破骨细胞和成骨细胞之间的平衡由于缺氧有利于破骨细胞而被破坏[7-8]。Terzi等[9]的研究显示,OSAHS与骨密度呈负性作用。呼吸功能不良和慢性阻塞性肺病与骨密度降低和骨质疏松风险增加有关[10-11]。本研究提示试验组与对照组骨密度及骨质疏松发生率差异无统计学差异,但是AHI与T值有相关性,呈负相关,支持OSAHS与骨密度呈负性作用,3组患者骨质疏松发生率无统计学差异,可能与样本量少及3组间样本数差异有关。 李幸等[12]通过Meta分析结果显示睡眠障碍会增加老年人的跌倒风险,其中睡眠障碍包括失眠、嗜睡、睡眠呼吸障碍(通过PSG明确)。有研究报道睡眠障碍导致跌倒风险增加可能与睡眠障碍加速蛋白质水肿,导致骨骼肌减少有关[13],另外睡眠障碍可引起认知功能减退、反应减慢导致跌倒风险增加。睡眠缺氧可能是老年男性跌倒和骨折的新危险因素,夜间低氧增加与跌倒风险显著相关[14]。本研究结果表明,AHI与跌倒风险呈正相关,重度OSAHS组跌倒风险与对照组及轻中度组差异有统计学意义,支持上述研究结果。夜间缺氧可能是导致跌倒风险的危险因素。随着夜间缺氧的增加,跌倒风险增大。本研究的局限性包括缺乏评估日光暴露、营养、钙摄入、日常活动水平、饮食习惯、家人陪同情况、护理等因素,这些因素可能会影响骨密度及跌倒风险。1.3 跌倒风险评价指标
1.4 统计学方法

2 结 果
2.1 三组患者骨密度结果比较

2.2 各项指标与AHI的相关性分析

2.3 三组患者跌倒风险比较及AHI与跌倒风险的相关性分析
3 讨 论