阿苯达唑对小鼠动脉血管狭窄的干预效果及机制研究
2020-07-06路芳芳姚佳璐钮晓音
路芳芳,姚佳璐,钮晓音,翁 震,何 杨,
1.江苏省血液研究所,苏州大学附属第一医院,苏州 215006;2. 江苏省苏州市立医院心内科,苏州 215002;3. 上海交通大学医学院,上海市免疫学研究所,上海 200025;4. 苏州大学血液和血管疾病诊疗药物技术教育部工程研究中心,苏州 215123
血管再狭窄(restenosis)是一类源于新生内膜增殖的血管病变,在心脏和外周血管成形术、旁路移植术、动脉内膜切除术及人工动静脉篓术后均有可能出现,被认为是影响血管置换术和血管成形术远期疗效的主要原因[1]。临床研究[2-3]显示,血管再狭窄在进行血管重建术后的发生率仍然高达30%~50%。目前在临床上,对于血管再狭窄的治疗仍未找到较好的治疗方法。近年来,研究[4]表明,内侧动脉层中过度的血管平滑肌细胞(vascular smooth muscle cells,VSMCs)增殖和迁移在内膜增生性疾病的发病机制中起着重要作用。因此,如何有效抑制和控制VSMCs 的增殖和迁移是血管再狭窄疾病治疗的重要切入点。
阿苯达唑(albendazole,ABZ)是一种咪唑衍生物类广谱驱肠虫药物[4-5]。通过抑制寄生虫细胞中微管形成和葡萄糖摄取发挥驱虫作用。除了在驱虫方面的作用外,ABZ还可以通过抑制肿瘤细胞的增殖或者通过某些信号通路上调肿瘤坏死因子的表达来诱导细胞凋亡,从而发挥抗肿瘤的作用。有研究[6-7]表明,微管的组装和排列能够影响VSMCs 的迁移。因此,我们推测ABZ 可能通过影响VSMCs 的生物学特性,包括增殖、迁移及凋亡,从而影响血管再狭窄的过程。本研究探讨在外周套管诱发狭窄的小鼠模型中,ABZ 作为潜在治疗药物的作用效应,并探究其作用机制。
1 材料与方法
1.1 材料
人血管平滑肌细胞购自美国Life Technology 公司;ABZ、二甲基亚砜(DMSO)购自美国Sigma 公司;细胞培养试剂包括DMEM/F12 培养基、胎牛血清及100×青霉素-链霉素溶液购自美国Thermo Fisher 公司;细胞迁移实验试剂I 型胶原蛋白及材料Transwell 小室(孔径8 µm)购自美国Millipore 公司;血小板衍生的生长因子BB(PDGF-BB)购自美国R&D 公司;抗体包括兔抗人磷酸化及总肌球蛋白轻链2、兔抗鼠磷酸化及总丝切蛋白(cofilin,CFL)、GAPDH 购自美国Cell signaling Technology 公司;Annexin V-PI 细胞凋亡试剂盒及细胞裂解液RIPA 液购自中国南通碧云天生物技术研究所。
1.2 实验动物
雄性8 ~10 周龄C57BL/6 小鼠(体质量22 ~25 g)购自北京维通利华公司,所有动物置于SPF 环境中进行饲养。动物生产许可证号为SCXK(京)2019-0009,使用许可证号为SYXK(苏)2017-0043,动物实验及处理方案经过苏州大学动物伦理委员会审批(审批号201810A530)。
1.3 细胞增殖实验
将VSMCs 调整浓度至2×104个/mL 后接种于48 孔板中,每孔0.5 mL。随后将培养板置于37 ℃、5% CO2的培养箱中静置6 h 使细胞贴壁。随后在不同孔中加入浓度为0.5、1 μmol/L 的ABZ 或等体积的DMSO 进行孵育培养,并在24 h 及48 h 时间点加入MTT 溶液,通过酶标仪进行细胞存活率测定吸光度[D (490 nm) ]。
1.4 Transwell 细胞迁移实验
参照相关文献[8],将500 μL Ⅰ型胶原蛋白(3.79 mg/mL) 与50 μL 的NaOH(0.2 mol/L)和100 μL 的100× 青 霉素-链霉素溶液混合后置于冰上,然后在混合溶液中加入3×105个重悬于250 μL DMEM/F12 的经过血清饥饿处理5 ~6 h 的VSMCs,并充分混合。将等分的含有VSMCs的上述混合溶液(100 μL)转移至24 孔Transwell 小室的上室中,随后将Transwell 小室在37 ℃下孵育20 min以形成凝胶,取出后在下室中加入0.6 mL 含2.5% FBS、PDGF-BB 和ABZ(0.5 或1 μmol/L)或DMSO 对 照 的DMEM/F12 培养基。同时,在上室的凝胶上部加入含有2.5% FBS 和相同浓度的ABZ 或DMSO 对照的DMEM/F12 培养基(0.1 mL)进行覆盖。然后,将Transwell 板置于37 ℃、5% CO2细胞培养条件下孵育48 h。为了量化VSMCs 通过凝胶和Transwell 孔迁移至多孔膜下部腔室表面的过程,收集上部小室并通过浸入4%多聚甲醛中进行固定。用棉签去除凝胶并拭去上室膜表面未迁移的细胞。割下Transwell 的多孔膜后,按照产品说明书用Diff-Quik染色套件(德国Siemens 公司)染色。于100 倍正置显微镜下随机选取每个膜的4 个区域进行计数并求和,得出迁移细胞的总数。
1.5 流式细胞术评估细胞凋亡
将VSMCs 调整浓度至3×104个/mL 后接种于6 孔板中,每孔2 mL。随后将培养板置于37 ℃、5% CO2的培养箱中静置6 h 使细胞贴壁。随后在不同孔中加入浓度为0.5、1 μmol/L 的ABZ 或等体积的DMSO 进行孵育培养,并在48 h 后采用Annexin V-FITC/PI 染色法评估细胞凋亡。将处理后的细胞与5 μL Annexin V-FITC 混合,在室温下避光孵育10 min,随后通过PBS 洗涤后加入10 μL PI于室温下避光孵育10 min。使用Beckman-Coulter Gallios流式细胞仪进行细胞凋亡检测,通过仪器自带的Kaluza Analysis 软件分析结果。
1.6 小鼠股动脉外周套管血管狭窄模型构建及ABZ 处理
术前将小鼠通过腹腔注射50 mg/kg 戊巴比妥钠进行麻醉。将其以仰卧位固定并置于解剖显微镜下,采用眼科剪在小鼠腿内侧切开一条1 ~2 cm 的纵向切口,并使用显微镊从股神经和股静脉与股动脉分离,长度为3 mm。采用长度为2.0 mm 纵向切开细孔PE 管(内径0.41 mm,外径0.51 mm;英国Smith 公司)套在股动脉周围,两端套管通过6/0 缝合线结扎以实现血流部分阻断。通过连续缝合针法缝合切口皮肤后,将小鼠置于干净鼠笼静待复苏。
将建模后的小鼠进行分组,每组各10 只小鼠。①实验组:每天用溶解于芝麻油中的1.5 mg ABZ 进行灌胃。②对照组:每天采用等体积的芝麻油进行灌胃。在模型建立后第2 天上午开始第一次灌胃,并将实验组和对照组小鼠在模型建立后置于含有高脂饲料(TP28600,南通特洛菲饲料有限公司)的笼中进行饲养。4 周后通过心脏灌注含4%甲醛的PBS 处死动物,并获得股动脉进行组织学 分析。
1.7 组织学和形态分析
切下两侧股动脉,包埋在石蜡块中,切成5 μm 薄片并进行苏木精 - 伊红(H-E)染色。采用Leica DM2000 显微镜图像采集后,从每条动脉中选择每600 mm2截取的3 个 横截面进行定量。使用Image J 软件分析图像。测量内膜(intima)和中膜(media)区域,并计算内膜与中膜的比例(I/M)。
1.8 蛋白质印迹法(Western blotting)分析
将VSMCs 在0.5 或1 μmol/L ABZ 或 等 体 积DMSO存在的情况下,联合20 ng/mL PDGF 处理24 ~48 h 后,使用适量的RIPA 溶液将VSMCs 裂解,12 000×g、4 ℃下离心15 min,获得含有蛋白的上清溶液。经过BCA 法进行蛋白定量后,将含有30 ~50 μg 蛋白的样品溶液在10% SDS-聚丙烯酰胺凝胶上电泳分离,并转移到PVDF膜上。在室温下,将膜用5%脱脂牛奶中封闭2 h 后,在4 ℃条件下与一抗(1:1 000)孵育过夜。将PVDF 膜在含1% Tween-20 的PBS 中洗涤3 次后,与适当浓度的HRP标记的二抗(1:50 000 稀释)于室温下孵育1 h,重复上述洗膜后,采用ECL 底物试剂盒显影曝光,对特异性蛋白条带采用Image J 软件进行半定量分析。采用GAPDH蛋白作为内参对照。
1.9 统计学分析
采用GraphPad Prism 7 软件进行统计学分析,数据以±s 表示。多组间比较采用单因素方差分析结合Tukey HSD 与SNK 检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 ABZ 浓度确定
将VSMCs 与不同浓度的ABZ 进行孵育后,构建IC50的曲线以明确ABZ 的使用浓度。结果显示,ABZ 浓度为0.5 ~1 μmol/L 时能够实现对细胞生长的半数抑制(图1)。 因此,采用0.5 和1 μmol/L 作为后续实验的浓度。
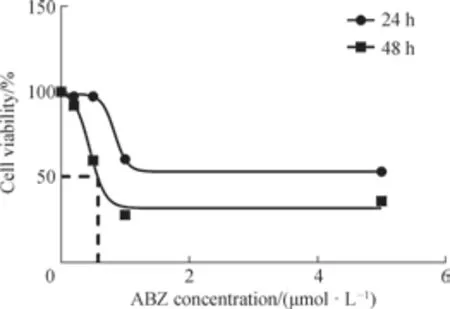
图1 ABZ 对细胞起效的最低浓度Fig 1 Minimum concentration of ABZ to act on cells
2.2 ABZ 对VSMCs 增殖和迁移的抑制作用
0.5 和1 μmol/L ABZ 均 能 够 显 著 抑 制VSMCs 的 增殖(图2A)。细胞迁移实验结果显示0.5 和1 μmol/L ABZ均能够显著抑制VMSCs 的迁移(图2B、2C)。通过流式细胞术观察48 h 时ABZ 对VSMCs 凋亡的影响,结果显示1 μmol/L ABZ 能够显著增加VSMCs 的凋亡,而在0.5 μmol/L 时无此效应。
2.3 ABZ 对再狭窄小鼠模型新生内膜增生的抑制作用
体外实验结果提示ABZ 能够影响VSMCs 的增殖和迁移,进一步通过股动脉外周套管法构建了小鼠血管再狭窄的模型验证ABZ 在体内的作用效应。结果显示,与对照组小鼠比较,ABZ 灌胃能够显著降低新生内膜面积及I/M比值(图3),但是对中膜面积并无显著效应。
2.4 ABZ 干预血管再狭窄的作用机制
相较于对照溶剂DMSO 处理,0.5 和1 μmol/L ABZ处理均能够显著抑制CFL 去磷酸化和肌球蛋白轻链(myosin light chain,MLC)的磷酸化,且呈现浓度依赖的趋势(均P<0.05),见图4。

图2 ABZ 对VSMCs 增殖、迁移及凋亡的影响Fig 2 Effects of ABZ on proliferation, migration and apoptosis of VSMCs
3 讨论
VSMCs 在许多血管疾病中起着重要作用。在发生动脉损伤时,VSMCs 通过从静止的收缩表型转变为具有增殖性和迁移性的表型进行应答。通过增生、迁移和细胞外基质的产生,VSMCs 有助于在动脉粥样硬化以及支架置入后再狭窄中出现的阻塞性血管病灶的形成[9]。随着社会经济发展、生活水平的提高以及人口老龄化趋势的到来,阻塞性血管病的发病率和死亡率呈增高趋势。尽管目前在临床上使用的药物洗脱支架已成功地预防了再狭窄,但是由于每年植入支架患者的数量巨大,再狭窄和复发性再狭窄仍然很普遍。因此,在临床实践中仍需安全有效的方法来治疗复发性再狭窄。
ABZ 是苯并咪唑氨基甲酸酯类驱虫药,其最初作为抗寄生虫药于1975 年问世,并以其对人体和农场动物的功效和低毒性而备受关注[9]。ABZ 作为能够结合β-微管蛋白受体的激动剂,通过改变微管蛋白聚合实现对寄生虫的抑制[9]。ABZ 破坏微管聚合的潜在机制,促进了其作为微管结合剂用于抗肿瘤药物的实验研究。先前的研究[6,10]已经确定了几种苯并咪唑氨基甲酸酯(包括ABZ)在多种肿瘤细胞系中的抗肿瘤效应,主要包括肺癌、白血病和皮下鳞癌。另外,也有研究[11]评价了关于ABZ 与 2-甲氧基雌二醇或紫杉醇的组合的协同抗肿瘤作用。此外,ABZ 可抑制血管内皮生长因子的分泌并防止恶性腹水的形成。据报道[11],ABZ 可以通过SIRT3/ROS/P38 MAPK/TTP 轴上调肿瘤坏死因子α(TNF-α)的水平,从而发挥抗肿瘤的作用。

图3 ABZ 在再狭窄小鼠模型中对内膜增生的抑制作用Fig 3 Effect of ABZ on intimal hyperplasia in a murine model of restenosis

图4 ABZ 对CFL 和MLC 磷酸化的影响Fig 4 Effects of ABZ on CFL and MLC phosphorylation
本研究结果表明,ABZ 还可以抑制血管平滑肌细胞的增殖和迁移。这与微管组织的破坏和其他细胞骨架成分如丝状肌动蛋白分布的继发变化有关。ABZ 处理可能导致细胞骨架蛋白的重排,从而影响了VSMCs 的生物学功能。尽管由ABZ 诱导的凋亡可能有助于抑制作用,但该因素在血管狭窄模型中并非主要决定因素。重要的是,ABZ治疗可有效减少动脉损伤后新内膜的形成,而该作用被认为是通过在损伤部位抑制VSMCs 增殖和迁移介导的,而且并不影响体内血管的再内皮化。因此,该疗法可用于治疗与病理性VSMCs 增殖有关的血管疾病。另外,ABZ 的优势还在于具有较低的不良反应风险,并且这种低毒效应即使在人体中进行长期服用亦是如此[9]。在本研究中,我们也未观察到明显的不良反应。
目前,有关VSMCs 迁移的分子机制已得到充分描述,其始于将外部配体结合转化为内部生化事件的生长因子和炎症细胞因子受体的结合,包括PDGF、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)和肿瘤坏死因子在内的多种可溶性配体复合物能够在VSMCs诱导迁移[12]。而参与VSMC 迁移的蛋白主要包括GTPases(如RhoA 和Rac1)、丝裂原激活的蛋白(mitogen-activated protein,MAP)激酶(如p38)以及细胞骨架和肌动蛋白重构蛋白[如CFL、MLC 及热休克蛋白(heat shock protein,HSP)27]。这些蛋白的协调激活使平滑肌细胞突出伪足,实现肌动蛋白重构,并允许细胞向趋化刺激迁移。MLC 磷酸化是SMC 迁移中必不可少的生化事件,因为它启动了肌球蛋白ATPase 活性、肌动蛋白聚合以及组织定向细胞运动所必需的功能性肌动蛋白-肌球蛋白运动单位[13]。许多趋化性细胞因子通过激活MLC 磷酸化来启动迁移[13]。另外,MAPK 诱导的细胞迁移需要MLC 磷酸化[13]。本研究检测到ABZ 处理后能够显著降低MLC 的磷酸化。之前的研究[8]显示,CFL 在未刺激的VSMCs 中以磷酸化状态存在,当出现PDGF 激活后,其活性受去磷酸化作用的调节,从而使其能够与迁移细胞的主要片状脂膜上的F- 肌动蛋白结合影响VSMCs 的迁移。在本研究中,我们观察到了CFL磷酸化水平在ABZ 处理的细胞中出现升高的现象。
本研究存在一些不足之处。在ABZ 对细胞增殖抑制的分子机制上,之前的研究显示ABZ 能够通过影响细胞周期蛋白复合物M 期促进因子(M-phase promoting factor,MPF)中Cdc2、cyclinA 及cyclin B 的磷酸化抑制细胞由G2期向M 期的转化[9],本研究并未进行检测,可能需要在以后的研究中进一步明确。其次,有研究认为,在发生损伤的血管中,VSMCs 会出现表型转化,其特征为收缩标志物表达减少,同时增殖、迁移和细胞外基质标志物表达增加[14]。本研究中对血管的H-E 染色结果提示,VSMCs 在损伤血管中的增殖和迁移显著增加。然而,在具体的分子信号机制中,仍需进一步探索。
综上所述,本研究结果表明,ABZ 通过影响细胞骨架蛋白上CFL 和MLC 的磷酸化,抑制VSMCs 迁移和内膜增生。该结果提示,ABZ 可能是新内膜增生和血管阻塞性疾病的重要治疗药物。
参·考·文·献
[1] Harskamp RE, Williams JB, Hill RC, et al. Saphenous vein graft failure and clinical outcomes: toward a surrogate end point in patients following coronary artery bypass surgery?[J]. Am Heart J, 2013, 165(5): 639-643.
[2] Antoniadis AP, Mortier P, Kassab G, et al. Biomechanical modeling to improve coronary artery bifurcation stenting: expert review document on techniques and clinical implementation[J]. JACC Cardiovasc Interv, 2015, 8(10): 1281- 1296.
[3] Buccheri D, Piraino D, Andolina G, et al. Understanding and managing in-stent restenosis: a review of clinical data, from pathogenesis to treatment[J]. J Thorac Dis, 2016, 8(10): E1150-E1162.
[4] Chistiakov DA, Orekhov AN, Bobryshev YV. Vascular smooth muscle cell in atherosclerosis[J]. Acta Physiol (Oxf), 2015, 214(1): 33-50.
[5] Küster T, Stadelmann B, Aeschbacher D, et al. Activities of fenbendazole in comparison with albendazole against echinococcus multilocularis metacestodes in vitro and in a murine infection model[J]. Int J Antimicrob Agents, 2014, 43(4): 335-342.
[6] Zhang QL, Lian DD, Zhu MJ, et al. Antitumor effect of albendazole on cutaneous squamous cell carcinoma (SCC) cells[J]. Biomed Res Int, 2019, 2019: 3689517.
[7] Zhou F, Du J, Wang J. Albendazole inhibits HIF-1α-dependent glycolysis and VEGF expression in non-small cell lung cancer cells[J]. Mol Cell Biochem, 2017, 428(1-2): 171-178.
[8] Ji Y, Weng Z, Fish P, et al. Pharmacological targeting of plasminogen activator inhibitor-1 decreases vascular smooth muscle cell migration and neointima formation[J]. Arterioscler Thromb Vasc Biol, 2016, 36(11): 2167-2175.
[9] Zhang X, Zhao J, Gao X, et al. Anthelmintic drug albendazole arrests human gastric cancer cells at the mitotic phase and induces apoptosis[J]. Exp Ther Med, 2017, 13(2): 595-603.
[10] Králová V, Hanušová V, Staňková P, et al. Antiproliferative effect of benzimidazole anthelmintics albendazole, ricobendazole, and flubendazole in intestinal cancer cell lines[J]. Anticancer Drugs, 2013, 24(9): 911-919.
[11] Wang LJ, Lee YC, Huang CH, et al. Non-mitotic effect of albendazole triggers apoptosis of human leukemia cells via SIRT3/ROS/p38 MAPK/TTP Axismediated TNF-α upregulation[J]. Biochem Pharmacol, 2019, 162: 154-168.
[12] Ray M, Autieri MV. Regulation of pro- and anti-atherogenic cytokines[J]. Cytokine, 2019, 122: 154175.
[13] Karki P, Birukov KG. Rho and reactive oxygen species at crossroads of endothelial permeability and inflammation[J]. Antioxid Redox Signal, 2019, 31(13): 1009-1022.
[14] Zhang YN, Xie BD, Sun L, et al. Phenotypic switching of vascular smooth muscle cells in the 'normal region' of aorta from atherosclerosis patients is regulated by mir-145[J]. J Cell Mol Med, 2016, 20(6): 1049-1061.
