生物质气化工艺废水特征及预处理实验研究*
2020-07-06谢建军陈程远杨文申
谢建军,陈程远,杨文申,郎 林
(1.中国科学院广州能源研究所,广州 510640;2.中国科学院可再生能源重点实验室,广州 510640;3.广东省新能源和可再生能源研究开发与应用重点实验室;4.中国科学院大学,北京 100049)
0 引 言
生物质气化技术需配套净化、余热回收工艺以提高燃气洁净度并增加能量利用效率。燃气净化及余热利用设备如水喷淋塔、余热回收锅炉等通常以水为介质,高温粗燃气与之直接或间接接触进行净化或换热,在这些过程中水往往循环使用。但随循环次数增加,水体中逐渐混入大量粉尘、飞灰和焦油,水质由此变差。循环水中特征污染物[1]为有机污染物、挥发酚、NH3-N、固体颗粒,属难降解高浓度有机废水;且经历循环后水温维持在50℃~60℃,较高温度导致无组织排放少量恶臭气体。危害用水设备的顺利运行且污染现场工作环境。因此亟需开展生物质气化工艺废水处理研究。
煤气化废水与生物质气化产生的废水具有一定相似性,其处理方法可作为借鉴参考[2-5]。综合起来,针对此类废水的处理有物理、化学与生物法。物理处理法[6-7]主要有萃取、吸附、膜分离等。化学处理法[7-9]是指利用化学反应来处理废水的方法,包括化学沉淀法、焚烧法、化学氧化法、等离子体氧化法等,经上述处理可满足排放的要求。生物法[10-12]是在无氧或有氧条件下,废水中的有机物作为相关微生物的营养物质而被氧化分解,从而降低废水中有机物浓度来达到净化的目的。
生物质气化废水组成区别于煤气化废水,前者含有大量的焦油、粉尘等杂质[13]。其中含有的化合物数量达300 多种,多为单环、多环芳烃;粉尘是半焦、灰分、残炭的总称。因此,生物质气化废水净化有其独特性和复杂性[14-16]:生物质气化废水是液固混合悬浊液,所含有机物浓度是煤气化废水的数倍,处理起来难度很大;新增废水量较少,且可生化降解性能差,不适宜采用生化处理法。
现阶段缺乏对生物质气化废水水质成分特性分析数据,更无针对性的简单且有效的处理手段。本文拟对生物质气化试验现场产生的废水进行水质水量分析,并以生物质气化废水为对象,进行减压蒸馏、芬顿氧化预处理实验研究,探索废水中化学需氧量(chemical oxygen demand,COD)、NH4-N 等的最佳预处理条件。实验结果得到的较洁净废水一方面可作为燃气净化及余热回收设备的循环回用补充水,另一方面亦可降低后续生物处理的进水负荷,为开发生物质气化废水深度净化工艺提供基础数据。
1 实验部分
1.1 实验水样
实验使用的废水水样取自生物质气化试验现场的储水池。储水池与粗燃气水喷淋塔、余热回收锅炉等相连,生物质气化工艺配套公用工程的排水、循环回用水经混合池混合后储存于此。废水呈深棕色,并混有较多黑色颗粒物而相对黏稠。
1.2 废水处理方法
废水预处理实验包括减压蒸馏、芬顿氧化两步序贯操作,具体如下。
1.2.1 减压蒸馏
减压蒸馏实验装置包括旋转蒸发仪、恒温水浴锅、低温冷却水循环泵和真空泵4 个主要部分。减压蒸馏实验步骤如下:①将低温冷却水循环泵开启,设置水温5℃,并连接旋转蒸发仪;②在抽滤装置上滤去废水中的大颗粒固体杂质;③取过滤后的废水150 mL,置入旋转蒸发仪的蒸馏瓶;④连接真空泵,加热恒温水浴锅的水浴温度至70℃~95℃;⑤设置旋转速率为50~100 r/min;⑥将蒸馏瓶置入恒温水浴,并设置真空度开始蒸馏。待实验完毕后留置蒸出液及蒸余液,测定各项水质指标,并记录旋转蒸发时间、蒸出液与蒸余液体积。蒸出液继续经芬顿氧化处理;蒸余液含碳量较高,具有一定的热值,可与生物质原料混合后送入气化炉气化。
1.2.2 芬顿氧化
芬顿氧化指以H2O2为氧化剂,对废水中的还原态化合物进行无选择性氧化,以去除COD 等污染物的过程。Fe2+离子存在时可强化H2O2的氧化能力[7]。实验过程为将1.2.1 节减压蒸馏实验得到的清液20 mL 倒入平底烧杯,加入FeSO4粉末,再用磁力搅拌子搅拌至完全溶解后,加入H2SO4溶液将蒸馏清液的pH 值调为2~4,混合均匀后再缓慢加入H2O2常温搅拌反应若干小时,随即加入少量NaOH溶液将pH 调节到10 左右,并在70℃水浴中反应2 h,以使Fe2+及Fe3+离子完全沉淀。然后在8 000 r/min转速下离心沉淀5 min,取上清液二次离心后,再在70℃水浴里反应1.5 h,以确保未完全反应的H2O2被NaOH 分解。
1.3 分析方法
利用HACH DR3900 分光光度计分别采用消解比色法、水杨酸法[17]测定废水中的COD 和NH4-N含量。在测定COD 之前,需将废水于150℃下采用HACH DRB200 消解反应仪消解2 h。
采用德国Elementar 仪器公司Vario TOC 分析仪测定水样中的溶解性总有机碳(total organic carbon,TOC)和总氮(total nitrogen,TN)。测定前需对样品进行预处理,以避免其中的强碱腐蚀测试仪器。样品预处理过程如下:①加入适量色谱纯磷酸,将样品中的NaOH 中和,使呈弱酸性;②将样品稀释至一定浓度,使其在仪器上的响应正好处于事先标定好的工作曲线区间内;③利用水相纳滤滤膜将样品过滤,避免样品中固体颗粒损坏仪器。
经过预处理后,先用样品冲洗TOC 分析仪约2 min,待分析仪信号稳定后即可进样;利用事先做好的标准曲线进行定量计算,扣除空白样数值,并根据稀释倍数进行换算,即可得TOC、TN 含量,结果以mg/L 表示。
2 结果与讨论
2.1 生物质气化工艺废水特征
2.1.1 水量特点
位于广东省某地的生物质气化试验现场采用固定床将生物质气化得到可燃气体。该气化炉最大加料量为1 500 kg/h,负荷在30%~100%之间连续可调。
进入气化炉的生物质原料通常含5%~30%水分,部分参与生物质的水蒸气气化反应被消耗,其余水分则呈气态混入高温粗燃气中;此外,原料中H 组分被氧化后,也以水蒸气的形式存在于粗燃气。这些水蒸气经后续的粗燃气余热回收及水喷淋净化后,最终流入储水池。这两部分水是构成生物质气化工艺废水增加量的主要来源。
循环水在水喷淋塔、间接换热器内与温度较高的粗燃气换热而被加热至60℃左右,由于水喷淋塔底部的水封、澄清池、储水池与大气相通,循环水可能蒸发并逃逸到周围的大气环境,从而导致总水量减少。因此整个工艺的废水量是否增加,与水蒸发、水冷凝、生物质水蒸气气化反应、气温、晴雨天气等气象因素,或增加盖板等封闭措施有关。
生物质气化原料为玉米秸秆颗粒、松木树皮颗粒与废纸,加料量约500 kg/h,连续运行的每天9:00记录澄清池水位,计算得到废水增量。结果见表1。
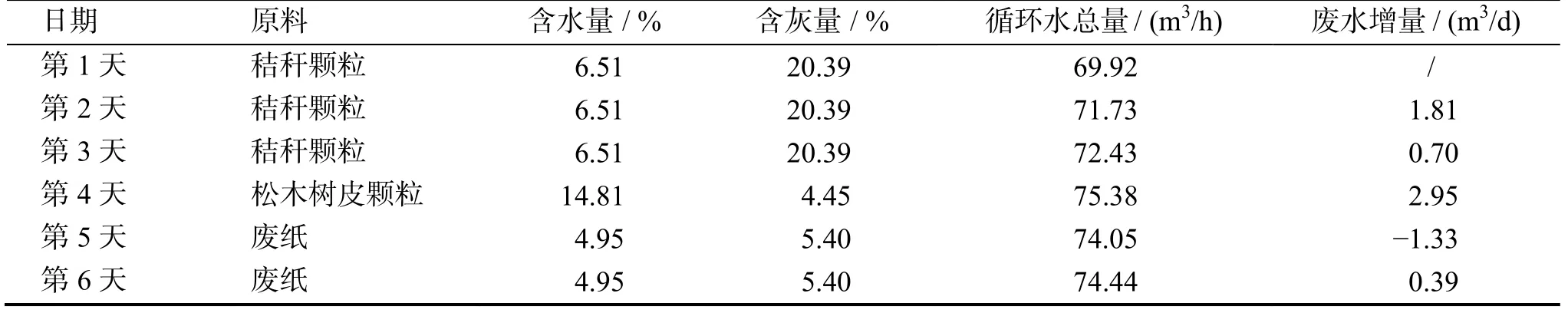
表1 生物质气化工艺循环用水总量与增加量Table 1 Total amount and increase of circulating wastewater for biomass gasification process
由表1 可见,在6 天连续运行过程中,试验装置系统循环水总量为69.92~75.38 m3/h,废水增加总量为4.52 m3。所使用的几种原料水分在5%~15%之间,其中烧秸秆颗粒(含水量6.5%)时,水分增加较缓慢;当烧含水量14.8%的树皮颗粒时,水量增加较明显;接着改烧废纸(含水量5%)后,废水总量增加不明显甚至有小幅度下降,表明原料含水量对废水增量影响较大。
2.1.2 水质特点
取储水池中的废水进行挥发酚、TN、NH4-N、五日生化需氧量(BOD5)、COD 等水质参数分析,结果见表2。

表2 生物质气化工艺废水水质分析结果Table 2 Analysis of wastewater from biomass gasification
由表2 可见,生物质气化工艺废水水质有如下特点:①有机物浓度较高,COD 值为8.00×104mg/L,远大于煤炭焦化废水;②含挥发酚1.81×103mg/L,其含量高、毒性大,不利于大部分生化细菌的生长;③所含挥发酚、NH4-N 与煤焦化废水基本处于相同数量级水平;④计算得到BOD5/COD 值为0.12,表明该废水可生化降解性能较差(<0.30)。
2.2 废水预处理实验
2.2.1 减压蒸馏
本节考察蒸发温度、真空度、旋转速率等因素对废水减压蒸馏过程的影响。实验发现,提高蒸发温度和真空度,均可使废水蒸发速度加快,从而减少处理时间,并得到较多的蒸出液。当废水含灰量较高时,起始沸腾需要相对较高的真空度;当废水COD 较高时,起始沸腾可在较低的真空度下进行。最佳实验条件为温度85~90℃、真空度 −0.07~−0.095 MPa、旋转速率50~100 r/min。在此条件下,150 mL 废水经旋转蒸发30~60 min 后,得到的蒸馏清液呈较澄清透明的淡黄色。取原废水、蒸出液进行COD、NH4-N、TN、TOC 分析,结果如图1所示。

图1 原废水与减压蒸馏蒸出液的水质参数对比Fig.1 Comparison of water quality parameters between raw wastewater and distillated from vacuum distillation
由图1 可见,经过减压蒸馏,废水COD 含量从8.00×104mg/L 下降为2.05×104mg/L,COD 脱除率为74.38%;蒸余液COD 含量3.00×105mg/L。蒸馏清液的其他水质参数如NH4-N、TN、TOC 的脱除率超过75%,尤其是NH4-N 含量,从2.58×103mg/L下降至143 mg/L,降低幅度达94.46%,可能与废水中的铵盐受热后更易以NH3的形式逃逸有关。这表明减压蒸馏具有较好的清污分离效果。
实验还发现,蒸余液与蒸馏清液体积(分别为22 mL、120 mL)之和略小于原废水体积。这主要是如下两方面的原因:①部分液体残留在冷凝管及容器壁无法完全回收;②由于冷凝效率所限,可能部分物质如水及低沸点有机物等未被全部冷凝,被真空泵的负压所带出而损失。
2.2.2 芬顿氧化
取2.2.1 节减压蒸馏清液进行芬顿氧化预处理研究,考察了H2O2与蒸馏清液质量比、H2O2与Fe2+摩尔比、反应时间、H2O2浓度等因素对COD、NH4-N、TOC、TN 等脱除率的影响。
(1)H2O2与蒸馏清液质量比的影响
在Fe2+与H2O2的摩尔比1∶1、H2O2与蒸馏清液的质量比2.10%~33.50%、反应时间8 h 条件下,考察了H2O2与蒸馏清液的质量比的影响。实验过程中发现,取30%H2O2加入到蒸馏清液30 s 后,开始冒出气泡,约1 min 后水面上的泡沫开始消失,此时溶液从淡黄色变成红褐色,且放热剧烈,用手触摸烧杯壁能察觉明显的温升,表明有机物被氧化并伴随CO2析出;约1 h 后,溶液再次变为酒红色至砖红色,这表明Fe2+被氧化成为了Fe3+。图2 给出了H2O2与蒸馏清液质量比对COD、TOC、NH4-N、TN 浓度的影响。
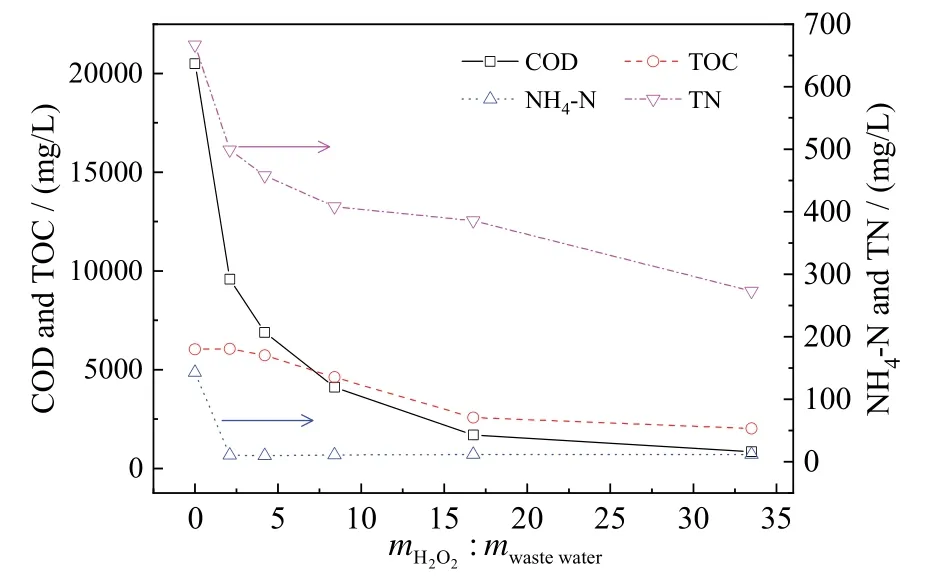
图2 H2O2 与蒸馏清液质量比对COD、TOC、NH4-N、TN浓度的影响Fig.2 Effect of mass ratio of H2O2 to distilled liquid on concentrations of COD,TOC,NH4-N,and TN
H2O2产生自由氧的半反应如下:

O∙能将有机物无选择性地氧化,尤其是可对含苯环的物质氧化矿化,因此理论上H2O2与蒸馏清液质量比越高越好。由图2 可见,随H2O2加入量增加,蒸馏清液COD、TOC、NH4-N、TN 均出现不同程度的下降。当加入2.10%的H2O2后,蒸馏清液COD、TOC、NH4-N 含量均急剧下降,其中NH4-N 的含量下降至10.5 mg/L,下降趋势最为明显,但TN 的含量基本保持不变;随H2O2加入量继续增加,COD、TOC、TN 等的含量进一步下降,并最终达到稳定值。总体而言,当H2O2与蒸馏清液的质量比从2.10%增加到33.50%,COD、TOC 从最初的2.05×104mg/L、6.04×104mg/L分别下降至843 mg/L、2.02×103mg/L;NH4-N、TN 从143 mg/L、667 mg/L 分别降至11.6 mg/L与273 mg/L,下降幅度很明显。这表明H2O2是良好的废水氧化剂,且氧化性能的高低与H2O2加入量的大小呈明显的正相关关系。
由图2 计算得到,H2O2与蒸馏清液的质量比为33.50%时,出现COD、TOC、TN 脱除率最大值,分别为95.89%、66.53%和59.06%。在所研究的实验范围,NH4-N 脱除率则介于91.89%~92.66%之间,基本保持不变。由图2 还可得出,上述4 种污染物被H2O2氧化的难易程度顺序为NH4-N>COD>TN>TOC。这可能与特征污染物的氧化−还原反应电位及初始浓度有关。为降低H2O2使用成本,最佳H2O2与蒸馏清液质量比以8%~15%为宜。
(2)H2O2与Fe2+摩尔比的影响
Fe2+离子存在时可强化H2O2的氧化能力,由于Fe2+离子可与H2O2反应生成氧化能力更强的HO·自由基:

因此,较高的Fe2+浓度有利于脱除污染物,但H2O2浓度过高可能会使Fe2+迅速氧化为Fe3+,从而抑制HO∙自由基的生成。本节研究H2O2与Fe2+摩尔比对蒸馏清液中几种典型污染物脱除率的影响。在实验过程中,恒定30%H2O2质量与蒸馏清液质量的比值为8.40%不变,并通过改变FeSO4∙7H2O 的加入质量来调节Fe2+与H2O2摩尔比至0.13~2.00 之间,搅拌反应持续8 h 后考察蒸馏清液中COD、NH4-N、TOC、TN 等污染物的脱除率。实验结果如图3。

图3 Fe2+与H2O2 摩尔比对COD、NH4-N、TOC、TN 脱除率的影响Fig.3 Effect of molar ratio of Fe2+ to H2O2 on removal efficiencies of COD,NH4-N,TOC and TN
由图3 可见,随Fe2+/H2O2摩尔比上升,NH4-N与TN 脱除率呈现单调递增的规律,但提高幅度不大;而COD 及TOC 的脱除率则出现先降低后上升的变化趋势。综合考虑COD、NH4-N、TOC、TN这4 种特征污染物的脱除性能,最佳的脱除率出现在Fe2+与H2O2摩尔比为1.0 的情形,在此条件下,COD、NH4-N、TOC、TN 脱除率分别为79.21%、90.84%、66.16%和88.37%,这与理论计算的结果相一致[8]。
(3)反应时间的影响
对于给定的化学反应而言,随反应进行,反应物浓度会不断降低,反应速率因而也变得越来越慢。该情形下反应速率虽慢但化学反应还在继续进行,因此反应物尚在消耗,产物得率亦随之缓慢上升。然而从废水处理工程实践的角度,往往希望能在较短的时间里得到最佳的反应效果。因此本节考察了废水芬顿氧化反应时间对污染物脱除率的影响。
在H2O2与蒸馏清液质量比为33.50%、H2O2与Fe2+摩尔比为1.0 条件下,分别反应到第8 h 和第21 h 后取样,分析蒸馏清液COD、NH4-N、TOC、TN 含量并计算其脱除率,实验结果见图4。由图4可见,将反应时间从8 h 延长到21 h,对提高COD及NH4-N 脱除率并无帮助,但可大幅度提高TOC与TN 的脱除率,这可能和COD、NH4-N 与H2O2的氧化−还原反应速率较快有关,即反应在8 h 内已达化学平衡,因此蒸馏清液中COD 及NH4-N 浓度基本保持不变。而TOC、TN 较COD、NH4-N 更难被H2O2氧化,因此延长反应时间有利于提高TOC、TN 脱除率。

图4 H2O2 与蒸馏清液的质量比为33.50%时反应时间对COD、NH4-N、TOC、TN 脱除率的影响Fig.4 Effect of reaction time on the removal efficiencies of COD,NH4-N,TOC and TN when the mass ratio of H2O2 to distilled liquid was kept at 33.50%
(4)H2O2浓度的影响
生物质气化废水组成复杂,化学活泼性各异,既有结构简单的脂肪酸,也有较稳定的烷基、甲氧基苯,还有多种酚类化合物,它们与H2O2的反应速率也有差别。由于H2O2在Fe2+作用下分解成羟基自由基HO∙的速度很快,HO∙具有很高的电负性或亲电性,如果在废水中搅拌不充分、或局部区域HO∙过剩的情况下,可能发生HO∙与其他物质分子之间的湮灭反应,从而降低特征污染物的脱除效率。因此本节考察了H2O2的质量浓度对特征污染物脱除率的影响。
实验过程中保持H2O2与蒸馏清液的质量比为8.40%、Fe2+与H2O2摩尔比为0.25,改变H2O2的质量百分比浓度(10%~30%),反应8 h 后,取样分析并计算蒸馏清液特征污染物的脱除率。结果如图5 所示。

图5 H2O2 浓度对COD、NH4-N、TOC、TN 脱除率的影响Fig.5 Effect of H2O2 concentration on removal efficiencies of COD,NH4-N,TOC and TN
由图5 可见,将H2O2的质量百分比浓度从10%提高到30%,COD、TOC、NH4-N 的脱除率基本保持不变,分别为82.8%、81.2%、42.4%;TN 脱除率略有上升,从18.1%提高到24.3%。这表明改变H2O2浓度对上述几种特征污染物脱除率的影响不大。
3 结 论
对生物质气化试验现场产生的废水进行了水质水量分析,并进行了废水减压蒸馏、芬顿氧化预处理实验研究,结论如下:
(1)生物质气化工艺废水COD 为8.00×104mg/L,具有有机物浓度高、可生化降解性差、水量小的特点。
(2)在85~90℃、真空度−0.07~−0.095 MPa条件下进行废水减压蒸馏,得到较澄清的蒸馏清液,其体积约为原废水的90%;COD、NH4-N 脱除率分别为74.38%、94.46%。蒸余液含碳量较高,可直接回气化炉进行气化。
(3)芬顿氧化过程中将H2O2(30%质量浓度)与蒸馏清液的质量比从2.10%提高到33.50%,污染物脱除率上升;当H2O2与蒸馏清液质量比为8.40%,可将COD 从2.05×104mg/L 降至4.11×103mg/L,NH4-N 从143 mg/L 降至11.1 mg/L。经处理后废水的NH4-N 已满足国家污水排放二级标准,但COD尚需进一步处理。
