UPLC/Q Exactive MS 快速测定食蟹猴体内黄藤素的血药浓度
2020-07-04张培培崔佳丽周艺佳刘红斌
张培培,崔佳丽,周艺佳,刘红斌,柯 瑾
(1) 昆明卫生职业学院药学院,云南昆明 650600;2) 云南白药集团药物安全性评价中心,云南昆明 650111;3) 云南中医药大学中药学院,云南昆明 650500)
黄藤为防己科植物黄藤Fibraurea recisa Pierre.的干燥藤茎,又名天仙藤、土黄连、金锁匙、藤黄连等,主要分布在我国的云南、广西、广东等地以及越南、柬埔寨、缅甸,是当地少数民族常用的中药和天然染料[1]。现收载于2015年版《中国药典》,其味苦,性寒,归心、肝经,具有清热解毒、泻火通便的功效[2],而且能够防治多种感染性疾病,如妇科炎症、外科感染、菌痢、肠炎、呼吸道感染、眼结膜炎等[3]。黄藤中抗菌主要有效成分为黄藤素(C21H22ClNO4,387.86),又名盐酸巴马汀、盐酸棕榈碱、掌叶防已碱、非洲防已碱等,是中国首先自行研制的纯天然植物药,被当代医学称为“植物抗生素”。在一定程度上,弥补化学抗生素问题[4]。
随着现代分析仪器的发展,黄藤素的体内、外药物分析方法不断优化,早期有学者[5-6]采用紫外分光光度法进行黄藤素测定,随着高效液相色谱仪(HPLC) 的普及,逐渐采用HPLC 法[7-12]测定黄藤素片、注射液、粉针剂等制剂中黄藤素的含量。黄藤素体内药物分析方法很多,有高效液相色 谱-荧 光 检 测(HPLC-FLU) 法[13]、(RP)-HPLC 法[14-15]等。由于黄藤素口服吸收较差[16-17],体内血药浓度较低,因此需要建立灵敏度更高的分析测定方法。有学者[18-19]采用液质联用的技术进行黄藤素血药浓度分析。为了进一步提高分析速度、简化样品处理过程,本研究建立一种特异性强、准确、快速、灵敏的UPLC-Q Exactive-MS 测定方法[20],按照《中国药典》 (2015年版) 四部“生物样品定量分析方法验证指导原则”项下进行方法学验证,为黄藤素药代及毒代研究提供方法参考。
1 材料与方法
1.1 材料
1.1.1 试药黄藤素对照品(盐酸巴马汀,PMH,C21H22ClNO4,相对分子量为387.86,含量为86.8%,批号110732-201611,中国食品药品检定研究院) ;内标盐酸小檗碱对照品(C20H18ClNO4,相对分子量为371.81,含量为86.7%,批号110713-201212,中国食品药品检定研究院);食蟹猴空白血浆(广东悦源动物养殖有限公司,合格证号:SCXK(粤) 2015-0038,15%EDTA-Na2 抗凝)。
1.1.2 试剂甲酸(批号10K11-F211,Admas);乙腈为质谱纯(J.T.Baker),实验用水为超纯水。
1.1.3 仪器Thermo UltiMate 3000 液相色谱系统(美国赛默飞),Qexactive 四极杆-静电场轨道阱高分辨质谱仪(美国赛默飞),MD200 氮气吹扫仪(杭州奥盛仪器有限公司),DV215CD 分析天平(奥豪斯仪器(上海) 有限公司),XW-80A 涡旋混合仪(上海精科实来有限公司),Allegra64R 高速离心机(美国BECKMAN COULTER 公司),Research 移液器(美国Eppendorf 公司)。
1.2 方法
1.2.1 含量测定条件研究色谱柱Hypersil GOLD Dim C18(100 mm×2.1 mm,1.9 μm);流动相为乙腈B-水A(含0.1%甲酸),流速为0.3 mL/min,柱温30℃,进样10 μL,分析时间为5 min。
质谱条件研究:电喷雾离子源(ESI),正离子方式检测;喷雾电压3.50 kV;毛细管温度350℃;离子源温度350℃;鞘气和辅助气分别为35 arb 和12 arb;S-lens RF 电压为50 V;扫描方式采用正离子t-SIM 模式,分辨率(R) 70000FWHM,自动增益控制(AGC) 和离子注入时间(IT) 分别设为5e4 和200 ms;isolation window 设为4.0 m/z,选择离子通道:PMH,[M-Cl]+,m/z 352.154 33;盐酸小檗碱(IS),[M-Cl]+,m/z 336.12303。喷雾气为氮气,碰撞气为高纯氮气。
1.2.2 试剂配制(1) PMH 对照品溶液的配制:分别精密称取黄藤素对照品5.91、5.87 mg,至已校验25 mL 容量瓶中,加乙腈溶解后定容至刻度,摇匀,得浓度分别为0.205 和0.204 g/L(浓度计算时以含量86.8%进行折算) 的黄藤素标准储备液,同法配制两份,其中浓度高的作为校正曲线用储备液,另一份作为质控用储备液,2 ℃~8℃冰箱保存备用。并进行配制重现性考察和2℃~8℃冷藏70 d 稳定性考察,结果显示配制重现性符合要求,此条件下PMH 稳定。临用前,校正曲线储备液用乙腈按比例稀释制成浓度分别为0.525、1.05、2.62、6.56、16.4 和41.0 mg/L 系列PMH 标准工作液;质控储备液同法制成浓度分别为0.832、5.20和32.6 mg/L 系列质控工作液;(2) 盐酸小檗碱标准溶液配制:精密称取内标盐酸小檗碱5.86 mg,转至已校验50 mL 容量瓶,加乙腈溶解后定容至刻度,摇匀,得浓度为0.102 g/L (浓度计算时以含量86.7%进行折算) 的内标储备液,取盐酸小檗碱内标储备液10~1 000 mL 容量瓶中,加乙腈定容至刻度,混匀,得浓度为1.02 mg/L 的盐酸小檗碱工作液,2℃~8℃冰箱保存备用;(3) 0.1%甲酸溶液配制:精确吸取甲酸1.0 mL,用超纯水稀释并且定容到1 L,0.22 μm 微孔滤膜抽滤后,超声5 min 后再使用。
1.2.3 血浆样品处理精密吸取食蟹猴血浆50 μL至对应用记号笔标识的1.5 mL 离心管中,再精密加入400 μL 盐酸小檗碱内标工作液,涡旋2 min,于2~8 ℃,15 000 r/min 离心10 min,取上清液50 μL,加入乙腈950 μL 涡旋混匀,再从前述混匀液中取50 μL,加入乙腈950?L 涡旋混匀,于2~8℃,15 000 r/min 离心10 min,取出上清液适量至进样瓶中,即得。
1.2.4 体内药物分析方法学验证(1) 特异性 取食蟹猴空白血浆5 份、空白血浆+MPH+IS 1 份、预实验中获得的第1 批给药后第1 个采血时间点任一样品,按“1.2.3 血浆样品处理”项下操作,比较各图谱,考察方法特异性。(2) 残留考察 按“1.2.3 血浆样品处理”项下操作,制备5 份空白样品、5 份标曲最低浓度点样品及1 份标曲最高浓度点样品,按照“高浓度-空白样品”间隔进样,计算每一空白血浆样品中黄藤素峰面积与5 份标曲最低浓度点测定所得峰面积平均值的比值,应小于20%;同时计算每一空白血浆样品中IS 峰面积与5份标曲最低浓度点测定所得IS 峰面积平均值的比值,应小于5%。(3) 基质效应考察 精密吸取5 μL 低、中、高浓度PMH(0.832、5.20 和32.6 mg/L) 质控样品溶液,再精密吸取“1.2.2(2) 盐酸小檗碱标准溶液”项下1.02 mg/L 的盐酸小檗碱工作液20 μL,常温氮吹至干。取50 μL 空白食蟹猴血浆至另一1.5 mL 离心管中,精密加入400 μL乙腈,涡旋2 min,于2℃~8℃条件下15 000 r/min离心10 min,精密移取上清液225 μL 至前述1.5 mL 离心管中,后续按“1.2.3 血浆样品处理”项下操作,各浓度平行5 份,分析测定得到的黄藤素峰面积(PS 有) 和盐酸小檗碱峰面积(PIS 有)。以水代替空白食蟹猴血浆,精密吸取10 μL 低、中、高浓度PMH 质控样品溶液,按“1.2.3 血浆样品处理”项下操作,各浓度平行5 份,分析测定得到的黄藤素峰面积(PS 无) 和盐酸小檗碱内标峰面积(PIS 无)。
黄藤素基质效应计算分公式:MFS%=PS 有/PS 无×100。
盐酸小檗碱基质效应计算公式:MFIS%=PIS有/PIS 无×100。
同一样品黄藤素的基质效应与内标盐酸小檗碱的基质效应的比值,即为归一化基质效应因子。归一化基质效应因子相对标准差应小于15%。(4)线性关系考察 精密吸取浓度为0.525、1.05、2.62、6.56、16.4 和41.0 mg/L 系列PMH 标准工作液10?L,氮气吹干后,按“1.2.3 血浆样品处理”项下操作,以盐酸巴马汀峰面积(Ab) 和内标峰面积(Ah) 的比值为纵坐标Y,盐酸巴马汀工作液浓度的1/5 为横坐标X,用加权(1/X2) 最小二乘法拟合,不过原点,分别获得每一批标准曲线回归方程。方程相关系数r2应不小于0.99。(5) 批内与批间精密度考察 精密吸取10 μL 低、中、高浓度PMH(0.832、5.20 和32.6 mg/L) 质控样品溶液和0.525 mg/L 的PMH 校正溶液,按“1.2.3 血浆样品处理”项下操作,各浓度平行5 份,连续测定3 批(每天一批),用随行校正曲线计算质控样品的浓度,分别表示批内与批间精密度,定量下限的RSD<20%,其余浓度RSD<15%。(6) 批内与批间准确度考察 与前述“(5) 批内与批间精密度考察”平行进行,用随行校正曲线计算质控样品的浓度后,计算每一浓度测定的平均值与标示值的比值?100%,分别表示批内与批间准确度,定量下限批内与批间准确度应在80%~120%,其余浓度应在85%~115%范围内。(7) 稳定性考察 进样溶液稳定性考察:精密吸取10 μL 低、中、高浓度PMH(0.832、5.20 和32.6 mg/L) 质控样品溶液,氮气吹干后,按“1.2.3 血浆样品处理”项下操作,制备成进样溶液后,分别置室温和2℃~8℃存放置2 d,每个浓度每个时间点平行5 份。
未处理血浆样品稳定性考察:精密吸取10 μL 低、中、高浓度PMH(0.832、5.20 和32.6 mg/L) 质控样品溶液,氮气吹干后,加入50 μL 空白血浆,涡旋混匀后,分别于室温放置1 d、-20℃存放35 d 室温冻融3 次和-20℃存放1 d、10 d、35 d 的稳定性。每个浓度每个时间点平行5份,后按“1.2.3 血浆样品处理”项下操作。
随行校正曲线计算质控样品的浓度后,计算每一浓度测定的平均值与标示值的比值×100%,应在85%~115%范围内。
1.3 统计学处理
回归方程及测定浓度为仪器工作站软件“Thermo Xcalibur”处理,其余数据应用SPSS 统计学软件进行处理,以均数±标准差() 表示。
2 结果
2.1 含量测定色谱条件
黄藤素(PMH) 和盐酸小檗碱(IS) 的保留时间分别为2.46 min 和2.47 min。洗脱条件见表1。
2.2 方法学验证结果
2.2.1 特异性考察特异性样品中虽然检测到目标物PMH 及内标盐酸小檗碱,但目标物干扰组分影响率均小于20%,内标干扰组分影响率均小于5%,说明空白血浆中的内源性物质对样品测定无干扰,见图1。
2.2.2 残留考察从测定结果可知,PMH 和内标的残留率分别为7.73%~10.37%、0.37%~0.97%,本方法的残留量对定量下限的影响可以忽略不计。
2.2.3 基质效应考察黄藤素与内标的归一化基质效应因子相对标准偏差RSD%小于15%,符合要求,见表2。
2.2.4 线性关系考察以血药浓度对峰面积比值建立回归方程,得到血浆样品中黄藤素的标准曲线,见表3。由表3 可知,血浆中黄藤素浓度在105.0~8 200 μg/L 内浓度与峰面积之间有良好的线性关系(r2>0.999)。
2.2.5 批内与批间精密度考察批内及批间精密度的RSD%均小于15%,检测方法的精密度满足要求,见表4。
2.2.6 批内与批间准确度考察不同浓度批内及批间准确度均在85%~115%范围内,检测方法的准确度满足要求,见表5。
2.2.7 稳定性考察(1) 进样溶液稳定性考察(表6):从表6 结果可知,进样溶液在室温和2~8℃存放置2 天稳定性符合要求;(2) 未处理血浆样品稳定性考察:未处理血浆样品在室温放置1 d、-20℃存放35 d 室温冻融3 次和-20℃存放1 d、7 d、35 d 的稳定性符合要求,见表7。

表1 梯度洗脱条件Tab.1 Gradient elution conditions
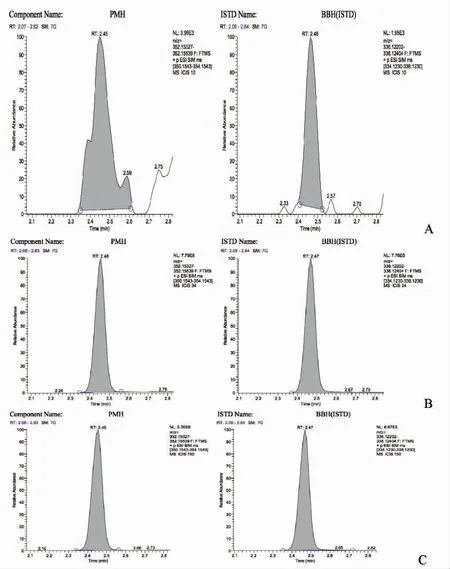
图1 血浆样品的特异性考察(SIM)Fig.1 Inspection on specificity of monkey plasma sample(SIM)
表2 黄藤素与内标基质效应[n=5,()]Tab.2 Linear relationship of PMH and IS in monkey plasma [n=5,()]

表2 黄藤素与内标基质效应[n=5,()]Tab.2 Linear relationship of PMH and IS in monkey plasma [n=5,()]

表3 黄藤素在血浆中的线性关系Tab.3 Linear relationship of PMH in monkey plasma
表4 精密度实验结果[n=5,()]Tab.4 The results of precision [n=5,()]

表4 精密度实验结果[n=5,()]Tab.4 The results of precision [n=5,()]
表5 准确度实验结果[n=5,()]Tab.5 The results of accuracy[n=5,()]
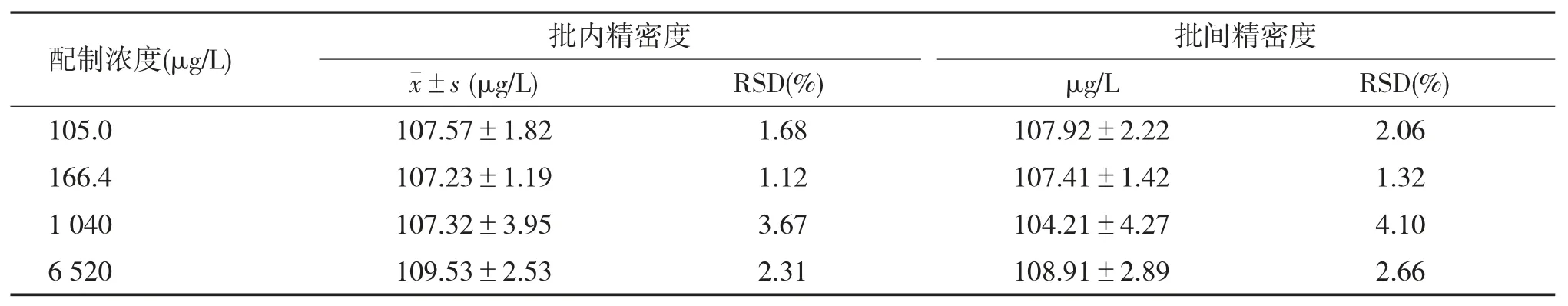
表5 准确度实验结果[n=5,()]Tab.5 The results of accuracy[n=5,()]
表6 进样溶液稳定性考察结果[n=5,()]Tab.6 The results of stability in injection solution [n=5,()]

表6 进样溶液稳定性考察结果[n=5,()]Tab.6 The results of stability in injection solution [n=5,()]
3 讨论
充分利用现代分析检测设备,建立科学、灵敏、特异、快速的黄藤素检测技术与方法,是进行黄藤素新产品研发的必要途径,是实现药品质量可控性的有力保证,也是展开药代动力学等更深层次研究的重要技术手段。本研究建立的UPLC/Q Exactive MS 快速测定食蟹猴体内黄藤素的血药浓度的方法,线性范围宽,分析时间短,准确度好、灵敏度高、特异性强,适于黄藤素药代及毒代动力学分析检测。
实验研究中发现,进样溶液浓度在0.2625~20.50 μg/L 基础上还可以降低20 倍,依然符合定量下限10 倍信噪比的要求,可为黄藤素药代动力学研究提供参考。
表7 未处理血浆稳定性考察结果[n=5,()]Tab.7 The results of stability in injection solution [n=5,()]
