紫草素通过TLR4/NF-κB信号通路抑制由LPS诱导的人牙髓细胞炎症研究
2020-07-01杜暘金鼎高秀秋
杜暘 金鼎 高秀秋
牙体牙髓病在人类口腔疾病中比较常见,由于龋病等因素导致牙髓产生炎症,会引起患牙的剧烈疼痛并导致功能障碍,给患者带来极度的不适,影响生活质量[1]。但是,有关牙髓炎症损伤修复的分子机制目前尚不明确,需进一步探索。脂多糖(lipopolysaccharide,LPS)能够引起牙髓组织发生炎症反应,从而抑制牙髓细胞的增殖、分化等[2]。Toll样受体 (Toll-likereceptors,TLRs)能识别LPS,是LPS作用受体之一,促进炎症因子释放,激活炎症相关靶基因的表达[3]。核转录因子-κB(Nuclear factor kappa B,NF-κB)以非活性的p65/p50/NF-κB抑制因子α(inhibitor of NF-κB-α,IκB-α)三聚体复合物形式存在于细胞质中[4],可以被多种因素激活,包括LPS和理化因素(X射线、氧化剂及化疗药物制剂)等[5]。在炎症疾病系统中转录因子NF-κB起着关键的作用[6],当炎症发生时,炎症细胞因子大量释放,如白细胞介素6(interleukin-6,IL-6)、白细胞介素1β(interleukin-1β,IL-1β)肿瘤坏死因子α(tumor necrosis factor,TNF-α)等[7]。TLR4/NF-κB信号通路是否参与了LPS诱导的人牙髓细胞(human dental pulp cells,HDPCs)细胞炎症目前暂无统一结论,并且开发能够拮抗LPS诱导牙髓组织炎症的天然药物是迫切解决的问题。
紫草素,又名紫草醌,是植物紫草(Lithospermiun erythrorhizon Sieb.et Zucc)中的一种有效成分,具有较强的抗炎作用[8]。研究发现[9-10],紫草素能抑制炎性反应和促炎因子的释放,促进巨噬细胞免疫负调控抑制因子白细胞介素-10(IL-10)的表达。紫草素的抗炎机制可能与TLR4和NF-κB的p65亚基磷酸化有关[11-12],但具体的分子机制还未发现。本实验研究紫草素对LPS诱导HDPCs细胞炎症的影响,初步探讨其可能的分子机制。
1 材料与方法
1.1 主要试剂与仪器
紫草素(Enzo Biochem,美国);DMEM低糖培养基、I型胶原酶、胎牛血清(FBS)、0.25%胰蛋白酶、PBS(Gibco,美国);脂多糖(LPS)、甲基噻唑基四唑(MTT)(Sigma-Aldrich,美国);Human IL-1β Platinum Elisa、Human IL-6 Platinum Elisa、Human TNF-alpha Platinum Elisa、Human IL-10 Platinum Elisa(eBioscience,美国);裂解液、SDS-PAGE配胶试剂盒、BCA蛋白试剂盒(北京康为世纪生物公司);TLR4、p-NF-κB、β-actin抗体(Cell Signaling,美国)。
1.2 HDPCs体外培养[13]
经患者知情同意后,收集锦州医科大学附属第二医院口腔科门诊就诊的患者,由于正畸或者阻生而拔除的完整并且健康的牙齿。在无菌条件下超净台中,取出牙髓组织,用PBS反复清洗3 次,剪成小块,直径约为0.5 cm,放入含3 mg/ml的I型胶原酶的EP管中,在培养箱中消化30 min,在1 000 r/min条件下,离心5 min,然后弃上清液,加入适量含20% FBS的低糖DMEM原代培养液,然后将组织块转移在25 cm2培养瓶中,倒置于5% CO2、37 ℃、相对湿度为100%的恒温培养箱中培养,6~8 h后翻瓶,在显微镜下观察细胞是否贴壁,细胞贴壁后,每3 d换液1 次。细胞长至80%时,用0.25%消化胰酶进行消化,1∶2比例进行传代培养。
1.3 MTT法检测紫草素和LPS对HDPCs的细胞毒性
取对数生长期的HDPCs(5×104个/ml)接种于96 孔板中,每孔200 μl,培养24 h,细胞长至70%~80%,吸弃孔内培养基,加入100 μl用DMEM培养基稀释含不同药物浓度的培养液(紫草素终浓度为0、12.5、25、50、100、200、400、800 μmol/L;LPS终浓度为0、0.125、0.25、0.5、1、2、4、8 μg/ml),培养24 h后,每孔加入20 μl 5 mg/ml的MTT溶液,孵育4 h。吸弃孔中液体,每孔加入150 μl DMSO,摇床上晃动10 min,用多功能酶标仪(Biotek,美国)490 nm测取吸光度,同时设置对照孔,每组设6 个复孔。
1.4 紫草素对LPS诱导的HDPCs炎症模型细胞存活率的影响
将HDPCs分为4 组,正常对照组(DMEM培养基)、模型组组(培养基中LPS浓度为1 μg/ml)、紫草素低剂量组(培养基中LPS浓度为1 μg/ml+25 μmol/L紫草素)和紫草素低剂量组(培养基中LPS浓度为1 μg/ml+50 μmol/L紫草素)。取对数生长期的HDPCs(5×104个/ml)接种于96 孔板中,每孔200 μl,培养24 h,细胞长至70%~80%,吸弃孔内培养基,按照上述分组进行给药,培养24 h后,每孔加入20 μl 5 mg/ml的MTT溶液,孵育4 h。吸弃孔中液体,每孔加入150 μl DMSO,摇床上晃动10 min,于490 nm处进行吸光度检测,同时设置对照孔,每组设6 个复孔,测定紫草素对HDPCs细胞存活率的影响。
1.5 ELISA检测细胞培养液中IL-1β、IL-6、TNF-α、IL-10含量
取对数生长期的HDPCs(1×106个/ml),接种于6 孔板中,按照“1.4”中实验分组分别加入不同受试物,培养24 h后,收集HDPCs上清液,12 000 r/min离心10 min,吸取上清至EP管中,按照ELISA试剂盒步骤测定IL-1β、IL-6、TNF-α、IL-10水平。
1.6 Western blot法检测蛋白水平
取对数生长期的HDPCs(1×106个/ml),接种于6 孔板中,按照“1.4”中实验分组分别加入不同受试物,在培养箱中培养24 h后,吸弃孔中培养基,用PBS轻轻洗涤2 次,每孔中加入60 μl裂解液,放在冰浴裂解20 min,12 000 r/min离心10 min,获得总蛋白样品。BCA法测定蛋白浓度定量后,在蛋白样品中加入适量SDS-PAGE蛋白缓冲液,金属浴变性沸腾10 min。上样量为40 μg,经电泳分离后,电转移至PVDF膜上,用5%脱脂牛奶封闭2 h,加入一抗抗体TLR4、p-NF-κB和β-actin(β-actin作为内参蛋白),4 ℃过夜,TBS-T洗膜4 次,每次5 min,然后加入对应的荧光二抗,室温避光孵育2 h,TBS-T洗膜4 次,每次5 min,显影和扫描使用荧光影像分析仪(LI-COR,USA)。ImageJ 1.41 软件(Bethesda,美国)进行数据分析。
1.7 统计学分析
2 结 果
2.1 紫草素和LPS对HDPCs细胞毒性的影响
如图1所示,在不同浓度的紫草素和LPS的处理下,HDPCs被药物作用24 h,在0~400 μmol/L浓度范围内,紫草素对HDPCs基本没有细胞毒性,浓度超过400 μmol/L时细胞存活率显著降低。在不同浓度梯度的LPS处理下,结果表明,在0~0.25 μg/ml给药浓度范围内,没有产生细胞毒性,当浓度是1 μg/ml时,细胞存活率显著降低(P<0.01),说明此浓度的LPS对HDPCs产生细胞损伤,成功建立细胞炎症模型。
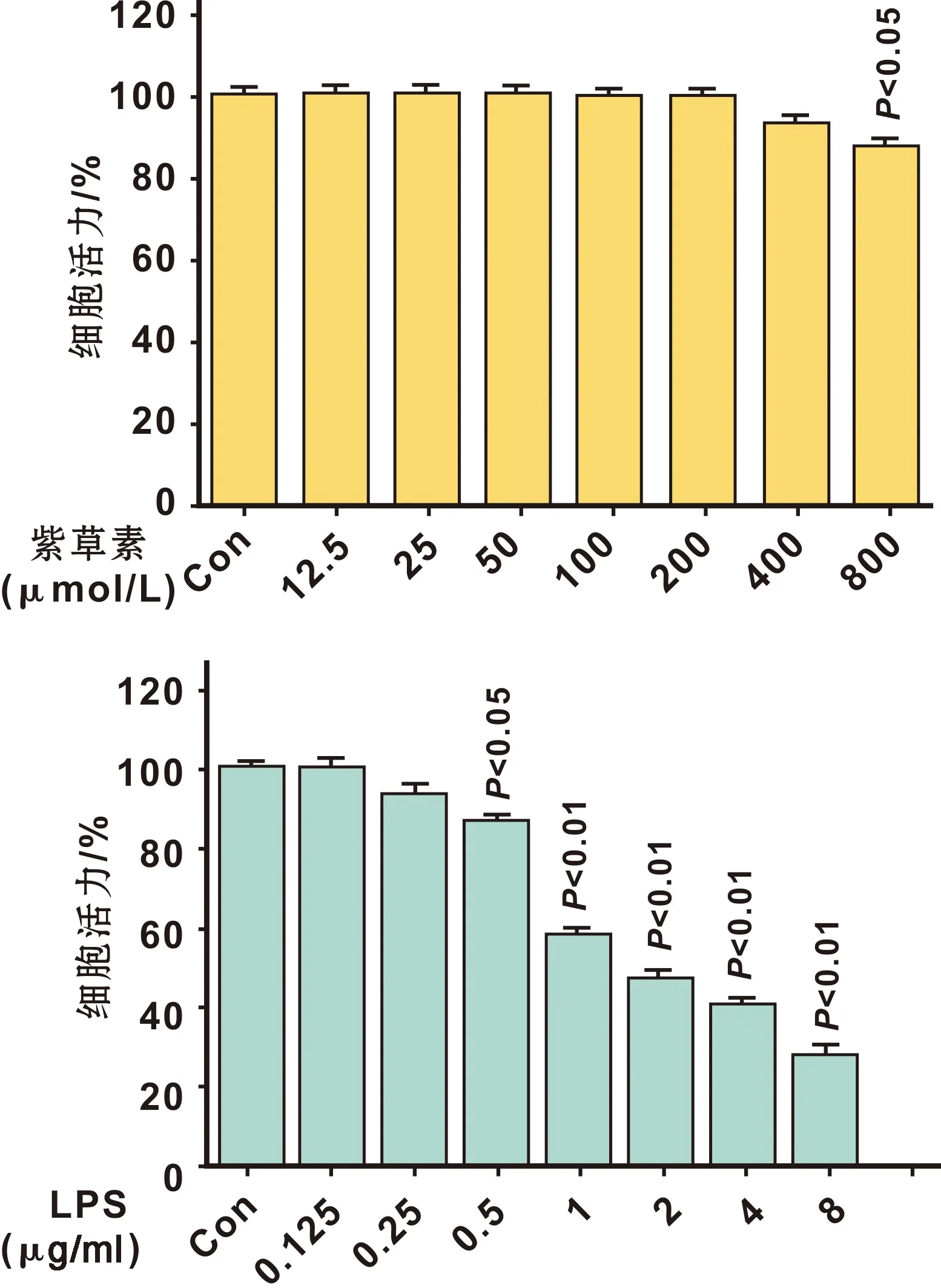
图1 紫草素和LPS对HDPCs细胞毒性 Fig 1 The cytotoxicity of shikonin and LPS on HDPCs n=6)
2.2 紫草素对LPS诱导的HDPCs细胞炎症模型细胞存活率的影响
如图2A所示,与正常组相比,模型组细胞存活率显著降低(P<0.01),说明LPS对HDPCs造成炎症损伤;与模型组相比,在紫草素的作用下,细胞存活率显著升高(P<0.05),为剂量依赖性,说明紫草素可以减少LPS引起的炎症损伤,提高细胞存活率。
2.3 紫草素对LPS诱导的HDPCs中IL-1β水平的影响
如图2B所示,与正常组相比,模型组IL-1β水平明显升高(P<0.01),说明LPS能够刺激IL-1β细胞炎症因子的释放,引发炎症反应;与模型组相比,给药组中的IL-1β水平显著降低(P<0.01),并且存在剂量依赖性,说明紫草素能对抗LPS引起的细胞炎症,抑制促炎因子IL-1β的释放。
2.4 紫草素对LPS诱导的HDPCs中IL-6水平的影响
如图2C所示,与正常组相比,模型组IL-6水平明显升高(P<0.01),说明LPS能够刺激IL-6细胞炎症因子的释放,引发炎症反应;与模型组相比,给药组中的IL-6水平显著降低(P<0.05),并且存在剂量依赖性,说明紫草素能对抗LPS引起的细胞炎症,抑制促炎因子IL-6的释放。
2.5 紫草素对LPS诱导的HDPCs中TNF-α水平的影响
如图2D所示,与正常组相比,模型组TNF-α水平明显升高(P<0.01),说明LPS能够刺激TNF-α细胞炎症因子的释放,引发炎症反应;与模型组相比,给药组中的TNF-α水平显著降低(P<0.01),并且存在剂量依赖性,说明紫草素能对抗LPS引起的细胞炎症,抑制促炎因子TNF-α的释放。
2.6 紫草素对LPS诱导的HDPCs中IL-10水平的影响
如图2E所示,与正常组相比,模型组IL-10水平显著降低(P<0.01),说明LPS抑制IL-10的释放;与模型组相比,给药组IL-10水平显著升高(P<0.05),呈现剂量依赖性,说明紫草素能够提高抑炎因子IL-10的释放,抑制LPS引起的细胞炎症,具有一定的抗炎作用,并且高浓度的紫草素炎症的缓解作用较低浓度的紫草素强。
2.7 紫草素对LPS诱导的HDPCs中TLR4蛋白表达的影响
如图3所示,蛋白印记结果表明,与正常组相比,模型组中TLR4蛋白表达显著升高(P<0.01),说明LPS能够使TLR4蛋白表达升高,发生炎症反应,引起HDPCs炎症损伤;与模型组相比,给药组中TLR4表达显著降低(P<0.01),并且呈剂量依赖性,说明紫草素能够降低LPS引起的细胞炎症,降低TLR4蛋白的表达,具有明显的抗炎作用,并且高剂量紫草素组的作用效果强于低剂量组紫草素组。
2.8 紫草素对LPS诱导的HDPCs中p-NF-κB蛋白表达的影响
如图3所示,与正常组相比,模型组中p-NF-κB蛋白表达显著升高(P<0.01);与模型组相比,给药组中p-NF-κB蛋白表达显著降低(P<0.01),并且呈剂量依赖性,说明紫草素能够降低LPS引起的炎症,降低p-NF-κB蛋白的表达,具有明显的抗炎作用。
3 讨 论
牙髓是牙髓腔内疏松的结缔组织,具有重要的生理功能,如形成牙本质、营养、感觉、修复等,HDPCs则是牙髓组织中重要的细胞器[14]。LPS作为革兰阴性菌细胞壁的成分之一,能够诱导促炎细胞因子在牙髓组织中发生免疫应答[15],引起牙髓病和龋病[16],LPS诱导疾病机制可能是通过激活TLR4分子及其下游的NF-κB和MAPK信号通路蛋白的表达[17],增加炎症因子IL-1β、IL-6和TNF-α的释放,抑制IL-10的分泌[18],然而紫草素具有很强的抗炎作用[19],能够抵抗LPS导致的炎症反应[20]。
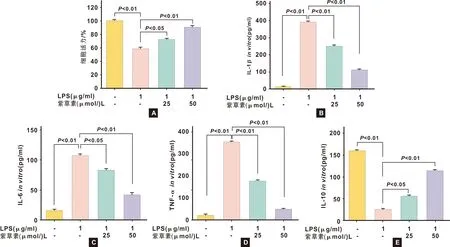
A:各组细胞炎症模型细胞存活率;B:IL-1β分泌水平;C:IL-6分泌水平;D:TNF-α分泌水平;E:IL-10分泌水平图2 紫草素对LPS诱导的HDPCs细胞存活率,IL-1β,IL-6,TNF-α,IL-10分泌的影响 A:The viability of HDPCs of the groups;B:The release level of IL-1β;C:The release level of IL-6;D:The release level of TNF-α;E:The release level of IL-10Fig 2 The effects of shikonin on LPS-induced HDPCs cell survival and the secretion of IL-1β,IL-6,TNF-α and IL-10 n=6)
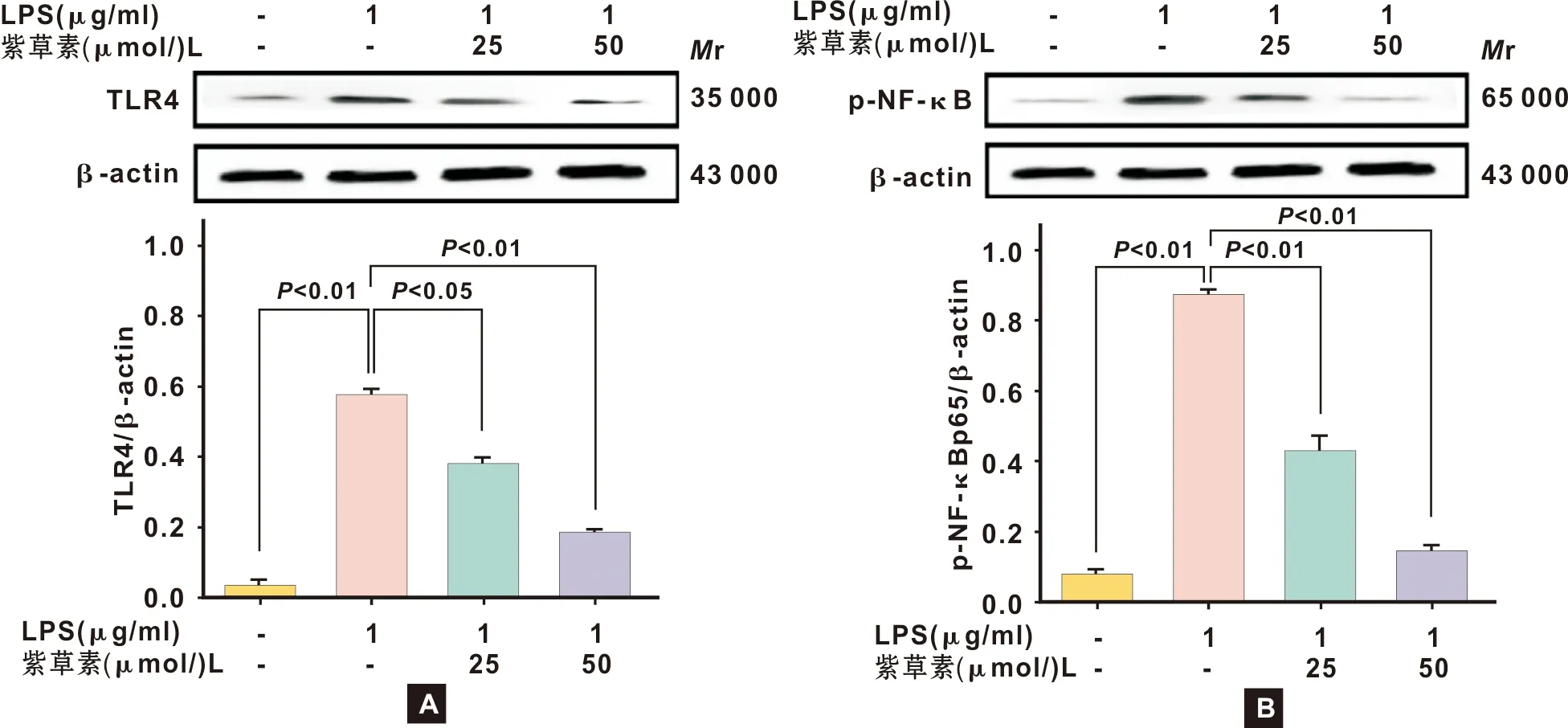
A:TLR4蛋白表达;B:p-NF-κB蛋白表达图3 紫草素对LPS诱导的HDPCs中TLR4及p-NF-κB蛋白表达的影响 A:TLR4 protein expression;B:p-NF-κB protein expressionFig 3 The effects of shikonin on the expression of TLR4 and p-NF-κB in HDPSs induced by LPS n=3)
本研究结果表明紫草素能够升高由LPS诱导的HDPCs细胞存活率的降低,诱导细胞毒性,引起细胞损伤。在LPS的刺激下,IL-1β、IL-6和TNF-α细胞促炎症因子的表达显著升高,IL-10抑炎因子水平显著降低;TLR4/NF-κB信号通路被激活,TLR4和p-NF-κB蛋白表达显著升高。在紫草素的治疗下,炎症细胞因子IL-1β、IL-6和TNF-α水平显著降低,IL-10抑炎因子水平显著升高,说明紫草素能够抑制LPS引起的细胞炎症,降低促炎因子的释放,提高抑炎因子的分泌,并且存在剂量依赖性;而且紫草素能够抑制LPS引起的TLR4/NF-κB信号通路的激活,降低TLR4和p-NF-κB蛋白的表达,由此说明紫草素具有很强的抗炎作用,其作用机制可能是通过调节TLR4/NF-κB信号通路来抑制LPS引起的炎症反应,这将为牙髓病的治疗提供新思路和新靶点,有利于开发治疗牙髓病且毒副作用小的天然新药。
