金属-有机骨架材料用于水中痕量药物污染物的吸附脱除
2020-06-29赵英杰赵慧芳王婷刘大欢
赵英杰,赵慧芳,王婷,刘大欢
(北京化工大学化学工程学院,北京100029)
近年来,随着药物使用的增加,许多药物未被完全代谢而以痕量的浓度持续排入环境中,也被称为“假性持续性”污染[1-3]。因此,药物作为一种新兴污染物(emerging contaminants,ECs)引起了人们广泛的关注[4]。这些残留的药物在环境中的各个地方均有分布,比如土壤、地下水、地表水、淤泥等[5-11]。据报道,世界各国的环境中已经检测到超过600种不同的药物,其在环境中不断积累,给人类的健康和生态系统带来了严重的危害[12]。例如,抗生素在环境中长期存在使细菌产生抗药基因,从而变成超级细菌;长期饮用被药物污染的水,会使消化道菌落失调,引起胃肠道感染,而且会导致人体内的耐药菌增加[13]。废水处理厂水处理工序的设计通常是处理浓度较高(在mg/L 范围)且容易降解的有机污染物,而水体中药物分子的浓度非常低(ng/L~μg/L),而且药物分子的结构复杂,具有多个电离位点和多态性[14-15]。此外,一些药物具有较强的杀菌作用,不仅很难被微生物分解,而且对微生物的生长有抑制甚至杀灭作用,因此,一般的水处理方法(如活性污泥曝气法、厌氧生物法)无法有效处理痕量药物污染[16]。通常处理药物污染物的方法包括光催化法、高级氧化法、膜分离法、电化学氧化法、生物降解法等[17-21],但这些方法存在较多缺点,如生物降解的过程中易产生高毒性代谢中间体等[22]。相对而言,基于高效吸附材料的吸附法操作简单、能耗低、吸附效率高、处理过程不破坏药物分子,不仅可有效避免高毒代谢物的产生,同时也方便富集并回收此类分子,被认为是最具前景的有效手段之一[4]。而这其中的核心是高效吸附材料,其化学与结构组成直接影响脱除效果。目前使用的主要是传统吸附材料,包括活性炭、沸石、分子筛、膨润土等,但由于吸附位点较少、吸附剂和吸附质间的作用力弱,使得其吸附能力较低、吸附速率较慢;同时,这些材料的结构、功能可设计性相对较差,对其改性困难。因此,亟需引入新型功能材料,以满足对此类复杂客体分子高效去除的需求。
金属-有机骨架材料(metal-organic frameworks,MOFs)是一类由有机配体与金属中心组成的、高度有序的功能性多孔晶体材料,由于其超高比表面积/孔隙率、高度化学/结构可调性以及可设计性等优点,在多个领域展现出优异的应用前景,包括吸附、分离、荧光、催化等[23-28]。近年来,MOFs 被用来研究水体中多种污染物的脱除,包括重金属离子、染料、药物等,并表现出优于传统吸附材料的性能[29-35]。目前,已有多篇综述对这方面的研究进展进行了总结,但以药物分子为主并基于药物分子与MOFs 材料间相互作用力而进行的讨论综述较少。因此,本文简要总结了近年来MOFs用于吸附去除水体中抗生素和其他类常见药物污染物的研究,通过研究MOFs材料以及引入不同官能团或其他物质(如碳纳米管、磁性Fe3O4等)对脱除效果的影响,分析了其间的相互作用,包括氢键、π-π相互作用、酸-碱作用等,为充分利用MOFs 可设计性和可功能化强的特点,针对于特定药物分子结构而开发高效吸附与富集材料,提供有用的参考信息。
1 MOFs简介
金属有机骨架材料又被称为多孔配位聚合物,是由有机配体与无机金属中心(金属离子或金属簇)通过配位键形成的多孔晶体材料。自1995 年合成了第一个具有稳定孔结构的MOFs材料后[36],研究者们利用不同的方法设计并制备了成千上万种MOFs材料。相比于沸石材料,MOFs材料更易合成[37]。常见的MOFs材料的制备方法包括:水热/溶剂热合成法、微波合成法、超声合成法等[38]。其中水热/溶剂热合成法是最常用的方法,微波合成法和超声合成法可以明显缩短合成时间[39-40]。除此之外,MOFs材料还有许多其他的特点:结构可设计性、可功能化强、高比表面积和高孔隙率以及存在开放金属位点等[41-42]。根据这些特点,MOFs 材料可通过有机配体与无机结构单元的特定组合实现定向的设计;亦可通过前合成或后合成改性的方法在不改变MOFs材料的拓扑结构的情况下,引入更多的官能团以增加其活性位点,实现其功能化,进而提高材料的性能[43-44]。
2 不同种类药物分子的吸附
2.1 四环素类抗生素
四环素类抗生素可用于恶性肿瘤的诊断和治疗各种囊肿等疾病,是一类具有并四苯结构的广谱抗生素,结构中含有氨基和大量的羟基官能团,这些有机官能团在吸附的过程中起着至关重要的作用,如氨基可以与金属簇发生配位作用,苯环与苯环之间可以发生π-π 共轭/堆叠作用等,从而提高对其的吸附能力。根据四环素类分子的结构特点,Chen 等[45]选用UiO-66 吸附水中的盐酸四环素分子(TC),其最高吸附量为23.1mg/g。由于TC 中的氨基和卤化铵盐的伸缩振动,导致吸附后的红外谱图中在3400cm-1处的峰宽变宽并且宽带中心向小波长偏移;同时,光电子能谱(X-ray photoelectron spectroscopy,XPS)中出现的C O/C N特征谱图,证明水中的TC确实存在于UiO-66骨架中。通过分析XPS谱图,作者认为TC在UiO-66的吸附主要是由于Zr-O团簇与TC中含氮基团的配位作用,而静电作用和π-π 相互作用也存在于吸附的过程,但并不占主导地位。Li 等[46]发现,咪唑环与四环素(TCN)/氧四环素分子(OTC)间存在π-π 相互作用,使得ZIF-8在水溶液和实际废水中都表现出高效的脱除能力:在水溶液中,ZIF-8对TCN和OTC的最高吸附量分别为303.0mg/g 和312.5mg/g,且吸附过程符合准二级动力学模型和Langmuir 模型;在实际废水中(来源于福建省养猪场),TCN 和OTC的去除率分别为90.7%和82.5%。

对于尺寸较大的客体分子,吸附材料的孔尺寸/孔体积以及吸附位点数目对吸附能力有重要的影响;同时,大孔径的存在也有助于提高客体分子的传质速率。因此,研究者采用多种策略构造具有大孔径的MOF 材料,以提高其脱除效果。Zhang等[48]利用金属有机聚合物作为模板剂,在UiO-66中引入缺陷,得到两种多级孔材料H-UiO-66s,其缺陷孔径分别为3.8nm和17.3nm,且孔体积均高于UiO-66,尤其是H-UiO-66-17.3nm(1.06cc/g,1cc/g=1mL/g),几乎是UiO-66(0.59cc/g)的2倍。因此,所得两种材料对TCN 的脱除能力比UiO-66 分别提高430%和288%(666.67mg/g 和487.80mg/g)见图1。而且经过4 次循环再生,其吸附量几乎没有改变。类似地,Chen等[49]利用聚二烯丙基二甲基氯化铵(PDDA)作为结构导向剂调节晶体生长过程(见图2),合成了具有多级孔结构的HpZIF-8(D)[其中D 为加入PDDA 的量,D=1.0mL, 1.5mL, 2.0mL]。TC 的吸附实验表明,HpZIF-8-10(D)(D=0.5mL,1.0mL, 1.5mL, 2.0mL)和mZIF-8-10 对TC 的吸附均在5min 内达到平衡,且HpZIF-8-10(D)(D=1.0mL,1.5mL,2.0mL)的吸附能力分别为46.5mg/g、49.3mg/g和44.1mg/g,均高于HpZIF-8-10(0.5)和mZIF-8-10。其中HpZIF-8-10(1.5)对TC 的脱除率可高达98.6%,比mZIF-8-10 高出37.7%。另一方面,阳离子的PDDA 引入也增加了TC 的吸附位点,进而提升了吸附量。
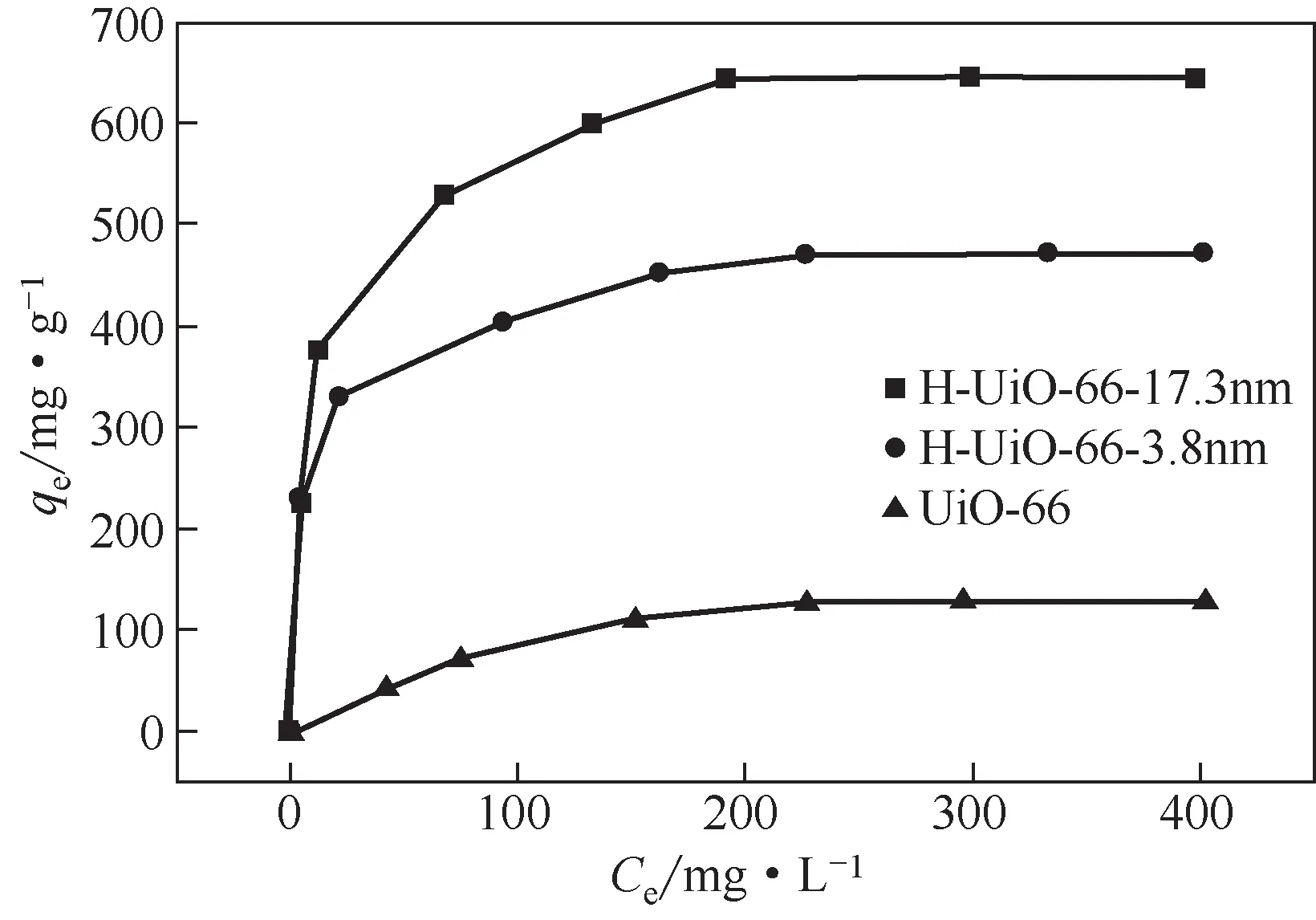
图1 UiO-66和H-UiO-66s对TC的吸附等温线[48]
除了MOFs 材料的本体优势外,在MOFs 材料中添加其他物质以提高MOFs材料的比表面积、增加更多的作用位点,也可以提高其对药物分子的吸附能力。如Xiong 等[50]将多壁碳纳米管(MWCNT)引入到MIL-53(Fe)中,得到了复合材料MWCNT/MIL-53(Fe)。MWCNT 的修饰作用使得MWCNT/MIL-53(Fe)的比表面积、孔体积和孔径分别是MIL-53 的1.2 倍、1.6 倍和1.4 倍。实验结果表明,复合材料对TCN、OTC和氯四环素(CTC)的吸附量 分 别 为364.37mg/g、325.59mg/g 和180.68mg/g,均高于MIL-53 和MWCNT。三种四环素类抗生素吸附量的差异,主要是由于其分子尺寸的不同,小分子(CTC)更容易扩散到材料的孔道中,吸附量也相应较高。经过四次再生循环,MWCNT/MIL-53(Fe)对三种四环素类抗生素的吸附能力没有明显改变,表明该材料具有良好的再生性能。Jin 等[51]将金属Cu 和Co 掺杂到MIL-101(Cr)中,引入了更多的作用位点。不同金属和不同比例的双金属掺杂对复合材料的吸附能力有不同程度的提升,TCN的吸附量顺序为MIL-101<Co/MIL-101<Cu/MIL-101<MIB-8[掺杂量Cu2+∶(Cu2++Co2+)的比为0.8],这表明材料对TCN 的吸附受Cu 和Co 纳米颗粒的协同作用。虽然负载后材料的比表面积有所下降,但是吸附量较MIL-101 提高了140%,作者认为这可能是因为材料中的Cu和Co纳米微粒对TCN的化学键作用;除了金属掺杂增加材料的作用位点外,在吸附过程中也可能存在其他相互作用,如氢键、π-π堆积、酸-碱作用、静电作用等,其中静电作用占主要地位,其他作用有待进一步分析,见图3。此外,作者研究了离子强度和腐殖酸对吸附过程的影响,随着增加NaCl 和Na2SO4的浓度,材料对TCN的脱除率从83.6%变为71.4%和63.6%(离子强度从0变为0.1mol/L),即带有负电荷的离子在吸附的过程会与TCN 存在竞争吸附;而腐殖酸的加入,则会使三者之间存在复杂的表面络合作用,进而提高了材料对TCN的吸附能力。

图2 ZIF-8的合成反应过程和核与PDDA的相互作用示意图[49]
2.2 β-内酰胺类

图3 CuCo/MIL-101的合成与TCN的吸附示意图[51]



图4 MIL-101-NH2的质子化过程示意图[52]
本文作者研究组[53]对头孢拉定分子的吸附进行了研究,考虑到头孢拉定分子相对较大且具有芳香性,选择了一种具有π电子的配体(卟啉)的高比面积、大孔径MOF 材料(PCN-222)。静态吸附实验结果表明,PCN-222 对头孢拉定的平衡吸附量可以达到333.33mg/g,高于当时文献报道的所有材料。红外谱图中卟啉环的伸缩振动峰从1401cm-1偏移到1409cm-1,表明在吸附过程中PCN-222与头孢拉定分子之间发生了π-π共轭作用;而溶液pH对吸附量的影响表明,静电作用也起到了比较重要的作用。此外,MOFs材料的形貌也是影响β-内酰胺类抗生素的吸附效果的关键因素之一。Abazari等[54]利用溶剂热法和超声合成法合成了一种单晶Zn-MOFs材料[Zn6(IDC)4(OH)2(Hprz)2]n,并通过调控反应时间、金属盐和配体的浓度,得到具有不同形貌的MOFs(包括纳米片和纳米花等结构),这些材料具有不同的比表面积。实验结果表明,纳米花形态的MOFs 材料对氨苄青霉素、阿莫西林和邻氯青霉素三种抗生素具有最高的脱除效率,原因是材料的高比表面积和较小的颗粒尺寸。此外,该材料表现出良好的可再生吸附能力,经过4次吸附循环,对阿莫西林的脱除率几乎不变。
2.3 磺胺类
磺胺类抗生素是一种具有对氨基苯磺酰胺结构的抗菌药物,常用来治疗急性和慢性尿道或呼吸道感染等疾病。根据这类药物的结构特点,Cychosz等[55]率先研究了一系列MOFs 材料(MOF-177、MOF-5、HKUST-1、MOF-505、UMCM-150、MIL-100)的水稳定性,并利用水稳定的MIL-100 作为吸附剂,去除水中柳氮磺胺吡啶。对浓度为1.4μg/mL的柳氮磺胺吡啶溶液,MIL-100的吸附量为6.2mg/g。Azhar 等[56]利用HKUST-1,实现了水体中磺胺二甲基嘧啶(SCP)的快速(15min)和高效地脱除(饱和吸附量达到384mg/g)。作者认为材料的不饱和金属位点是材料表现出较快的脱除速率的主要原因。红外谱图表明,SCP 中氨基上的氢原子可与HKUST-1 金属簇中的氧原子形成氢键,同时苯环之间也存在π-π相互作用;不同pH下吸附量的对比表明两者之间也存在静电作用,见图5。随后,该研究组[57]还发现UiO-66 对SCP 具有更优异的脱除能力:可在10min内达到吸附平衡,饱和吸附量为417mg/g,其主要原因是材料的疏水性和更强的π-π 相互作用,而静电作用影响影响较小(约占20%),见图6。
MIL-53(M)作为一种典型的柔性MOFs 材料,其孔道主要有四种形状,即非常狭窄的孔道(MIL-53vnp)、过渡态孔道(MIL-53int)、狭窄的斜形孔道(MIL-53np)和大孔道(MIL-53lp),这四种形状取决于材料中金属节点和吸附到孔道中的水分子含量[58]。Gao 等[59]根据材料中不同金属节点对孔道尺寸大小的影响,研究了MIL-53(Cr)、MIL-53(Al)和MIL-53(Fe)对磺胺甲唑(SMZ)的吸附能力和机理。结果表明,这三种MOFs的饱和吸附量分别为1.85 mmol/g、1.78mmol/g 和0.314mmol/g。其中,MIL-53(Fe)中的吸附量明显低于MIL-53(Cr)和MIL-53(Al),原因是在吸附过程中MIL-53(Fe)孔道形状为非常狭窄孔道(MIL-53vnp)和狭窄的斜形孔道(MIL-53np),且为亲水性孔道,见图7。通过分析pH 的影响、X 射线衍射(XRD)谱图和红外谱图可知,吸附过程的机理主要是由于材料的“呼吸”效应、疏水作用、静电作用、氢键以及π-π相互作用的协同效果。

图5 HKUST-1对磺胺二甲基嘧啶的可能吸附机理[56]
以前大多数的研究都是针对于一种药物分子,而实际废水中往往存在多种药物的混合物。为此,Peng 等[60]研究了MOF 材料同时脱除磺胺地索辛(SDM)、磺胺间甲氧嘧啶(SMM)和磺胺二甲基嘧啶(SMZ)三种药物的能力。结果表明,MIL-101(Cr)可以同时高效地吸附这三种混合污染物,吸附量为340.90mg/g(溶液浓度为100mg/g),而对其单独的最高吸附量分别是588.24mg/g、196.08mg/g 和142.86mg/g。其吸附机理与之前的研究类似,为静电作用、π-π 相互作用和氢键的共同作用。其中SDM 和SMM 有相似的嘧啶基团,在共吸附时会有一定程度的竞争。
2.4 喹诺酮类
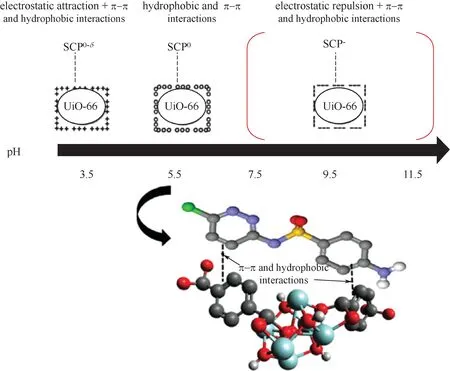
图6 UiO-66对SCP的吸附机理示意图[57]
喹诺酮类抗生素广泛用于泌尿生殖系统疾病、胃肠疾病以及呼吸道、皮肤组织的革兰阴性细菌感染的治疗等,是一类具有1,4-二氢-4-氧代喹啉-3-羧酸结构的分子,此类药物中含有—COOH、—F等有机官能团,这些官能团可以与吸附剂形成氢键、静电作用等。Jin 等[61]利用富含不同官能团的配体H4PDAD(见图8)[(5,5’)-(吡啶-3,5-二羰基)双(氮杂二基)二间苯二甲酸]和硝酸铜合成了具有优异稳定性的PCN-124-stu(Cu),并研究了该材料对三种具有不同分子尺寸的喹诺酮类抗生素的脱除性能。由于孔道中的氨基、羧基基团与三种喹诺酮类抗生素分子中的氟元素、羧基和末端氨基的氮原子之间(仅诺氟沙星分子)可以产生氢键作用,PCN-124-stu(Cu)对这三种喹诺酮类抗生素[诺氟沙星(NOR)、氧氟沙星(OFL)和恩诺沙星(ENR)]的吸附能力分别为198mg/g、292mg/g 和354mg/g,这与其分子大小顺序一致,即NOR>OFL>ENR。作者通过构型偏倚蒙特卡洛模拟(configurational bias Monte Carlo simulation,CBMC)计算发现,三种药物分子主要位于Cu 不饱和金属位点和氨基官能团附近,验证了所提出的吸附机理。
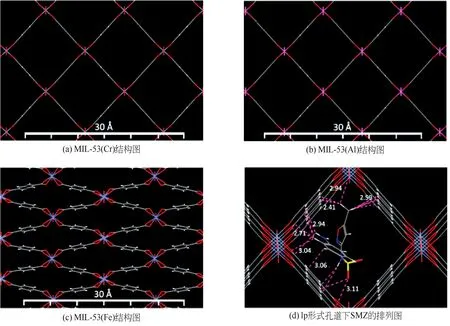
图7 MIL-53(Cr)、MIL-53(Al)和MIL-53(Fe)结构图以及lp形式孔道下SMZ的排列图[59](虚线为SMZ与骨架的距离)

图8 配体的设计示意图[61]
近年来,与传统的分离技术(如过滤和离心分离)相比,磁性吸附剂引起了广泛的关注,可在外部磁场的条件下方便地实现分离和回收再利用。Wu 等[62]将Fe3O4与MOFs 材料复合,合成了具有磁性的复合材料Fe3O4/HKUST-1,该材料对环丙沙星(CIP)和诺氟沙星(NOR)表现出优异的吸附能力。一方面,Fe3O4/HKUST-1 可以在30min 内达到吸附平衡,其吸附速率高于所有已报道的材料。另一方面,对CIP和NOR的最大吸附量分别可以达到538mg/g 和513mg/g,高于大多数的其他吸附剂;而且经过10次循环再生,Fe3O4/HKUST-1仍保持高效的脱除效率。分析HKUST-1 和两种抗生素的结构表明,可能存在的吸附机理包括:①HKUST-1中Cu不饱和金属位点与以两性分子存在的CIP和NOR中羧基基团的配位作用;②HKUST-1 中Cu-O-Cu与两种分子中 NH 基团的氢键作用;③HKUST-1与两种分子中苯环间的π-π 相互作用。此外,静电作用也起着重要的作用。许多废水中通常包括抗生素分子和重金属离子,对其同时去除一直以来都是一个重大的挑战。Zhou等[63]利用ZIF-8实现了同时去除水体中的金属离子(Cu2+)和抗生素污染物(NOR),脱除率分别为95.4%和80.3%。吸附过程符合准二级动力学模型和Freundlich 模型,其中对Cu2+的吸附机理为离子交换,而对NOR则是由于静电作用和π-π堆叠作用,见图9。

由于某些MOF 材料的亲水性特点,使得其在水环境中不能稳定存在,因此研究者们利用MOFs材料的高度有序性结构,将其作为牺牲模板通过热解法制备了具有高疏水性和功能化的多孔炭材料,用于水体中污染物去除的研究[65-66]。Li 等[67]研究了不同温度碳化的ZIF-8 对CIP 的脱除性能,发现700℃碳化的材料NPC-700 的吸附性能高于500℃、600℃和900℃,这种差异主要是因为在500℃和600℃时,ZIF-8的骨架未被完全碳化,有效的孔相对较少,而900℃时,由于温度太高破坏了多孔炭材料的结构。作者认为NPC-700对CIP的吸附作用主要是两者之间的静电作用和氢键作用。随着NaCl和腐殖酸的加入,材料对CIP的吸附能力均有提高,且经过7次循环再生实验,NPC-700表现出良好的吸附能力,因此MOFs衍生的碳材料有望成为具有前景的吸附剂用于水中抗生素的脱除。
由于其可调的元素组成和规则的多孔结构,MOFs材料已被广泛用于制备中空纳米结构材料[68]。Liang 等[69]利用ZIF-67 为模板,合成了中空结构的Co3S4,该材料对CIP 的最高吸附量为471.7mg/g,吸附等温线符合Langmuir 模型。吸附机理研究表明,中空结构的Co3S4与CIP之间存在静电和疏水作用,使得材料对CIP表现出优异的脱除能力。该材料经过5次再生实验,其吸附量维持在80%以上。
2.5 其他类抗生素
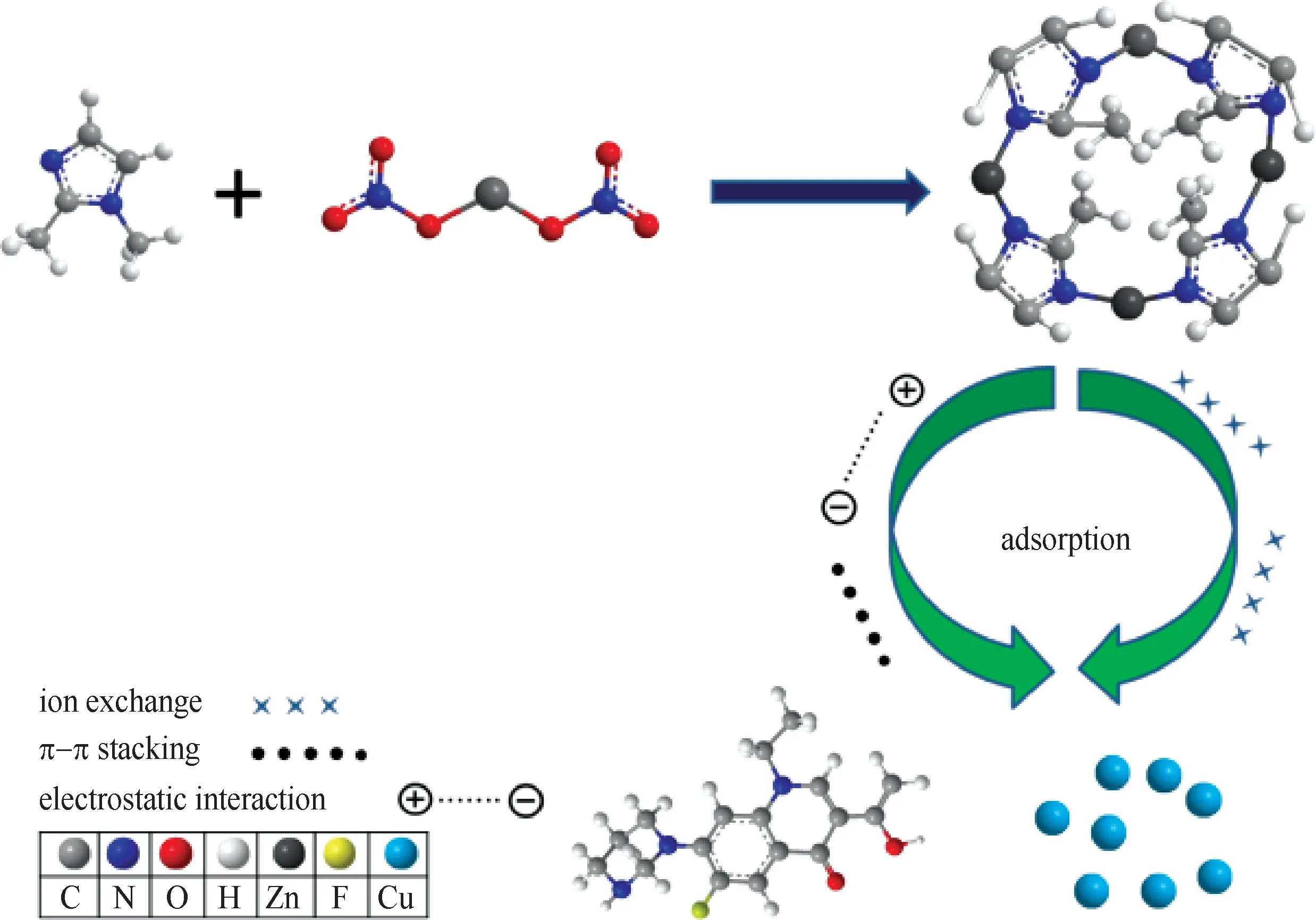
图9 ZIF-8吸附混合污染的机理示意图[63]


硝基呋喃类抗生素广泛应用于畜禽及水产养殖业,以治疗由大肠杆菌或沙门氏菌所引起的肠炎、疥疮、赤鳍病、溃疡病等,是一类5-硝基-2 取代呋喃衍生物。Wang等[73]设计并合成了两种Zr-MOF(BUT-12 和BUT-13),它们均对呋喃西林(NZF)和呋喃妥因(NFT)具有良好的吸附能力和检测能力,可达到预浓缩和选择性检测污染物的目的。作者推断可能的吸附机理为:合适的孔尺寸和孔道的疏水作用;而优异的检测能力主要是由于主-客体之间的电子和能量转移的综合作用。Zhang 等[74]设计并合成了具有镧系金属铽的双功能MOFs 材料Tb-MOF,利用高比表面积和合适的孔道尺寸,以及骨架的坍塌和光致电子转移效应,对NZF和NFT也表现出高效的传感和吸附能力。通过计算配体H3TCPB 和两种呋喃类抗生素分子的LOMO 和HOMO值,解释了荧光猝灭的现象。


2.6 非甾体抗炎药及其他药物

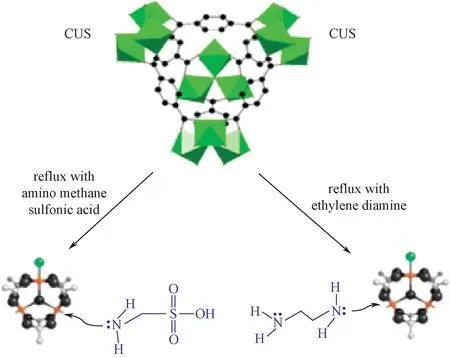
图10 在MOF的不饱和金属位点引入酸性和碱性官能团[77]

图11 基于吸附剂的单位质量和比表面的NAP吸附等温线[78]

Akpinar 等[80]研究了UiO-66 对水体中CBZ 的脱除机理,表明吸附过程中存在的相互作用为疏水作用、CBZ 中的氨基与材料中苯环间π-π 相互作用以及静电作用。而UiO-67 则表现出非常快的脱除速率和高效的脱除能力,利用疏水和π-π 相互作用,可以在2min 内可以去除95%的CBZ(CBZ 浓度为100mg/g),而在相同条件下,商业活性炭(F400)需要1h多才能去除88%的CBZ。
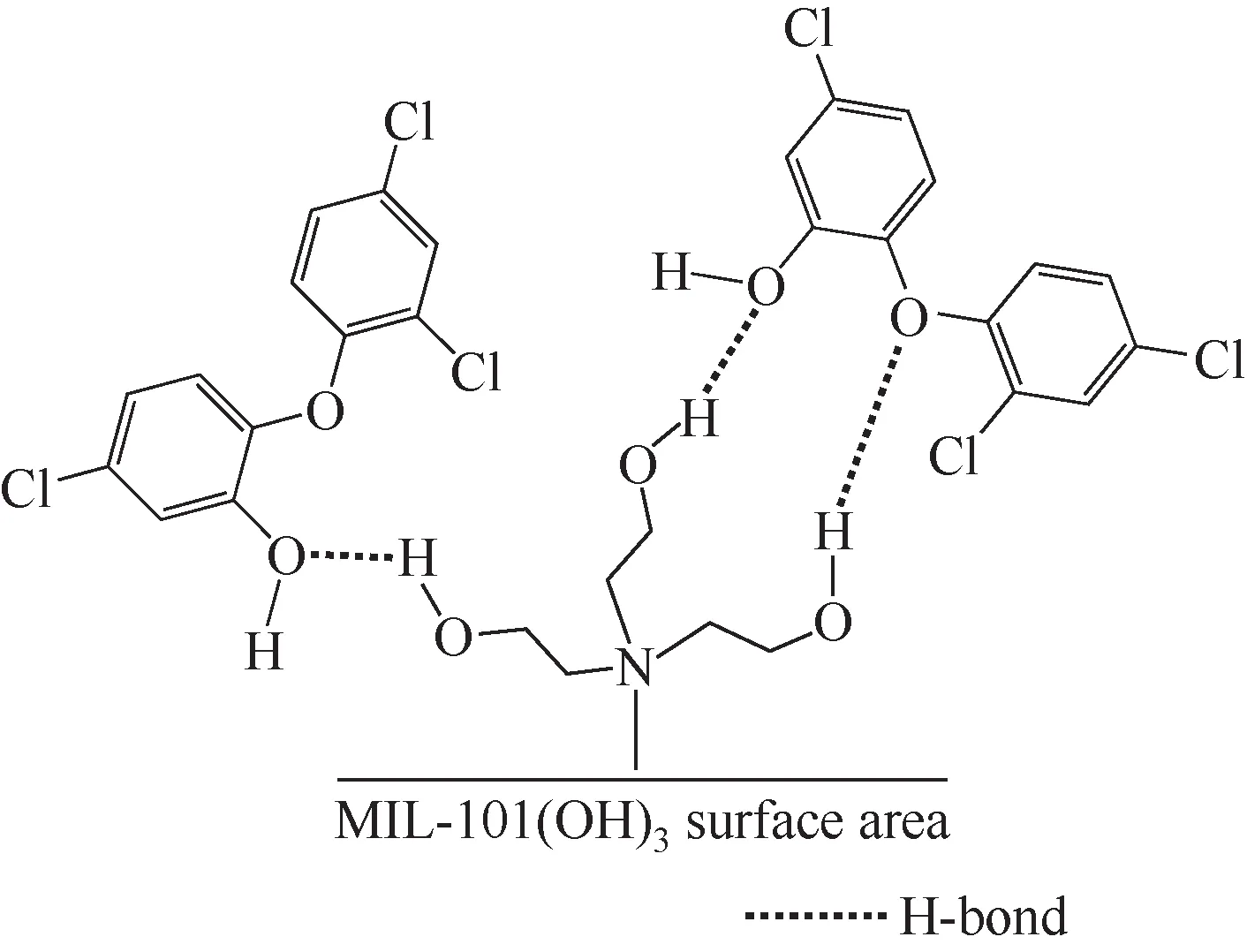
图12 MIL-101-(OH)3和TCS间的氢键示意图[79]
对于药物脱除的相关报道已有很多,但研究金属簇与药物分子间的相互作用并不多。Lin 等[83]采用三种未完全配位的Zr(Ⅳ)基金属-有机骨架材料(UiO-66、MOF-808 和MOF-802)对水中非甾体类抗炎药物(呋喃苯胺酸和水杨酸)进行吸附,发现由于骨架中未被完全配位的Zr6簇与呋喃苯胺酸和水杨酸等阴离子类药物的可产生配位作用(化学吸附),使得UiO-66 和MOF-808 具有优异的去除能力和较快的去除速率,这与理论计算得到的MOFs 材料与药物分子间的结合能一致。此外,材料的吸附能力在三次循环再生后基本不变。
Bhadra 等[84]首 次 利 用 生 物 型bio-MOF-1 在1000℃下热解得到其衍生碳材料(BMDCs)吸附去除水中阿替洛尔(ATNL)和CA,其吸附能力分别为552mg/g 和540mg/g,高于文献报道的所有材料。经过四次再生循环,材料的吸附能力几乎保持不变。BMDCs对ATNL的高脱除能力主要是由于吸附剂和吸附质间的静电作用,而对CA 的脱除则是由于两者之间的氢键作用,其中CA 中的氧为H 的接受者,BMDC 为H 的提供者。Sarker 等[85]将不同质量离子液体(IL)负载到铝基MOF 材料中,并将其碳化形成了氮掺杂的多孔炭材料(CDIL@AlPCP),其中CDIL(0.5)@AlPCP 具有更高的比表面积,对三种药物分子[TCS、对氯间二甲苯酚(PCMX)和对乙酰氨基酚(ACP)]均表现出高效的脱除能力,尤其是对PCMX的脱除能力是目前最高(338mg/g),其原因也是由于氢键作用,其中对氯间二甲苯酚分子为H的提供者,材料中的N和O元素为H的接受者。

在物理吸附作用之外,MOFs 材料还可以同时引入光催化降解作用处理水中的药物污染[88]。Gao等[89]制备了具有光催化作用的MIL-53(Fe),并研究了其对水中两种典型的药物CA 和CBZ 的吸附和光催化能力,其最大吸附量分别约为0.80mmol/g 和0.57mmol/g,光降解效率均达到90%。通过研究pH的影响,提出吸附机理主要是静电相互作用和π-π相互作用。此外,MIL-53(Fe)在可见光下具有较高的光催化活性和稳定性,而且加入少量H2O2可以显著提高光催化效率,高于Fe(Ⅱ)/H2O2和TiO2在可见光下的光降解效率,这主要是光激发的MIL-53(Fe)中直接生成的类芬顿反应、载流子和H2O2的协同作用。
3 吸附机理
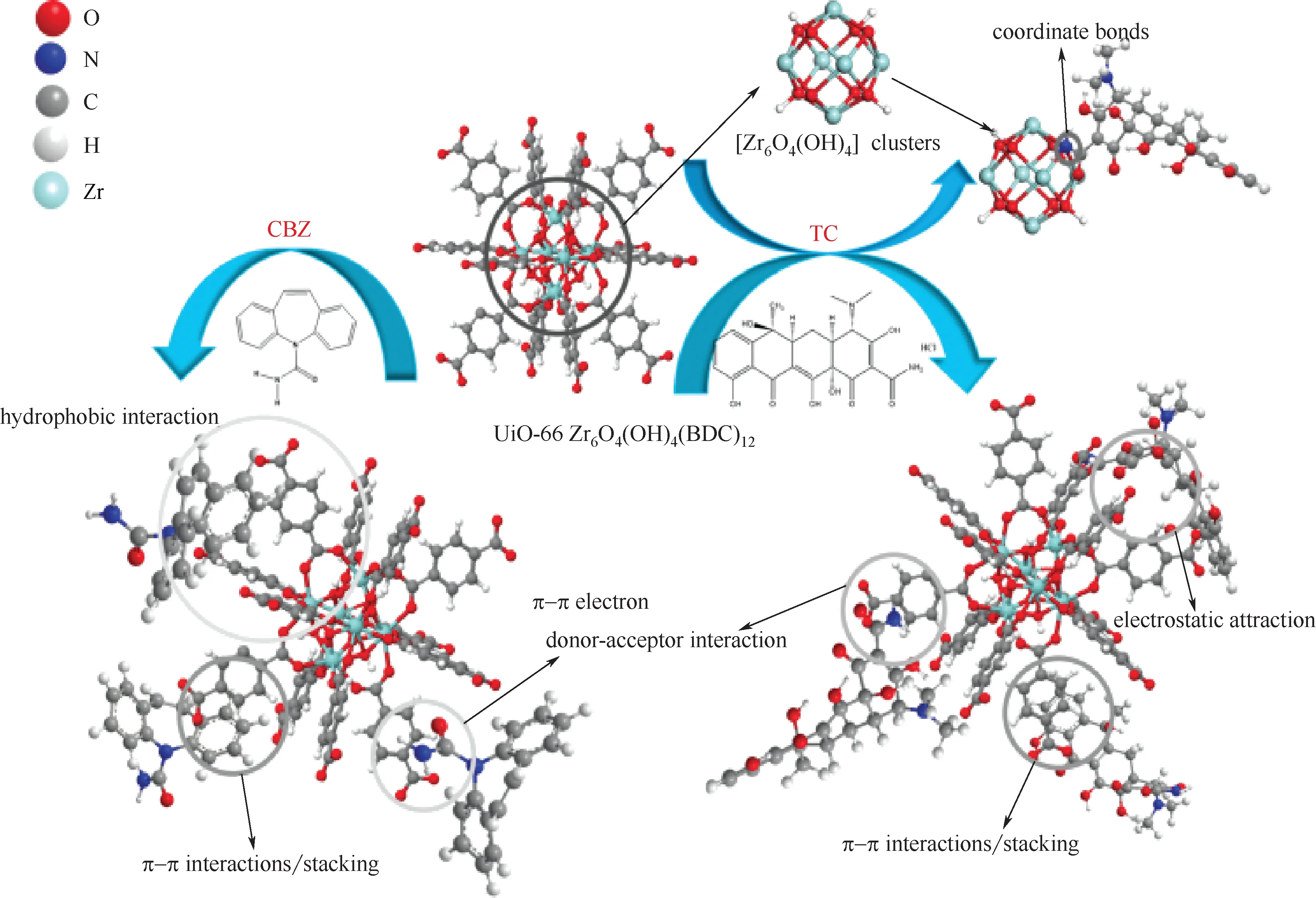
图13 吸附机理示意图[45]
理想的吸附剂应该具有优异的吸附能力、吸附速率、高选择性和再生能力等。不同的药物分子具有多种不同的官能团,这些官能团与吸附剂间的相互作用对于药物的脱除起着至关重要的作用。已有的工作表明,MOF 材料与水中药物分子之间的吸附机理主要有静电作用、酸-碱相互作用、氢键、π-π堆叠/相互作用、疏水作用、配位作用等,不同的吸附机理是由MOFs中特定的官能团、合适的孔尺寸与客体分子中特殊官能团之间的相互作用,如UiO-66 对TC 的吸附脱除主要由于Zr-O 团簇与含氮基团的配位作用,而对CBZ 的吸附是由于疏水作用、π-π相互作用和较弱的静电作用,见图13[45]。



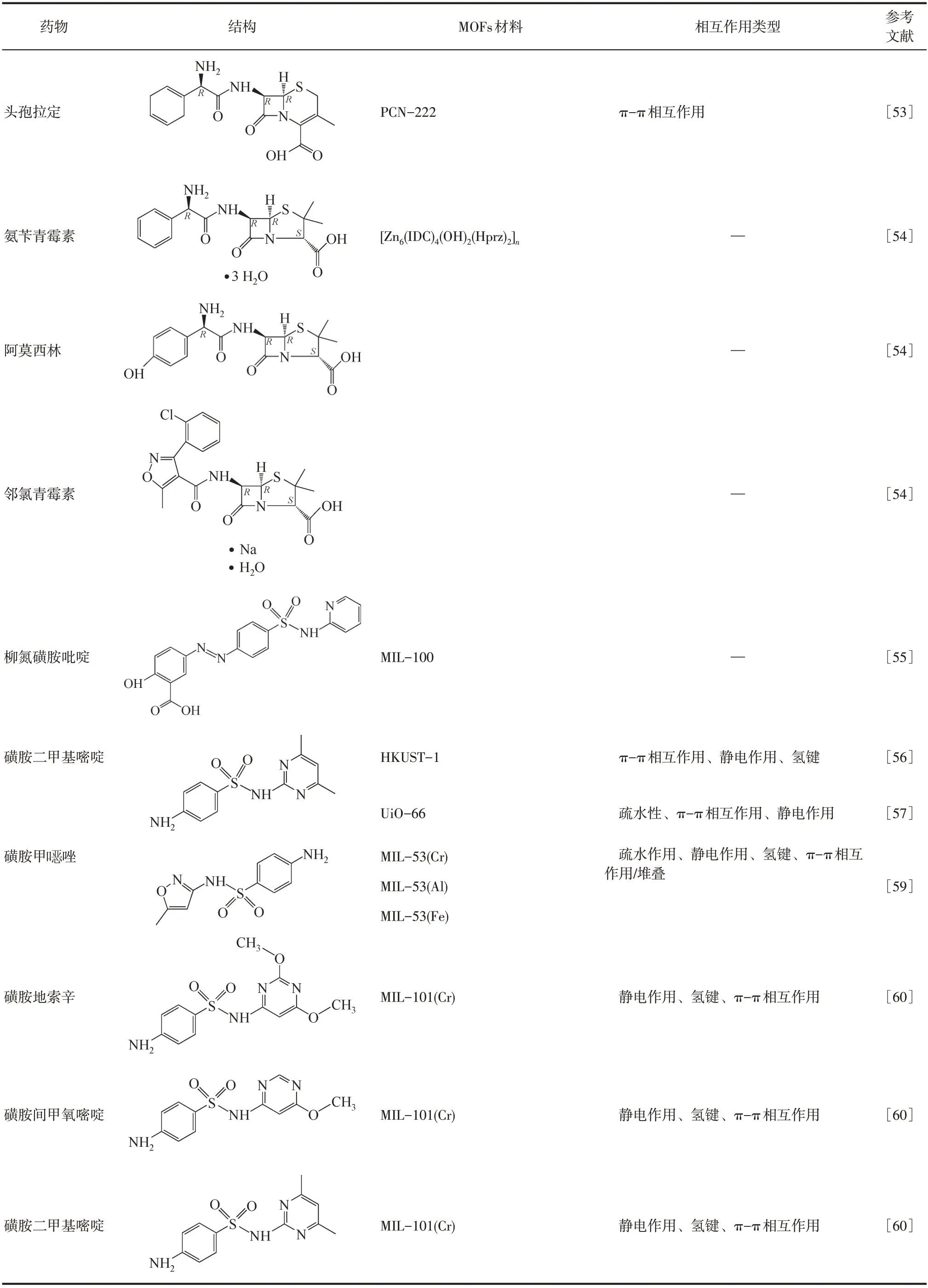
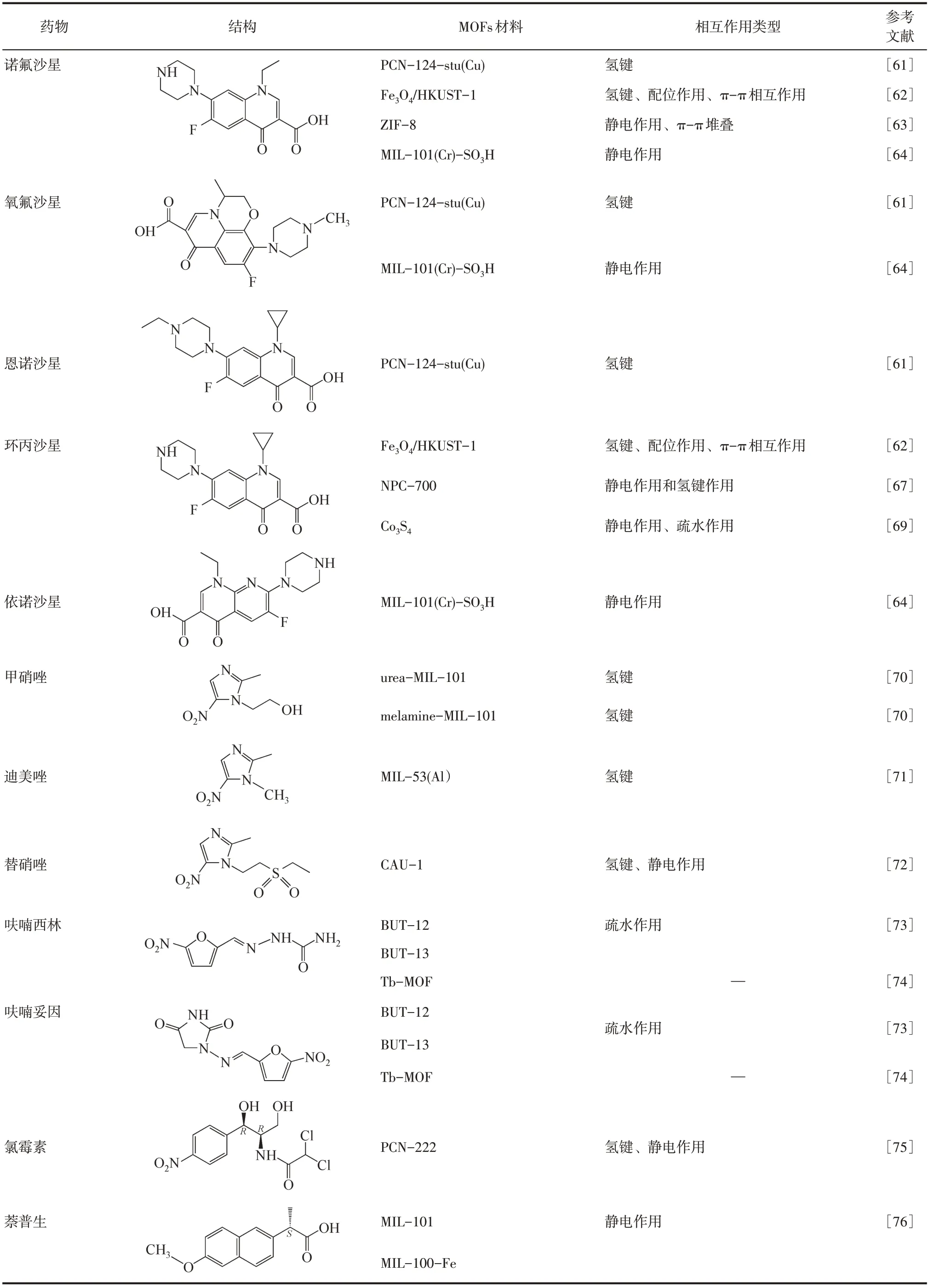
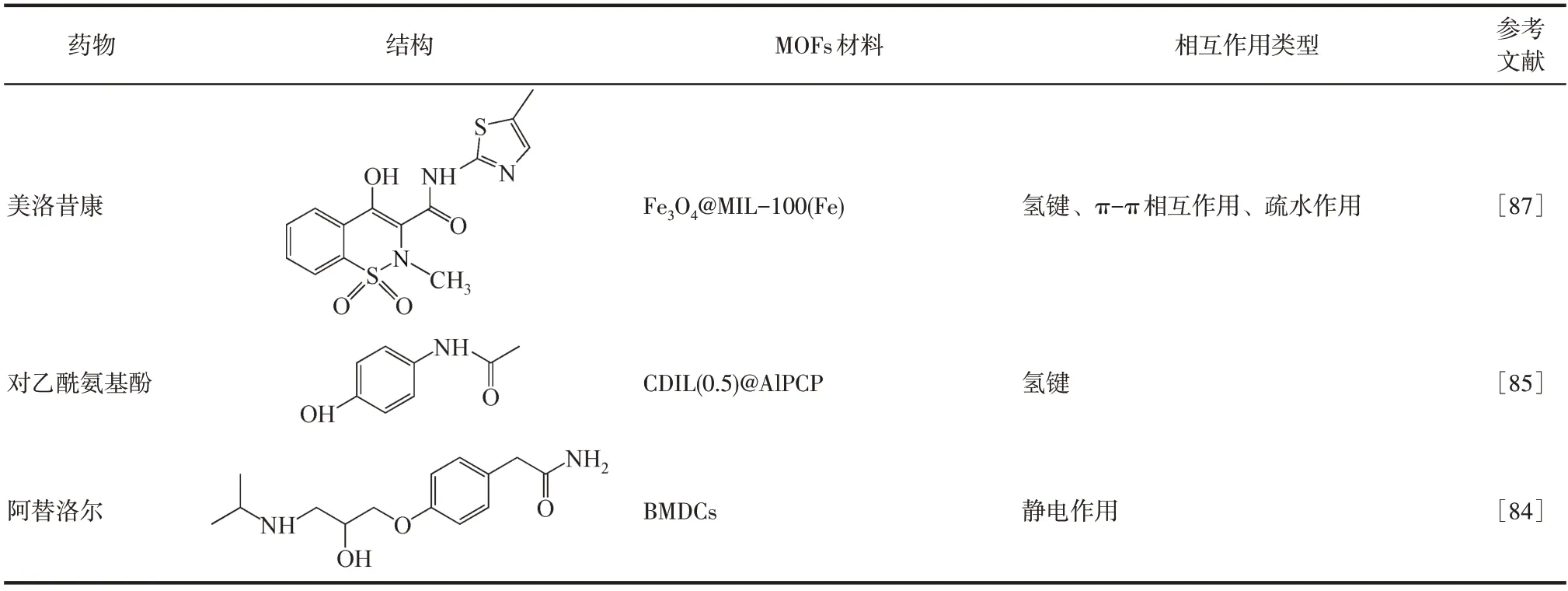
表1 吸附剂与吸附质间的相互作用
续表
续表

续表
续表
4 总结与展望
MOFs 材料由于其结构的可设计性、易官能团化的孔道表面以及高比表面积和高孔隙率等特点,对于水中痕量的药物分子表现出优异的脱除能力。通过有针对性地调控MOFs骨架与客体分子之间的静电作用、酸-碱相互作用、氢键、π-π堆叠、疏水作用、配位作用等,可实现高吸附量、快吸附速率以及高选择性的吸附。虽然取得了一定的进展,但这方面的研究目前还存在一定的问题,需要进一步的系统研究。
(1)药物分子结构复杂,存在多种因素协同作用,需要借助于先进的理论计算工具,结合因素隔离方法,获得相关构效关系规律,进而开发更高效的MOFs吸附材料。
(2)MOFs 种类繁多,从实验的角度去筛选材料用于药物分子的脱除任务量大,效率低。而通过计算的手段筛选材料用于药物分子的脱除可节省大量时间,减少任务量。在此方面,基于材料基因组学方法进行大规模筛选,可以提供重要的参考信息。本文作者所在的仲崇立教授研究组在前期工作中,初步建立了MOF/COF 材料基因组学方法,利用MOFs材料可设计性和可功能化强等特点,构建带有权重的MOFs 基因片段库,建立大规模MOFs材料数据库。在此基础上,可以采用底层设计的思路,构建并筛选适用于不同种类药物分子的吸附材料。
(3)虽然多种MOFs 材料表现出良好的热力学平衡吸附能力,但对动力学吸附性能的研究较少,特别是对影响动力学吸附的因素。根据对热力学和动力学吸附性能的调控结果,设计并构建适当的吸附装置,有助于将实验室的研究成果应用于实际工程中,不仅可以为废水中痕量药物分子的深度脱除提供技术储备,同时也可以促进MOFs 及MOFs 复合材料的实际应用。
