腹腔镜胃穿孔修补术治疗胃穿孔的效果及对IL-6、TNF-α、CRP水平的影响
2020-06-22李建勋
李建勋
海南省澄迈县中医院外科,海南澄迈 571900
胃穿孔属于胃溃疡最严重的并发症之一,具有起病急、进展迅速的特点,如不采取及时的治疗措施,则极易引发急性腹膜炎和感染性休克,严重威胁着患者的生命安全[1]。临床上多使用开腹修补术进行治疗,它可在短时间内对黏膜进行完整性的修补,但对患者造成的创伤较大,且术后并发症较多。近年来腹腔镜胃穿孔修补术因其创伤小、恢复快、术后效果佳的特点,目前在临床上被广泛应用[2]。本研究探讨了腹腔镜胃穿孔修补术治疗胃穿孔的效果,结果如下。
1 资料与方法
1.1 一般资料
选取我院2018 年5 月~2019 年6 月收治的胃溃疡并发胃穿孔患者112 例,按照手术方法的不同分为对照组和实验组,各56 例。对照组男31 例,女25 例;年龄30 ~70 岁,平均(37.8±6.2)岁;病程3 ~15h,平均(4.25±1.10)h;穿孔部位:胃窦部25 例,胃体16 例,胃大弯10 例,胃小弯5 例。实验组男33 例,女23 例;年龄30 ~70 岁,平均(37.7±6.4)岁;病程3 ~15h,平均(4.33±1.30)h;穿孔部位:胃窦部24 例,胃体17 例,胃大弯9 例,胃小弯6 例。两组基本资料经比较差异无统计学意义(P >0.05),具有可比性。诊断标准:经胃镜检查确诊为胃溃疡并发穿孔。纳入标准:(1)符合上述诊断标准者;(2)凝血指标正常者;(3)患者及家属对本研究均知情同意等。排除标准:(1)合并肠道梗阻患者;(2)有胃部手术史者;(3)合并心、肝、肾等功能障碍者。
表1 两组手术相关指标比较

表1 两组手术相关指标比较
组别 手术时间(min) 住院时间(d) 切口长度(cm) 术中出血量(mL)对照组(n=56) 85.90±10.65 7.62±1.43 14.78±2.14 81.85±10.53实验组(n=56) 74.35±11.28 5.76±1.04 3.75±0.66 48.46±8.60 t 5.572 7.872 36.857 18.379 P <0.05 <0.05 <0.05 <0.05
表2 两组手术前后IL-6、TNF-α、CRP水平变化比较
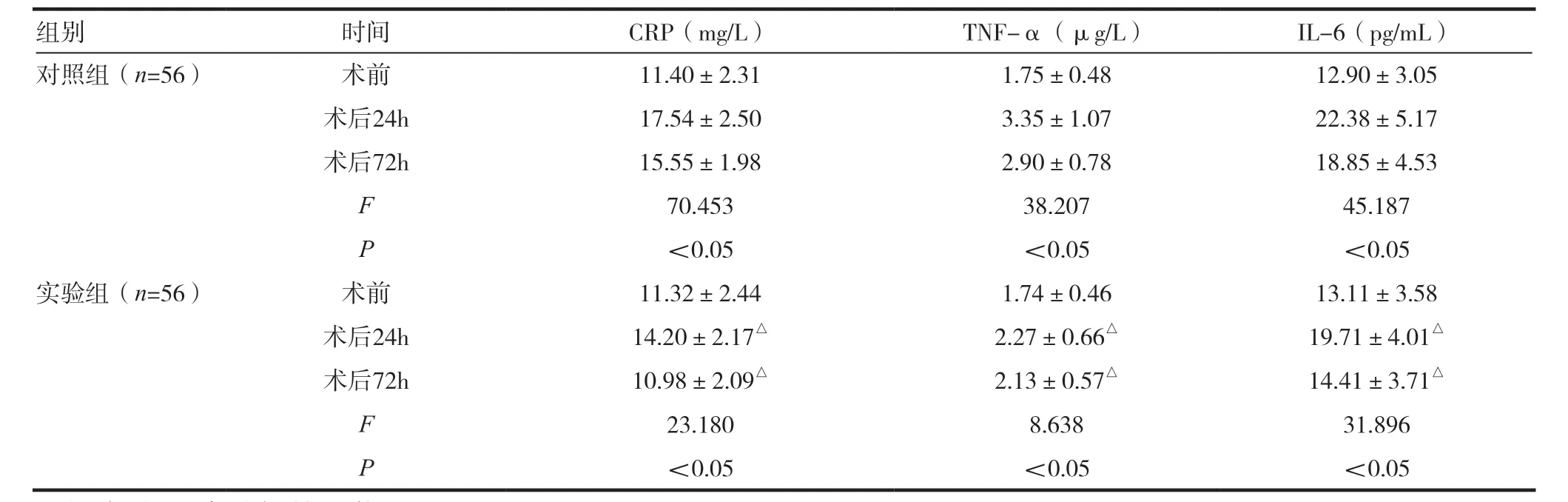
表2 两组手术前后IL-6、TNF-α、CRP水平变化比较
注:与对照组各对应时间比较,△P <0.05
组别 时间 CRP(mg/L) TNF-α(μg/L) IL-6(pg/mL)对照组(n=56) 术前 11.40±2.31 1.75±0.48 12.90±3.05术后24h 17.54±2.50 3.35±1.07 22.38±5.17术后72h 15.55±1.98 2.90±0.78 18.85±4.53 F 70.453 38.207 45.187 P <0.05 <0.05 <0.05实验组(n=56) 术前 11.32±2.44 1.74±0.46 13.11±3.58术后24h 14.20±2.17△ 2.27±0.66△ 19.71±4.01△术后72h 10.98±2.09△ 2.13±0.57△ 14.41±3.71△F 23.180 8.638 31.896 P <0.05 <0.05 <0.05
1.2 方法
对照组使用传统开腹手术,首先对患者进行全麻,取患者上腹正中位置,做一个横向15cm 左右的切口,使穿孔部位完全暴露,对坏死组织切除后进行修补,随后使用氯化钠溶液进行冲洗,放置引流管并缝合伤口。实验组使用腹腔镜胃穿孔修补术治疗,具体操作方法如下:对患者全麻以后建立人工CO2气腹(气腹压力在13 ~15mm Hg),之后在脐下穿刺10mm Trocar 进行探查,于剑突偏右置入10mm Trocar 进行手术操作,探查穿孔部位后清除胃内容物,并对病灶周围组织进行清除,于穿孔部位边缘进行修补,修补后使用大网膜覆盖,清除渗液后置入引流管,并于术后2 ~3d 拔除。两组均于术后进行抗感染、抑酸治疗。
1.3 观察指标
(1)比较两组手术相关指标,包括手术时间、术中出血量、切口长度、住院时间。(2)比较两组术前与术后白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、C 反应蛋白(CRP)水平的变化,分别于术前、术后24h 及术后72h 抽取两组空腹静脉血,使用酶联免疫吸附法进行检测。(3)比较两组术后并发症发生情况,包括肠梗阻、切口感染、切口裂开、腹腔感染。
1.4 统计学方法
数据应用SPSS20.0 软件分析,计量资料与计数资料分别以()及[n(%)]表示,组间比较分别采用t 及χ2检验,多组间比较采用重复测量方差分析,以P <0.05 为差异有统计学意义。
2 结果
2.1 两组手术相关指标比较
与对照组比较,实验组的手术时间、住院时间、切口长度均明显缩短,术中出血量明显减少,差异有统计学意义(P <0.05)。见表1。
2.2 两组手术前后IL-6、TNF-α、CRP水平变化比较
与术前比较,术后24 ~72h 两组IL-6、TNF-α、CRP 水平均先升高后降低,且术后24、72h 实验组升高与降低的幅度均低于对照组,差异有统计学意义(P <0.05)。见表2。

表3 两组术后并发症发生情况比较[n(%)]
2.3 两组术后并发症发生情况比较
实验组的并发症发生率为10.71%,低于对照组的26.79%,差异有统计学意义(P <0.05)。见表3。
3 讨论
胃穿孔发生的原因是在胃溃疡的基础上暴饮暴食所致,其临床症状多表现为患者突然发生剧烈腹痛,且随着时间的推移,疼痛可由穿孔部位扩散至整个腹部,进而导致大量十二指肠液、胆汁等进入腹腔,大大增加了细菌感染、炎症的发生风险,严重者甚至出现失血性休克[3-4]。临床上多行开腹手术进行治疗,取得了一定的疗效。但相关研究[5]显示,部分胃溃疡并发胃穿孔患者行开腹手术后,再次发生胃穿孔的几率可达5%以上,且术后极易产生切口愈合不良、脂肪液化及血肿现象。
与传统开腹修补术比较,腹腔镜胃穿孔修补术的优点在于:(1)建立人工CO2气腹,经穿刺孔放置腹腔镜,可以在不牵动腹腔器官的情况下对病变部位进行观察,从而清晰、准确地探查胃穿孔情况,使漏诊、误诊的几率降低。(2)由于腹腔镜修补术处于密闭的环境中,并未完全暴露腹腔,避免了细菌对腹腔的污染,减少了腹腔感染的发生;且术中切口较小,可促进患者术后伤口的愈合;同时患者可早日下床活动,有助于患者早日恢复胃肠功能。(3)使用腹壁打孔取代了上腹正中切口,可避免神经、血管等的损伤,减少肌肉层次的粘连,最大限度地减少对肠道的损害。(4)腹腔镜手术对于癌肿瘤病灶的牵拉传递较低,可避免手术操作中的邻近胃黏膜受损,降低胃穿孔的复发率,提高生存预后[6-9]。本研究结果显示,与对照组比较,实验组的手术时间、住院时间、切口长度均明显缩短,术中出血量明显减少,且术后并发症发生率较低,与胡加文[10]的研究结果一致。
IL-6、TNF-α、CRP 在促进机体炎症反应、加剧组织损伤中占重要作用[11]。临床研究[12]表明,腹腔镜手术可在病灶修补效果的基础上,降低对机体炎症反应的刺激,使细胞炎症因子处于稳定状态,其可能机制在于:(1)腹腔镜手术几乎不牵动腹腔器官,从而使术后机体诱导产生的 IL-6、TNF-α、CRP 等因子数量减少;(2)腹腔镜手术中进行的双极电凝等操作,可在一定程度上抑制胃黏膜引起的单核细胞激活,避免了细胞因子的大量分泌[13-15]。本研究结果显示,与术前比较,术后24 ~72h 两组IL-6、TNF-α、CRP 水平均先升高后降低,且实验组升高与降低的幅度均低于对照组, 提示腹腔镜胃穿孔修补术可以显著降低胃穿孔患者机体的炎症反应,有利于患者改善预后。
综上,腹腔镜胃穿孔修补术用于治疗胃穿孔时的手术时间、住院时间、切口长度较短,术中出血量较少且并发症发生率较低,同时可显著降低患者术后的炎症反应,值得推广应用。
