酪氨酸激酶抑制剂治疗慢性髓性白血病的预后系统及因素的比较分析
2020-06-19张淳嘉郑小玲郑丹钿夏维林苏秀连
张淳嘉 郑小玲 郑丹钿 夏维林 苏秀连

【摘要】 目的 分析比較Sokal、Euro和EUTOS积分系统以及3个月、6个月的早期分子学反应(early molecular response,EMR)在酪氨酸激酶抑制剂(Tyrosine kinase inhibitors,TKI)治疗慢性髓性白血病慢性期(chronic myeloid leukemia-chronic phase,CML-CP)中的预后意义。
方法 回顾性分析2012年1月1日至2019年9月1日收治的以伊马替尼为一线治疗药物的CML-CP患者共72例,研究Sokal积分、Euro积分、EUTOS积分三大预后系统,以及治疗3个月、6个月的EMR对总生存期(Overall survival,OS)及无进展生存期(Progression-free survival,PFS)的影响,生存分析采用Kaplan-Meier方法,各组生存率的比较采用log-rank检验。
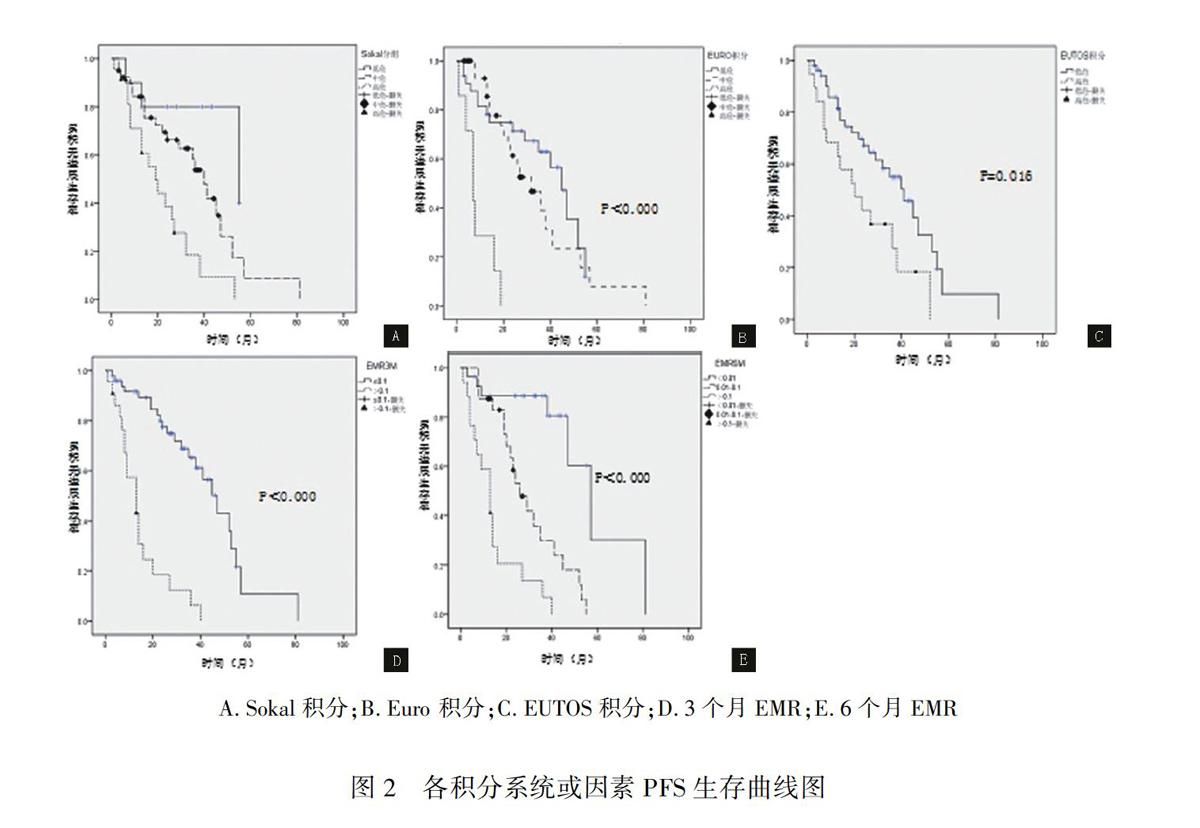
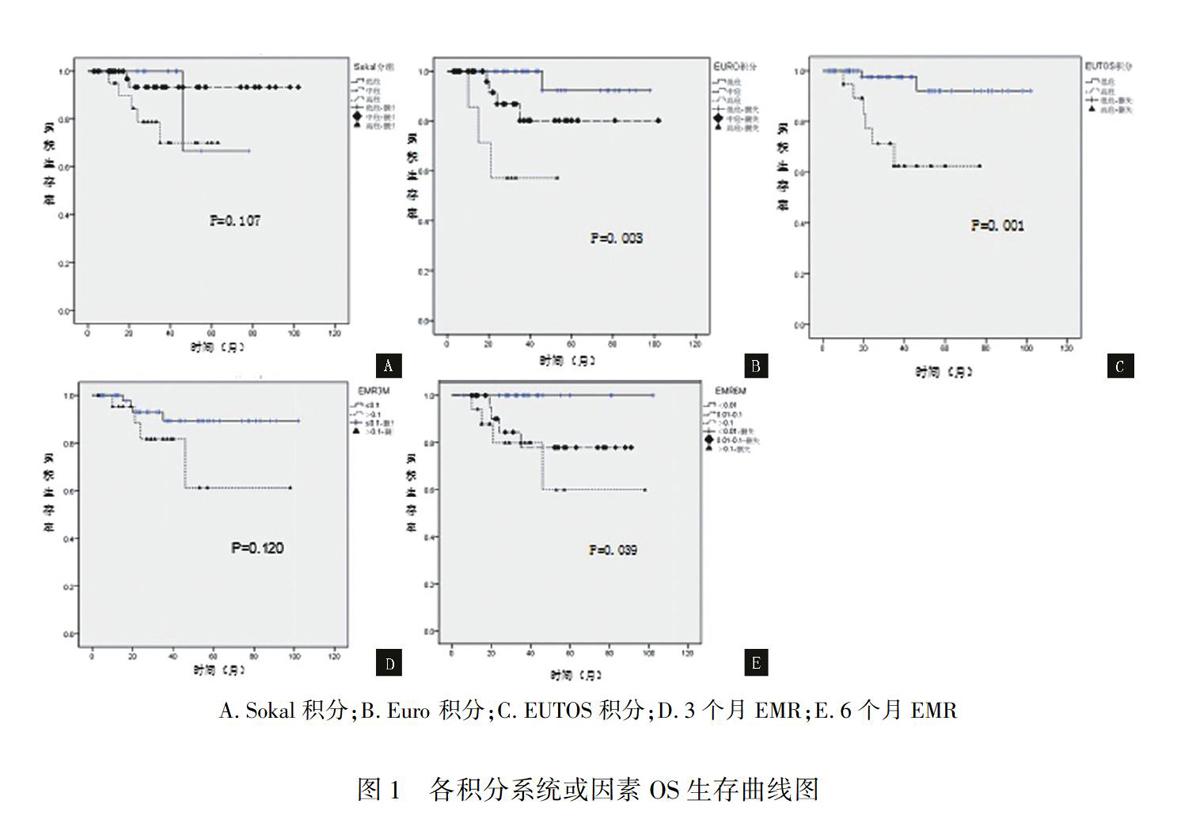
结果 入组72例患者,男39例,女33例,初诊中位年龄 45(10~81)岁。截至2019年12月31日,伊马替尼治疗后中位观察期为61(4~96)个月,有8例患者死亡,中位5年OS率为88.89%;有42例患者出现疾病进展,中位5年PFS率为41.67%。各组OS率显示,Euro积分系统(96.97% VS 87.50% VS 51.14%)、EUTOS积分系统(96.23% VS 31.58%)、6个月的EMR(100.00% VS 83.33% VS 76.47%),各组OS率差异有统计学意义,P值分别为0.003、0.001、0.039;Sokal积分系统(90.00% VS 94.87% VS 78.26%)及3个月EMR(92.00% VS 81.82%),各组中位5年OS差异无统计学意义,P值分别为0.107、0.120;Sokal积分系统(70.00% VS 41.03% VS 26.09%)、Euro积分系统(51.52% VS 40.63% VS 0.00%)、EUTOS积分系统(49.06% VS 21.05%)、3个月 EMR(54.00% VS 13.64%)、6个月的EMR(74.07% VS 20.83% VS 5.88%),各组中位5年 PFS差异均有统计学意义,P值分别为0.002、<0.001、0.016、<0.001、<0.001。
结论 Euro积分系统、EUTOS积分系统、6个月的EMR可预测TKI治疗CML-CP患者的OS,Sokal积分系统、Euro积分系统、EUTOS积分系统、3个月 EMR、6个月的EMR均对PFS有明显预测作用。
【关键词】 慢性髓性白血病;酪氨酸激酶抑制剂;预后因素
中图分类号:R733.72 文献标志码:A DOI:10.3969/j.issn.1003-1383.2020.05.004
Comparative analysis of prognostic systems and factors of chronicmyeloid leukemia treated with tyrosine kinase inhibitors
ZHANG Chunjia,ZHENG Xiaoling,ZHENG Dantian,XIA Weilin,SU Xiulian
(Department of Hematology,Jieyang People' s Hospital,Jieyang 522000,Guangdong,China)
【Abstract】 Objective To analyze and compare the prognostic significance of Sokal,Euro and EUTOS integral systems and early molecular response(EMR) at 3 and 6 months in the treatment of chronic myeloid leukemia-chronic phase (CML-CP) with tyrosine kinase inhibitors(TKI).
Methods Retrospective analysis was carried out on CML-CP patients admitted to hospital from January 1,2012 to September 1,2019 who were treated with imatinib as first-line therapy.The effects of Sokal score,Euro score and EUTOS score,as well as EMR at 3 and 6 months of treatment on overall survival(OS) and progression-free survival(PFS) were studied.Kaplan Meier method was used for survival analysis,and log-rank test was used for comparison of survival rates of each group.
Results 72 patients were enrolled(39 males and 33 females),and the median age was 45(10-81) years.Up to December 31,2019,the median observation period was 61(4-96) months,8 patients died,and the median 5-year OS rate was 88.89% after imatinib treatment.42 patients had disease progression,with a median 5-year PFS rate of 41.67%.The OS rate of each group showed that Euro integral system was(96.97% VS 87.50%VS 51.14%),EUTOS integral system was (96.23% VS 31.58%),6 months EMR was (100.00% VS 83.33% VS 76.47%),and the difference of OS rate of each group was statistically significant,P values were 0.003,0.001 and 0.039,respectively.Sokal integral system was (90.00% VS 94.87% VS 78.26%) and 3 months EMR (92.00% VS 81.82%),and the difference of median 5-year OS in each group was not statistically significant,P values were 0.107 and 0.120,respectively.Sokal integral system was (70.00% VS 41.03% VS 26.09%),Euro integral system was (51.52% VS 40.63% VS 0.00%),EUTOS integral system was (49.06% VS 21.05%),EMR of 3 months was (54.00% VS 13.64%),EMR of 6 months was (74.07% VS 20.83% VS 5.88%),and the difference of median 5-year PFS in each group was statistically significant,P values were 0.002,<0.001,<0.016,<0.001 and <0.001,respectively.
Conclusion The Euro score,EUTOS score and 6 months EMR can predict the OS in the patients with CML-CP treated with TKI,and Sokal score,Euro score and EUTOS score,3 months EMR and 6 months EMR can predict PFS.
【Key words】 CML;TKI;prognostic factors
慢性髓性白血病(chronic myeloid leukemia-chronic phase,CML)是一种多能造血干细胞引起的恶性血液病,具有特征性的BCR/ABL融合基因和(或)费城染色体[1],针对该融合基因的酪氨酸激酶抑制剂(Tyrosine kinase inhibitors,TKI)的靶向治疗,使CML的治疗效果发生革命性的改变,由此CML的治疗进入了TKI时代。但仍有部分患者在治疗过程中发生疾病进展、耐药、无法达到深度缓解。这部分患者通常可能存在一个或多个危险因素,导致治疗效果不佳。关于CML预后的评估,最经典的有Sokal[2]、Euro[3]、EUTOS[4]等积分系统,近年来国内外发现治疗早期分子学反应(early molecular response,EMR)也是重要的预后因素[5~7],包括3个月的EMR及6个月的EMR。这些系统在真实世界中的应用意义如何,本研究通过回顾性分析过去几年在我院收治的CML患者的诊治资料,综合对上述五个系统或因素进行研究,旨在评估各个预后因素在真实世界中的预后意义。
1 病例与方法
1.1 病例选择
回顾性分组研究2012年1月1日至2019年9月1日在我院就诊的CML-CP患者,筛选出符合入组标准的患者共72例作为研究对象。入组标准:(1)诊断均符合中国慢性髓性白血病诊断与治疗指南(2016年版)慢性髓性白血病慢性期的诊断标准[8];(2)以第一代TKI伊马替尼作为一线治疗药物,初始治疗剂量为 400 mg,QD;(3)具有完整初诊资料和治疗过程监测资料。
第1例患者的入组日期为2012年4月27日,最后1例患者的入组日期为2019年8月25日,随访方式包括查阅住院资料、门诊随访,随访截止日期为2019年12月31日,失访病例5例,失访日期记为截尾值,伊马替尼治療后中位观察期为61(4~96)月,约5年。
1.2 研究参数
计算Sokal、Euro、EUTOS积分并分别进行危险分层,按危险分层分组,搜集第3个月的分子转录水平(分为≤10%、>10%两组)及第6个月的分子转录水平(分为<1%、1%~10%、>10%三组)。Sokal积分公式[2]:exp[0.0116(年龄-43.4)]+0.0345(脾脏大小-7.51)+0.188[(PLT/700).2-0.563]+0.0887(原始细胞-2.1),以积分0.8分及1.2为界分为低危、中危、高危三组;Euro积分公式[3]:0.666(当年龄≥50岁)+(0.042×脾脏大小)+1.0956(当PLT≥1500×10.9/L)+(0.0584×原始细胞)+0.203 99(当嗜碱粒细胞>3%)+(0.0413×嗜酸粒细胞)×100,以781分及1480分为界分为低危、中危、高危三组。
以上两种积分的计算均通过意大利慢性髓性白血病合作研究小组官网(http://www.icsg.unibo.it/index.asp)积分系统进行计算。
EUTOS积分公式[4]:脾脏大小(肋下至下缘厘米数)×4+外周血嗜碱粒细胞(%)×7,≤87分为低危组,>87分为高危组。
采用国际标准化RQ-PCR进行第3个月、第6个月BCR-ABL分子转录水平的监测,符合中国慢性髓性白血病诊疗监测规范(2014年版) [9]的监测标准,以BCR-ABLIS表示。
1.3 观察指标
截至2019年12月31日,比较各因素内各分组的总生存期(Overall survival,OS)及无进展生存期(Progression-free survival,PFS)。PFS定义为发病至发生第一次疾病进展的时间,疾病进展定义包括:(1)至少每3个月一次的分子转录水平监测发现较上一次的水平增加10%;(2)发生激酶突变;(3)转变成加速期或急变期。OS及PFS的时间以月(m)作为单位。
1.4 统计学方法
应用 SPSS 21.0 软件分析结果,所得数据计量资料采用均数(范围)表示,计数资料采用百分率表示,生存分析采用Kaplan-Meier方法,各组OS及PFS比较采用log-rank检验,检验水准:α=0.05,双侧检验。
2 结果
2.1 病例的基线临床特征
72例符合入组标准,其中男39例,女33例,初诊时中位年龄45(10~81)岁,白细胞计数153.13(102.17~714.93)×10.9/L,血红蛋白100.5(41~166)g/L,血小板计数422.5(118~982)×10.9/L,嗜碱性粒细胞比例6.05(1.2~10)%,嗜酸性粒细胞比例1.75(0.3~9.3)%,肋下脾长度6.85(0~13)cm,外周血原始细胞比例4(0~6)%。
2.2 分组与治疗结果
中位Sokal积分1.25(0.52~6.35)分,其中低危组10例,中危组39例,高危组23例;中位Euro积分1324(224.1~2556.37)分,其中低危组33例,中危组32例,高危组7例;EUTOS积分73.3(28.9~110.7)分,其中低危组53例,高危组19例;72例患者均有治疗第3个月的BCR/ABL分子转录水平记录,其中≤10% 50例,>10% 22例;因有4例患者至研究截止日期2019年12月31日尚未达到评估治疗第6个月的分子转录水平,故只有68例患者具备治疗第6个月BCR/ABL分子转录水平记录,其中<1% 27例,1%~10% 24例,>10% 17例。
截至2019年12月31日,伊马替尼治疗后中位观察期为61(4~96)月,有8例患者死亡,失访5例,失访时间记录为截尾值,中位5年OS为88.89%;有42例患者至少出现一次疾病进展事件,中位5年PFS为41.67%。
42例发生过至少一次进展的患者中,均有发生分子转录水平明显升高,其中单纯发生分子转录水平明显升高25例,在改用二代TKI后重新获得原来分子学缓解深度,甚至更佳。检测到发生激酶突变的有7例,有3例首次发生T315I突变,2例检测到时已经发生急变,均有口服第三代TKI普纳替尼和(或)联合化疗后好转,至今2例患者仍存活。有1例患者发生F317L突变,更换尼洛替尼后好转,半年后出现T315I突变,口服第三代TKI普纳替尼联合化疗好转,但1个月后不幸再次急变死亡;其他突变患者2例,分别为E255V、V299L,更换敏感TKI后改善。发生加速或急变12例,死亡8例,其中5例进行异基因造血干细胞移植,至随访结束仍有3例存活。
2.3 各组OS与PFS比较
各分组患者中位5年OS率及PFS率比较如表1所示。OS与PFS生存曲线图如图1、图2所示。
3 讨论
研究显示第一代TKI伊马替尼作为一线治疗药物使CML患者的10年生存率达85%~ 90%[10]。本研究72例患者,中位5年OS达到88.89%,与该数据相近。但本研究72例患者中位5年的PFS仅为41.67%,有超过一半的患者在第一代TKI的治疗过程中出现了耐药、疾病恶化,意大利成人血液病研究组[11]展开了一项纳入556例CML-CP患者的临床研究,在大于6年的中位治疗期中,只有65%的患者仍然用伊马替尼治疗,35%无继续服用伊马替尼的患者,其主要原因为耐药或疾病恶化,说明对于部分患者而言,第一代TKI并不是获得长期PFS的理想选择,这部分患者可能存在预后不良因素。国内外关于慢性髓性白血病患者的预后研究有很多[12~13],最经典的为本文最初提到的三大积分预后系统,还有近年来热门的早期分子学反应。但这些预后系统或因素对预测TKI时代CML患者的治疗反应是否都有显著的预测作用,目前仍存在一定爭议[14~16]。
Sokal积分预后系统是SOKAL教授等人[2]在1984年提出,主要是针对白消安和羟基脲治疗CML的预后,而Euro积分预后系统[3]是HASFORD教授团队在1998年提出,主要针对干扰素治疗CML的预后,这两个系统都是在TKI时代出现之前提出的,包括了年龄、血小板计数、外周血嗜酸及嗜碱性粒细胞、肋下脾长度等。2011年,通过一个纳入2060例CML病例的临床研究,HASFORD教授团队[4]提出TKI时代第一个预后系统EUTOS积分系统,该积分系统较Sokal及Euro预后积分系统所需数据明显减少,仅包括了外周血嗜碱性粒细胞的比例以及肋下脾长度两个因素,而研究结果显示,这个系统可预测患者的完全遗传学缓解和PFS。
国内有研究[17]比较上述三个系统,结果显示,与Sokal、Euro评分系统相比,EUTOS评分与患者5年预期OS、PFS、EFS的一致性较高,以Sokal或Euro评分系统划分的低危、中危、高危组,5年OS、EFS及PFS之间差异无统计学意义。冯格格等[18]回顾性分析113例CML患者,比较3种积分系统的预后作用,结果显示三种积分系统均能显著区分各危险组患者生存期的差异,其中EUTOS积分系统可能更为准确。国外学者BACCARANI等[19]亦对三个系统进行比较,发现EUTOS评分可以更好地预测总体生存率和完全遗传学缓解率。
本研究显示EUTOS不管是预测OS还是PFS都有明显的预测作用,而三个系统均可较好预测患者的PFS。说明Sokal与Euro系统对于TKI治疗CML有一定的预测作用,但相关性不如EUTOS,与上述研究结果相似。相比EUTOS,Sokal及Euros积分系统计算更繁琐,需要的基线资料更多,故EUTOS积分系统比Sokal及Euro预后积分系统在预测TKI治疗CML的疗效上更具备优势。
近年国内外研究认为早期分子学缓解[6~7],即第3个月的BCR/ABLIS≤0.1,对CML的预后至关重要,也有人发现,即使没有达到早期分子学缓解,在第6个月达到较好的分子学反应的患者也可以获得理想的治疗效果[20]。MARIN等[21]甚至认为3个月的EMR是预测深度缓解的唯一指标。本研究3个月、6个月的EMR分层在PFS上均有明显的区别,但对于OS的预测,3个月的EMR并没有表现出较好的预测作用,结合其他研究结果,考虑是否3个月的EMR对于预测深度缓解及PFS、EFS有更强相关性。
TKI使CML获得长期生存的机会,但长期服药面临着不适及经济负担重等现实问题,国内外临床研究[22~23]探讨停药的可行性,虽然仍然未有停药的全球共识,但获得深度缓解至少2年是目前都认可的停药条件之一。临床研究[24]显示新一代的TKI作为CML患者的一线治疗,可使患者更快获得深度缓解,但由于二代TKI相对一代价格高,目前我国大部分中心依然将一代TKI作为CML的一线选择,但如本研究所示,部分患者并不能通过服用第一代TKI获得长期PFS,最终需改用新一代TKI,可能耽误了更快获得深度缓解的机会,甚至造成疾病恶化,假如将一部分存在不良预后因素的患者以二代TKI作为一线治疗,可能可以提升这部分患者的PFS,让患者更早获得长期稳定的深度缓解,更早达到停药的目的。
综上,Euro积分系统、EUTOS积分系统、6个月的EMR可预测TKI治疗时代CML-CP患者的OS,Sokal积分系统、Euro积分系统、EUTOS积分系统、3个月 EMR、6个月的EMR均对PFS有明显预测作用。EUTOS预后积分系统相对其他两个积分系统对预后相关性更强,且更易操作,对初诊患者进行EUTOS积分,按危险分层选择一线药物,而在治疗的过程中,监测早期分子学反应,对于不能到达理想早期分子学反应的患者及时更换TKI,可能可使患者获得更好的治疗效果。由于本研究的样本量不多,存在不足,有待后续增加样本量进一步研究。
参 考 文 献
[1] HEHLMANN R,HOCHHAUS A,BACCARANI M,et al.Chronic myeloid leukaemia[J].Lancet,2007,370(9584):342-350.
[2] SOKAL J E,COX E B,BACCARANI M,et al.Prognostic discrimination in "good-risk" chronic granulocytic leukemia[J].Blood,1984,63(4):789-799.
[3] HASFORD J,PFIRRMANN M,HEHLMANN R,et al.A new prognostic score for survival of patients with chronic myeloid leukemia treated with interferon Alfa.Writing Committee for the Collaborative CML Prognostic Factors Project Group[J].J Natl Cancer Inst,1998,90(11):850-858.
[4] HASFORD J,BACCARANI M,HOFFMANN V,et al.Predicting complete cytogenetic response and subsequent progression-free survival in 2060 patients with CML on imatinib treatment:the EUTOS score[J].Blood,2011,118(3):686-692.
[5] JAIN P,KANTARJIAN H,NAZHA A,et al.Early responses predict better outcomes in patients with newly diagnosed chronic myeloid leukemia:results with four tyrosine kinase inhibitor modalities[J].Blood,2013,121(24):4867-4874.
[6] KIM D D,LEE H,KAMEL-REID S,et al.BCR-ABL1 transcript at 3 months predicts long-term outcomes following second generation tyrosine kinase inhibitor therapy in the patients with chronic myeloid leukaemia in chronic phase who failed Imatinib[J].Br J Haematol,2013,160(5):630-639.
[7] YUE Y H,GUI X M,HE X F,et al.Deep molecular responses achieved in chronic myeloid leukemia in chronic phase patients with BCR-ABL1 >10% at 3 months who are early switched to nilotinib[J].Hematology,2016,21(4):213-217.
[8] 中華医学会血液学分会.中国慢性髓性白血病诊断与治疗指南(2016年版)[J].中华血液学杂志,2016,37(8):633-639.
[9] 中华医学会血液学分会实验诊断学组,中国慢性髓性白血病联盟专家组.中国慢性髓性白血病诊疗监测规范(2014年版)[J].中华血液学杂志,2014,35(8):781-784.
[10] KALMANTI L,SAUSSELE S,LAUSEKER M,et al.Safety and efficacy of imatinib in CML over a period of 10 years:data from the randomized CML-study IV[J].Leukemia,2015,29(5):1123-1132.
[11] CASTAGNETTI F,GUGLIOTTA G,BRECCIA M,et al.Long-term outcome of chronic myeloid leukemia patients treated frontline with imatinib[J].Leukemia,2015,29(9):1823-1831.
[12] CASTAGNETTI F,GUGLIOTTA G,BACCARANI M,et al.Differences among young adults,adults and elderly chronic myeloid leukemia patients[J].Ann Oncol,2015,26(1):185-192.
[13] NIEVERGALL E,REYNOLDS J V,KOK C H,et al.TGF-α and IL-6 plasma levels selectively identify CML patients who fail to achieve an early molecular response or progress in the first year of therapy[J].Leukemia,2016,30(6):1263-1272.
[14] JABBOUR E,CORTES J E,NAZHA A,et al.EUTOS score is not predictive for survival and outcome in patients with early chronic phase chronic myeloid leukemia treated with tyrosine kinase inhibitors:a single institution experience[J].Blood,2012,119(19):4524-4526.
[15] MARIN D,IBRAHIM A R,GOLDMAN J M.European Treatment and Outcome Study (EUTOS) score for chronic myeloid leukemia still requires more confirmation[J].J Clin Oncol,2011,29(29):3944-3945.
[16] GIONA F,SAGLIO G,SANTOPIETRO M,et al.Early response does not predict outcome in children and adolescents with chronic myeloid leukaemia treated with high-dose imatinib[J].Br J Haematol,2018,180(6):895-898.
[17] 黃菁,赵谢兰.3种预后评分系统评估慢性髓细胞白血病的预后比较[J].中南大学学报:医学版,2016,41(8):809-814.
[18] 冯格格,王建虹,姜玉杰,等.Sokal、 Hasford和EUTOS积分系统在慢性髓性白血病中的临床意义[J].中华血液学杂志,2014,35(8):743-746.
[19] BACCARANI M,DEININGER M W,ROSTI G,et al.European Leukemia Net recommendations for the management of chronic myeloid leukemia[J].Blood,2013,122(11):872-884.
[20] KIM D D,HAMAD N,LEE H G,et al.BCR/ABL level at 6 months identifies good risk CML subgroup after failing early molecular response at 3 months following imatinib therapy for CML in chronic phase[J].Am J Hematol,2014,89(6):626-632.
[21] MARIN D,IBRAHIM A R,LUCAS C,et al.Assessment of BCR-ABL1 transcript levels at 3 months is the only requirement for predicting outcome for patients with chronic myeloid leukemia treated with tyrosine kinase inhibitors[J].J Clin Oncol,2012,30(3):232-238.
[22] 朱晓健,游泳,段明辉,等.慢性髓性白血病患者酪氨酸激酶抑制剂自动停药的多中心回顾性研究[J].中华血液学杂志,2018,39(12):994-997.
[23] HUGHES T P,ROSS D M.Moving treatment-free remission into mainstream clinical practice in CML[J].Blood,2016,128(1):17-23.
[24] CORTES J E,SAGLIO G,KANTARJIAN H M,et al.Final 5-year study results of DASISION:the dasatinib versus imatinib study in treatment-naive chronic myeloid leukemia patients trial[J].J Clin Oncol,2016,34(20):2333-2340.
(收稿日期:2020-03-23 修回日期:2020-04-23)
(編辑:潘明志)
基金项目:广东省医学科学技术研究基金项目(A2019350)
作者简介:张淳嘉,女,主治医师,医学硕士,研究方向:血液系统疾病。E-mail:chunkid@126.com
[本文引用格式]张淳嘉,郑小玲,郑丹钿,等.酪氨酸激酶抑制剂治疗慢性髓性白血病的预后系统及因素的比较分析[J].右江医学,2020,48(5):339-344.
