糖皮质激素在新型冠状病毒肺炎重症患者中的应用▲
2020-06-19周甘平黄华田韦定春谢华志戴小英
兰 博 周甘平 黄华田 韦定春 谢华志 戴小英 郑 立
(广西壮族自治区江滨医院1 临床药学科,2 重症医学科,3 呼吸内科,南宁市 530021,电子邮箱:1187274546@qq.com)
【提要】 及时有效的炎症干预与新型冠状病毒肺炎(COVID-19)重症患者的预后息息相关。近期,COVID-19重症患者病情的突然加重被认为可能与机体细胞因子风暴有关,但目前并无针对的特效药。而糖皮质激素能够抑制机体炎症风暴从而为该类患者的救治赢得时间,但其亦可能抑制机体免疫应答、延缓病毒清除从而饱受争议。本文结合相关文献,对糖皮质激素在COVID-19重症患者中的应用进行探讨,以期为临床治疗提供参考。
自2019年12月份以来,湖北省武汉市陆续出现了多例新型冠状病毒肺炎(COVID-19)患者,该病具有传播迅速且广泛、传染性强、各类人群普遍易感等特点[1-2]。其中危重症患者发病率约为5%,危重症患者病死率约为49%[3],当前疫情形势仍然严峻。研究表明,COVID-19重症患者的病情严重程度与机体炎症反应过度激活密切相关,如果患者体内出现过度的炎症反应(即“细胞因子风暴”)会导致多器官功能衰竭,严重者甚至死亡[4]。因此,对于COVID-19重症患者,除了积极抗病毒治疗外,免疫治疗策略显得尤为重要。国家卫健委医政医管局最新发布的《新型冠状病毒肺炎诊疗方案(试行第六版)》[5]将糖皮质激素纳入COVID-19重型、危重型患者的诊疗方案中,通过免疫抑制达到抑制细胞因子风暴的目的。但是,使用糖皮质激素可能会造成原有感染加重、病程延长等不良反应,且大剂量长时间使用糖皮质激素可导致骨折、股骨头坏死、高血糖、消化道出血等严重后遗症[6-7]。本文将分析糖皮质激素治疗COVID-19的理论依据及临床证据、用药选择及存在的争议,并就其合理使用及药学监护提出建议,以期为COVID-19的临床治疗提供参考。
1 细胞因子风暴的概述
细胞因子风暴由Ferrara[8]在1993年首次提出,从2003年SARS开始,细胞因子风暴由于引起多器官功能衰竭并导致极高的死亡率[9],从而逐步引起关注。细胞因子风暴是机体对细菌、病毒等外界刺激产生的一种过度免疫反应[4]。病毒攻击机体时,可刺激大量炎症因子产生而引发细胞级联反应,造成机体过度免疫应答,从而引起肺部弥漫性损伤、多器官功能衰竭,严重时可导致死亡[10]。
细胞因子风暴的机制目前尚未完全明确。当病原体入侵人体后,上皮细胞及自然杀伤细胞分别产生干扰素-α/β、白细胞介素(interleukin,IL)-1β及干扰素-γ以激活巨噬细胞,活化后的巨噬细胞释放大量肿瘤坏死因子(tumor necrosis factor,TNF)-α、IL-12等细胞因子反过来激活自然杀伤细胞,即形成“正反馈”调节,从而导致细胞因子急剧增多[11]。正常情况下,一旦机体在“正反馈”调节下控制住入侵的病原体,抗原信号提呈给适应性免疫系统的信号减弱,细胞因子释放就会开始减少,炎症反应也会逐步减弱,从而形成“负反馈”调节[12]。Huang等[13]发现COVID-19重症患者粒细胞集落因子、干扰素诱导蛋白10、单核细胞趋化蛋白1、巨噬细胞炎性蛋白1α、TNF-α水平高于非重症患者,表明细胞因子风暴与COVID-19 疾病严重程度相关。
2 糖皮质激素治疗细胞因子风暴的理论依据
目前,糖皮质激素用于治疗IL-6受体拮抗剂治疗无效的难治性细胞因子风暴已得到广泛认可[14]。糖皮质激素进入血液后,大部分与皮质激素结合蛋白及白蛋白相结合形成复合体,少量游离的糖皮质激素通过扩散作用透过细胞膜而进入胞浆,与糖皮质激素受体结合后,进入细胞核诱导或抑制炎症相关基因的表达,发挥抗炎作用[15]。
3 糖皮质激素应用于COVID-19的治疗
3.1 糖皮质激素用于治疗COVID-19的临床证据 糖皮质激素曾被广泛应用于治疗严重急性呼吸综合征(severe acute respiratory syndrome,SARS)和中东呼吸综合征(Middle East respiratory syndrome,MERS),在此次COVID-19疫情中其也联合其他药物用于重症、危重症患者的救治。目前,在COVID-19重症患者中使用小至中等剂量的糖皮质激素的证据,主要来源于针对SARS及H1N1流感病毒的研究。一项纳入401例SARS患者的研究表明,合理使用糖皮质激素可以降低SARS重症患者的病死率并缩短住院时间,且未明显增加患者新发感染及其他并发症的发生率[16]。国内一项纳入2 141例甲型H1N1流感病毒性肺炎患者的前瞻性队列研究也表明,小至中等剂量的糖皮质激素(25~150 mg/d甲泼尼龙或等效剂量的其他品种糖皮质激素),可以降低氧合指数低于300 mmHg患者的病死率,且并未明显增加患者感染、消化道出血等不良反应发生率[17]。此外,亦有Meta分析表明,糖皮质激素能够降低社区获得性肺炎重症患者的死亡率,并缩短患者机械通气时间[18]。
3.2 用于治疗COVID-19重症的糖皮质激素 糖皮质激素可分为短、中、长效三类,不同品种糖皮质激素的抗炎强度及作用时间均不相同(见表1)。《新型冠状病毒肺炎诊疗方案(试行第六版)》[5]中关于糖皮质激素使用的推荐意见为等效甲泼尼龙1~2 mg/(kg·d)。甲泼尼龙成为治疗COVID-19首选的糖皮质激素,是因为其对糖皮质激素受体亲和力高,抗炎作用强,能够较好地抑制机体细胞因子风暴,且对下丘脑-垂体-肾上腺素轴的抑制作用较长效糖皮质激素地塞米松弱,停药不良反应相对较轻[19-20]。临床若无甲泼尼龙可选时,可酌情选用等效剂量的其他品种糖皮质激素。
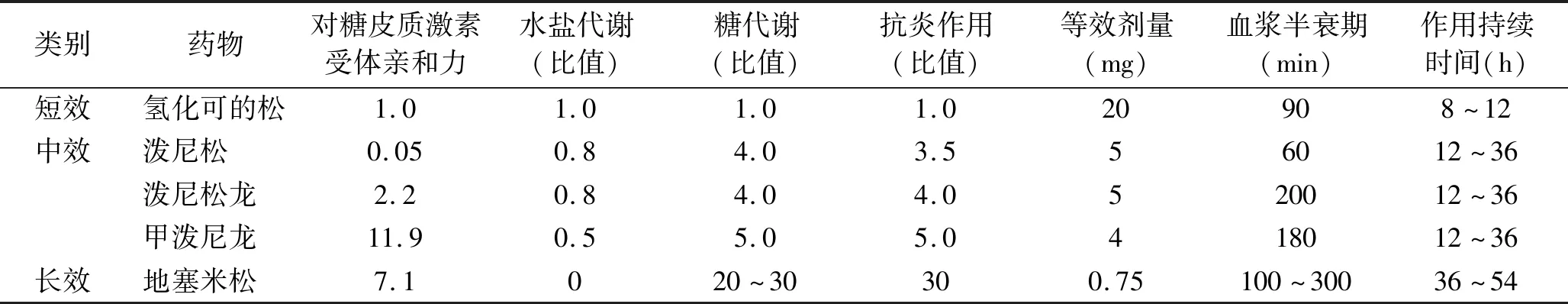
表1 常用糖皮质激素类药物比较
注:水盐代谢、糖代谢、抗炎作用的比值均以氢化可的松为1进行计算。
3.3 应用糖皮质激素治疗COVID-19重症患者的争议 一项纳入309例MERS重症患者的回顾性研究显示,糖皮质激素的使用与患者90 d病死率无关,但与呼吸道分泌物中病毒RNA的延迟清除相关,因此认为接受糖皮质激素治疗的患者可能更需要呼吸机支持、血管活性药物以及肾脏替代治疗[21]。另一项纳入6 548例流感肺炎患者的Meta分析提示,糖皮质激素治疗增加了患者病死率,延长重症患者的住院时间,并且增加了继发细菌或真菌感染的发生率[22]。基于此,有研究者反对在COVID-19重症患者中使用糖皮质激素,认为糖皮质激素虽然可以抑制肺部炎症,但同样可以抑制免疫应答和病原体的清除。此外,世界卫生组织发布的COVID-19临床指南[23]以及Russel等[24]的研究均表明,除非有其他需要使用糖皮质激素的指征,否则不建议COVID-19重症患者常规使用糖皮质激素。
3.4 糖皮质激素用于治疗COVID-19的原则 目前,糖皮质激素在COVID-19重症患者中的应用尚存争议,因此临床应谨慎使用,需严格把握适应证和用量。应遵循“轻病人治病,重病人救命”的原则,临床医生在制定COVID-19治疗方案时需要去权衡是否使用糖皮质激素,对于氧合指标进行性恶化、影像学表现进展迅速的COVID-19重症患者,酌情使用糖皮质激素来延缓疾病的进程,为进一步的救治争取宝贵时间或许也是一种尝试。我院援鄂医疗队在救治COVID-19重症肺炎患者时,使用小剂量短疗程的糖皮质激素[甲泼尼龙1 mg/(kg·次),1次/d,连续给药5 d],取得了不错的疗效;“快上快下,适量使用,见好就收”的原则既抑制了机体过度的炎症反应,又尽可能地降低了糖皮质激素副作用发生风险,值得临床医生参考借鉴。使用糖皮质激素治疗COVID-19重症患者时,或可参考以下思维导图(见图1)。
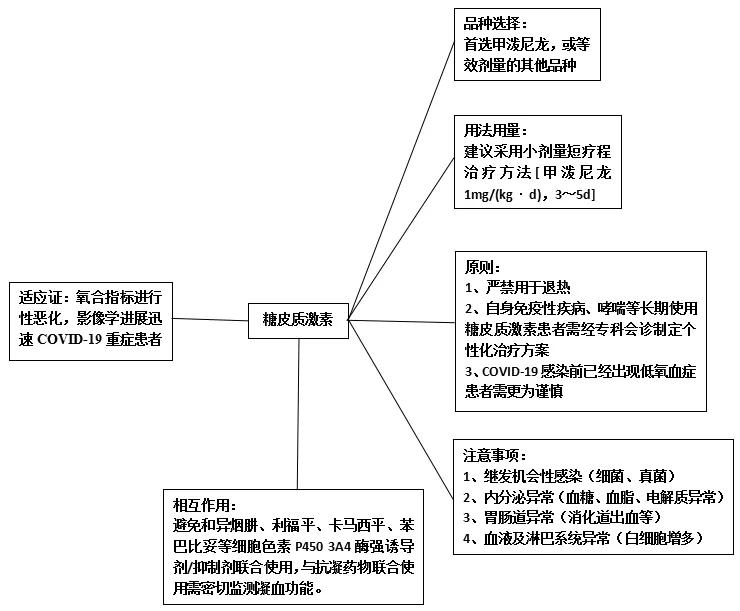
图1 糖皮质激素应用于COVID-19重症的临床思维导图
3.5 药学监护 对于使用糖皮质激素治疗的COVID-19重症患者,注意积极评估患者胸部影像学表现及氧合情况,如无明显改善应及时停用。使用糖皮质激素期间,注意密切评估患者继发性感染情况,以避免掩盖真实病情;同时积极观察患者是否出现消化道出血、淋巴系统异常、电解质紊乱、水钠潴留等不良反应,并及时对症处理;若患者病情允许可将静脉用糖皮质激素逐步过渡为口服。
4 小 结
糖皮质激素在COVID-19重症患者中的应用目前尚缺乏高质量证据,对于氧合指标进行性恶化、影像学表现进展迅速的COVID-19重症患者可酌情使用小剂量短疗程糖皮质激素治疗,并积极评估患者影像学表现及氧合情况,密切监测相关不良反应。随着相关研究的深入和临床数据的积累,我们会持续关注并评估糖皮质激素用于治疗COVID-19的效果,为COVID-19的药物治疗提供参考。
