基于网络药理学和分子对接分析探讨消炎退热合剂干预新型冠状病毒肺炎的可行性△
2020-06-10周瑞刘妍如王征张军武李宏许洪波何姬张玉茹唐志书
周瑞,刘妍如,王征,张军武,李宏, 许洪波,何姬,张玉茹,唐志书*
1.陕西中医药大学 陕西中药资源产业化省部共建协同创新中心/ 秦药特色资源研究与开发国家重点实验室(培育)/陕西省创新药物研究中心,陕西 咸阳 712083; 2.陕西中医药大学 制药厂/陕西省博士后创新基地,陕西 咸阳 712046
2019年12月开始,在我国湖北武汉及周边城市发生了新型冠状病毒(2019-nCoV或SARS-CoV-2)引起的急性肺炎。此次引起流行的病毒与2003年的SARS病毒相似,都属于冠状病毒科的β属冠状病毒,传播快,人群普遍易感[1-2]。新型冠状病毒肺炎(COVID-19)轻度患者出现发热、乏力、干咳等症状,严重者可出现呼吸困难、呼吸窘迫综合征或脓毒症休克等症[3]。采用中西医结合对症治疗已取得满意的疗效,特别是在减少轻症转化为重症,减少重症,病死率方面体现了明显的优势[5-6]。
中医认为病毒导致的传染病属于“瘟疫”的范畴,中医药在我国治疗各种疾病已有千年历史,《温病条辨》《伤寒论》《黄帝内经》等中医典籍中也记载了大量对这类疾病的诊疗方法和处方。中医认为新型冠状病毒的病因为感受疫戾之气[7],病位在肺,基本病机特点为“湿、热、毒、瘀”。在防控紧迫的局势下,从临床现有疗效确切的抗炎抗病毒中药方剂中,寻找可以有效防治COVID-19的药物是更快速、更安全、更有效的策略。消炎退热合剂是陕西中医药大学制药厂生产的1种中药复方制剂,临床针对病毒性感冒发热、咳嗽等症具有显著疗效。该复方由大青叶、蒲公英、紫花地丁、甘草4味中药组成。方中君药为大青叶和蒲公英,臣药为紫花地丁,佐以甘草解毒调和诸药,共同发挥清热解毒之功效[8-11],其中大青叶、甘草和蒲公英在全国防治COVID-19的中药方剂中出现频次较高[12]。消炎退热合剂全方重在围绕热毒而设,非常切合目前COVID-19的中医病机。因此,本研究推测该复方可能通过抑制病毒复制、调节免疫,有效地阻断病毒感染引起的炎症风暴等,实现防治COVID-19。
近年来,网络药理和分子对接方法对于研究阐明中药多成分、多靶点整体治疗疾病的机制提供了很好的技术[13-15]。本研究拟通过网络药理学筛选出消炎退热合剂的作用靶点,并进行聚类分析,预测消炎退热合剂中具有抗病毒作用的核心活性化合物,进而运用分析软件对药材-化合物-靶点进行分子对接以及信号通路分析,并预测其治疗COVID-19的作用机制,为消炎退热合剂用于治疗COVID-19提供理论参考。
1 方法
1.1 化学成分收集及筛选
借助中药系统药理学分析平台(TCMSP)(http://tcmspw.com/)和Pubchem有机小分子生物活性数据库(https://pubchem.ncbi.nlm.nih.gov/)检索,以“大青叶Isatidis Folium”“蒲公英Taraxaci Herba”“紫花地丁Violae Herba”“甘草Glycyrrhizae Radix et Rhizoma”为关键词检索消炎退热合剂的化学成分。进一步以口服生物利用度(Oral Bioavailability,OB)≥30%或类药性(Drug Likeness,DL)≥ 0.18作为条件,对化合物进行进一步筛选。
1.2 “化合物-疾病靶点”筛选
从TCMSP和Pubchem数据库中搜索化合物对应的靶点,以UniProt数据库(http://www.uniprot.org/uniprot/)对收集的靶点进行规范化和校正,得到成分相关的基因靶点。在MalaCards数据库(https://www.malacards. org/)、TTD数据库(Therapeutic Targets Database,http://bidd.nus.edu.sg/BIDD-Databases/TTD/TTD.asp)和OMIM数据库(http://www.ncbi.nlm.nih.gov/omim)中输入关键词“Severe Acute Respiratory Syndrome”“Respiratory Failure”,搜索已报道的与冠状病毒感染肺炎和重症呼吸道疾病相关的基因。剔除重复和假阳性基因后,整理得到与冠状病毒感染肺炎相关的靶点基因。
1.3 “成分-疾病-靶点”网络构建
将上述得到的化合物相关靶点和疾病相关靶点以Venn工具(2.1.0,https://bioinfogp.cnb.csic.es/tools/venny/)取靶点交集。将交集内靶点导入STRING 11.0数据库(https://string-db.org/),以人类(Homosapiens)为种属,查询蛋白相互作用信息,从而构建PPI(Protein to Protein Interaction)网络。整合PPI网络的蛋白互作信息,“成分-疾病-靶点”及“中药-成分”信息,将数据导入Cytoscape3.7.2(http://www.cytoscape.org/)软件,构建“中药-成分-疾病-靶点”预测网络。以网络的节点和边线来描述化合物与中药、疾病和靶点之间的关系,以Cytoscape的Network analysis插件分析并提取网络节点和边的特征。
1.4 生物过程注释及靶点的通路分析
为了分析消炎退热合剂的作用机制,采用R软件包(3.6.2)的Cluster profiler包对交集靶点进行GO (Gene Ontology)生物信息学富集分析,用3个本体(Ontology)来描述基因靶点的分子功能(Molecular Function,MF)、所处的细胞位置(Cellular Component,CC)和参与的生物过程(Biological Process,BP)。然后以KEGG(Kyoto Encyclopedia of Genes and Genomes,https://www.kegg.jp/)数据库对靶点基因参与的主要生化代谢途径进行富集和注释,显著性差异设定卡值为P<0.05,以R软件包(3.6.2)的ggplot2包进行绘图。最终整合冠状病毒感染肺炎的病理学、分子生物学机制研究,对消炎退热合剂的多成分、多靶点、多途径协同抗病毒感染肺炎机制进行阐释。
1.5 成分-靶点分子对接
采用ChemOffice软件构建化合物的3D结构,保存为*mol2格式并使其能量最小化。从PDB数据(https://www.rcsb.org/)下载ACE2蛋白质(PDBID:2ajf)的3D结构*PDB格式,采用LibDock分子对接方法,其打分函数LibDockScore>100即表明受体与配体能较好地结合,其值越大则表明对接产生的复合物构象越稳定,配体与受体的亲和作用越好。
2 结果
2.1 活性化合物的筛选
结合前期发表的消炎退热合剂成分鉴定结果与TCMSP数据库收载的组方中药化学成分数据,基于样本量、后续数据分析的复杂性以及研究价值的考虑,以OB≥30%或DL≥0.18作为进一步筛选条件,得到符合筛选标准的活性化合物117个。
2.2 化合物靶点与疾病靶点相互作用网络
通过TCMSP平台和Pubchem数据库中找到消炎退热合剂化学成分对应的靶点共498个,以Uniprot数据库搜索校正后生成“成分-靶点”集合。从MalaCards数据库、TTD数据库和OMIM 数据库中得到关于冠状病毒“Severe Acute Respiratory Syndrome”和“Respiratory Failure”相关的靶点共计144个,生成“疾病-靶点”集合。将上述得到的“成分-靶点”和“疾病-靶点”集合以Venn工具 2.1.0取靶点交集,得到交集靶点27个(见图1A)。将交集内靶点导入STRING 11.0,构建PPI(Protein to Protein Interaction)网络(见图1B)。
2.3 “成分-疾病-靶点”网络
将筛选得到的27个靶点与4个中药进行映射,筛选出18个核心化合物。来自大青叶的4个,蒲公英的1个,紫花地丁的7个,甘草的6个。将中药、归经及18个核心化学成分进行映射并生成关联表,与PPI网络生成的互作表导入Cytoscape3.7.2软件构建消炎退热合剂的“中药-化合物-靶点”关联网络(见图2)。

注:A. 消炎退热合剂中化学成分靶点与疾病网络交集;B. PPI网络。图1 消炎退热合剂“化合物-疾病”靶点相互作用分析
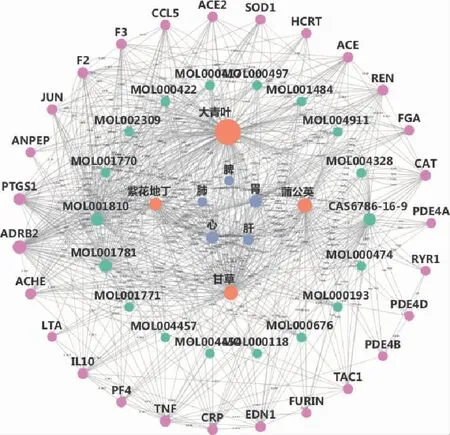
注:蓝色节点代表归经;橘黄色节点代表中药;绿色节点代表活性成分;紫粉色节点代表疾病靶点。图2 消炎退热合剂中“中药-归经-成分-靶点”网络图
用Cytoscape3.2.1软件构建中药-归经-化合物-靶点网络,图中总共涉及125个节点,706个边。不同颜色的圆点代表了消炎退热合剂中中药-归经-成分-靶点网络。图中节点大小代表度数大小,度数越大,说明该节点在网络中越重要,接近中心度越大,说明节点在网络中越接近中性。分析4种中药在网络图的连接度值可知,君药大青叶度值最高为162,其次是蒲公英和甘草度值为72,紫花地丁度值为48。根据组成药物的归经信息分析,可以看到,网络中连接度最大的是胃和心2个节点,连接度分别是45和41,其次是肝的连接度值为20,脾和肺的连接度值均是6。此结果表明消炎退热合剂主要归于胃和心,其次是肝、脾、肺。分析化学成分的连接度值,发现大青叶中的核心化合物靛蓝(indigo),6-(3-氧代吲哚啉-2-亚基)吲哚[2,1-b]喹唑-12-酮{6-(3-oxoindolin-2-ylidene)indolo[2,1-b]quinazolin-12-one},以及蒲公英的化合物蒲公英萜酮(taraxerone),连接度值均是48,说明这3个化学成分很可能是消炎退热合剂治疗疾病的主要化学成分。其余化合物如邻苯二甲酸二丁酯(DBP)、山柰酚、毛蕊异黄酮等连接度值是8,靛蓝、十八碳二烯酸(ODD)、β-谷甾醇等连接度值是4。通过对靶点连接点度值分析得出,排名前5位的靶点分别是肾上腺素能受体β2抗体(ADRB2)(度值=57)、前列腺素过氧化物合酶1(PTGS1)(度值=39)、肿瘤坏死因子(TNF)(度值=25)、凝血酶原(F2)(度值=23)、肾素(REN)(度值=22)。我们同时发现,与COVID-19密切相关的靶点ACE2的连接度值为14。这结果说明消炎退热合剂中化学成分可能不仅通过抗炎、调节免疫实现治疗疾病,还可能直接作用于病毒受体,实现防治COVID-19的作用。此结果初步阐明“中药-归经-成分-靶点”的互作关系,揭示了消炎退热合剂治疗疾病的多靶点、多途径属性,其中大青叶节点度数较大,说明其君药的用药合理性。核心关键化合物为靛蓝、γ-谷甾醇、β-谷甾醇、十八碳二烯酸等,主要归经为胃、心经,表明消炎退热合剂可能通过多成分、多途径、多靶点协同发挥作用。
2.4 靶点通路分析
为了阐明消炎退热合剂抗病毒感染肺炎作用的分子机制,将“成分-疾病”对应的27个靶点通过Cluster profiler进行GO富集分析和KEGG通路注释,共富集到GO条目910,其中生物学过程(BP)867条(见图3A),分子功能(CC)6条(见图3B),细胞组成(MF)条目37条(见图3C),分别占95%、0.6%、4%。富集到KEGG信号通路10条(见图4),这些靶点主要分布于质膜外侧(GO:0009897,external side of plasma membrane)、钙离子通道电压门控(GO:0005891,voltage-gated calcium channel complex)和钙离子通道复合体(GO:0034704,calcium channel complex)。其分子功能主要与受体配体活性(GO:0048018,receptor ligand activity)、G蛋白耦联受体结合(GO:0001664,G protein-coupled receptor binding)、细胞因子活性(GO:0005125,cytokine activity)有关。其生物过程(BP)主要涉及脂多糖反应(GO:0032496,response to lipopolysaccharide)、细菌来源分子效应(GO:0002237,response to molecule of bacterial origin)和血压调控(GO:0008217,regulation of blood pressure)。这些靶点主要调控的代谢通路为cAMP信号通路(hsa04024,cAMP signaling pathway)、病毒蛋白与细胞因子受体间相互作用(hsa04061,Viral protein interaction with cytokine and cytokine receptor)、肿瘤坏死因子信号通路(hsa04668,TNF signaling pathway)、细胞因子相互作用受体通路(hsa04060,Cytokine-cytokine receptor interaction)、肾素-血管紧张素系统(hsa04614,Renin-angiotensin system)等。以上结果表明消炎退热合剂中核心化合物可能通过干预ADRB2、PTGS1、TNF、F2、REN、ACE、ACE2等靶点来产生治疗疾病的作用,并作用于cAMP通路、病毒蛋白与细胞因子相互作用、TNF信号通路等减轻病毒诱发的炎症风暴损伤,并且有可能调控肾素-血管紧张素系统直接作用于病毒与宿主的结合。
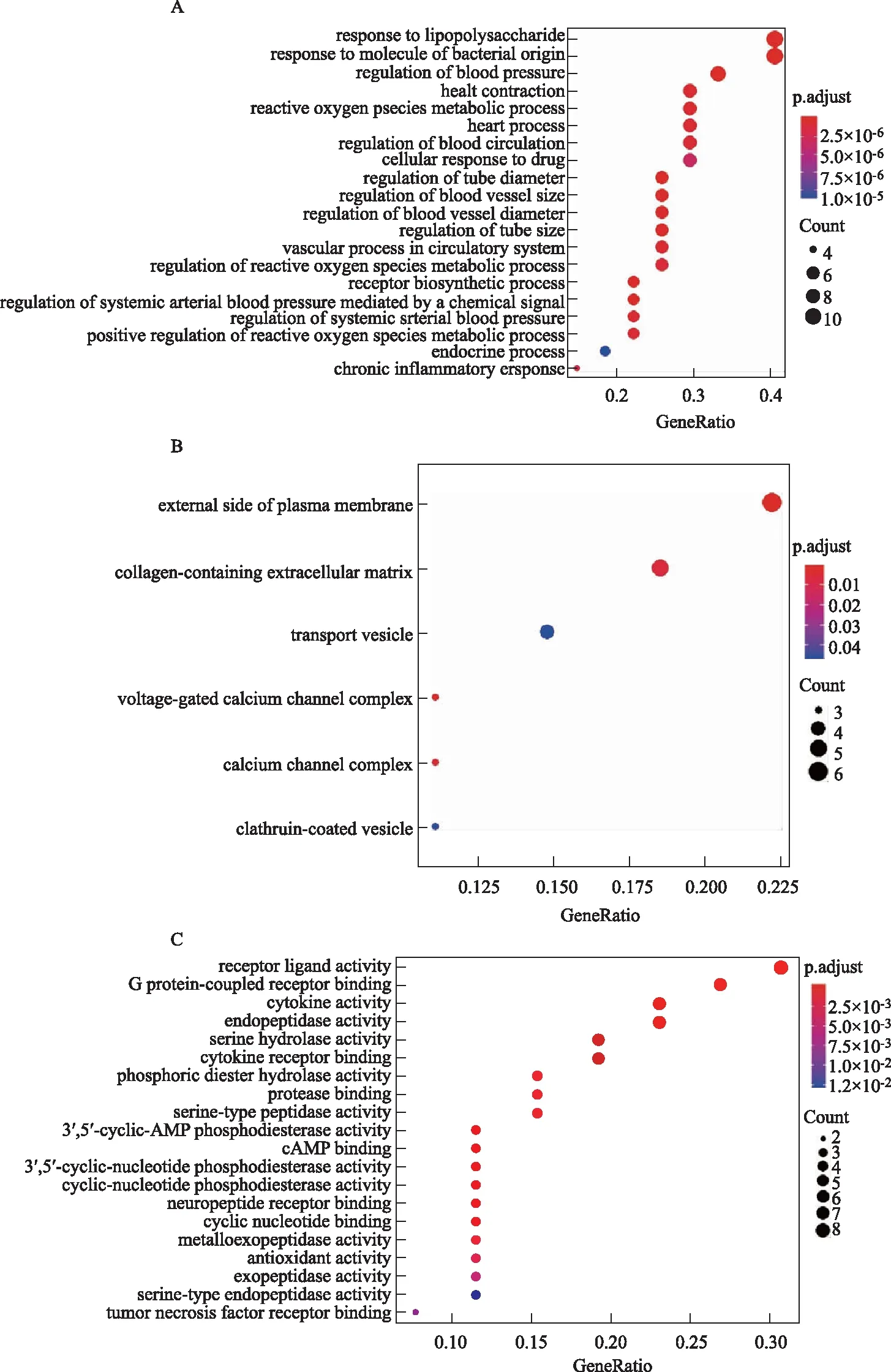
注:A.GO(BP)结果分析图B:GO(CC)结果分析图;C.GO(MF)结果分析图。图3 消炎退热合剂作用靶点的GO富集分析图

图4 消炎退热合剂KEGG富集分析图
2.5 消炎退热合剂中活性化合物与ACE2的分子对接结果分析
在网络药理学筛选的基础上,我们进一步将筛选出消炎退热合剂的18个核心化学成分与病毒的结合受体ACE2进行对接,通过DS筛选出消炎退热合剂中潜在的核心治疗疾病的化合物。采用LibDock分子对接方法,其打分函数LibDock Score是基于配体与受体对接时的亲和力、相对能量和对接模式等进行综合打分,打分值>100说明配体与受体具有很好的结合。消炎退热合剂中18个核心化学成分与ACE2的对接打分结果见表1。
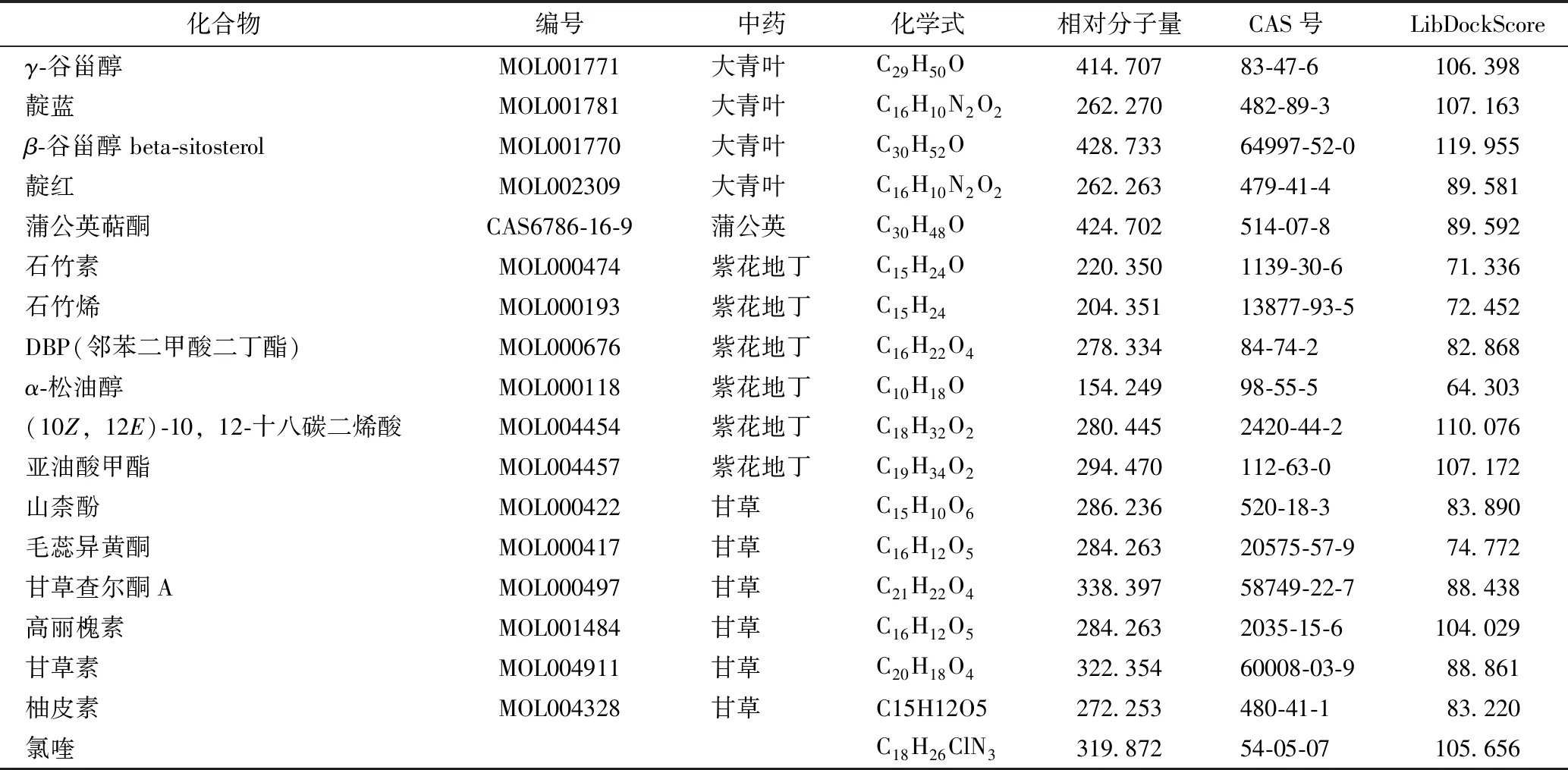
表1 消炎退热合剂中核心化合物与ACE2的分子对接结果
从结果中可以看出,来自大青叶的活性化合物靛蓝(107.163)、γ-谷甾醇(106.398)、β-谷甾醇(119.955),来自紫花地丁的活性化合物ODD(110.076)、亚油酸甲酯(107.172),及来自甘草的高丽槐素(104.029)的对接分值接近或高于与临床推荐治疗COIVD-19的药物氯喹(105.656)。因此,通过分子对接技术,本文最终筛选出消炎退热合剂中6个核心化合物可能是治疗COCID-19的核心活性成分(见表1)。β-谷甾醇、ODD、靛蓝及高丽槐素与ACE2蛋白相互作用的3D及2D示意图见图5。

注:A.β-谷甾醇与ACE2蛋白结合3D图;B.β-谷甾醇与ACE2蛋白相互作用2D图;C.ODD与ACE2蛋白结合3D图;D.ODD与ACE2蛋白相互作用2D图;E.靛蓝与ACE2蛋白结合3D图;F.靛蓝与ACE2蛋白相互作用2D图;G.高丽槐素与ACE2蛋白结合3D图;H.高丽槐素与ACE2蛋白相互作用2D图。图5 消炎退热合剂中核心成分与ACE2蛋白相互作用图
3 讨论
中医在防治瘟疫方面疗效独特,以“辨证施治、扶正祛邪”为治疗原则。中医药在出血热、甲流等流行性传染病防治中,均发挥了重要的作用,尤其是在2003年的SARS中,中医药治疗的安全性和有效性得到了广泛认可[16-17]。国际病毒分类委员会(ICTV)已将新型冠状病毒正式命名为严重急性呼吸综合征冠状病毒2(SARS-CoV-2),表明SARS-CoV-2是SARS冠状病毒(SARS-CoV)的近亲。目前,中医药对于COVID-19的治疗起到了重要作用。2020年2月14日,湖北省政府召开发布会,邀请中医药专家介绍中医药参与COVID-19疫情防控的有关情况。专家指出临床采用中西医联合救治COVID-19能明显提高救治的质量,减少死亡,减少重症变成危重症的发生率。
本研究提出的消炎退热合剂是临床用于抗流感病毒的中药制剂。本研究用网络药理学方法系统地分析预测消炎退热合剂对于COVID-19的潜在作用机制。首先通过数据库查询获取消炎退热合剂中各个中药的活性成分及其作用靶点,然后构建中药活性成分-靶点进行分析,找到消炎退热合剂的117个活性成分及其对应的498个潜在作用靶点,同时与找到冠状病毒“Severe Acute Respiratory Syndrome”和“Respiratory Failure”相关的144个靶点,与消炎退热合剂活性成分-靶点网络进行交集分析,初步筛选出消炎合剂核心活性成分包括γ-谷甾醇、β-谷甾醇、靛蓝、ODD等18个,以及对应的疾病靶点27个。网络药理学结果分析消炎退热合剂中药物主要归心、胃经,活性成分作用的主要疾病靶点可为几个大类,一是与炎症免疫相关的靶点有PTGS1、病毒蛋白与细胞因子受体相互作用、TNF;二是与病毒宿主结合复制相关的靶点有ACE、ACE2;三是与肺炎损伤机体的并发症相关靶点如F2,F2是静脉血栓形成的重要靶点,肺炎重症患者长期卧床易患静脉血栓,以上均是消炎退热合剂核心成分γ-谷甾醇、β-谷甾醇以及靛蓝的作用靶点。2019-nCoV感染导致强烈的免疫反应和炎症风暴,此过程中大量细胞因子被激活[18]。已有研究发现炎症因子风暴在新冠肺炎的病理进展中起着非常关键的作用。因此,抑制细胞因子的产生也是治疗COVID-19的关键目标[19-20]。KEGG分析得到与ADRB2、PTGS1、TNF、F2、REN、ACE、ACE2靶点相关且排名前6的通路,分别为炎症细胞因子相关通路如病毒蛋白与细胞因子相互作用通路、TNF信号通路、细胞因子受体相互作用通路等,推测消炎退热合剂可能通过调节这些信号通路起到抑制活化的细胞因子、缓和过激的免疫反应、消除炎症的作用。文献报道表明[21],ADRB2、REN、ACE、ACE2靶点和病毒蛋白细胞因子相互作用通路、肾素-血管紧张素系统等在影响RNA病毒的结合、复制以及在治疗肺炎的过程中起关键作用,说明利用网络药理学预测消炎退热合剂治疗COVID-19的潜在化学成分具有一定可靠性。cAMP通路是环核苷酸系统的一种,具有参与机体的发热机制和炎症的作用[22],消炎退热合剂也可能通过调控cAMP信号实现散热、退热的作用。研究人员发现感染SARS-CoV的细胞中分离出肾素(REN)和血管紧张素II(Ang II),它们可以和SARS-CoV的刺突蛋白高效结合,且细胞ACE2的表达量与SARS-CoV的S 蛋白的易感性正相关[23]。肾素-血管紧张素II是2019-nCoV结合ACE2受体激活的经典途径[24-25]。本研究发现消炎退热合剂的活性成分不仅对ACE2的靶点有作用,且可以调节肾素-血管紧张素系统信号通路,说明该复方可能含有直接抑制病毒与宿主结合的活性成分,网络药理学的结果预测消炎退热合剂中潜在的治疗病毒感染肺炎的多成分、多靶点的分子机制。
2013年Nature报道[26],冠状病毒的刺突蛋白三聚体先与ACE2的细胞外催化结构域的“疏水口袋”结合,继而细胞发挥内吞作用,病毒包膜与细胞膜融合,最终进入宿主细胞。研究发现[27],2019-nCoV中病毒感染的途径也是通过其表达的S蛋白与ACE2的结合,导致病毒侵入机体而致病。本研究通过网络药理学筛选出消炎退热合剂中靛蓝、β-谷甾醇、γ-谷甾醇、ODD等18个核心化学成分,进一步通过分子对接技术发现与ACE2具有较强结合力的6个化学成分,为靛蓝、β-谷甾醇、γ-谷甾醇、ODD、亚油酸甲酯及高丽槐素,与目前临床上推荐用药氯喹的结合力相当,说明消炎退热合剂可能对COVID-19具有潜在的治疗作用。靛蓝、β-谷甾醇、γ-谷甾醇、ODD、亚油酸甲酯及高丽槐素是否可以通过作用于ACE2受体调节多条信号通路抗病毒有待进一步工作的验证。
综上所述,通过网络药理学和分子对接技术,本研究应用网络药理学方法对消炎退热合剂的化学成分、作用靶标进行了系统性的分析,从分子水平阐述了该复方可能通过多成分、多靶点对机体的整体调控,筛选出6个潜在的抗病毒活性化学成分,为该复方干预COVID-19提供了理论支持。
猜你喜欢
——基于正交试验优化的皂化反应法△