AMD3100联合G-CSF对2型糖尿病小鼠骨髓EPCs动员的培养
2020-06-08潘满昌林晓莹汪虹冷敏
潘满昌 林晓莹 汪虹 冷敏

摘要:目的 研究AMD3100联合G-CSF对糖尿病骨髓内皮祖细胞的培养方法和生物学功能。方法 选用6周龄健康雄鼠,将10只db/db小鼠设为db/db组,10只db/+小鼠设为db/+组。采用AMD3100与CSF联合动员骨髓内皮祖细胞的方法,每只小鼠第1天注射AMD3100,后续连续注射5 d G-CSF,在第10天心脏采血制备EPCs。采用流式细胞仪检测CD34+/CD133+/CD309+细胞的比例进行鉴定,鉴定成功的EPCs采用CCK-8法、Matrigel檢测细胞增殖及成管功能。采用PCR检测细胞表面标志物:血管内皮生长因子(VEGF)、基质细胞衍生因子(SDF-1)、趋化因子受体4(CXCR4)基因表达情况。结果 ①从处理后的第3天开始,db/+组的OD450值较db/db组增高(P=0.05);②0和48 h db/+组EPCs迁移面积分别为(204088.100±219.200)μm、 (144724.900±199.400)μm,大于db/db组的(200985.700±232.600)μm、(155075.300±213.100)μm(P<0.05);③db/+组管腔形成数量为(29.330±1.764)个,多于db/db组的(24.000±2.082)个(P<0.05)。结论 采用AMD3100联合G-CSF动员2型糖尿病骨髓内皮祖细胞的方法成功从外周血中分离出EPCs,经体外培养发现2型糖尿病状态下EPCs的增殖,迁移和成管等功能均受损。
关键词:糖尿病;内皮祖细胞;联合动员;移植
中图分类号:R587.2;R-33 文献标识码:A DOI:10.3969/j.issn.1006-1959.2020.09.018
文章编号:1006-1959(2020)09-0057-06
Cultivation of Bone Marrow EPCs in Type 2 Diabetic Mice by AMD3100 and G-CSF
PAN Man-chang,LIN Xiao-ying,WANG Hong,LENG Min
(Department of Burns,the Second Affiliated Hospital of Kunming Medical University,Kunming 650000, Yunnan,China)
Abstract:Objective To study the culture method and biological function of AMD3100 combined with G-CSF on diabetic bone marrow endothelial progenitor cells.Methods Six-week-old healthy male rats were selected, 10 db/db mice were set as db/db group, and 10 db/+ mice were set as db/+ group. AMD3100 and CSF were used to mobilize bone marrow endothelial progenitor cells. Each mouse was injected with AMD3100 on the first day, followed by continuous injection of G-CSF for 5 d, and blood was collected on the 10th day to prepare EPCs. Flow cytometry was used to detect the ratio of CD34+/CD133+/CD309+ cells for identification. Successful EPCs were identified by CCK-8 method and Matrigel to detect cell proliferation and tube formation function. PCR was used to detect cell surface markers: vascular endothelial growth factor (VEGF), stromal cell-derived factor (SDF-1), and chemokine receptor 4 (CXCR4) gene expression.Results ①From the third day after treatment, the OD450 value of the db/+ group was higher than that of the db/db group (P=0.05); ②The migration area of EPCs in the 0 and 48 h db/+ groups was (204088.100±219.200) μm, (144724.900±199.400) μm,(200985.700±232.600) μm and (155075.300±213.100) μm (P<0.05) greater than the db/db group; ③The number of lumens formed in the db/+group was (29.330±1.764), which was more than (24.000±2.082) in the db/db group (P<0.05).Conclusion In this experiment, AMD3100 and G-CSF were used to mobilize type 2 diabetic bone marrow endothelial progenitor cells. EPCs were successfully isolated from peripheral blood, and the proliferation, migration and tube formation of EPCs in type 2 diabetes were impaired by in vitro culture.
Key words:Diabetes;Endothelial progenitor cells;Joint mobilization;Transplantation
内皮祖细胞(endothelial progenitor cells,EPCs)是一类旁分泌各种血管生成因子参与内皮细胞功能的前体细胞。自1997年首次用磁珠法从成人外周血(PB)中分离出来,越来越多证据表明EPCs在病理生理下参与血管新生[1-3]。近年大量研究发现糖尿病状态下EPCs被“拘留”于骨髓,致EPCs在外周血中数量减少、功能障碍及生物学活性降低[3,4]。因此,糖尿病EPCs的动员和体外分离培养成为研究的热点。近年虽国内外很多有关EPCs报道[5-7]。但有关糖尿病EPCs联合动员后外周血的分离培养研究报道尚少。既往研究发现糖尿病小鼠联合动员第10天EPCs达到峰值。本研究以期通过联合动员获得糖尿病状态下峰值的EPCs进行体外培养,獲得外周血EPCs分离培养方法,并通过细胞增殖、迁移和成管等情况,获得EPCs体外培养的可靠来源,为深入研究糖尿病EPCs的功能障碍及以后临床应用作参考。
1材料与方法
1.1实验动物 选取6 周龄SPF级db/db小鼠(25~30 g)和db/+小鼠(25~30 g)各10只雄性,db/db小鼠(糖尿病状态) 是由C57小鼠(非糖尿病状态)近亲交配株常染色体隐性纯合子遗传衍化建立的2型糖尿病模型;db/+小鼠是由C57小鼠近亲交配株常染色体杂合子遗传衍化,无糖尿病症状。购自常州卡文斯实验动物有限公司,许可证号:SCXK(苏)2016-0010。饲养于昆明泉港生物科技有限公司实验动物中心饲养。
1.2主要的试剂和器材 AMD3100(Selleck 公司),rhG-CSF(齐鲁制药有限公司),0.9%氯化钠注射液(上海百特医疗用品有限公司),肝素钠注射液(江苏万邦生化医药股份有限公司),PE/Cy7 anti-mouse CD34(abcam公司),APC anti-mouse CD133(abcam公司),PE anti-mouse CD309(Flk-1)(abcam公司),FAC SCantoⅡ流式仪(BD 公司)。
1.3实验动物的分组及给药方法 选取6周龄健康雄鼠,将10只db/db小鼠设为db/db组,10只db/+小鼠设为db/+组。①db/db组动员方案为AMD3100+G-CSF:取10只db/db雄鼠,每只小鼠第1天注射AMD3100,后续连续注射5 d G-CSF,在第10天心脏采血制备EPCs。②db/+组:方法同db/db组。
1.4 AMD3100、G-CSF的注射剂量及配制 AMD3100和G-CSF动员EPCs皮下注射剂量参照国内外文献:AMD3100 6 mg/(kg·d),G-CSF 100 mg/(kg·d)[8,9]。AMD3100 注射液配制方法如下:将AMD3100用PBS溶解,配制成浓度为50 mg/ml的溶液,并置于-20 ℃冰箱中贮存备用。而G-CSF可直接进行皮下注射,置于4 ℃冰箱中贮存备用。
1.5实验方法
1.5.1小鼠外周血中EPCs的分离培养及收集 采用1%的戊巴比妥将实验小鼠麻醉,用2.5 ml含有肝素的注射器在胸前心尖搏动最明显部位采血。然后采用密度梯度离心法提取单个核细胞,用PBS洗涤 2次,用含10%胎牛血清的内皮组细胞培养液重悬细胞,制成单细胞悬液分别接种到50 ml培养瓶中,37℃、5% CO2件下培养,每3 d换液1次,收集15 d细胞进行实验。
1.5.2流式细胞术分析鉴定 将细胞消化后用100 μl staining buffer重悬细胞,加入适量荧光标记表面抗体(PE/Cy7 anti-mouse CD34/APC anti-mouse CD133/PE anti-mouse CD309)染色,室温避光染色30 min,然后洗涤细胞并使用Guava easyCyteTM流式细胞仪(Millipore,Billerica,USA)分析。
1.5.3 EPCs荧光双染色鉴定 取14 d的细胞在含Dil-acLDL(10 μg/ml)和FITC-UEA-1(10 μg/ml)的培养液中避光孵育,然后在激光共聚焦荧光显微镜进行观察。
1.5.4 CCK-8细胞增殖实验 将细胞传代在96孔板中,并处于对数生长期的各细胞消化、计数,均匀的铺在96孔板(5000个/孔)。各孔加入10 μl CCK8试剂测定第1、3、5、7 天增殖情况,用酶标仪检测OD450(optical density),单位:nm,绘制曲线。
1.5.5划痕迁移实验 将EPCs制成单细胞悬液接种到6孔细胞培养板。EPCs接种48 h后用枪头在单细胞层上轻轻划一道伤痕。划痕结束后用 PBS洗去除划下细胞,拍照记录0 、48 h对迁移面积拍照6张照片,并放大(×40),重复实验3次。用软件 Image J 计算细胞迁移率(Rn):Rn(%)=24h迁移面积(0 h的划痕面积-24 h的划痕面积)与0 h面积的比值。
1.5.6管腔形成实验 在6孔板中加入100 μl基质胶,常温离心20 min、 1500 r/min。在培养箱放置1 h,水化1 ml EPCs后将其缓慢预铺基质胶孔内,8 h后在显微镜(×100)下拍照,每个孔随机拍照8张,重复实验3次,每孔平均值为管腔形成数目,统计分析。
1.6统计学处理 使用 SPSS 17.0 统计软件处理所有的数据,计量资料采用(x±s)表示,相同时间点不同组别之间采用单因素方差分析,两两比较采用LSD-t法,同一组别不同时间点之间的比较采用配对样本t检验。以P<0.05 为差异有统计学意义。
2结果
2.1实验动物的基本情况 两组小鼠在动员药物皮下注射结束后,精神状况良好,饮食、体重无明显变化,均无意外死亡情况。
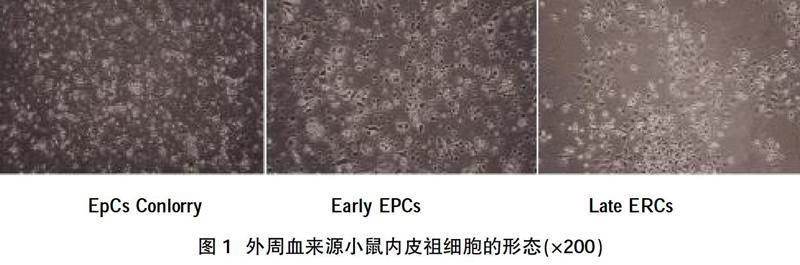
2.2细胞的形态学观察 分离的单个核细胞第2天细胞密集,较小的类圆形,呈悬浮状态;第6天细胞在倒置显微镜观察下活力比较旺盛,折光度好,细胞形态呈椭圆形或梭形,大小不等,可以见部分细胞已贴壁。传至第15天细胞逐渐变大,伸出伪足样突起,成纺锤体形细胞,形态此时较稳定,倒置显微镜下贴壁细胞透亮度增强,成单层细胞贴壁生长,见图1。
2.3培养后EPCs鉴定
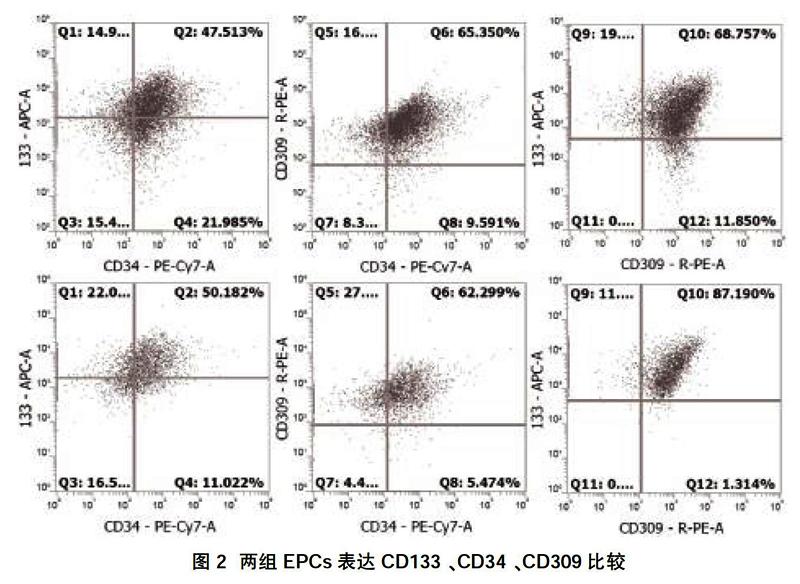
2.3.1流式细胞术分析 db/+小鼠外周血培养第15天 EPCs表达CD34、CD133及CD309,表达率分别为(72.23±3.84)%、(75.09±17.92)%及(80.98±0.53)%。db/db小鼠培养的第15 天EPCs表达CD34、CD133及CD309,表达率分别为(64.49±4.64)%、(85.19±18.39)%及(88.90±0.56)%,以上培养的细胞都是EPCs,见图2。
2.3.2 EPCs荧光双染色鉴定 荧光显微镜观察可见:PBMC提取培养15 d的EPC,细胞吞噬FITC-UEA-1示绿色荧光;细胞吞噬Dil-acLDL示红色荧光;Merge为前两张照片的融合图,即EPCs是双阳性染色摄取Dil-acLDL并结合FITC-UEA-1,呈现黄色荧光的细胞认为是分化状态的EPCs,见图3。
2.4 CCK-8细胞增殖实验 通过对db/db与db/+小鼠外周血培养15天的EPCs,在第1、3、5、7天的增殖情况显示:db/+小鼠EPCs的增殖曲线较陡。比较各时间点各组OD450时发现,从处理后的第3天开始,db/+组的OD450值较db/db组均显著增高(F=9.777,P=0.000),见表1。
2.5 划痕迁移实验 将EPCs接种到6孔细胞培养板上培养0 h与48 h迁移距离,结果显示:0 h 和48 h db/+组EPCs迁移面积分别为(204088.1±219.2)μm、(144724.9±199.4)μm,大于db/db组的(200985.7±232.6)μm、(155075.3±213.1)μm,差异有统计学意义(P<0.05),见图4。
2.6管腔形成实验 将培养的EPCs 种植在 Matrigel 上8 h形成毛细血管样网状结构。db/+组管腔形成数量(29.330±1.764)个,大于db/db组的(24.000±2.082)个,差异有统计学意义(P<0.05),见图5。
3讨论
目前全球有4.25亿糖尿病患者,每11位成人中就有1位罹患糖尿病,此外还有3.5亿多糖尿病高危人群。预计到2045年,将会有近7亿糖尿病患者。流行病学研究显示,超过1/3的慢性难愈合创面患者是因糖尿病造成的,已经代替创伤成为造成慢性难愈合创面的首要原因[10]。利用EPCs趋化到受损血管部位,修复受损内皮细胞并增殖分化新的内皮细胞进而修复血管功能,近年来成为创面修复领域成为一个新策略。
EPCs可从骨髓、脐血、胚胎肝和外周血中(15∶10∶2∶1)分离培养获得,而骨髓中所占比例最大[11]。成年后主要来源于骨髓,能够替代损伤的血管内皮细胞,维持血管内皮的完整性[12]。外周血中EPCs主要来源于骨髓[13]。而糖尿病EPCs数量稀少,功能障碍及活性降低,成功培养糖尿病EPCs成为学者进一步研究的难点。而本课题组前期研究发现通过AMD3100联合G-CSF可增加外周血中EPCs的数量,即EPCs在db/db小鼠外周血比例约占1.88%,在db/+小鼠外周血约占2.35%[9];而正常情况下EPCs仅占骨髓和外周血的0.01%[14]。该方法已经大幅度提高了外周血中EPCs的含量,且占比高于骨髓。但其相关功能和活性变化还未明确,因此,本研究对糖尿病小鼠动员后的EPCs进行分析。
本研究采用db/db小鼠是由C57小鼠近亲交配株常染色体隐性遗传衍化建立的2型糖尿病模型,以胰岛素抵抗和胰岛β细胞功能减退为特征,该模型是未经任何有意识的人为处置,在自然条件下发生糖尿病的小鼠模型,其优点为模型小鼠糖尿病的发生发展进程与人类2型糖尿病相似,近阶段具有较高的应用价值[15,16]。首先,动员后采集外周血提取单个核细胞,用内皮祖细胞培养基诱导培养,经流式细胞术检测EPCs特异性的表达产物CD34、CD133及CD309表达率达80%~90%,以及EPCs可摄取植物凝集素(UEA-1)和结合乙酰化低密度脂蛋白(acLDL),并表达内皮细胞和祖细胞的混合表型,证实绝大多数的细胞是EPCs。细胞的形态和功能检测也表明已经成功分离培养出EPCs。本实验采用密度离心法从动员后的小鼠外周血中分离单个核细胞,经离心制成重悬的细胞,移入含有血管内皮生长因子等多种生长因子的特殊培养基,诱导细胞分化成EPCs。在第6天倒置显微镜下观察细胞成椭圆形或梭形,大小不等,细胞密集,可见有部分细胞贴壁;此时细胞形态还未稳定。到达第15天可见细胞逐渐伸出伪足,形成纺锤体样,细胞基本完全贴壁,细胞融合成铺路石样生长。经流失细胞术和摄取UEA-1和结合acLDL双荧光染色鉴定已经成功分离。
EPCs具有增殖,迁移和成管的生物学特性,在一定的刺激下可募集,归巢到血管受损处,参与血管的重建和修复。目前认为 EPCs 促进血管新生的机制包括两个方面:一方面是通过自身的分化增殖而形成新生血管,无需依赖原来的血管系统;另一方面,EPCs 本身可以分泌血管内皮生长因子(vascular endothelial growth factor,VEGF)等细胞因子,通过旁分泌效应增强局部血管内皮细胞,即增强血管生成效应[17]。而大量研究发现糖尿病状态下的EPCs功能和活性受到抑制[3,4]。Maiorino MI等[18]发现循环CD34+细胞水平的降低提示日本2型糖尿病患者冠心病的发生有关,此外,与非糖尿病患者相比,2型糖尿病损害了急性心肌梗死后CD133+细胞数量的增加和趋化反应,这可能解释了缺血后血管延迟愈合和心肌恢復[19]。有研究将健康人和糖尿病患者的EPCs移植到裸鼠损伤的颈动脉内,发现与健康人EPCs比,糖尿病患者EPCs在体内再内皮化和抑制内膜增厚能力更低。
本实验检测了2型糖尿病EPCs的体外功能,发现功能较正常小鼠低,这与之前的研究一致。糖尿病状态下EPCs的数量和功能是修复创面的关键因素。目前虽有大量有关改善糖尿病环境下EPCs功能文献报道。如抑制炎症反应,氧化应激,促进动员,抑制凋亡等。但阐明糖尿病EPCs功能障碍的机制对于将其应用于创面修复是至关重要。而通过体内动员,外周血体外扩大增殖培养自体移植可以避免免疫反应及骨髓穿刺的痛苦。这有望成为治疗和预防糖尿病等难治愈创面的新希望。
参考文献:
[1]Asahara T,Murohara T,Sullivan A,et al.Isolation of putative progenitor endothelial cells for angiogenesis[J].Science,1997,275(5302):964-967.
[2]Altabas V,Altabas K,Kirigin L.Endothelial progenitor cells(EPCs)in ageing and age-related diseases:How currently available treatment modalities affect EPC biology,atherosclerosis,and cardiovascular outcomes[J].Mech Ageing Dev,2016(159):49-62.
[3]Hu L,Dai SC,Luan X,et al.Dysfunction and Therapeutic Potential of Endothelial Progenitor Cells in Diabetes Mellitus[J].J Clin Med Res,2018,10(10):752-757.
[4]章容,李素梅.内皮祖细胞在糖尿病血管病变中的作用及干预治疗[J].国际病理科学与临床杂志,2009,29(4):353-356.
[5]Lu Q,El-hashash AHK.Cell-based therapy for idiopathic pulmonary fibrosis[J].Stem cell investigation,2019(6):22.
[6]Pysna A,Bem R,Nemcova A,et al.Endothelial Progenitor Cells Biology in Diabetes Mellitus and Peripheral Arterial Disease and their Therapeutic Potential[J].Stem Cell Rev Rep, 2019,15(2):157-165.
[7]Ross MD.Endothelial Regenerative Capacity and Aging:Influence of Diet,Exercise and Obesity[J].Curr Cardiol Rev,2018,14(4):233-244.
[8]Nishimyra Y,Ii M,Qin G,et al.CXCR4 antagonist AMD3100 accelerates impaired wound healing in diabetic mice[J].J Invest Dermatol,2012,132(3 Pt 1):711-720.
[9]林晓莹,汪虹.AMD3100联合G-CSF对糖尿病小鼠骨髓内皮祖细胞的动员作用[J].重庆医科大学学报,2019,44(3):247-254.
[10]姜玉峰.中国体表慢性难愈合创面流行病学研究[D].解放军医学院,军医进修学院,解放军总医院,2011.
[11]Fadini GP,Avogaro A.Potential manipulation of endothelial progenitor cells in diabetes and its complications[J].Diabetes,Obesity&Metabolism,2010,12(7):570-583.
[12]Haider KH,Aziz S,Al-reshidi MA.Endothelial progenitor cells for cellular angiogenesis and repair:lessons learned from experimental animal models[J].Regen Med,2017,12(8):969-982.
[13]Asahara T,Kawamoto A,Masuda H.Concise review:Circulating endothelial progenitor cells for vascular medicine[J].Stem Cells,2011,29(11):1650-1655.
[14]Hristov M,Erl W,Weber PC.Endothelial progenitor cells:mobilization,differentiation,and homing[J].Arterioscler Thromb Vasc Biol,2003,23(7):1185-1189.
[15]胡紹波,李珊,邹毅,等.生长分化因子11对db/db糖尿病小鼠胰岛β细胞功能的保护作用及机制研究 [J].临床和实验医学杂志,2020,19(2):121-125.
[16]Alawi LF,Emberesh SE,Owuor BA,et al.Effect of hyperglycemia and rosiglitazone on renal and urinary neprilysin in db/db diabetic mice[J].Physiological Reports,2020,8(3):e14364.
[17]Kawakami Y,Matsumoto T,Mifune Y,et al.Therapeutic Potential of Endothelial Progenitor Cells in the Field of Orthopaedics[J].Curr Stem Cell Res Ther,2017,12(1):3-13.
[18]Maiorino MI,Bellastella G,Petrizzo M,et al.Circulating endothelial progenitor cells in type 1 diabetic patients with erectile dysfunction[J].Endocrine,2015,49(2):415-421.
[19]Wils J,Favre J,Bellien J.Modulating putative endothelial progenitor cells for the treatment of endothelial dysfunction and cardiovascular complications in diabetes[J].Pharmacol Ther,2017(170):98-115.
收稿日期:2020-03-10;修回日期:2020-03-22
编辑/肖婷婷
基金项目:国家自然科学基金资助项目(编号:81660321)。
作者简介:潘满昌(1990.1-),男,云南昆明人,硕士,住院医师,主要从事慢性创面愈合方向的研究
通讯作者:汪虹(1963.10-),男,云南昆明人,硕士,主任医师,主要从事创面修复方向的研究
