江苏省成人癌症疼痛诊疗规范(2020年版)
2020-06-05
疼痛是一种与组织实际或潜在损伤相关的感觉、情感、认知和社会维度的痛苦体验[1]。疼痛被认为是继心率、血压、脉搏和呼吸之外的第五大生命体征。及早、充分、持续且有效的控制疼痛是患者的基本权益,也是医务人员的职责义务。
疼痛可分为急性疼痛与慢性疼痛。慢性疼痛是一种疾病,长期的疼痛刺激可引起中枢神经系统的病理性重构,导致疼痛疾病的进展和愈加难以控制[2]。及早控制疼痛,可以避免或延缓此过程的发展。2019年3月在中国正式实施的第11版国际疾病分类(ICD-11)中,将“慢性癌性疼痛”列为独立病种。
疼痛也是癌症患者最常见的症状之一,严重影响癌症患者的生活质量。初诊癌症患者的疼痛发生率约为25%,晚期癌症患者的疼痛发生率约为60%~80%,其中1/3患者为重度疼痛。癌症疼痛(下述简称癌痛)如果得不到缓解,患者将感到极度不适,可能会引起或加重患者的焦虑、抑郁、乏力、失眠和食欲减退等症状,严重影响患者日常活动、自理能力、交往能力及整体生活质量[3]。
为进一步推动江苏省癌痛规范化治疗病房创建工作,规范江苏省医务人员对于癌痛的临床诊断、治疗和研究行为,完善重大疾病规范化诊疗体系,保障医疗质量和医疗安全,在本规范2017年版的基础上,参照国家卫生健康委员会发布的《癌症疼痛诊疗规范》(2018版)[4]和《NCCN成人癌痛临床实践指南》(Version 3.2019)[5],并结合江苏省癌痛规范化治疗病房创建工作中出现的问题,特制定本规范。
1 癌痛病因、机制及分类
1.1 癌痛病因
癌痛的原因多样,主要分为下述3类:
•肿瘤相关性疼痛:指肿瘤压迫或侵犯软组织、皮肤、黏膜、骨、神经、脊髓、血管、脑膜、内脏,空腔脏器的穿孔或梗阻和脑转移导致的颅内压升高等导致的疼痛。
•肿瘤治疗相关性疼痛:指手术治疗、化学治疗、放射治疗、分子靶向、免疫治疗和介入治疗等抗肿瘤治疗导致的疼痛。如外科手术后(开胸术后、乳房切除术、截肢术等)引起的神经损伤、疤痕增生、脏器黏连、残肢痛和幻肢痛等。化疗后引起的黏膜炎、周围神经变性(痛性多发性神经病)、栓塞性静脉炎、骨无菌性坏死等。放疗引起的周围神经损伤、软组织纤维化、口腔炎等。诊疗操作导致的疼痛也可归入此类,如食管镜、胃镜和结肠镜检查、伤口护理、皮下或肌肉注射、动静脉置管、经皮穿刺肿瘤活检、骨髓穿刺活检、腰椎穿刺等,需要预先镇痛和(或)镇静处理。
•与上述均无关的疼痛:肿瘤患者的其他合并症、并发症以及社会心理因素等非肿瘤因素导致的疼痛。如肿瘤患者高发的带状疱疹神经痛、压疮、肌筋膜痛综合征,其他疼痛性疾病或伴有疼痛的其他疾病(原发性三叉神经痛、糖尿病周围神经病变、痛风)和恐惧、焦虑等精神心理因素诱发、加重的疼痛等。
1.2 癌痛机制与分类
•根据病理生理学机制,癌痛可分为:伤害感受性疼痛和神经病理性疼痛。癌痛多为混合性疼痛,既有伤害感受性疼痛又有神经病理性疼痛。
伤害感受性疼痛是由伤害性刺激作用于机体或器官组织并破坏其结构而引起的疼痛,其感觉神经系统是正常的。伤害感受性疼痛包括躯体痛和内脏痛[6]。神经病理性疼痛为一种躯体感觉神经系统的损伤或疾病直接造成的疼痛,是痛觉传递神经纤维或疼痛中枢产生异常神经冲动所致[7]。癌性神经病理性疼痛由肿瘤或治疗对神经的直接损伤引起,可促进递质释放,造成伤害性感受器局部酸中毒,释放炎性因子,如肿瘤坏死因子等[8],从而导致伤害性感受器的敏化。持续的外周敏化将导致中枢敏化,形成顽固性疼痛。神经病理性疼痛的特征为自发性疼痛、痛觉过敏和痛觉超敏,主要表现为放电样痛、枪击样疼痛、针刺样痛、烧灼样痛、麻木痛和麻刺痛。
•根据疼痛的持续时间,疼痛可分为急性疼痛和慢性疼痛,还有一种发作迅速、持续时间短、疼痛强度剧烈的疼痛称为爆发性疼痛(下述简称爆发痛)。急性疼痛和慢性疼痛的肿瘤患者均可发生爆发痛。
癌性爆发痛是指在背景痛控制相对稳定、镇痛药物充分应用的前提下,自发或在某些可预知或不可预知因素的诱发下突然出现的短暂疼痛加重[9]。典型的爆发痛发作强度为中度至重度疼痛,发生迅速(数分钟内)、持续时间相对较短(中位时间为30 min)。癌性爆发痛的诊断标准如下:1)在过去的1周患者是否存在持续性疼痛(背景痛);2)在过去的1周患者的背景痛是否充分控制(数字化疼痛评分≤3分);3)患者是否存在短暂疼痛加重的现象(数字化疼痛评分≥4分),上述条件全部满足才可诊断为癌性爆发痛[10]。爆发痛分为自发性和诱发性。与没有爆发痛患者相比,爆发痛患者遭受疼痛相关功能损害和心理创伤(抑郁和焦虑)显著增多,生活质量下降。
2 癌痛规范化诊疗流程
癌痛规范化治疗的目标是将癌痛缓解至患者可接受的生活质量水平[11],其核心为建立癌痛规范化诊疗流程,包括常规筛查、全面评估、合理诊断、有效镇痛、预防和控制不良反应、积极患教和定期随访,医护人员和临床药师等参与全程管理。
2.1 癌痛常规筛查
癌痛筛查为评估癌症患者是否发生疼痛或存在发生疼痛的风险,应把握与患者接触的每次机会进行癌痛筛查(见图1),包括初次接诊、每次后续接触以及新的治疗、操作开始前。如下述临床场景应及时进行癌痛筛查:患者门诊首诊和首日入院时,要筛查患者是否存在疼痛;当病情变化时,要筛查患者是否存在疼痛;接受有创性操作(如穿刺、置管和拔管等)时,要筛查患者是否有发生疼痛的可能并预先处理;癌症患者存在疼痛客观行为表现(面部表情、呻吟和躯体动作等)时,要筛查患者是否有疼痛等[12]。

图1 癌痛筛查流程图
2.2 癌痛评估
癌痛评估是合理且有效进行镇痛治疗的前提,评估过程应在保证患者舒适度的前提下尽可能做到准确、全面并遵循“常规、量化、全面、动态”的原则。门诊患者应在癌痛治疗前及时评估,住院患者应在入院后8 h内初步评估,24 h内完成全面评估,并体现在病历中。
•常规评估原则:医护人员应主动询问癌症患者有无疼痛,常规评估疼痛程度,并进行相应的病历记录。对于有疼痛症状的患者,应将疼痛评估列入护理常规监测和记录。疼痛评估应区分与肿瘤急症相关和无关的疼痛,前者如病理性骨折、脑转移、感染以及肠梗阻或穿孔等导致的疼痛。
•量化评估原则:使用疼痛程度评估量表等量化标准来评估患者疼痛主观感受程度,需要患者密切配合。量化评估疼痛时,应重点评估24 h内患者最严重、最轻微以及通常情况下的疼痛程度。根据患者的实际情况选用评估量表:1)对于认知和语言交流能力均良好的患者,癌痛量化评估可使用视觉模拟评分量表(visual analogue scales,VAS)、数字评分量表(numeric rating scales,NRS)、语言评分量表(verbal rating scales,VRS)和面部表情评分量表(faces pain scale,FPS)等疼痛强度量表(见附件1),其中FPS还适用于语言交流困难的老人、儿童、文化程度低、存在语言或文化差异的患者;2)对于无法语言交流的认知障碍或智力障碍的患者,行为观察是疼痛评估的有效方法,可参见晚期痴呆者疼痛评估量表(pain assessment in advanced dementia scale,PAINAD)(见附件2);3)意识障碍的机械通气患者参见重症监护患者疼痛观察工具(critical-pain observation tool,CPOT)(见附件3)。
•全面评估原则:癌痛全面评估是指对癌症患者疼痛情况及相关病情进行全面评估。根据评估量表的评估内容可分为:1)评估疼痛强度和疼痛性质等综合因素建议使用简明疼痛评估量表(brief pain inventory,BPI)(见附件4)和简式McGill疼痛问卷(short-form of McGill pain questionnaire,SF-MPQ)(见附件5);2)评估疼痛性质(即鉴别伤害感受性疼痛与神经病理性疼痛)建议使用疼痛性质的评估量表DN4问卷(douleur neuropathique 4 questions,DN4)(见附件6)和ID pain量表(见附件7);3)评估患者焦虑抑郁心理因素建议使用广泛性焦虑问卷(generalized anxiety disorder-7,GAD-7)(见附件8)和PHQ-9抑郁症筛查量表(patient health questionnaires-9,PHQ-9)(见附件9);4)爆发痛的评估量表国内主要采用数字评分量表(NRS)、语言评分量表(VRS)和视觉模拟评分量表(VAS)[10],而国外常用爆发痛问卷(breakthrough pain questionnaire,BPQ)(见附件10)和爆发痛评估工具(breakthrough pain assessment tool,BAT)(见附件11)[13]。
•动态评估原则:癌痛动态评价是指对患者的疼痛症状及变化进行持续、动态的评价,包括对疼痛的原因、部位、性质、程度、爆发痛、疼痛缓解及加重因素的评价,和对镇痛治疗的不良反应的评价。动态评价对镇痛药的剂量滴定具有重要意义。
2.3 癌痛治疗
2.3.1 治疗原则 癌痛应采取规范化、个体化治疗的原则。根据患者的病情和身体状况,采用各种治疗方法,及早、充分、持续、有效地消除疼痛,预防和控制药物不良反应,减轻患者可能产生的心理负担和障碍,达到优化患者生活质量的目的。
2.3.2 治疗方法 癌痛的治疗方法包括:病因治疗和对症治疗。
1)病因治疗
癌痛的主要原因是由肿瘤或肿瘤治疗引起的,因此需要针对癌痛原因进行治疗,如手术、放疗、化疗、内分泌治疗、免疫治疗、介入治疗及中医药治疗等,可能减轻或消除癌痛。
2)对症治疗
即治疗不针对引起癌痛的病因,仅为缓解症状,包括药物治疗和非药物治疗。
(1)药物治疗
①基本原则:根据世界卫生组织(WHO)《癌痛三阶梯止痛治疗指南》和《NCCN成人癌痛临床实践指南》(2019.V3),癌痛药物镇痛治疗的5项基本原则改进如下:
•口服给药。口服方便,是最常用的给药途径。
•按阶梯用药。应当根据患者疼痛程度,有针对性地选用不同性质、作用强度的镇痛药物。
轻度疼痛(1分≤NRS≤3分):可选用非甾体类抗炎药物(NSAID)和对乙酰氨基酚;
中度疼痛(4分≤NRS≤6分):可选用弱阿片类药物或低剂量的强阿片类药物,可联合应用非甾体类抗炎药物或对乙酰氨基酚以及辅助镇痛药物(抗惊厥类药物、抗抑郁类药物、糖皮质激素、局部麻醉药和双膦酸盐类药等);
重度疼痛(7分≤NRS≤10分):首选强阿片类药,并可合用非甾体类抗炎药物或对乙酰氨基酚以及辅助镇痛药物(抗惊厥类药物、抗抑郁类药物、糖皮质激素、局部麻醉药和双膦酸盐类药等)。
•按时用药。应当按照规定时间间隔规律性给予镇痛药,有助于维持稳定、有效的血药浓度。目前,缓释药物临床使用日益广泛,可以用缓释阿片类药物作为基础用药进行疼痛滴定,出现爆发痛时给予即释阿片类药物对症处理。单纯使用即释阿片类药物进行滴定的有持续性疼痛的患者,应在滴定完成后转换为等效剂量的缓释阿片类药物。
•个体化给药。应当按照患者具体病情和个体化差异,使用合适的药物、剂量和给药途径使疼痛得到充分缓解,制定个体化用药方案。
•注意具体细节。对使用镇痛药的患者要加强监护,密切观察其疼痛缓解程度和不良反应情况,注意药物联合应用的相互作用和配伍禁忌,以便在镇痛药物疗效和不良反应之间取得平衡。
②药物选择与使用
根据癌症患者疼痛的性质、强度、加重或减轻因素、过去和现在的治疗方法、合并疾病等情况,合理选择镇痛药物,个体化调整给药剂量、给药途径和给药频率,积极防治不良反应,从而获得最佳的镇痛效果。
根据作用机理将镇痛药物分为下述3类:
•非甾体类抗炎药物和对乙酰氨基酚
非甾体类抗炎药物和对乙酰氨基酚是癌痛治疗的常用药物。两种非甾体药物联合应用并不增加疗效而可能增加不良反应,故不主张联合使用。
非甾体抗炎药通常会引起消化性溃疡,胃肠道出血,血小板功能障碍,肾功能损伤、肝功能损伤和心脏毒性等不良反应。上述不良反应的发生与药物的剂量和持续时间有关,因此使用非甾体类抗炎药物和对乙酰氨基酚应定期进行风险评估和监测,项目包括:基础血压、尿素氮、肌酐、肝功能、全血细胞计数、大便隐血。风险评估的内容包括:肾毒性的高危人群:年龄>60岁、体液失衡、多发性骨髓瘤、糖尿病、间质性肾炎、肾乳头坏死、同时使用其他肾毒性药物和经肾排泄的化疗药物;胃肠道不良反应的高危人群:年龄>60岁、消化性溃疡病或酗酒史、重要器官功能障碍、长期使用或大剂量使用非甾体类抗炎药、同时使用皮质激素或低剂量阿司匹林;心脏毒性的高危人群:心血管病史或心血管疾病或并发症高危患者,如果充血性心力衰竭或高血压病进展或恶化,停用非甾体抗炎药;非甾体类抗炎药物与抗凝药物(如华法林或肝素)合用可显著增加出血风险,避免在预防性或治疗性抗凝治疗的情况下口服NSAIDs。外用NSAIDs,如双氯芬酸凝胶或贴剂,可能适用于这类人群[5]。当非甾体类抗炎药或对乙酰氨基酚用药剂量达到一定水平时,再增加用药剂量并不能增强其镇痛效果,而药物不良反应将明显增加。所以NCCN成人癌痛指南(Version 3.2019)规定正常肝功能患者日限制剂量为:布洛芬3.2 g/d,塞来昔布0.4 g/d,对乙酰氨基酚4 g/d(短期用药)或3 g/d或更少(长期用药)[5]。但是根据《中华人民共和国药典临床用药须知》(2015版)规定:布洛芬日限制剂量为2.4 g/d;塞来昔布0.4 g/d,镇痛连用不超过7 d;对乙酰氨基酚用于镇痛日剂量不宜超过2 g/d,连用不宜超过10 d,用于骨关节炎日剂量不超过4 g/d(疗程遵医嘱),复方制剂则不宜超过1.5 g/d[14]。如果需要长期单独使用非甾体类抗炎药或对乙酰氨基酚已达到限制性用量或不良反应无法耐受,可考虑更换为阿片类镇痛药;如为联合用药,则非甾体类抗炎药物和对乙酰氨基酚剂量不应超过日限制剂量。考虑到长期使用对乙酰氨基酚的肝脏毒性,对乙酰氨基酚和阿片类镇痛药的复方制剂使用须谨慎。
需要注意的是,根据《麻醉药品和精神药品管理条例》有关规定,国家药品监督管理局、公安部、国家卫生健康委员会决定2019年9月起将含羟考酮复方制剂(如氨酚羟考酮)等品种列入精神药品管理:口服固体制剂每剂量单位含羟考酮碱>5 mg,且不含其他麻醉药品、精神药品或药品类易制毒化学品的复方制剂列入第一类精神药品管理;口服固体制剂每剂量单位含羟考酮碱不超过5 mg,且不含其他麻醉药品、精神药品或药品类易制毒化学品的复方制剂列入第二类精神药品管理。
•阿片类药物
阿片类药物是中、重度癌痛治疗的首选药物。对于慢性癌痛治疗,推荐选择阿片受体激动剂。阿片受体混合激动-拮抗剂是指某些阿片类药物对某型阿片受体产生激动作用,而对另一型阿片受体产生拮抗作用,一般不用于癌痛治疗。对于阿片依赖患者,从阿片受体激动剂转换为混合激动-拮抗剂可能会引起戒断症状[5]。国内常见的阿片受体混合激动-拮抗剂有地佐辛、喷他佐辛和布托啡诺等。
剂量滴定:阿片类镇痛药的有效性和安全性存在较大的个体化差异,需要逐渐调整剂量,以获得最佳药效(既充分镇痛又无不可耐受的不良反应),称为剂量滴定。短效口服药物的滴定流程如下见图2。
除短效口服药物滴定方法外,也可使用缓释口服阿片类药物作为基础给药,备用短效阿片类药物治疗爆发痛的方法进行滴定(图3)。对于阿片类药物未耐受患者,阿片类口服缓释制剂起始基础剂量可根据患者疼痛程度、身体状况来选择(一般口服缓释吗啡10~30 mg/q12 h给药或缓释盐酸羟考酮10~20 mg/q12 h给药。
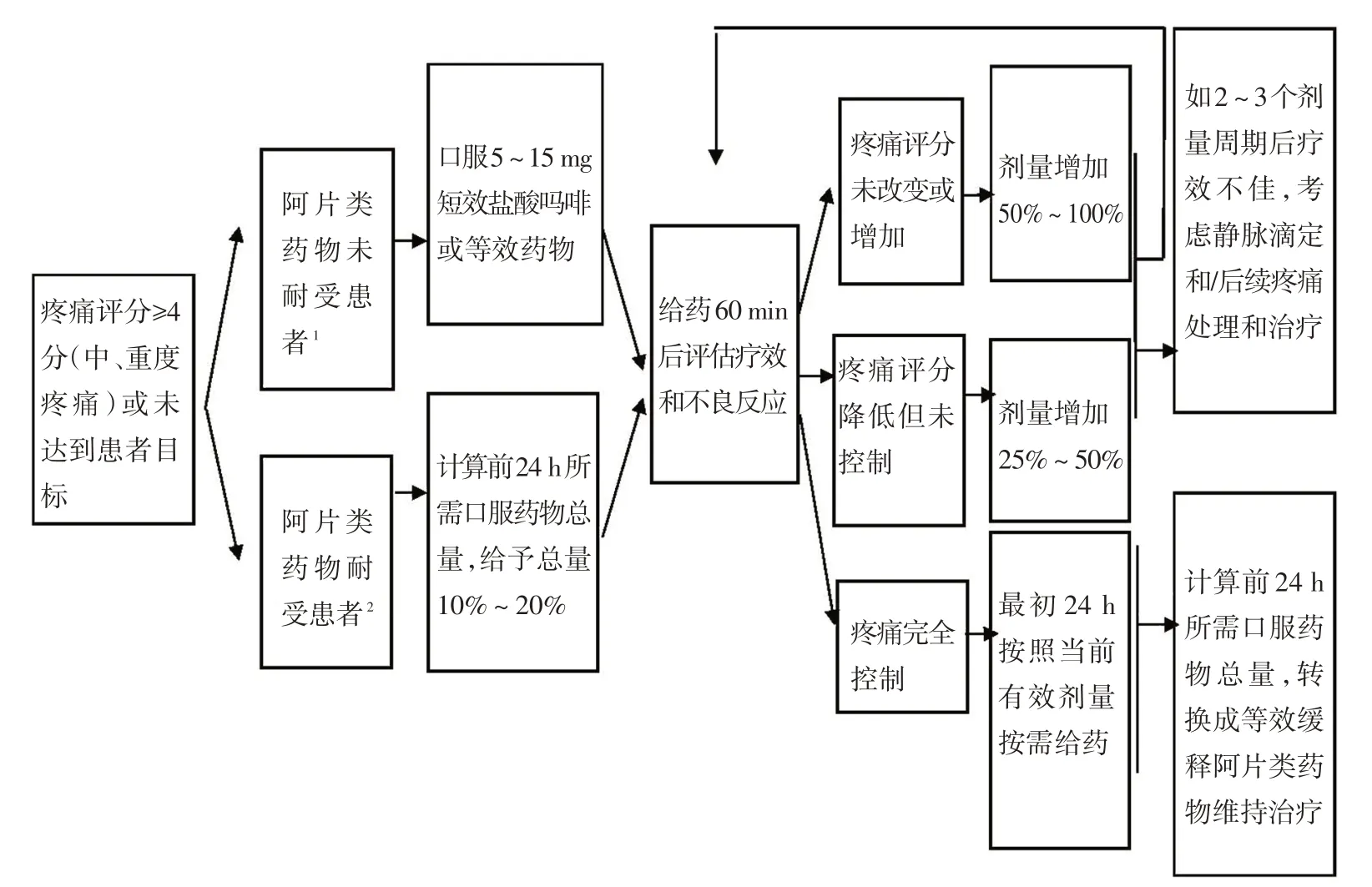
图2 短效口服药物的滴定流程
对于阿片类药物已耐受患者,可根据滴定前24 h阿片类药物用药总量确定基础给药剂量,参照图3进行滴定,尽可能在24 h内使疼痛得到控制。如果阿片类药物不良反应不能缓解,患者疼痛强度<4分,滴定剂量可考虑减少10%~25%,然后重新评估镇痛效果并密切观察或随访。
维持用药:在中国常用的长效阿片类药物有吗啡缓释片、羟考酮缓释片和芬太尼透皮贴剂等。在应用长效阿片类药物期间,应备用短效阿片类(如吗啡口服即释剂、羟考酮口服即释剂、吗啡或羟考酮注射剂等)作为解救药物治疗爆发性疼痛。爆发痛解救剂量为前24 h用药总量的10%~20%。每日短效阿片解救用药次数≥3次时,应当考虑将前24 h解救用药剂量换算成长效阿片类药按时给药。对于复杂机制的癌痛通常需要根据不同机制在阿片类药物的基础上联合使用其他相应的辅助镇痛药物,一般两种长效阿片类药物不联合使用。
等效剂量换算:阿片类药物之间的剂量换算可参考换算系数表(表1)。一种阿片药物转换为另一种阿片类药物时,仍需仔细观察患者病情的变化,并进行个体化的剂量滴定。
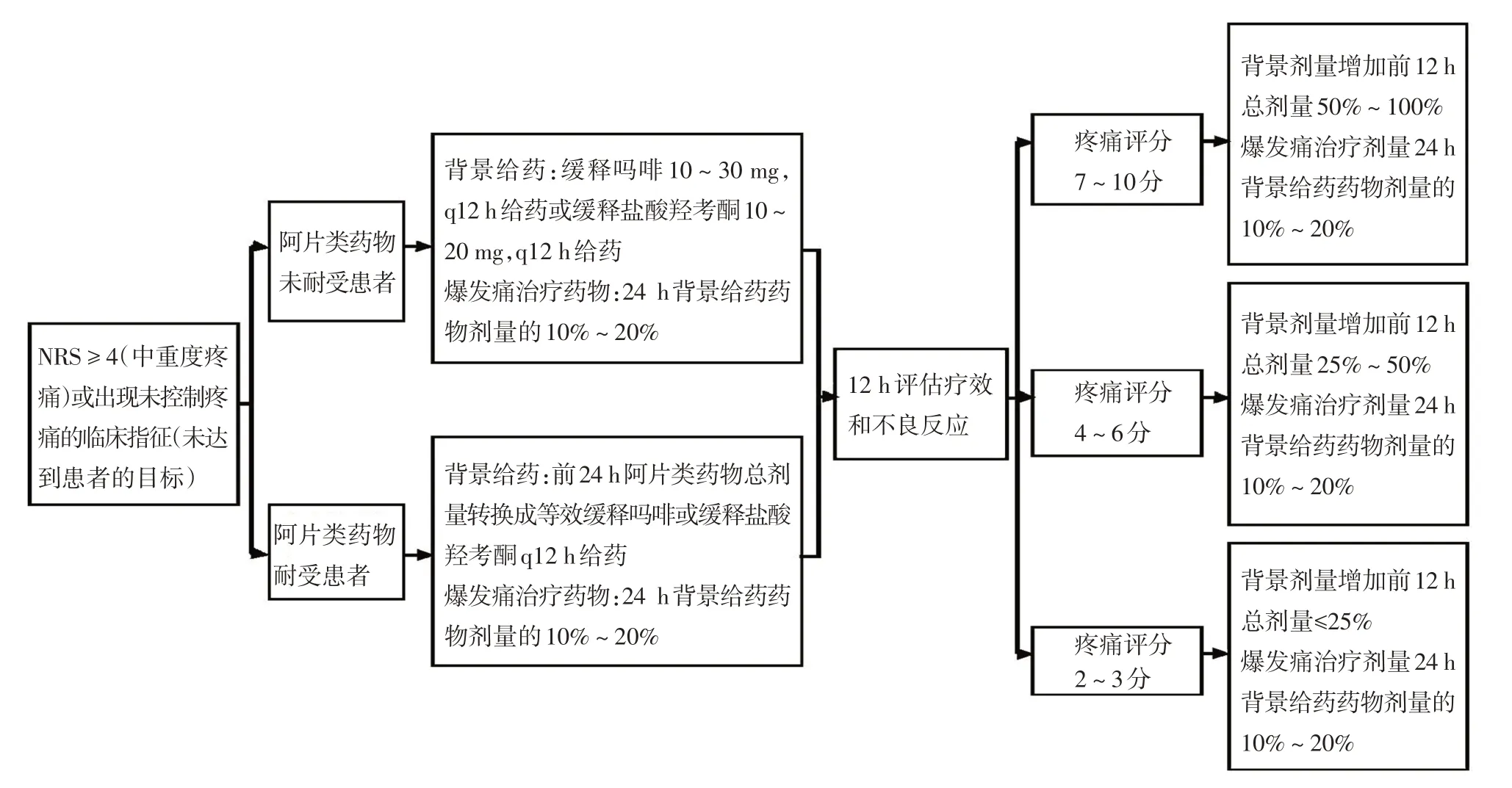
图3 以缓释阿片类药物为背景用药的滴定流程
减量或停药:如果阿片类药物需要减少或停止使用,应逐渐减少剂量。一般情况下,阿片类药物剂量可按照10%~25%每日剂量减少,直至日剂量相当于口服吗啡30 mg,2日后可考虑停药。
不良反应防治(见附件12):阿片类药物的不良反应很常见,主要包括便秘、恶心、呕吐、嗜睡、瘙痒、头晕、尿潴留、谵妄、认知障碍、呼吸抑制等。因此,需要重视阿片类药物的不良反应,更需要积极预防和处理阿片类药物的不良反应,使疗效与不良反应平衡,患者获益最大化。除便秘外,阿片类药物的其他不良反应一般会随着时间的推移而逐渐减轻。对患者、家属和照护者进行宣教,有利于不良反应的管理。
便秘:阿片类药物最常见且不可耐受的不良反应,通常会持续发生于阿片类药物镇痛治疗全过程。对于使用阿片类药物的患者应早期防治便秘,目标为1~2 d非强制性排便1次。预防措施:患者及家属的健康教育,足量饮水,适量运动;刺激性泻药:比沙可啶、酚酞(果导)等;根据症状调节饮食结构,调整刺激性泻药剂量,养成规律排便的习惯。治疗措施:评估便秘原因和严重程度;合理增加刺激性泻药剂量;中重度便秘可增加其他类型的泻药:渗透性泻药(乳果糖、镁盐、聚乙二醇等)、润滑性泻药(液状石蜡、甘油等)、促肠液分泌药物(鲁比前列酮)、灌肠剂(磷酸钠、生理盐水等)或缓泻直肠栓剂等;注意可能发生的水、电解质异常;中性粒细胞或血小板减少患者禁止使用直肠栓剂和(或)灌肠剂;当泻药效果不佳时,可考虑外周作用的阿片受体拮抗剂,如甲基纳曲酮或纳洛酮;需注意某些患者合并症和合并用药的情况也会加重便秘,包括慢性功能性便秘、结肠癌所致肠梗阻、神经功能受损(帕金森病、糖尿病等)、合并使用导致便秘的药物(三环类抗抑郁药,5-HT3受体拮抗剂、利尿药、抗胆碱类药物或补铁剂等);中医的一些通便中成药也可以酌情选用,包括行气导滞类(六味安消胶囊、木香槟榔丸、枳实导滞丸)、清热通便类(牛黄上清丸、牛黄解毒丸、牛黄清火丸、新清宁片、番泻叶冲剂)、益气滋阴类(麻仁润肠丸、麻仁软胶囊、苁蓉通便口服液)等,应辨证施治。
恶心、呕吐:一般发生于阿片类药物的使用初期,症状多在1~2 周内缓解,应排除其他原因(如便秘、脑转移、化疗、放疗或高钙血症等)。预防措施:确保患者大便通畅;对于既往有阿片类药物恶心呕吐史的患者,建议使用止吐药物进行预防性治疗。治疗措施:根据需要选用甲氧氯普胺或氟哌啶醇,老年体弱患者长期使用这些药物可能会导致迟发性运动障碍;必要时使用5-HT3 受体拮抗剂(如格拉司琼、昂丹司琼等,可避免中枢神经系统不良反应但会引起便秘,需谨慎使用),也可考虑其他替代药物,如奥氮平崩解片可用于肠梗阻患者;可考虑地塞米松;症状持续1 周以上,经上述措施治疗仍未缓解者,需重新评估恶心、呕吐的原因及严重程度。
皮肤瘙痒:主要出现在使用阿片类药物的初期,短期一般可耐受。治疗措施:评估瘙痒的其他原因(如使用其他药物),如并发皮疹、荨麻疹或呼吸急促需考虑过敏反应;抗组胺药物,苯海拉明、西替利嗪等;加用小剂量阿片受体混合激动-拮抗剂(纳布啡等);持续静脉输注纳洛酮(0.25~1.00 μg·kg-1·h-1,从最低剂量开始滴定,剂量过大将拮抗镇痛效果)[5],同时需要注意纳洛酮的不良反应和禁忌证;试用5-HT3受体拮抗剂(昂丹司琼等)。
谵妄:出现谵妄时应排除引起谵妄的其他原因(如感染、高钙血症、中枢神经系统疾病、脑转移、其他精神药物),必要时使用抗精神病药物(如氟哌啶醇、奥氮平、利培酮),并注意心电监测QTc 间期是否延长。长时间服用这些药物,由于消除半衰期长,可能有必要降低剂量。
运动和认知障碍:稳定剂量的阿片类药物(>2周)或许不能影响患者上述功能,但在滴定期间应予以监测,并警惕驾驶障碍。
过度镇静:在阿片类药物使用的最初几天内可能出现头晕、嗜睡或过度镇静等不良反应,一般1 周左右症状自行消失。如果患者出现镇静及嗜睡并持续2~3天以上时应排除其他原因,如严重疲劳、脑转移、使用其他镇静药、感染、脱水、高钙血症等。治疗措施:症状较轻者避免大幅度活动(如突然坐起、站起等),使用浓茶、咖啡等饮食调节;兴奋剂治疗:咖啡因、哌甲酯等,尽可能不在下午以后使用以避免夜间失眠;症状持续1 周以上,经上述措施治疗仍未缓解者,需重新评估过度镇静的原因及严重程度。
呼吸抑制:是阿片类药物最严重的不良反应。呼吸抑制的临床表现:针尖样瞳孔,呼吸次数减少(<8次/分)和(或)潮气量减少,潮式呼吸,紫绀,嗜睡甚至昏迷,骨骼肌松弛,皮肤湿冷,有时可出现心动过缓和低血压。预防措施:规律用药,小剂量起用,根据病情逐渐加量;对于年老体弱者、严重心肺功能不全者在使用阿片类药物时应密切观察其呼吸、神志、精神状态等。治疗措施:给予1 mL纳洛酮(0.4 mg/mL)加入生理盐水稀释至10 mL,每30~60 s静脉给药1~2 mL,直到症状改善,必要时重复给药,如果10 min内仍无效且纳洛酮给药总量达到1 mg,需重新评估呼吸抑制的原因及严重程度;因为纳洛酮半衰期短,对于半衰期长的阿片类药物,考虑静脉持续输注纳洛酮,同时防止过度拮抗导致疼痛复发。
·辅助镇痛药物
辅助镇痛药物可增强阿片类药物的镇痛效果,或直接产生一定的镇痛作用,包括抗惊厥药、抗抑郁药、皮质激素、N-甲基-D-天冬氨酸受体(NMDA)拮抗剂和局部麻醉药等(见附件13)。辅助药物能够减少阿片类药物用量,常用于辅助治疗神经病理性疼痛、骨痛等。辅助用药的种类选择及剂量调整,需要个体化对待。
常用于神经病理性疼痛的辅助药物[15-16]:抗惊厥类药物:用于神经损伤所致的撕裂痛、放电样疼痛等,如加巴喷丁、普瑞巴林;抗抑郁药:用于中枢性或外周神经损伤所致的麻木样疼痛、烧灼样疼痛等,该类药物也可以改善心情和睡眠,如阿米替林、度洛西汀和文拉法辛等;神经压迫或炎症试用糖皮质激素或非甾体药物;局部外用药物:利多卡因、双氯芬酸钠和氟比洛芬酯等的凝胶、乳膏或贴片。
常用于骨转移性癌痛的辅助药物[17]:非甾体类药物;骨吸收抑制剂:双膦酸盐,地诺单抗;放射性核素;抗惊厥药物;抗抑郁药物;局部外用药物。
常用于癌性内脏痛的辅助药物[18-19]:抗抑郁药物;肠梗阻治疗药物如类固醇激素、H2 受体拮抗剂、抗胆碱能药和奥曲肽。
(2)非药物治疗
用于癌痛治疗的非药物治疗方法主要有:介入治疗(包括阻断神经传导通路的神经阻滞/毁损术、神经电刺激疗法、脑室内/椎管内药物输注通道植入术等)、放射治疗、物理方法(按摩、冷热敷、经皮神经电刺激、针灸等)、认知训练(想象、催眠、放松、积极应对训练、行为激活等)、社会心理支持治疗等。适当应用非药物疗法,可作为药物镇痛治疗的有益补充。
介入治疗前,应当综合评估患者的一般情况、预期生存时间、抗肿瘤治疗指征、介入治疗适应证和禁忌证、预期收益和风险等。
良好的疼痛控制还需要多学科团队合作,建立肿瘤科、疼痛科、神经外科、骨外科、影像介入科、身心医学科、康复科、药学部、营养科等多学科参与的诊疗模式,集思广益,根据具体情况为患者制定规范化、综合化和个体化的镇痛方案。
2.4 临床药师在癌痛治疗中的作用
已有多项研究结果显示,临床药师在癌痛管理中具有重要作用,临床药师参与合理用药的过程不仅能够提高疼痛治疗的规范性,并且明显改善患者疼痛控制情况、提高患者生活质量[20-21]。因此,癌痛治疗团队中应有疼痛专科临床药师参与。临床药师应参加临床交班、查房、病例讨论等医疗活动,及时了解患者病情变化,组织开展多模式的临床药学实践活动。
2.4.1 评估用药风险 临床药师应采集并评估患者伴发疾病、合并用药、近期药物治疗史、过敏史、药物不良反应史等情况,综合评估癌痛药物治疗中的用药风险,对存在用药风险的患者,应制定适宜的药学监护计划并负责实施。
2.4.2 药学查房 对住院患者进行药学查房,根据药学监护计划观察镇痛药物疗效,监测镇痛药物不良反应,评估用药依从性,对患者进行用药教育,解答患者及家属给予用药咨询。发现患者存在用药问题应及时指导纠正。指导出院患者带药用法、用量及注意事项等,并提供书面用药教育材料。
2.4.3 医嘱审核 医嘱审核包括:麻醉、精神药品处方开具规范性,癌痛治疗药物适应证、用法用量、特殊人群剂量调整、药物相互作用、用药途径、溶媒配伍等。临床药师应熟练掌握阿片类及其他镇痛药物滴定剂量和转换剂量的计算,对阿片类药物剂量的审核应考虑前24 h内疼痛程度、用药情况、爆发痛次数等。
2.4.4 患者教育 癌痛患者用药教育内容包括:阿片类药物不良反应预防及处理、阿片类药物急性中毒反应的识别、NSAIDs 类药物长期用药的不良反应监测、口服缓控释剂型药品使用注意事项、透皮贴剂使用注意事项等内容。可采取口头指导、书面材料指导、观看视频指导等形式。
2.4.5 不良反应监测 针对阿片类药物的常见不良反应包括便秘、恶心、呕吐、嗜睡、瘙痒、尿潴留、谵妄及认知障碍等,应进行主动监测,及时发现且参与不良反应的评估,并提供指导。
2.4.6 药学会诊 临床药师参加顽固性癌痛患者、特殊人群癌痛患者(如肝功能减退、肾功能减退、基础用药品种多等)会诊或多学科综合诊疗,参与个体化药物治疗方案的制定。
2.4.7 药学信息 负责癌痛治疗相关药学信息的搜集,根据临床及患者的需要,及时、准确地提供癌痛治疗药物药理学、药代动力学、药物相互作用、特殊人群用药、配伍禁忌、规格、剂型、储存方法等相关信息。
2.4.8 癌痛用药评价 制定癌痛治疗药物专项处方点评方案,定期开展癌痛治疗药物的专项处方点评。内容应包括麻醉或精神药品处方规范性、用药适应证、用法用量、药物相互作用等方面,点评结果应通过院内公示等方式有效反馈,对存在的不合理用药情况及时干预。
2.5 癌痛患者及家属教育
2.5.1 教育原则
1)疼痛教育由接受过疼痛相关专业知识培训的护士和临床药师实施。
2)疼痛教育应从接触患者时立即开始,并贯穿于整个治疗过程。
3)疼痛教育对象除了患者本人还应包括其家属。家属在患者的疼痛管理中发挥至关重要的作用,应为癌痛患者与家属提供全面的健康教育[22]。
4)评估患者及家属的文化水平、理解能力、语言习惯等,制定个性化教育计划,确保教育有效[23]。
5)疼痛教育内容重点应根据患者处于不同的疼痛治疗阶段来确定,教育的重点也应随着患者的改变随时调整。
6)疼痛健康教育后应评价教育效果。
2.5.2 教育方式
1)团体教育,定期举行疼痛相关知识讲座,对疼痛患者和家属存在的共性信息需求进行讲解,面对面将癌痛相关知识进行交流讨论或解答疑问[24]。
2)个体教育,护士基于患者的具体问题和需求提供有针对性地教育,鼓励患者表达癌痛及治疗后的感受[25]。
3)同伴教育,同伴教育者结合自己的经验和切身的感受,增加疼痛健康教育的效果。
4)疼痛教育宣传栏,每季度更新疼痛教育宣传栏相关内容。
5)多媒体疼痛健康教育,包括广播电台、电视台、报刊、自媒体(微博、微信公众号、直播、短视频)等。
2.5.3 教育内容
1)鼓励患者主动汇报疼痛。
2)教会患者使用疼痛评估工具进行评估和填写疼痛日记(见附件14)。
3)消除患者常见疼痛相关误区。①癌痛不是肿瘤晚期的标志,而长期存在或严重的癌痛会影响患者的生活质量及免疫力,甚至会造成焦虑、抑郁等不良情绪。对于癌痛应该“止”,不能“忍”;②镇痛药物及时、按时使用才能安全有效,而且所需要的镇痛药剂量也最低,切勿仅在疼痛剧烈时才使用镇痛药。按时用药,能保证体内维持有效的血药浓度,有效控制疼痛;③疼痛患者规范化使用阿片类药物成瘾风险极低,患者不必因担忧成瘾风险而惧怕使用阿片类药物;④患者担心一旦使用阿片类药物就可能终身用药,事实上,疼痛若得到控制,可以随时安全停用阿片类药物或换用非阿片类药物。
4)教会患者缓解疼痛方法,如转移注意力、呼吸放松疗法、冷敷热敷等。
5)指导患者用药相关注意事项。①按时规律服药,不得随意增减剂量;②告知患者镇痛治疗过程中常见的不良反应和应对方法,不良反应包括:便秘、恶心、呕吐、嗜睡、头晕、尿潴留、皮肤瘙痒等;③根据患者使用的药物,给予针对性的用药知识宣教;④患者居家用药过程中患者若出现以下情况,需及时就医:患者出现新的疼痛、疼痛有变化或药物不能缓解的疼痛;患者出现不可缓解的恶心、呕吐、头晕、嗜睡、尿潴留、便秘、谵妄等不良反应的状况。
6)建议患者居家期间监测并记录疼痛情况,提供出院后疼痛就医信息,发放信息卡,提供24 h紧急联系电话。
2.6 癌痛患者随访
癌痛患者随访是癌痛全程管理的重要组成部分。通过随访可以了解患者居家期间疼痛控制情况,指导患者正确服用止痛药物,预防和减少不良反应,提高患者依从性,达到最佳的治疗效果[26]。
2.6.1 随访原则
1)建立健全癌痛患者随访制度。
2)进行癌痛随访的人员应相对固定,需经过专业培训,具备癌症疼痛管理经验。
3)癌痛患者出院时,应评估患者及其家属对疼痛知识掌握情况,与患者和家属共同制订随访计划,提供随访卡和疼痛教育材料。
4)建立随访记录本,规范、连续记录随访内容。终止随访应写明原因,如住院、死亡、拒绝随访等。
2.6.2 随访对象 接受癌痛规范化治疗的患者,包括门诊和出院患者。
2.6.3 随访时间
1)出院1周内进行第1次随访。
2)对初次用药和疼痛控制不稳定的患者,应3天内进行第1次随访。
3)随访时间间隔根据患者情况合理安排,疼痛缓解后可1~2 周随访1次;疼痛控制不佳或用药副作用较大者,1周内可进行多次随访。
4)每1次随访结束根据具体情况预定下1次随访时间。
2.6.4 随访方式 医护人员可根据癌痛患者情况,通过电话、短信、微信、视频、手机App、居家访视等方式提供主动随访,或安排定期门诊随访。
2.6.5 随访内容
1)患者疼痛情况,包括疼痛强度、部位、性质;是否出现爆发痛,爆发痛次数、评分和解救用药。
2)疼痛对日常生活影响,包括饮食、睡眠、活动、情绪、人际关系等。
3)患者镇痛药物应用情况,包括药物名称、服用剂量、频次、方法;是否遵医嘱用药;是否出现药物不良反应,包括便秘、恶心、呕吐、嗜睡、尿潴留、瘙痒等。
4)根据随访中具体情况给予相应指导和建议,包括规范用药、药物不良反应应对、麻醉药品的取药方法等。在疼痛加重、每日出现3次及以上的爆发痛或影响睡眠时,应咨询医师或来医院治疗[26]。
专家委员会
专家组组长:
冯继锋 江苏省肿瘤医院
刘宝瑞 南京大学医学院附属鼓楼医院
陆建伟 江苏省肿瘤医院
束永前 江苏省人民医院
执笔人:
沈 波 江苏省肿瘤医院
杨 扬 江苏省肿瘤医院
申 文 徐州医科大学附属医院
周国仁 江苏省肿瘤医院
专家组成员(按姓氏汉语拼音排序):
陈 凯 苏州大学附属第一医院
陈小飞 淮安市第一人民医院
陈映霞 东部战区总医院八一医院
褚晓源 东部战区总医院
冯继锋 江苏省肿瘤医院
华 东 无锡市第四人民医院
黄俊星 泰州市人民医院
蒋书娣 江苏省人民医院
刘宝瑞 南京大学医学院附属鼓楼医院
吉爱军 江苏省肿瘤医院
陆建伟 江苏省肿瘤医院
李 婕 江苏省肿瘤医院
孟爱凤 江苏省肿瘤医院
倪美鑫 南通市肿瘤医院
邵 华 东南大学附属中大医院
申 文 徐州医科大学附属医院
沈 波 江苏省肿瘤医院
束永前 江苏省人民医院
魏 青 江苏省肿瘤医院
杨 磊 南通市肿瘤医院
杨 扬 江苏省肿瘤医院
袁 玲 南京大学医学院附属鼓楼医院
赵 敏 江苏省肿瘤医院
赵 云 江苏省肿瘤医院
周国仁 江苏省肿瘤医院
周晓蓉 江苏省肿瘤医院
朱余兵 南京市第一医院
秘书组成员:
吴 楠 江苏省肿瘤医院
羊 波 江苏省肿瘤医院
许潇月 江苏省肿瘤医院
朱家丽 江苏省肿瘤医院
徐思露 江苏省肿瘤医院
