西黄丸联合GP方案治疗晚期乳腺癌的疗效观察
2020-05-28徐炜丁少坤许宁宁石露露祁博宇
徐炜 丁少坤 许宁宁 石露露 祁博宇
乳腺癌是女性最常见的恶性肿瘤之一,近年来该病发病率逐年升高,且呈年轻化趋势[1,2]。目前,化疗仍是治疗晚期乳腺癌的主要手段,能够有效缩小肿瘤病灶,抑制肿瘤复发转移,延长患者生存期。但化疗药物种类众多,疗效不一,且长期化疗容易产生骨髓抑制等各种并发症,患者耐受性差[3]。西黄丸是由牛黄、麝香、乳香和没药组成的中药制剂,具有清热解毒、消肿散结的疗效,可用于晚期乳腺癌、肝癌等多种恶性肿瘤的临床治疗中[4]。本研究探讨了西黄丸联合GP方案治疗晚期乳腺癌的临床疗效及对血清肿瘤标志物、雌激素、血常规的影响,报告如下。
1 资料与方法
1.1 一般资料 选取2017年1月至2019年4月我院收治的110例晚期乳腺癌患者,随机分为对照组和观察组,每组55例。对照组:年龄33~64岁,平均年龄(42.75±5.48)岁;病程2~6年,平均(5.00±0.62)年;TNM分期:Ⅲ期30例,Ⅳ期25例。观察组:年龄35~66岁,平均年龄(43.12±5.56)岁;病程2~8年,平均(5.09±0.68)年;TNM分期:Ⅲ期32例,Ⅳ期23例。2组年龄、病程和TNM分期差异无统计学意义(P>0.05),具有可比性。
1.2 纳入与排除标准
1.2.1 纳入标准[5,6]:①符合晚期乳腺癌诊断标准,均经临床症状、实验室检查、病理学检查确诊;②TNM分期均为Ⅲ、Ⅳ期者;③预计生存时间≥3个月;④未发生远处组织器官转移者;⑤近1个月内未接受其他抗肿瘤治疗者;⑥患者及家属均签署知情同意书。
1.2.2 排除标准:①已发生远处转移者;②预计生存时间<3个月;③合并心脑血管病或肝肾等重要脏器功能不全者;④依从性差者;⑤过敏体质或对使用药物过敏者。
1.3 治疗方法 2组均给予GP化疗方案:吉西他滨(山东罗欣药业)1 000 mg/m2,第1、8 d,静脉滴注;顺铂(云南植物药业)20 mg/m2,第2~5 d,静脉滴注。观察组在化疗基础上加用西黄丸(北京同仁堂)治疗,3 g/次,2次/d。21 d为1个周期,2组均持续2个疗程。
1.4 观察指标
1.4.1 近期疗效:完全缓解(CR):病灶完全消失,且持续时间≥1个月;部分缓解(PR):病灶体积较治疗前缩小≥50%;稳定(SD):病灶体积较治疗前缩小,但未达PR水平,或者病灶体积较治疗前增大,但未达PD水平;进展(PD):病灶体积较治疗前增大≥25%或出现新发病灶。缓解率=(CR+ PR)例数/总例数×100%,疾病控制率=(CR+ PR+SD)例数/总例数×100%。
1.4.2 远期疗效:比较2组无进展生存时间(PFS)、总生存时间(OS)。PFS指化疗开始至疾病进展的时间;OS指化疗开始至死亡的时间。
1.4.3 复发率和生存率:随访1年,观察2组复发和生存情况,计算复发率和生存率。
1.4.4 不良反应发生情况:治疗期间观察并记录2组不良反应发生情况,包括恶心、呕吐、脱发、骨髓抑制、肝肾功能不全。
1.4.5 血清肿瘤标志物和雌激素:采集患者治疗前后空腹静脉血3 ml,4 000 r/min离心10 min,分离血清。采用酶联免疫吸附实验(ELISA)测定血清癌胚抗原(CEA)、糖类抗原125(CA125)、糖类抗原153(CA153)、雌酮(E1)、雌二醇(E2)。
1.4.6 血常规指标:采用全自动生化分析仪测定血红蛋白(Hb)、白细胞(WBC)、血小板(PLT)。
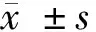
2 结果
2.1 2组近期疗效比较 对照组缓解率和疾病控制率分别为56.36%(31/55)、78.18%(43/55),观察组缓解率和疾病控制率分别为78.18%(43/55)、92.73%(51/55)。观察组近期疗效优于对照组,差异有统计学意义(P<0.05)。见表1。

表1 2组近期疗效比较 n=55,例(%)
注:与对照组比较,*P<0.05
2.2 2组远期疗效比较 对照组PFS和OS分别为(6.37±0.84)个月、(12.00±1.72)个月,观察组PFS和OS分别为(10.42±1.26)个月、(15.33±2.18)个月。观察组远期疗效优于对照组,差异有统计学意义(P<0.05)。见表2。
2.3 2组血清肿瘤标志物比较 2组治疗前血清CEA、CA125、CA153比较差异无统计学意义(P>0.05)。2组治疗后血清CEA、CA125、CA153均较治疗前降低(P<0.05),且观察组CEA、CA125、CA153低于对照组,差异有统计学意义(P<0.05)。见表3。
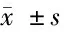
表2 2组远期疗效比较 n=55,月,
注:与对照组比较,*P<0.05
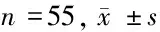

组别CEA(ng/ml)CA125(U/ml)CA153(U/ml)对照组 治疗前18.61±2.60123.77±9.2580.44±7.89 治疗后12.84±1.53∗85.92±6.22∗57.82±5.16∗观察组 治疗前19.23±2.71118.35±8.6977.92±8.10 治疗后5.99±0.74∗#40.14±4.06∗#30.15±3.52∗#
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
2.4 2组血常规比较 2组治疗前Hb、WBC、PLT比较差异无统计学意义(P>0.05)。2组治疗后Hb、WBC、PLT均较治疗前降低(P<0.05),且观察组Hb、WBC、PLT高于对照组(P<0.05)。见表4。
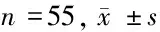
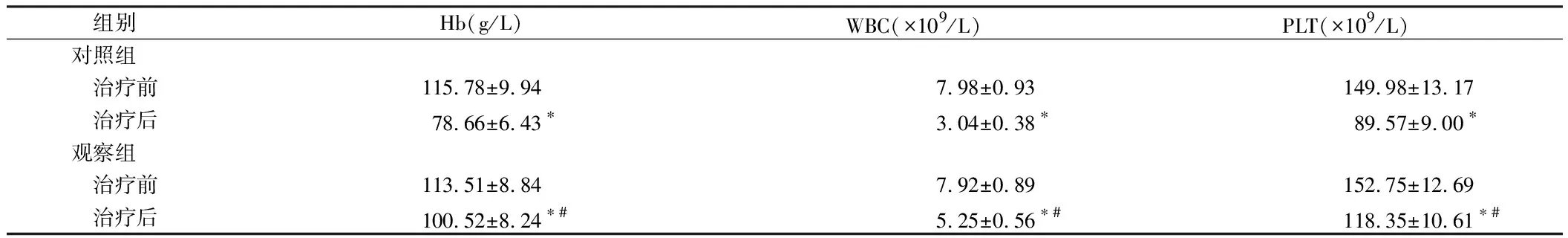
组别Hb(g/L)WBC(×109/L)PLT(×109/L)对照组 治疗前115.78±9.947.98±0.93149.98±13.17 治疗后78.66±6.43∗3.04±0.38∗89.57±9.00∗观察组 治疗前113.51±8.847.92±0.89152.75±12.69 治疗后100.52±8.24∗#5.25±0.56∗#118.35±10.61∗#
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
2.5 2组不良反应发生情况比较 2组患者的不良反应恶心、呕吐、脱发、肾髓抑制和肝肾功能不全的发生情况差异均无统计学意义(P>0.05)。见表5。

表5 2组不良反应发生情况比较 n=55,例(%)
2.6 2组血清雌激素水平比较 2组治疗前血清E1、E2比较差异无统计学意义(P>0.05)。2组治疗后血清E1、E2均较治疗前降低(P<0.05),且观察组E1、E2低于对照组(P<0.05)。见表6。
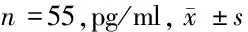
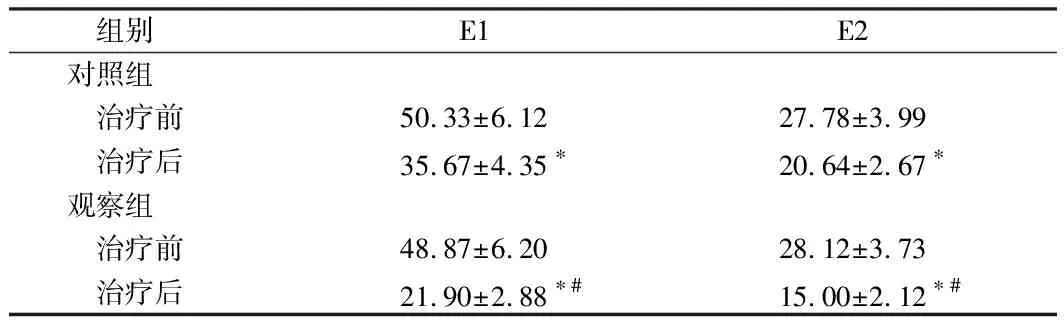
组别E1E2对照组 治疗前50.33±6.1227.78±3.99 治疗后35.67±4.35∗20.64±2.67∗观察组 治疗前48.87±6.2028.12±3.73 治疗后21.90±2.88∗#15.00±2.12∗#
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
2.7 2组复发率和生存率比较 对照组复发率和生存率分别为16.36%(9/55)、58.18%(32/55),观察组复发率和生存率分别为5.45%(3/55)、81.82%(45/55)。观察组复发率低于对照组,生存率高于对照组(P<0.05)。见表7。

表7 2组复发率和生存率比较 n=55,例(%)
注:与对照组比较,*P<0.05
3 讨论
乳腺癌是发生于乳腺导管上皮或乳腺小叶的恶性肿瘤,其主要发病人群是40~50岁女性,尤其是绝经期或更年期女性,患者主要表现为乳房肿块、酒窝征、 橘皮样改变、局域淋巴结肿大等典型症状体征。乳腺癌发病机制复杂,其中遗传、环境污染、不良生活习惯、内分泌和免疫系统紊乱等均是该病发生发展的高危因素。临床资料显示,我国每年新发乳腺癌病例约21万,乳腺癌已经成为我国女性发病率和死亡率最高的恶性肿瘤[7-9]。
乳腺癌早期无特征性临床表现,诊断困难,确诊时癌灶已转移至周围淋巴结或其他组织器官,不适合根治性手术切除治疗,患者病死率较高。对于已进展至Ⅲ~Ⅳ期的晚期乳腺癌患者,化疗仍是其主要治疗手段,尤其是两种化疗药物联合使用能够显著延长患者生存时间,改善患者预后,其中吉西他滨、顺铂组成的GP方案是治疗晚期乳腺癌的一线化疗方案,其治疗有效率可达21%~41%[6]。然而,随着治疗时间的延长,患者对化疗药物耐药性越来越严重。此外,化疗药物在杀伤肿瘤细胞同时也会产生骨髓抑制等不良反应,这是影响患者依从性和治疗效果的主要原因。因此,提高临床疗效的同时降低不良反应是治疗晚期乳腺癌的重要原则。
有研究显示,中医药疗法在恶性肿瘤整体治疗中发挥重要作用[10]。西黄丸是由牛黄、乳香、麝香、没药组成的中药制剂,具有解毒、消肿、散结等功效。基础研究证实,西黄丸通过抑制肿瘤细胞增殖和侵袭转移、诱导肿瘤细胞凋亡、逆转肿瘤EMT进程、调控雌激素合成等机制发挥抗肿瘤作用,与化疗、内分泌等疗法联合治疗晚期乳腺癌能够显著提高患者生存率,改善患者预后[10,11]。本研究结果表明,西黄丸联合GP方案治疗晚期乳腺癌的缓解率、疾病控制率、生存率高于单纯GP方案,复发率低于单纯GP方案,PFS和OS长于单纯GP方案(P<0.05);而不良反应方面,2组比较差异无统计学意义(P>0.05),说明西黄丸联合GP方案治疗晚期乳腺癌能够发挥增效减毒作用,不仅显著提高了治疗效果,且未增加不良反应发生率,安全性高。
肿瘤标志物是肿瘤细胞特异性分泌的一种活性物质,在疾病诊断和预后评估中具有重要价值。CEA作为一种可溶性糖蛋白,是乳腺癌诊断和疗效评估的敏感指标之一[12]。CA125是一种跨膜糖蛋白,在健康人血清中表达量极低,而在乳腺癌患者中阳性检出率高达40%[13]。CA153是由糖、多肽和抗原决定簇组成的糖蛋白,监测其水平可用于判断乳腺癌治疗效果、复发及预后[14]。另外,雌激素水平异常增高是乳腺癌发病的重要因素,E1、E2不仅能够刺激乳腺细胞增生,其代谢产物还具有诱导基因突变、加重DNA损伤等作用,从而造成乳腺癌发生发展[15,16]。本研究结果显示,2组治疗后血清CEA、CA125、CA153、E1、E2均较治疗前降低(P<0.05),且观察组血清CEA、CA125、CA153、E1、E2低于对照组(P<0.05),提示西黄丸联合GP方案治疗晚期乳腺癌能够降低血清肿瘤标志物和雌激素水平,因而减轻雌激素对肿瘤生长的刺激作用。不良反应方面,观察组治疗后Hb、WBC、PLT高于对照组(P<0.05),说明西黄丸能够降低化疗毒副反应发生率,保护肝肾功能,减轻骨髓抑制。
综上所述,西黄丸联合GP方案治疗晚期乳腺癌疗效确切,在提高临床疗效,降低血清肿瘤标志物和雌激素水平方面具有显著优势,且安全性高,不良反应发生率低,值得推广应用。
