昆仙胶囊治疗肾病综合征有效性和安全性的系统评价*
2020-05-28刘亚飞涂胜豪张军军邢国兰
刘亚飞 张 哲 涂胜豪 陈 哲 王 玉 吴 歌 张军军 邢国兰△
1郑州大学第一附属医院肾内科,郑州 450000
2华中科技大学同济医学院附属同济医院中西医结合科,武汉 430030
肾病综合征(nephrotic syndrome,NS)是以大量蛋白尿、低蛋白血症、高脂血症及水肿为特点的一种临床综合征[1-3]。国外报道NS占原发性肾小球疾病的34%~49.5%,国内报道占40%左右[4]。激素及免疫抑制剂被广泛用于NS的治疗[5],虽然部分患者能得到缓解,但是由于激素的毒副作用和易于产生抵抗或依赖性等问题,免疫抑制剂引起抵抗力低下、机会性感染等风险,临床应用受到了一定的限制,所以亟待新型药物出现用于治疗NS。雷公藤作为一种中药免疫抑制剂[6],已用于治疗NS 20余年[7]。昆仙胶囊属于雷公藤制剂,具有抗炎作用和免疫调节功能,已经被用于治疗风湿免疫性疾病[8-9]。动物实验[10]证明昆仙胶囊能减轻阿霉素诱导的NS大鼠尿蛋白排泄量,降低血脂,并对大鼠肾脏病理损伤有一定保护作用。昆仙胶囊治疗NS的疗效及不良反应仍鲜有报道,故本研究对昆仙胶囊治疗NS的随机对照试验进行系统评价,以期为临床应用提供依据。
1 资料和方法
1.1 文献检索
计算机检索以下文献数据库自建库至2019年12月的所有文献:外文数据库为Pub Med数据库,Cochrane Library和Clinical Trials.gov,检索词为“Kunxian capsule”和“nephrotic syndrome”;中文数据库为中国期刊全文数据库(CNKI),万方数字化期刊全文数据库,维普中文科技期刊数据库(VIP),中国生物医学文献数据库(CBM),中国临床试验注册中心,检索词为“昆仙胶囊”和“肾病综合征”。
1.2 文献纳入标准
①研究类型为随机对照临床试验;②研究对象为符合NS诊断标准且无其他并发症的患者,无种族、国籍、性别、年龄限制;③干预措施为对照组采用常规治疗(糖皮质激素、免疫抑制剂及降压、降脂等对症治疗),治疗组采用昆仙胶囊单药或昆仙胶囊联合常规治疗药物;④结局指标为24 h蛋白尿定量、血白蛋白、血肌酐、尿素氮、总胆固醇、甘油三酯、有效率、不良反应等。
1.3 文献排除标准
①无昆仙胶囊干预治疗;②个案报道、综述、回顾性研究;③非RCT试验;④无本研究设定的疗效判定指标;⑤从文献中无法获得相关的可用数据资料。
1.4 文献筛选与数据管理
由2名经过规范化培训的人员检索文献并下载全文后,独立根据上述纳入和排除标准筛选文献。对难以确定是否纳入的文献,通过讨论或由第三方裁决,以确定是否真正符合纳入标准。
1.5 文献质量评价与资料提取
文献质量根据Rev Man 5.3中的偏倚风险评估工具进行评价。评价内容包括:是否正确进行随机分配、是否隐藏分配方案、是否运用完善的盲法、是否有完整结果数据、是否选择性报告结果等。采用预先设计好的表格进行资料提取,包括文献基本信息(标题、作者、发表时间)、NS类型、干预和对照措施、疗程、各项生化指标、有效率、不良反应等。
1.6 统计学分析
采用Rev Man 5.3软件进行数据处理和分析。若各研究的异质性小(P>0.10),采用固定效应模型;反之则采用随机效应模型。Z值计算总的效应量,以P<0.05为差异有统计学意义。有效率、不良反应等计数资料用比值比(odds ratio,OR)分析统计量,计量资料采用均数差(MD)或标准化均数差(SMD)作为治疗效应,各效应值设95%可信区间(CI)。若某研究结局指标的文献≥10篇,采用漏斗图检验发表性偏倚。
2 结果
2.1 检索结果
初步检索34篇相关文献,剔除重复文献18篇,初步排除3篇动物实验,剩余13篇作为全文评估,进一步阅读全文剔除不符合纳入排除标准的文献8篇,最终纳入5篇[11-15]。见图1。
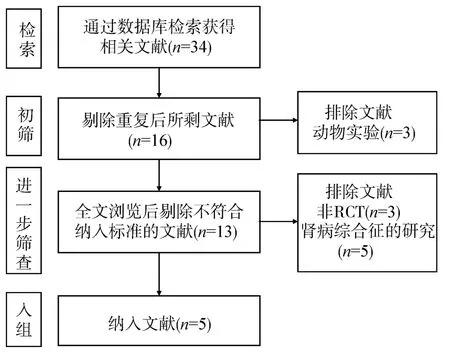
图1 文献筛选流程
2.2 纳入研究的基本信息
共有5篇文献[11-15]纳入研究,总样本量为437例,将治疗组分为2个亚组进行分析。有2项研究[13-14]的试验组用昆仙胶囊替代对照组中一种药物,称为昆仙胶囊替代治疗组(R组)。有3项研究[11,12,15]的试验组在对照组的基础上加用昆仙胶囊,称为昆仙胶囊添加治疗组(A组)。有2项研究[12-13]治疗难治型或激素抵抗型NS,1项研究[15]治疗原发性膜性肾病引起的NS,2项研究[11,14]治疗肾阳亏虚型NS。有3项研究[11,12,15]在对照组基础上加用了昆仙胶囊,1项研究[13]把昆仙胶囊和环磷酰胺进行对比,1项研究[14]以昆仙胶囊治疗为对照组与活血利水方对比。有3项研究[11-13]报道了不良反应。见表1。
2.3 纳入文献的质量评价
纳入的5个研究中均提及随机,均未描述分配隐藏,未提及是否采用盲法,未进行随访,均无样本退出,数据完整。见图2。
2.4 Meta分析结果
2.4.1 24 h蛋白尿
所纳入的5个研究[11-15]都进行了24 h尿蛋白比较,R组的结果显示昆仙胶囊降低尿蛋白效果不及对照组[P=0.02,MD=0.53;95%CI(0.09~0.97)]。A组的异质性检验结果显示各研究间异质性较小(P=0.15),因此采用固定效应模型进行Meta分析,结果显示昆仙胶囊降低蛋白尿效果优于对照组[P<0.000 01,MD=-0.82;95%CI(-0.98~-0.65)]。总体来看,昆仙胶囊降低蛋白尿效果优于对照组[P<0.000 01,MD=-0.65;95%CI(-0.80~-0.49)]。见图3。

表1 纳入文献的基本特征

图2 偏倚风险图
2.4.2 生化指标比较
2.4.2.1 血白蛋白 所纳入的5个研究[11-15]都进行了血白蛋白的比较,R组的异质性检验结果显示各研究间异质性较大(P<0.000 01),因此采用随机效应模型进行Meta分析,结果显示昆仙胶囊提高白蛋白效果与对照组差异无统计学意义[P=0.31,MD=-3.71;95%CI(-10.84~3.42)]。A组的异质性检验结果显示各研究间异质性较大(P<0.000 01),因此采用随机效应模型进行Meta分析,结果显示昆仙胶囊升高血白蛋白效果与对照组差异无统计学意义[P=0.05,MD=3.98;95%CI(0.08~7.87)]。总体来看,结果显示昆仙胶囊升高血白蛋白效果与对照组差异无统计学意义[P=0.79,MD=0.83;95%CI(-5.21~6.86)]。见图4。

图3 24 h蛋白尿的Meta分析森林图
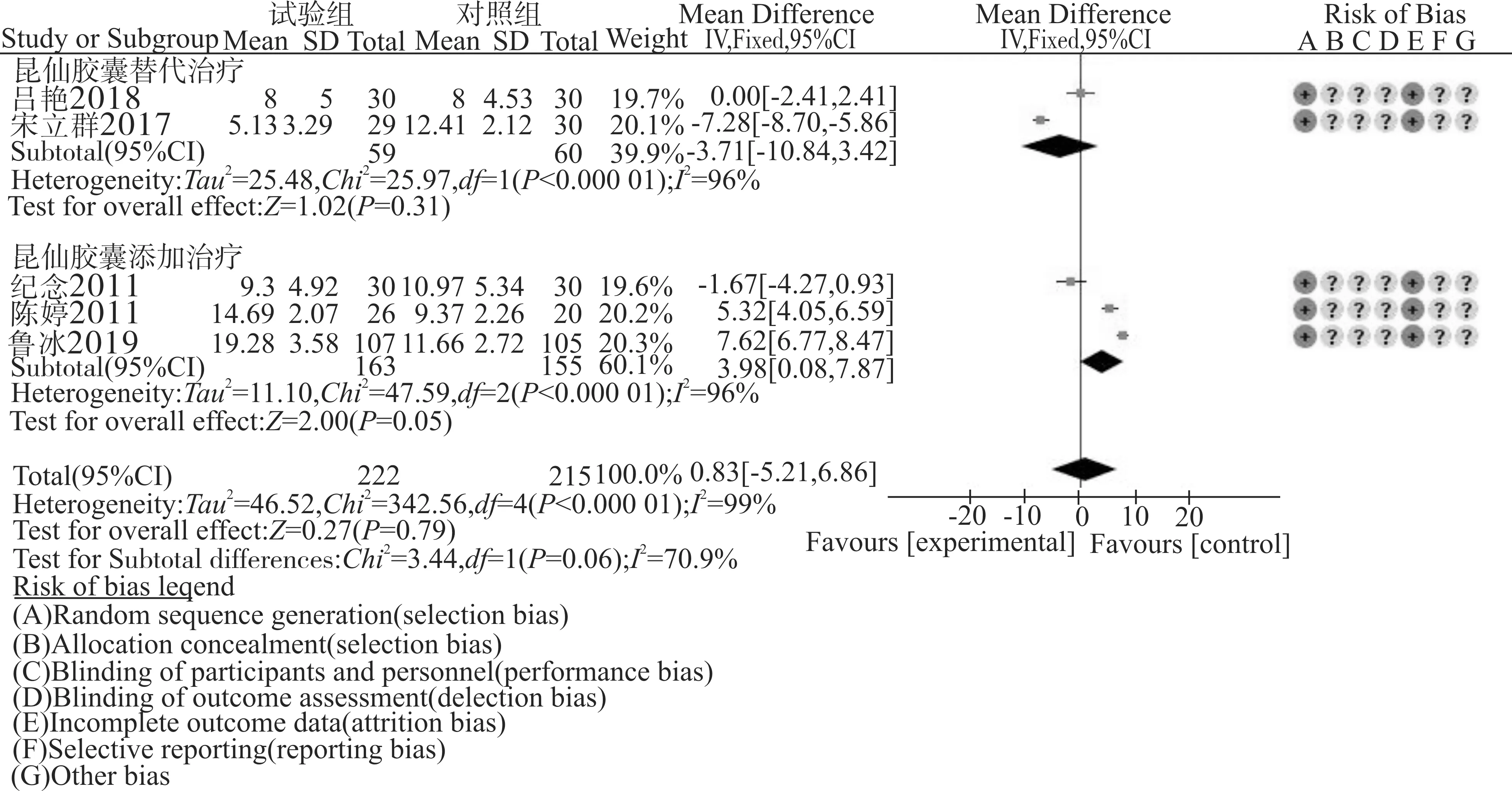
图4 血白蛋白的Meta分析森林图
2.4.2.2 血肌酐 所纳入的5个研究有3项[12,13,15]进行了肌酐的比较,R组只有1项研究[13]进行比较,结果显示昆仙胶囊降肌酐效果与对照组差异无统计学意义[P=1.00,MD=0.00;95%CI(-11.92~11.92)]。A组的异质性检验结果显示各研究间异质性较小(P=0.77),因此采用固定效应模型进行Meta分析,结果显示昆仙胶囊降肌酐效果优于对照组[P<0.000 01,MD=-9.57;95%CI(-13.12~-6.01)]。总的来看昆仙胶囊降血肌酐效果强于对照组[P<0.000 01,MD=-8.78;95%CI(-12.19~-5.37)]。见图5。
2.4.2.3 尿素氮 所纳入的5个研究有2项[12,13]进行了尿素氮的比较,R组有1项研究[13]进行比较,结果显示昆仙胶囊降低尿素氮效果与对照组差异无统计学意义[P=1.00,MD=0.00;95%CI(-0.85~0.85)]。A组有1项研究[12]进行比较,结果显示昆仙胶囊降低尿素氮效果与对照组差异无统计学意义[P=0.25,MD=-0.41;95%CI(-1.11~0.29)]。总的来看昆仙胶囊降低尿素氮效果与对照组差异无统计学意义[P=0.37,MD=-0.24;95%CI(-0.78~0.29)]。见图6。

图5 血肌酐的Meta分析森林图

图6 血尿素氮的Meta分析森林图
2.4.2.4 胆固醇 所纳入的5个研究有3项[11,13,14]进行了胆固醇的比较,R组的异质性检验结果显示各研究间异质性较大(P=0.02),因此采用随机效应模型进行Meta分析,结果显示昆仙胶囊降胆固醇效果与对照组差异无统计学意义[P=0.51,MD=0.84;95%CI(-1.67~3.34)]。A组有1项研究[11]进行比较,结果显示昆仙胶囊降低胆固醇效果强于对照组[P=0.003,MD=-1.40;95%CI(-2.32~-0.48)]。总的来看昆仙胶囊降胆固醇效果与对照组差异无统计学意义[P=0.97,MD=-0.04;95%CI(-1.65~1.58)]。见图7。
2.4.2.5 甘油三酯 所纳入的5个研究有3项[11,13,14]进行了甘油三酯的比较,R组的异质性检验结果显示各研究间异质性较小(P=0.15),因此采用固定效应模型进行Meta分析,结果显示昆仙胶囊降甘油三酯效果与对照组差异无统计学意义[P=0.32,MD=0.21;95%CI(-0.21~0.63)]。A组有1项研究[11]进行比较,结果显示昆仙胶囊降低甘油三酯效果强于对照组[P=0.03,MD=-0.97;95%CI(-1.83~-0.11)]。总的来看昆仙胶囊降甘油三酯效果与对照组差异无统计学意义[P=0.94,MD=-0.01;95%CI(-0.39~0.36)]。见图8。

图7 胆固醇的Meta分析森林图

图8 甘油三酯的Meta分析森林图
2.4.3 有效率 所纳入的5个研究[11-15]都进行了有效率比较,R组的异质性检验结果显示各研究间异质性较小(P=0.79),因此采用固定效应模型进行Meta分析,结果显示昆仙胶囊治疗NS的有效率与对照组差异无统计学意义[P=0.6,OR=0.77;95%CI(0.29~2.07)]。A组的异质性检验结果显示各研究间异质性较小(P=0.62),因此采用固定效应模型进行Meta分析,结果显示昆仙胶囊治疗NS的有效率优于对照组[P<0.000 01,OR=4.80;95%CI(2.76~8.36)]。总体来看昆仙胶囊治疗NS的有效率优于对照组[P<0.000 01,OR=3.09;95%CI(1.95~4.91)]。见图9。
2.4.4 不良反应比较 所纳入的5个研究有3项[11-13]进行了不良反应的比较。R组有1项研究[13]进行比较,结果显示对照组与试验组的不良反应差异无统计学意义[P=0.45,OR=0.56;95%CI(0.12~2.57)]。A组异质性检验结果显示各研究间异质性较小(P=0.36),因此采用固定效应模型进行Meta分析,结果显示对照组不良反应与试验组差异无统计学意义[P=0.85,OR=0.91;95%CI(0.34~2.42)]。总的来看对照组与试验组不良反应差异无统计学意义[P=0.56,OR=0.78;95%CI(0.34~2.42)]。见图10。
3 讨论
昆仙胶囊由昆明山海棠、淫羊藿、枸杞子和菟丝子组方而成,以昆明山海棠祛风除湿为君药[16],淫羊藿祛风湿、补肾强精为臣药[17],菟丝子、枸杞子为佐,与淫羊藿共同发挥补肾养血,强精健骨之功效[18,19]。经过以上各药物间的组方配伍,具有补肾通络、祛风除湿的作用,达到增效减毒的效果。昆仙胶囊可以通过抑制T细胞增殖、细胞因子表达及抑制免疫复合物形成等机体免疫反应的多个环节发挥免疫抑制作用[20],故我们探讨昆仙胶囊治疗NS的疗效及安全性。据我们所知,这是第一篇研究昆仙胶囊治疗NS疗效和安全性的系统性评价。
通过本研究分析,常规治疗方案加用昆仙胶囊有助于蛋白尿缓解。已有研究[21]通过动物实验超微结构发现昆仙胶囊可以减少肾小球上皮下电子致密物沉积,降低基底膜厚度,修复足细胞形态学损伤,此作用与激素作用相当。昆仙胶囊可能通过对足细胞的保护,从而减少蛋白尿[22]。
同时本研究发现昆仙胶囊加用常规治疗方案还可以降低肌酐,保护肾功能,考虑与昆仙胶囊降低蛋白尿、减轻肾脏负荷有关,但所有研究均未对肾小球滤过率进行评估。也有研究[23]证实昆仙胶囊通过抑制TGF-β1表达,达到抑制系膜细胞增生及细胞外基质(ECM)堆积的作用,从而达到治疗效果,其作用途径可能是通过Smad信号途径,下调靶蛋白(如ECM)的表达,从而减轻ECM聚积,延缓肾小球硬化的发生,改善肾功能。

图9 有效率的Meta分析森林图
在白蛋白、尿素氮、胆固醇、甘油三酯结局指标方面,有研究[24]表明昆明山海棠通过祛风除湿通络,有改善肾脏血液循环、增加肾脏血流量、减少尿蛋白的作用,从而达到改善低蛋白血症和调节血脂的作用。部分研究也发现昆仙胶囊可以升高血白蛋白,降低血脂,但本项Meta分析提示差异不具统计学意义。考虑原因可能如下:①纳入研究数目太少;②对照组中降压药、降脂药的效果,导致试验组与对照组差异较小;③各研究之间存在较大异质性;④蛋白尿减少后,血白蛋白及血脂的改善需要一定的时间[25]。
本研究分析发现昆仙胶囊的应用可以提高NS治疗的有效率,但各研究评价临床疗效的标准不尽相同。有2项研究[12,13]根据1992年全国原发性肾小球疾病分型与治疗诊断标准专题座谈会纪要关于原发性NS的疗效标准[26],有2项研究[11,14]根据2003年的肾脏病诊断与治疗及疗效标准专题讨论纪要[27]的疗效标准。有1项研究[15]根据临床症状、白蛋白水平、24 h尿蛋白定量水平及肾功能检查结果判定其临床疗效。故昆仙胶囊对有效率的影响还有待进一步评估。
在不良反应方面,治疗组与对照组并没有显著性差异,提示昆仙胶囊并不能减少副作用,也可能与纳入研究样本量小有关。也有研究表明[28]昆仙胶囊通过加入补肾益精的中药拮抗雷公藤的肝、肾、生殖毒性,发挥增效减毒的作用。尽管昆仙胶囊加入了补肾益精类的中药仍不能显著减少昆明山海棠的生殖毒性,但对大部分患者来说,短期服用昆仙胶囊无论是对肝功能、肾功能及肾小管功能均无明显影响,极少数的肝功能显著改变的患者在停药半年并加用护肝类中药后肝功能逐渐恢复正常[29]。对于育龄期青中年患者,若有生育要求,则应避免使用昆仙胶囊[30]。
本研究存在一定的局限性:①纳入研究数较少,且纳入研究的5篇文献[11-15]质量均不高;②因NS类型多样,对照组之间存在差异。有原发性膜性肾病、狼疮肾炎伴NS、肾阳亏虚型原发性NS、难治性NS等;③因对照组不同,各研究治疗方案、疗程也不同,缺少昆仙胶囊单药治疗NS的研究,本研究为了便于分析,将利尿消肿、抗凝、补钙、降脂等治疗归为常规对症治疗,在一定程度上也导致了临床异质性;④实验组用药不同,有的是用昆仙胶囊替代对照组中一种药物,有的是对照组基础上加用昆仙胶囊;⑤各研究评价有效率的标准不同;⑥缺少其他国家的研究。这些因素可能在一定程度上影响临床结果,从而使Meta分析的强度和结论的外推性受到影响。
综上所述,目前有限的证据表明昆仙胶囊辅助常规疗法治疗NS可以提高临床疗效;使用昆仙胶囊替代常规药物治疗NS,暂时无法证明可获得更明显收益;治疗过程可能会出现以生殖系统、消化系统为主的不良反应。昆仙胶囊在今后NS的治疗中具有较为广泛的应用前景,但本次研究存在一定的局限性,仍需要更多高质量多中心的随机对照临床试验进一步加以验证。

图10 不良反应的Meta分析森林图
