CHB 感染者经替诺福韦联合胸腺肽治疗后miR-122 和miR-21表达的研究
2020-05-25梁爽张宝李世龙吴丹牛蕊邸宝春王辉
梁爽,张宝*,李世龙,吴丹,牛蕊,邸宝春,王辉
(1.唐山市传染病医院,河北 唐山;2.唐 山 市人民 医 院检验科,河北 唐山)
0 引言
慢性乙肝是由乙型肝炎病毒(hepatitis B virus,HBV)感染引起的一种严重危害人体健康的传染病,其临床特点为病程长、反复发作,并可进一步发展为肝纤维化、肝硬化,甚至肝癌(HCC)。据资料统计,我国慢性HBV 感染者约9000 万例,其中CHB 患者约2800 万例[1]。目前,最主要的方法是抗病毒治疗,但无论是干扰素或是核苷(酸)类似物的治疗,只能抑制HBV-DNA 复制,不能彻底根治CHB,疗效有限[2]。本研究的目的是通过替诺福韦联合胸腺肽治疗慢性乙型肝炎,观察临床疗效。
1 资料与方法
1.1 一般资料
将2017 年10 月至2019 年3 月于我院收治且符合以下纳入和排除标准的96 例CHB 患者,采用随机数表法分为对照组和观察组,每组48 例。对照组患者中男性25 例,女性23 例,年龄19~60 岁,平均(39.45±8.51)岁,病程2~26 年,平均(11.3±2.2)年。观察组患者中男性28 例,女性20 例;年龄21~58 岁,平均(38.81±7.91)岁,病程3~18 年,平均(6.12±5.51)年。两组患者的一般资料比较差异均无统计学意义(P>0.05),具有可比性。
1.2 诊断标准
符合《慢性乙型肝炎防治指南(2015 年更新版)》[3]诊断标准进行诊断。
1.3 纳入与排除标准
①纳入标准:所有入选者均为已确定诊断的CHB 患者;血清HBsAg、HBeAg 均阳性,HBV-DNA 大于106至107copies/mL;未服用抗病毒类药物及免疫调节的时间大于6 个月;经过医院伦理委员会批准,自愿签署知情同意书,加入本治疗方案。②排除标准:重叠其他肝炎病毒感染及肝硬化、肝癌者;合并恶性肿瘤者;严重的心脑血管疾病、严重精神障碍患者及糖尿病、酗酒、肾功能障碍者;妊娠期及哺乳期妇女。
1.4 治疗方法
两组患者均给予常规保肝及对症治疗。在此基础上,观察组患者给予替诺福韦 (TDF)(生产厂家:葛兰素史克;进口注册证号H20130589),口服,每天1 片,每次300mg,空腹服用,同时给予胸腺肽肠溶片(生产厂家:黑龙江喜人药业集团有限公司;国药准字H20063310)口服,每天3 次,每次10mg。对照组患者给予替诺福韦口服,每天1 片,每次300mg,空腹服用。
1.5 观察指标
①采用全自动分析仪(7080 型,日立HITACHI 公司),试剂由宁波美康生物科技有限公司提供,检测肝功能指标:血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、谷氨酰转移酶(GGT)、总胆红素(TBil);②HBV 标记物:HBeAg 采用酶联免疫吸附法检测,HBV-DNA 定量采用荧光定量PCR 法检测,采用ABI PRISM7300RT-PCR 检 测 仪(美 国)进 行 定 量 检 测(试 剂:中山大学达安基因股份有限公司);③T 淋巴细胞亚群检测:采用流式细胞仪(艾森生物有限公司)检测患者外周血CD45+、CD45+CD3+、CD3+CD4+、CD3+CD8+等细胞绝对计数和CD3+CD4+/CD3+CD8+比值;④血清miR-122、miR-21 检测:PCR 热循环仪为德国Eppendorf 公司、实时荧光定量测定PCR 仪为美国Applied Biosystems 公司,特异性茎环逆转录引物由生工生物工程(上海)有限公司提供,RNA 提取试剂盒及荧光定量PCR 检测试剂盒购自宝生物工程(大连)有限公司。用RT-PCR 法检测血清miR-122、miR-21 的表达,采用U6 作为内参照PCR 的相对测定方法,均以2-△△Ct法计算miR-122、miR-21 相对表达量,ΔΔCt =待测样本的ΔCt-对照样本ΔCt,ΔCt =目的基因Ct 值-内参基因Ct 值。Ct 值为每个反应管内的荧光信号到达设定的阈值时所经历的循环数。
1.6 统计学方法
应用Graphpad Prism8.0 统计软件进行数据分析和绘制图形,计量资料用均值±标准差表示,采用t 检验,计数资料率的比较采用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗后肝功能指标变化情况
观察组治疗后ALT、AST、GGT、TBil 较对照组明显改善,差异有统计学意义(P 均<0.05);观察组治疗后HBeAg 阴转率和HBVDNA 应答率明显高于对照组,差异有统计学意义(P 均<0.05)。详见表1。
表1 观察组和对照组CHB 感染者治疗后肝功能和免疫学指标情况(n=48,

表1 观察组和对照组CHB 感染者治疗后肝功能和免疫学指标情况(n=48,
组别 ALT(U/L) AST(U/L) GGT(U/L) TBiL(umol/L) HBeAg 转阴率(%) HBV-DNA 转阴率(%)观察组 34.8±22.4 43.5±18.6 68.5±31.3 27.3±13.2 20(41.67) 39(81.25)对照组 51.9±21.7 60.3±23.1 89.3±43.6 46.8±19.2 11(22.92) 25(52.08)t 值/χ2 值 3.7987 3.9246 2.6850 5.7983 3.8589 9.1876 P 值 0.0003 0.0002 0.0086 0.0000 0.0495 0.0024
2.2 两组患者治疗后免疫功能指标变化情况
观察组治疗后CD45+,CD45+CD3+,CD3+CD4+,CD3+CD8+细胞绝对计数明显较对照组改善,差异有统计学意义(t=4.2443,P=0.0 0 0 1;t=7.3 1 4 8,P=0.0 0 0 0;t=3.6 2 2 2,P=0.0 0 0 5;t=3.4420,P=0.0009,P 均<0.05),观 察 组 治 疗 后CD3+CD4+/CD3+CD8+(1.83±1.05)较对照组(1.21±0.95)升高,差异有统计学意义(t=3.0336,P=0.0031<0.05),详见图1。

图1 观察组与对照组治疗后的T 细胞亚群绝对计数分布
2.3 两组患者治疗后血清中miR-122、miR-21 表达水平的变化情况
观察组治疗后,血清中miR-122、miR-21 表达水平较对照组明显下降,两组间差异有统计学意义(t=2.3878,P=0.0189; t=2.9198,P=0.0044。P 均<0.05),详见图2。
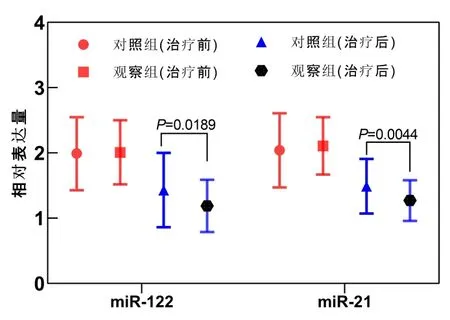
图2 观察组与对照组治疗前后的miR-122、miR-21 表达情况
3 讨论
慢性乙型肝炎是我国临床上常见的、高发的传染病,目前研究认为其发病机制主要是持续复制的高病毒载量和免疫介导的非特异性免疫应答损伤[4-5]及特异性T 淋巴细胞功能耗竭、凋亡[6]所致的肝细胞损伤及炎症发生。因此,在抑制CHB 复制的同时调节免疫是较理想的治疗方法。替诺福韦为一种单磷酸腺苷类似物,经水解、磷酸化产生替诺福韦二磷酸,参与病毒DNA 整合,阻碍病毒DNA 延长,从而抑制HBV 复制[7]。据研究资料显示,替诺福韦能快速、有效控制乙肝病毒,无论是在HBV-DNA 的阴转、HBeAg转换方面,还是在安全性、耐药性方面均优于其它核苷(酸)类似药物,并且还能有效延缓肝硬化进展及降低肝癌的发生率,改善病情,提高生活质量,为慢性乙型肝炎的首选药物[8-9]。胸腺肽能调节免疫,促进T 淋巴细胞成熟,诱导T 淋巴细胞亚群发育和成熟,增强巨噬细胞吞噬能力,提高白介素n 产生水平与受体表达水平,增加CD4+、CD8+T 淋巴细胞数量[10-11],从而调节和增强机体的细胞免疫功能,增强机体抵抗力,二者联合应用治疗CHB 患者可提高疗效。本研究对96 例CHB 患者在替诺福韦治疗基础上给予胸腺肽治疗,并以单独采用替诺福韦治疗进行对照,结果显示:治疗后观察组肝功能指标(ALT、AST、GGT、Tbil)、BeAg阴转率、HBV-DNA 水平及免疫功能指标(CD45+、CD45+CD3+、CD3+CD4+、CD3+CD8+、CD3+CD4+/CD3+CD8+)与对照组比较显著改善(P<0.05)。表明替诺福韦联合胸腺肽治疗能提高CHB 患者的临床效果。
miRNA 是一类内源性长度由20~25 个核苷酸组成的非编码单链小分子RNA,能够调节mRNA 的表达[12]。在慢性HBV 感染者中,miR-122、miR-21 血清含量的表达,可作为肝组织损伤的标志物,具有良好的敏感性和特异性[13-14]。并有研究发现,miR-122、miR-21 高表达及其表达水平与肝硬化及HCC 患者的临床分期、分化程度密切相关[15]。这说明miR-122、miR-21 的表达在乙肝病毒的复制、肝细胞的损伤和疾病的进展中可能起着重要作用。研究结果显示治疗后, 观察组miR-122、miR-21 的表达水平显著下降 ,与治疗前和对照组均有统计学差异 (P<0.05)。提示替诺福韦联合胸腺肽治疗可以降低CHB 患者血清中miR-122、miR-21的表达水平,从而减轻肝脏的炎症损伤,降低肝癌的发生率,并有助于疾病进展的评估与风险预测。
综上所述,替诺福韦联合胸腺肽治疗CHB 患者能有效促进肝功能恢复,抑制HBV-DNA 复制,提高HBeAg 阴转率,增强机体免疫力,降低血清中miR-122、miR-21 的表达水平,改善肝脏炎症损伤及降低肝癌的发生率,尤其是在以HBV 基因型C 基因型为主的唐山地区[16]具有积极的临床意义。
