锰渣硫酸浸出正交实验探究①
2020-05-24练强,张杰
练 强, 张 杰
(1.四川省安全科学技术研究院,四川 成都610045; 2.贵州大学 矿业学院,贵州 贵阳550003)
锰矿经酸浸电解湿法冶金工艺提炼金属锰后产生大量锰渣固体废弃物,锰渣的大量堆放不仅占用大片土地,而且还污染周边环境,破坏生态平衡[1-3]。 锰渣既是破坏环境的物质,同时又是一种可提炼并循环利用的珍贵资源[4]。
目前生产MnSO4溶液多采用加热升温的浸出方法[5],而加热需要消耗大量的能源。 本文在常温下直接向锰渣浆体中加入少量浓硫酸,利用浓硫酸水化放热效应促使反应进行,并通过正交实验,探索锰渣酸浸的工艺条件。
1 原料性质及实验药剂
实验原料为贵州省遵义地区某电解锰公司产生的湿法冶炼锰渣,因长期堆放,湿度较大,呈土块状,烘干后破碎,磨细至0.18 mm 备用,其化学组成(以氧化物计)见表1。

表1 锰渣化学成分(质量分数)/%
浸出剂使用工业级浓硫酸。
2 实验及结果分析
2.1 单因素实验
2.1.1 硫酸用量实验
取30 g 锰渣3 份,在液固比5 ∶1及不搅拌条件下,分别按锰渣(g)与硫酸(mL)比为10 ∶3、10 ∶4、10 ∶5,将浓硫酸加入锰渣浆体中反应2 h,考察硫酸用量对锰浸出率的影响,结果见图1。 结果表明,随着浓硫酸用量增加,锰浸出率增加,但增加到一定程度后增幅变缓。

图1 硫酸用量对锰浸出率的影响
2.1.2 反应时间实验
浓硫酸用量0.4 mL/g,其他条件不变,考察了反应时间对锰浸出率的影响,结果见图2。 结果表明,酸浸反应1~2 h 区间,锰浸出率变化较大,2~4 h 区间锰浸出率变化缓慢。

图2 反应时间对锰浸出率的影响
2.1.3 液固比实验
反应时间2 h,其他条件不变,液固比对锰浸出率的影响见图3。 结果表明,液固比为3 ∶1时锰浸出率最高。 液固比较小时,酸浸反应体系体积也小,加入浓硫酸时产生大量的热,这些热足以使有限的溶液沸腾或接近沸腾,为加快锰与H2SO4反应提供了热动力保证,强化浸出,这也是无外加热下浓硫酸浸出锰的关键所在[6-7]。
2.1.4 搅拌速度实验
液固比3 ∶1,其他条件不变,搅拌速度对锰浸出率的影响见图4。 结果表明,搅拌速度在50 ~100 r/min范围内变化对锰浸出影响不大,以100 ~150 r/min 为宜。 搅拌速度过快,易引起物料冒槽,使操作不易控制,而搅拌速度过小又不利于传质,影响锰浸出率。

图3 液固比对锰浸出率的影响

图4 搅拌速度对锰浸出率的影响
2.2 正交实验
为进一步确定各因素对锰浸出的影响大小关系,在单因素实验基础上,设计L9(34)正交实验,以确定锰的最佳浸出工艺条件。 正交实验结果见表2。 由表2 可知,各因素对锰浸出率产生的影响大小顺序为:硫酸用量>液固比>搅拌速度>反应时间,锰的最佳浸出条件为A3B2C2D3,即浓硫酸用量0.5 mL/g,反应时间2 h,液固比3 ∶1,搅拌速度150 r/min。
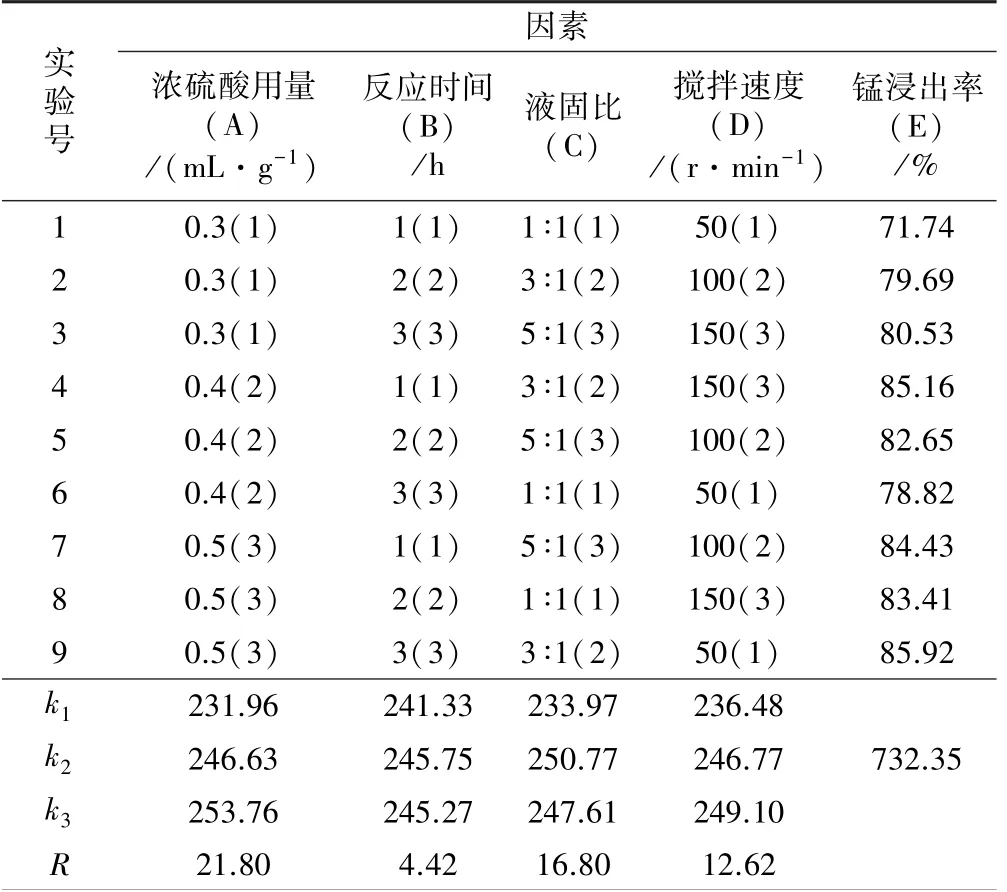
表2 L9(34)正交实验结果表
2.3 对比优化实验
正交实验锰的最佳浸出条件为A3B2C2D3,但在正交实验中该组合并未出现,故再进行了优化对比实验,并选定条件A2B1C2D3和A3B3C2D1进行对比,结果见表3。

表3 优化对比实验结果
从表3 可以看出,A3B2C2D3中锰浸出率最高,为最优实验条件,即在浓硫酸用量0.5 mL/g、液固比3 ∶1、反应时间2 h、搅拌速度150 r/min 条件下,锰浸出率可达到86.53%。
3 结 语
1) 以电解锰渣为原料,浓硫酸作浸出剂,利用浓硫酸水化放热效应,促使锰与H2SO4反应,实现自热浸出锰。
2) 探索了锰渣浸出工艺条件,结果表明,各因素对锰浸出率影响的大小顺序为:硫酸用量>液固比>搅拌速度>反应时间。 在浓硫酸用量0.5 mL/g、液固比3 ∶1、反应时间2 h、搅拌速度150 r/min 条件下,锰浸出率可达到86.53%。
3) 锰渣酸浸后锰、铁均进入浸出液中,由于实验条件所限未能开展锰、铁分离实验,建议下一步实验中可以开展相关方面的实验研究。
4) 通过酸浸降低了锰渣中锰、铁含量,可用于制备陶瓷墙地砖、工艺陶瓷等材料,对锰渣二次资源回收利用、改善生态环境具有积极的意义。
