高效液相色谱法分析植物油中9种抗氧化剂
2020-05-22赵慧男张艳侠郑文静祝建华刘艳明
赵慧男, 张艳侠, 薛 霞, 戴 琨, 郑文静, 马 骋, 祝建华, 刘艳明*, 张 峰
(1. 山东省食品药品检验研究院, 山东 济南 250101; 2. 中国检验检疫科学研究院, 北京 100176)
食品中的抗氧化剂是能够防止或延缓食品氧化性和延长储存期的食品添加剂,主要用于防止油脂和富脂食品的氧化酸败,以及由氧化所导致的褪色、褐变、维生素破坏等,分为天然和人工合成两大类。人工合成抗氧化剂因价格低廉、性质稳定而被广泛使用,较常用的人工合成抗氧化剂有叔丁基对羟基茴香醚(BHA)、2,6-二叔丁基对甲酚(BHT)、特丁基对苯二酚(TBHQ)、2,4,5-三羟基苯丁酮(THBP)、2,6-二叔丁基-4-羟甲基苯酚(Ionox-100)、没食子酸丙酯(PG)、没食子酸辛酯(OG)、没食子酸十二酯(DG)、正二氢愈创木酸(NDGA)等,此类化合物为苯酚类抗氧化剂[1-3]。研究表明,高剂量使用此类人工合成抗氧化剂会造成细胞凋亡、DNA裂解等潜在健康危害,其具有一定的毒性和致癌作用[4,5]。因此,美国、日本、欧盟等国家和地区已禁止使用一些合成抗氧化剂。植物油是日常生活中必不可少的食品,我国食品安全国家标准GB 2760-2014《食品安全国家标准 食品添加剂使用标准》对PG、BHA、BHT、TBHQ等抗氧化剂在油脂中的最大使用量也做出了严格规定[6],规定BHA、BHT和TBHQ的最大使用限量为0.2 g/kg, PG的最大使用限量为0.1 g/kg,对THBP、OG、DG、NDGA、Ionox-100等其他抗氧化剂暂无规定。
目前针对BHA、TBHQ、PG等抗氧化剂的检测方法主要有薄层色谱法[7]、比色法[7]、气相色谱法(GC)[7,8]、气相色谱-串联质谱法(GC-MS)[9,10]、高效液相色谱法(HPLC)[11-13]和液相色谱-串联质谱法(HPLC-MS)[14]。其中,薄层色谱法和比色法在定量方面存在缺陷。气相色谱法和气相色谱-串联质谱法常受到化合物极性、沸点等限制,且前处理方法相对复杂、耗时长。液相色谱-串联质谱法易受基质效应影响,定量存在局限性,且液相色谱-串联质谱仪器昂贵,设备普及率低,限制了此方法的应用。高效液相色谱法具有普及率高、定量准确、兼容性好等特点,现行国家标准《食品安全国家标准 食品中9种抗氧化剂的测定》[15]包含高效液相色谱法、液相色谱-串联质谱法、气相色谱法以及气相色谱-质谱法和比色法,其中仅高效液相色谱法适用于PG、THBP、TBHQ等9种目标抗氧化剂的同时检测。国标方法前处理采用正己烷溶解样品,再用乙腈进行萃取,C18固相萃取柱净化,整个过程繁琐,耗时较长。实验发现,该方法回收率较低,且实验过程中未加入保护剂,可能导致部分目标物损失,影响实验结果的准确性。
针对抗氧化剂检测过程中存在的问题,本文对目标物稳定性进行考察,确定标准储备溶液的储存条件,通过添加抗坏血酸棕榈酸酯(AP)的方式,提高目标物稳定性和回收率;对提取溶剂、除脂方式以及净化方式等进行讨论,最终建立了一种快速、简便、准确的高效液相色谱测定食用油中9种常用人工合成抗氧化剂的方法。
1 实验部分
1.1 仪器、试剂与材料
Thermo Ultimate 3000高效液相色谱仪(美国Thermo Fisher Scientific公司); AB204-S型电子天平(瑞士Mettler Toledo公司); SB-800DTD型超声波清洗器(中国宁波新芝生物科技股份有限公司); 3-18K型冷冻离心机(德国Sigma公司); Milli-Q纯水系统(美国Millipore公司); MS3涡旋混合器(德国IKA公司)。
TBHQ、THBP、BHT、BHA、OG、NDGA、Ionox-100、DG均购自北京曼哈格生物科技有限公司,纯度≥98% , PG购自德国Dr. Ehrenstorfer公司,纯度≥95% 。甲醇、乙腈(HPLC级)购自德国Merck公司,纯度>99.9% ; AP购自日本TCI公司,纯度>97% 。实验所用花生油、玉米油、大豆油等植物油样品均为市售。
1.2 实验条件
1.2.1 标准溶液的配制
称取9种抗氧化剂标准物质各10 mg(精确至0.1 mg),用甲醇溶解并定容至10 mL,分别配制成标准储备液(1 mg/mL),置于棕色玻璃小瓶中,于-18 ℃冷冻保存。移取各标准储备液,用甲醇(含50 μg/mL AP)稀释至适当浓度,得到抗氧化剂混合标准工作液,于-18 ℃冷冻保存。
1.2.2 样品前处理
称取2 g样品(准确至0.001 g),置于50 mL离心管中,加入10 mL甲醇,涡旋振荡2 min,超声提取20 min,以 8 000 r/min 离心5 min;用5 mL甲醇重复提取一次,合并上清液,于-18 ℃冷冻2 h除脂,用0.22 μm微孔滤膜过滤,待测。
1.2.3 色谱条件
色谱柱:Waters®XBridge色谱柱(250 mm×4.6 mm, 5 μm);柱温:35 ℃;流动相:(A)甲醇和(B)0.1%(v/v)甲酸水溶液;流速:1.0 mL/min。梯度洗脱条件:0~5 min, 50%A; 5~15 min, 50%A~80%A; 15~20 min, 80%A; 20~25 min, 80%A~90%A; 25~27 min, 90%A~50%A; 27~30 min, 50%A。进样体积:5 μL;检测波长:280 nm。
2 结果与讨论
2.1 抗氧化剂储存条件的优化
在抗氧化剂检测过程中,发现9种抗氧化剂混合标准储备液于4 ℃冷藏储存后,THBP和TBHQ响应面积迅速降低,导致定量不准,严重影响实验结果。同时,这种现象也可能会导致实验前处理过程中THBP和TBHQ两种物质回收率失真,实验结果准确度降低。因此,本文研究了抗氧化剂储存温度,并通过在标准物质配制和前处理过程中添加其他抗氧化剂的方式增加目标抗氧化剂稳定性,保证实验结果准确可靠。
2.1.1 温度对抗氧化剂的影响
用甲醇配制10 μg/mL 混合标准溶液,分别设置常温、4 ℃和-18 ℃ 3种储存温度,连续测定144 h。结果显示:PG、NDGA、BHA、Ionox-100、OG、BHT、DG等响应强度在不同温度下,不随时间发生明显变化,稳定性较好。而THBP和TBHQ两种物质的响应强度在常温和4 ℃冷藏两种储存温度下均发生不同程度的降低,-18 ℃冷冻时溶液中各成分含量稳定,未发生明显变化,其峰面积占0 h时峰面积的百分比如图1所示,因此建议标准溶液于-18 ℃冷冻储存。

图 1 不同储藏条件下THBP和TBHQ的含量变化Fig. 1 Changes of contents of THBP and TBHQ under different storage conditionsTHBP: 2′,4′,5′-trihydroxybutyrophenone; TBHQ: tert-butylhydroquinone.
2.1.2 AP对抗氧化剂的影响
9种目标物均为合成酚类抗氧化剂,其抗氧化机理为吸收氧化产生的自由基,阻断自由基链锁反应,将油脂被氧化产生的自由基转变为稳定的产物,消除脂类氧化的自由基反应[16]。AP是一种脂溶性营养性抗氧化剂,其在消除机体自由基的同时,还能在金属离子Ca2+、Fe3+等存在下,与O2反应最终生成脱氢抗坏血酸,从而消除O2或H2O2对机体的氧化损害作用,可推测AP抗氧化能力比目标物强。有文献[17]报道AP在猪油中抗氧化能力优于TBHQ,因此尝试在配制溶液和提取溶液中加入AP,以改善标准物质储存和前处理过程中THBP和TBHQ的不稳定。

图 2 甲醇溶剂中AP的质量浓度对THBP和TBHQ响应强度的影响Fig. 2 Effect of mass concentrations of AP in methanol on the responses of the THBP and TBHQAP: ascorbyl palmitate.

图 3 加入AP后9种抗氧化剂响应强度的变化Fig. 3 Changes of intensities of the nine antioxidants after adding APPG: propyl gallate; NDGA: nordihydroguaiaretic acid; BHA: butylated hydroxyanisole; Ionox-100: 2,6-di-tert-butylphenol; OG: octyl gallate; BHT: butylated hydroxy toluene; DG: dodecyl gallate.
用含不同浓度AP的甲醇溶液配制9种抗氧化剂的混合标准溶液,常温避光储存,测定目标抗氧化剂的稳定性。结果显示:AP质量浓度超过5 μg/mL 时,8 h内9种抗氧化剂含量基本稳定,8 h后THBP和TBHQ两种成分含量快速下降;当AP浓度不低于50 μg/mL 时,144 h内THBP和TBHQ含量稳定,其占0 h时峰面积的百分比见图2。加入AP(50 μg/mL)后混合溶液中包括THBP和TBHQ在内的9种成分在常温储存条件下144 h内含量均稳定,结果见图3。因此,为保证实验过程中目标物的回收率,在标准物质配制和实际样品检测过程中采用含50 μg/mL AP的甲醇溶液作为溶剂。
2.2 提取条件的优化
本实验考察了甲醇和乙腈分别作为提取溶剂时目标物的提取效率。当提取体积为10 mL、提取1次时,花生油样品中9种抗氧化剂的回收率见图4。结果显示:甲醇提取目标物时的回收率为76.4% ~93.4% ,乙腈提取时的回收率为65.0% ~89.0% ,甲醇的提取效率明显高于乙腈。推测原因可能是:对于酚类化合物,质子性溶剂有更好的提取效果,故选择甲醇作为提取溶剂。实验进一步对提取次数进行了考察,结果显示,甲醇提取2次时的回收率范围为90.1% ~102.6% ,继续增加提取次数,回收率无明显提高,因此选择提取2次。

图 4 两种提取溶剂对9种目标化合物回收率的影响Fig. 4 Effects of two extraction solvents on the recoveries of the nine target compounds
2.3 净化条件的优化
2.3.1 除脂方式
参考文献[13,18]方法,对于油脂样品多利用正己烷或冷冻等方式脱脂,本文提取溶剂为甲醇,而正己烷能部分溶解于甲醇,因此不采用正己烷进行脱脂。低温条件下,植物油中部分杂质和不饱和脂肪酸在甲醇中溶解度低,提取液经冷冻后过滤,能够去除部分杂质,有利于延长色谱柱使用寿命。实验证明,冷冻除脂前后,9种目标抗氧化剂基本没有损失,除脂后9种目标物的回收率为90.5% ~103.1% ,因此选择冷冻除脂。
2.3.2 固相萃取方式的优化
植物油样品中可能存在杂质,干扰目标物的分离,本研究首先考虑采用固相萃取方式对植物油样品进行净化,并通过此方式减少对色谱体系的污染。
现有文献[19]研究中对于抗氧化剂的净化多采用C18和HLB固相萃取柱,因此首先比较了上述两种固相萃取柱净化效果。结果显示,抗氧化剂在C18固相萃取柱上保留较弱,9种抗氧化剂回收率均小于20% ,分析发现,上样过程中损失44.9% ~75.6%的目标物。原因可能为抗氧化剂大多数是极性比较强的酚类化合物,而C18固相萃取柱以十八烷基硅胶为填料,通过强疏水作用保留非极性化合物,因此对目标物保留较弱;HLB固相萃取柱净化结果显示,由于抗氧化剂结构的差异性,不同抗氧化剂与HLB固相萃取柱作用能力不同,其中PG、THBP、NDGA、OG、DG回收率较好,超过66.7% , TBHQ、BHA、BHT、Ionox-100回收率仅为6.9% ~43.2% ,损失较多。
氨基柱具有较强的氢键结合能力,其正相萃取模式适用于吸附极性化合物,因此本研究后续尝试用氨基柱对目标物进行净化,但结果仍不理想,仅BHA、BHT和Ionox-100回收率分别为57.0% 、31.3% 、84.8% ,氨基柱对其他目标抗氧化剂保留较强,无法洗脱下来。
研究发现,C18、HLB和氨基柱3种固相萃取方式对9种目标抗氧化剂同时净化回收率均不理想。因此本研究不采用固相萃取净化方式,选择用甲醇提取目标抗氧化剂,冷冻除脂净化。多种植物油样品实验结果表明,此方法干扰较少,能够满足9种目标化合物分离以及定量的需求。
2.4 色谱条件的选择
实验比较了Waters Symmetry Shield C18(250 mm×4.6 mm, 5 μm)、Waters XBridge C18(250 mm×4.6 mm, 5 μm)和Waters Atlantis T3(250 mm×4.6 mm, 5 μm)3种色谱柱对分离效果的影响。结果显示,在相同的色谱条件下,Symmetry Shield C18色谱柱对目标物不能很好地分离,而Atlantis T3对目标物保留较强,出峰时间较晚,导致分析时间延长。因此实验最终选择XBridge C18色谱柱进行分离。

表 1 9种抗氧化剂的线性方程、相关系数、检出限和定量限Table 1 Linear equations, correlation coefficients (R2), limits of detection (LODs) and limits of quantification (LOQs) of the nine antioxidants
Y: peak area;X: mass concentration, μg/mL.
本文对流动相的水相进行了优化,考察了采用水、0.1%甲酸水溶液和0.5%甲酸水溶液时目标物的分离情况。结果显示:水相中不含甲酸,PG、THBP的峰形拖尾严重,不对称度分别为2.61和2.84。在水相中加入甲酸后,能够有效缓解拖尾情况,峰形得到改善,甲酸体积分数为0.1%和0.5%时峰形均较好,两者响应峰面积无明显区别,考虑甲酸体积分数过高会影响色谱柱寿命,因此选择0.1%甲酸水溶液作为流动相水相。优化条件后混合标准溶液(10 μg/mL)、空白花生油样品和加标花生油样品(5 mg/kg)的色谱图见图5。

图 5 混合标准溶液(10 μg/mL)、空白花生油样品和加标花生油样品(5 mg/kg)的色谱图Fig. 5 Chromatograms of mixed standard solution (10 μg/mL), blank peanut oil sample and peanut oil spiked sample (5 mg/kg)
2.5 线性范围、相关系数及定量限
用甲醇(含50 μg/mL AP)逐级稀释标准储备液,配制质量浓度为0.1、0.5、2.0、5.0、10.0、25.0 μg/mL 的系列标准工作液。将系列标准工作液按浓度从低到高的顺序进行测定,以抗氧化剂的峰面积(Y)对其质量浓度(X, μg/mL)进行线性回归,绘制标准曲线。采用空白植物油样品加标的方法,以信噪比(S/N)=3和10时得到的目标物含量分别定义检出限和定量限,结果见表1。目标化合物在0.1~25.0 μg/mL 之间线性关系良好,线性相关系数(R2)均在0.999以上。
2.6 回收率和精密度
向阴性样品中添加低、中、高3个加标水平的9种抗氧化剂,每个水平平行测定6次,得到方法的回收率及精密度,见表2。结果表明,9种抗氧化剂的加标回收率为85.3% ~104.1% ,相对标准偏差为0.3% ~5.0% 。
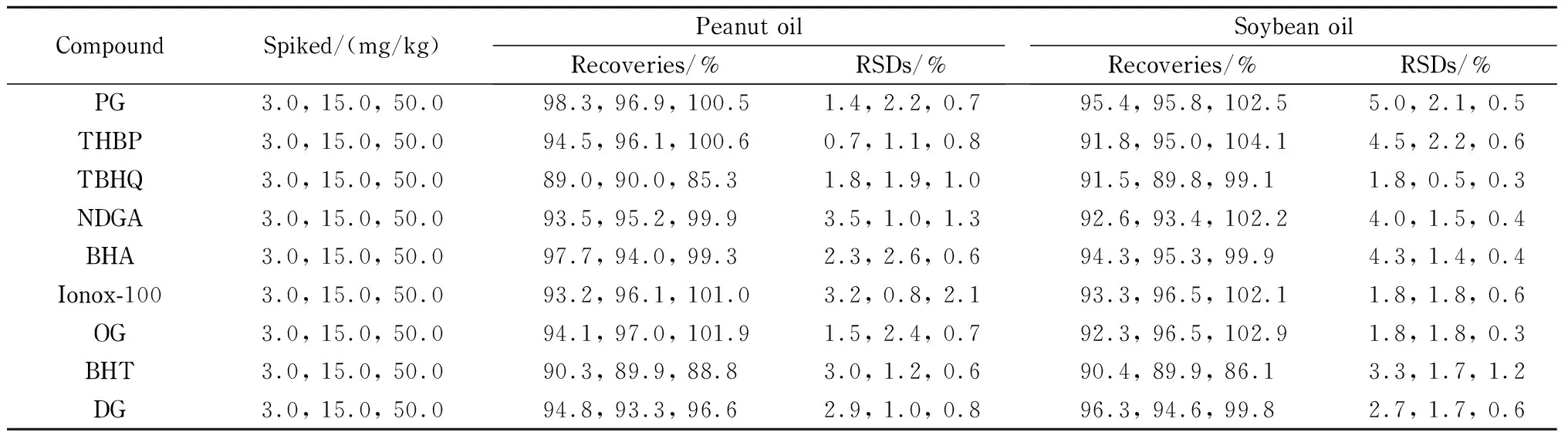
表 2 不同植物油中9种抗氧化剂的回收率及精密度(n=6)Table 2 Recoveries and RSDs of the nine antioxidants in different vegetable oils (n=6)
2.7 实际样品检测
应用本方法对市售的玉米油、调和油、花生油等20批次样品进行分析,检测结果为两批次胡麻油中Ionox-100有检出,含量分别为3.08 mg/kg 和25.6 mg/kg;一批次牡丹籽油中BHT有检出,含量为39.0 mg/kg;两批次紫苏油中NDGA有检出,含量分别为6.53 mg/kg 和16.8 mg/kg,其他种类植物油中未检出目标化合物。
3 结论
本文在现有抗氧化剂研究基础上,考察及比较了不同的提取溶剂、净化方式及色谱条件,对植物油中9种抗氧化剂高效液相色谱法进行了优化。本文通过对抗氧化剂稳定性的研究,确定标准储备溶液的储存条件,并通过在前处理过程中添加AP的方式,提高目标物稳定性和回收率,同时提出了一种快速、准确检测植物油中9种常用合成抗氧化剂的方法。该方法操作简单,快捷、准确,能够缩短检测时间,大大提高方法的回收率和准确度,能够更好地为植物油市场监管提供服务。
