医用聚氨酯弹性体的制备与性能*
2020-05-22段雪影
张 亮,段雪影,刘 超,李 颖
(1.西安交通大学医学院第一附属医院 招标采供办公室,陕西 西安 710061;2.西安科技大学 材料科学与工程学院,陕西 西安 710054)
随着现代医疗技术的不断发展以及有关生物医用材料对降低不良生物反应要求的提高[1-3],制备高生物相容性的聚氨酯材料越来越受到研究者的广泛关注[4]。聚氨酯是由多元醇(软段)、多元异氰酸酯与小分子扩链剂(硬段)通过逐步加成聚合生成的多嵌段共聚物[5-8],其分子结构的功能化设计自由度大,可以通过选择不同嵌段和调节软硬段间的比例,形成类似于“ 海岛”型的结构[9-12],从而赋予材料多重功能,合成出既具有良好物理机械性能又具有血液相容性和生物相容性的医用高分子材料[13-15]。聚氨酯弹性体[16]由于其优异的机械性能和弹性,广泛应用于医疗行业,在人体内使用时会变软,这种插入人体前具有足够硬度,而进入人体后变得柔韧的特性可确保患者感觉舒适[17]。可以通过浇注、混炼等方法加工成型医用聚氨酯弹性体[18-19],操作工艺简单且成本低廉,有利于推广应用。王连心[20]制备了一种独特的低游离4,4′-二苯基甲烷二异氰酸酯(MDI)基浇注型聚氨酯,是一种适合注射成型的材料,该创新技术将注射成型的加工优势与浇注型聚氨酯的优异性能相结合,为浇注型聚氨酯带来了新的应用前景。笔者通过两步法合成医用聚氨酯弹性体,以MDI与聚四氢呋喃醚二醇(PTMG)合成预聚体,采用3,3′-二氯-4,4′-二氨基二苯基甲烷(MOCA)作为扩链剂,以气相法白炭黑作为补强填料,制备医用聚氨酯弹性体。通过PTMG的引入改善材料硬度,赋予材料弹性,以匹配组织器官[21]。利用MOCA进行扩链,适当提升硬段比例,同时添加气相法白炭黑补强基体,使材料在柔韧基础上,还具有足够的力学强度,同时可通过浇注、混炼等方法加工成型。本研究提供了一种合成医用聚氨酯的新方法,并丰富了高分子材料在医学领域的应用。
1 实验部分
1.1 原料
MDI、PTMG:上海晶纯生化科技股份有限公司; MOCA:滨海县星光化工试剂有限公司;聚二甲基硅氧烷、端羟基线形聚二甲基硅氧烷:济南瀛裕化工有限公司;气相法白炭黑:中昊晨光化工研究所;二正丁胺:上海紫一试剂厂。
1.2 仪器及设备
傅里叶变换红外光谱仪:WQF-310,北京第二光学仪器厂;傅里叶变换衰减全反射红外光谱仪:FENSOR-27,德国布鲁克公司;综合热分析仪:ZRY-2P,上海精密科学仪器有限公司;电子控制万能实验机:KD-50,深圳凯利强电子有限公司;邵氏橡胶硬度计:LX-A型,深圳市三测精密量仪有限公司。
1.3 医用聚氨酯弹性体的制备
称取PTMG(8 g)加入烧杯中,在0.09 MPa、85 ℃条件下真空脱水3 h,将脱水后的PTMG冷却至60 ℃,向其中加入熔融后的MDI(3 g)并充分搅拌,于85 ℃条件下反应2.5 h,得到预聚体。将熔融后的MOCA(0.36 g)加入至预聚体中,再加入气相法白炭黑(0.1 g)和消泡剂(0.01 g),充分搅拌均匀。将混合物倒入预热好的模具中,硫化反应10 h后得到医用聚氨酯弹性体。制备工艺流程如图1所示,反应原理如图2所示。

图1 医用聚氨酯弹性体制备工艺流程图

图2 医用聚氨酯弹性体合成反应式
1.4 分析与测试
硬度按照GB/T 531.1—2008进行测试;拉伸强度按照GB/T 528—92进行测试;断裂伸长率按照GB/T 528—1998进行测试;化学结构采用红外光谱进行分析;热稳定性采用热失重分析;耐介质性采用磷酸盐缓冲溶液和环氧乙烷进行测试;对人皮肤成纤维细胞的增殖影响采用MTT法进行评价。
2 结果与讨论
2.1 化学结构分析
图3为聚氨酯、PTMG和MDI的红外光谱图。
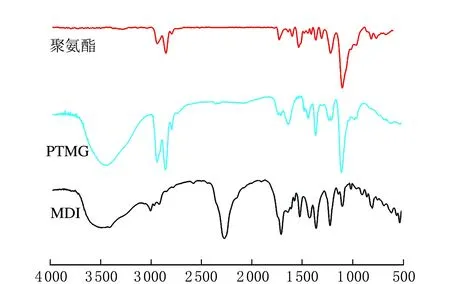
波数/cm-1图3 聚氨酯、PTMG和MDI的红外光谱图

2.2 力学性能分析
聚氨酯弹性体的力学性能主要与组成聚氨酯的硬段和软段的化学结构有关[22],既取决于二异氰酸酯和醇的种类及用量,同时也受填料气相法白炭黑影响而有所提升。图4为MDI与PTMG物质的量比对拉伸强度和邵尔A硬度的影响。

n(MDI)∶n(PTMG)(a)
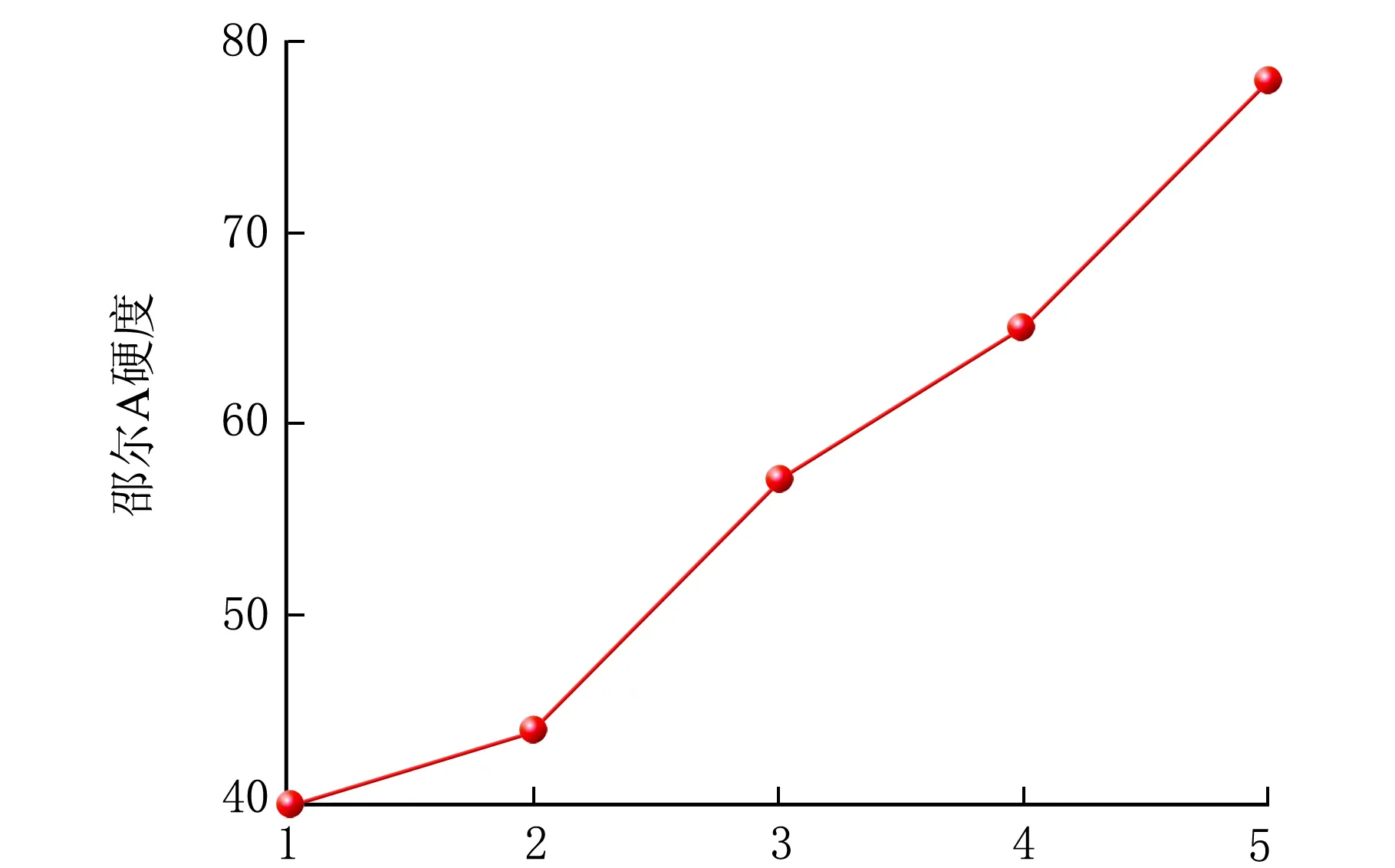
n(MDI)∶n(PTMG)(b) 图4 MDI/PTMG物质的量比对弹性体力学性能的影响
由图4(a)可知,当MDI与PTMG物质的量比为1时,拉伸强度最低,当MDI与PTMG物质的量比为3时,拉伸强度和断裂伸长率最高为10.72 MPa和550.8%,整体呈现先增大后减小的趋势。这与MDI和PTMG的化学结构有关,MDI作为硬段能够赋予材料一定的强度,PTMG作为软段能够赋予材料一定的韧性,反应初期随着异氰酸酯链节比例的增加,材料的拉伸强度上升,二者协同作用导致断裂伸长率也同步增加,但当MDI与PTMG物质的量比超过3∶1后,因异氰酸酯链节比例过大,导致样品脆性增加,此时拉伸强度反而下降,同时因PTMG用量不断降低导致断裂伸长率也在下降。从图4(b)可以看出,随着组成硬段的MDI用量的增加,样品的硬度也随之增大。由于弹性体硬度在60以下才符合使用要求,因此MDI和PTMG物质的量比为3∶1时,所制备的样品既符合弹性体特征又有足够的强度,适于用作具有一定力学性能的医用材料。
2.3 热性能分析
图5为医用聚氨酯弹性体热失重和失重速率曲线。从图5可知,热分解初始温度大于300 ℃,且失重速率适中,表明材料热稳定性良好,能达到植入及植入前热处理的耐热需求。原因是材料较高的结构规整度、MDI中的刚性基元以及二者协同作用赋予了材料优异的耐热性。
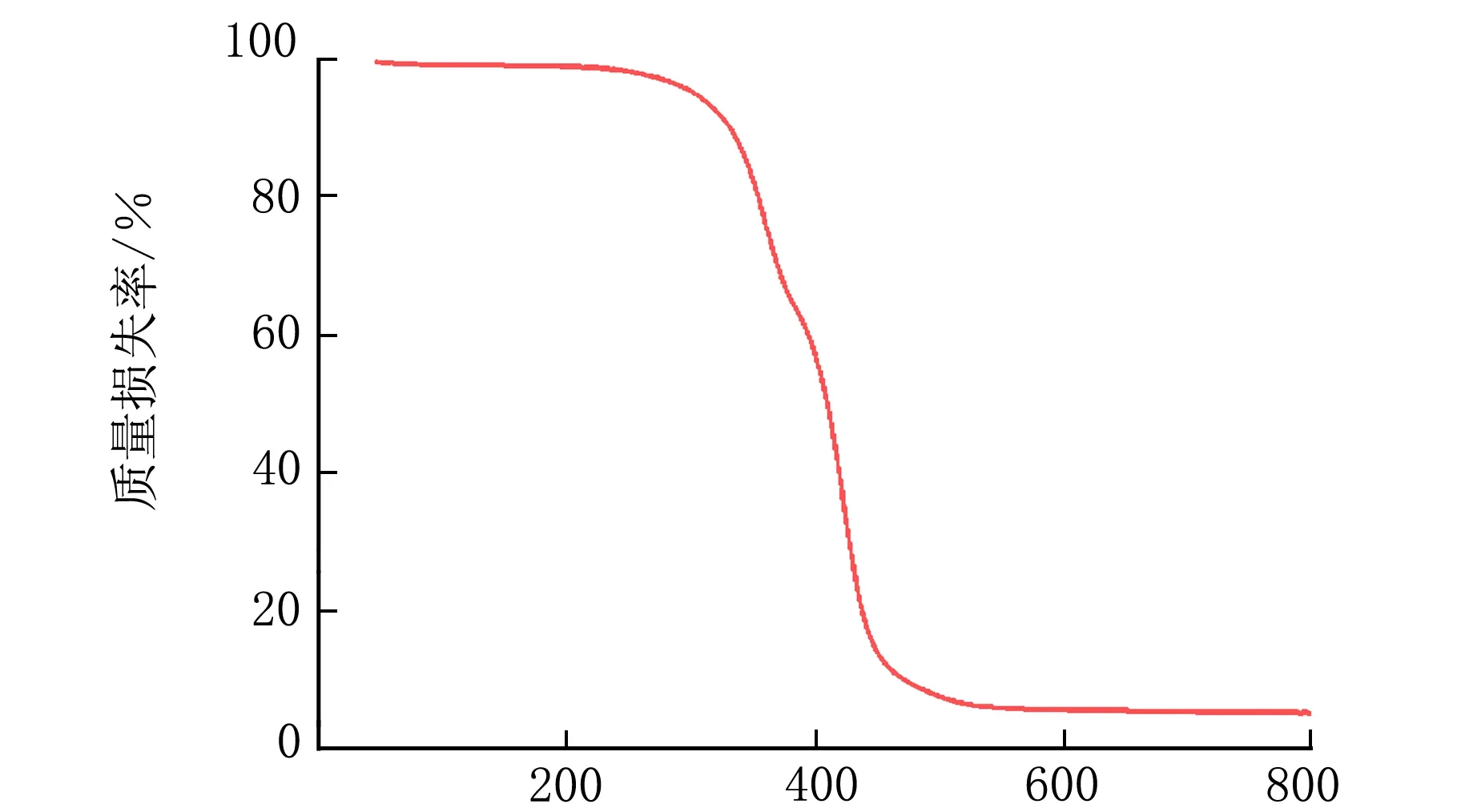
温度/℃(a) 热失重曲线

温度/℃(b) 失重速率曲线图5 医用聚氨酯弹性体的热性能曲线
2.4 医学性能分析
2.4.1 耐介质性测试
耐介质性测试结果如表1所示,配置质量分数为75%的乙醇、蒸馏水、pH值为0.8的盐酸、质量分数为3%的双氧水以及pH值为9的NaOH介质,其中盐酸和NaOH浓度均高于体液,模拟外界和人体内各个器官的化学环境,将医用聚氨酯弹性体浸泡其中14 d后取出,对比质量变化情况。
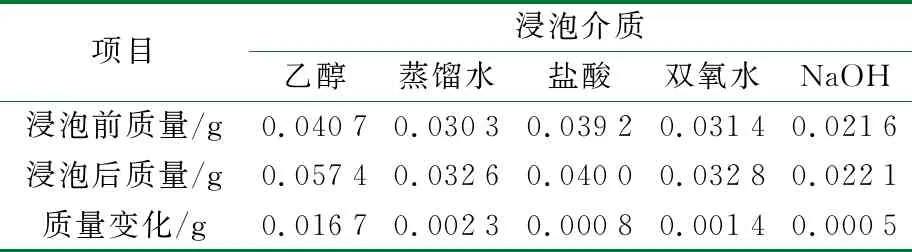
表1 耐介质性测试结果
从表1可知,除在乙醇介质中浸泡后质量变化略大外,其他变化甚微,说明可以适用于人体内环境,能作为介入材料长期使用。应该看到,虽然在乙醇中质量变化大,但乙醇只作为消毒介质使用,并不会长期和材料接触,故对材料性质影响不大,可以通过常规消毒来使用。
2.4.2 环氧乙烷灭菌测试
医用聚氨酯弹性体使用前,必须经过环氧乙烷灭菌后才能植入人体内,因此灭菌前后材料力学性能的变化是一项重要指标。从表2可知,经过环氧乙烷灭菌后,医用聚氨酯弹性体的力学性能变化很小,说明常规的消毒操作对材料性能几乎无影响,能满足医用要求。

表2 环氧乙烷灭菌测试结果
2.4.3 医用聚氨酯弹性体细胞毒性分析
细胞毒性是由细胞或者化学物质引起的单纯细胞杀伤事件,不依赖于凋亡或坏死的细胞死亡机理。本实验采用MTT法评价合成的聚氨酯材料对人皮肤成纤维细胞的增殖影响,各组测定结果如表3所示。其中OD值是吸光度,用来衡量菌体密度。而毒性分级用以评定细胞毒性,0级与1级判定为合格,2级及以上即认为该材料存在细胞毒性,不适于人体应用。由表3可知,细胞培养至第6天时实验组毒性分级仍为1级,符合医用材料的要求。

表3 MTT比色法各组测定结果1)
1) 分组1为阴性对照组;分组2为阳性对照组;分组3为医用聚氨酯弹性体浸提液原液。
3 结 论
(1)合成了医用聚氨酯弹性体,通过PTMG的引入改善了材料硬度,赋予材料弹性,以匹配组织器官。
(2)利用MOCA进行扩链,适当提升硬段比例,同时添加气相法白炭黑补强基体,使材料在柔韧基础上,还具有足够的力学强度。
(3)医用聚氨酯弹性体邵尔A硬度为51,拉伸强度为10.72 MPa,热分解初始温度大于300 ℃,符合介入材料力学性能和热性能要求。
(4)在类人体液及环氧乙烷环境下,力学性能稳定,细胞毒性测试为0 ~1级,满足医用材料要求。
(5)可通过浇注、混炼等方法加工成型,工艺简单且成本低廉,为医用聚氨酯的制备提供了新思路。
