MRI对非骨性跟距骨联合及引起并发症的诊断价值
2020-05-21许锦邱雷雨冯建钜
许锦 邱雷雨 冯建钜*
非骨性跟距骨联合被认为是距骨与跟骨间异常融合,病因可为先天性或获得性,先天性常见。临床症状主要表现为后足及内踝疼痛、活动受限,随着运动或久站逐渐加重,休息后缓解,易出现后足疲劳,部分患者出现反复踝关节扭伤。大部分放射科医师和临床医师对该病引起的并发症缺乏足够的认识及重视。国内文献报道过一两种并发症,但未进行细致的阐述。因此,作者收集了本院18例非骨性跟距骨联合患者及MRI资料,复习了国内外大量文献,从解剖及生物力学角度分析其继发改变,并观察继发改变在MRI下的表现,从而提高对本病全面的认识。
1 资料与方法
1.1 一般资料 收集本院从2012年9月至2018年9月非骨性跟距骨联合18例,其中男8例,女10例;发病年龄15~59岁,中位年龄25岁。临床症状主要表现为内踝疼痛、活动受限,运动或久站后症状加重,休息后缓解,易出现后足疲劳,部分患者出现反复踝关节扭伤。病史1月余至10余年。体检均触及内踝下方软组织内骨性隆起及跟距关节不同程度活动受限,7例Tinel征阳性。6例行手术治疗,其中2例手术证实为跟距骨桥旁腱鞘囊肿,其余保守治疗。所有病例均行MRI检查。为了更好的观察跟距关节及周围软组织解剖细节,选择5例健康志愿者。年龄16~30岁。
1.2 检查方法 采用GE signa HDxt 1.5T MRI扫描仪,使用踝关节专用线圈,扫描范围包括整个踝关节,患者仰卧位足先进,患侧踝关节中立位,扫描序列及参数:横断位快速自旋回波T1加权序列(TR400~500ms,TE9~16ms),冠状位及矢状位脂肪抑制快速自旋回波 T2加 权 序 列(TR2000~3500ms,TE70~90ms) 或脂肪抑制质子密度加权序列(TR2000~3500ms,TE20~40ms),层厚 3.0~4.0mm,扫描视野 12~16cm,扫描间隔1mm,激励次数2次。
1.3 图像分析 图像由2名从事骨肌阅片的高年资医师通过双盲法独立对MRI片进行分析,观察跟距关节位置、形态、关节间隙信号特点及周围肌腱、神经及骨是否有信号改变,如果存在意见不统一,则共同协商,达成一致意见。诊断标准:跟骨载距突与距骨内侧结节关节间隙不规则狭窄,呈裂隙状改变。关节面下骨质增生、骨赘形成,形成跟距骨桥,裂隙在FSE T1WI为低信号,脂肪抑制FSE T2WI为高信号,认为是软骨性联合。而裂隙在FSE T1WI、脂肪抑制FSE T2WI均为低信号,认为是纤维性联合。腱鞘内积液增多,且与关节腔内积液不呈比例,腱膜增厚,认为腱鞘炎。卡压神经邻近层面管径粗于近端神经,且T2WI或PDWI信号高于近端神经,认为神经增粗、肿胀。
2 结果
5位志愿者行踝关节MRI检查,均清晰显示跟距关节及毗邻的结构(见图1、2),跟骨载距突与距骨内侧结节对应构成内侧关节面。跟距关节内侧面构成了踝管外侧面,跟距关节从前内至后外依次毗邻胫后肌腱、趾长屈肌腱、胫神经足底内、外侧神经及踇长屈肌腱,并有脂肪组织填充。18例非骨性跟距骨桥,其中8例软骨性联合(见图3、5、6),10例纤维性联合(见图4、7~9),MRI表现均符合诊断标准。在非骨性跟距骨桥继发改变中,18例均出现骨赘(见图3~9),15例骨水肿(见图3、8、9),4例腱鞘炎(见图4),7例踝管综合征(见图5、6、8、9),2例腱鞘囊肿(见图3)。并对纤维性联合与软骨性联合引起继发改变分别做了记录,见表1。
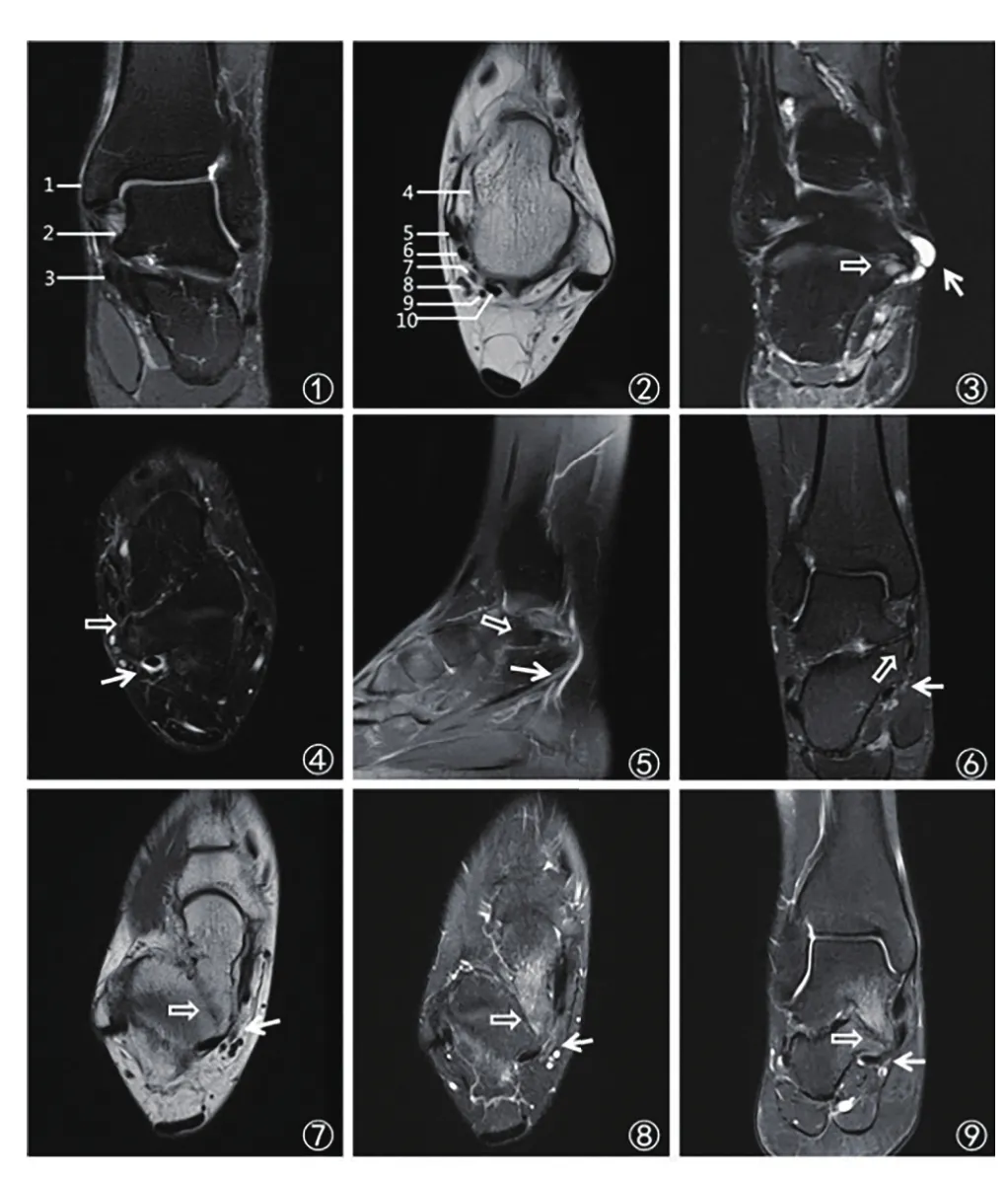
图1 ~2 男,36岁,志愿者,左踝MRI冠状位脂肪抑制T2WI、横断位T1WI。1、胫骨,2、距骨内侧结节,3、跟骨载距突,4、跟骨,5、胫后肌腱,6、趾长屈肌腱,7、胫神经足底内侧神经,8、胫后动、静脉,9、足底外侧神经,10、踇长屈肌腱;图3 男,57岁,右软骨性骨联合继发腱鞘囊肿,冠状位脂肪抑制FSE T2WI骨联合关节间隙呈裂隙状高信号,关节面骨赘形成,关节面下骨水肿、囊变(空心箭),腱鞘囊肿表现为串珠状高信号(实性箭);图4 女,27岁,左纤维性骨联合继发踇长屈肌腱鞘炎,横断位脂肪抑制T2WI腱鞘内环形高信号(实性箭);图5~6 女,23岁,右软骨性骨联合,矢、冠状位脂肪抑制T2WI关节间隙表现为裂隙状高信号(空心箭),足底内侧神经受压、肿胀(实性箭);图7~9 女,19岁,右纤维性骨联合,横断位T1WI、横断位、冠状位脂肪抑制T2WI骨联合关节间隙呈裂隙状低信号(空心箭),关节面骨赘形成,距骨内侧结节过度肥大,足底内外侧神经受压、肿胀(实性箭)

表1 纤维性联合与软骨性联合继发改变比较(n)
3 讨论
3.1 跟距骨联合的概述 跟距骨联合被认为是距骨与跟骨间异常融合。1877年Zuckerkandl等对跟距骨联合进行了第一次解剖学描述[1],其发生率低于1%[2]。分为骨性、软骨性和纤维性。病因可为先天性或获得性。先天性最常见的原因是常染色体显性遗传导致胚胎间充质组织分化失败[3],通常在出生时是纤维性或软骨性。许多人在青少年期开始骨化,因此,跟距骨联合的发病机制可视为一系列病理变化过程。获得性常见病变主要包括创伤、手术、关节炎、感染和肿瘤等[3],前者常见。发病时间常在青春期前后,亦可出现在成年以后。临床症状主要表现为后足及内踝疼痛、活动受限,随着运动或久站逐渐加重,休息后缓解,易出现后足疲劳。部分患者表现为扭伤后发病,甚至出现反复踝关节扭伤。典型的体征为触诊内踝下方软组织内骨性隆起及距下关节活动受限。骨性联合关节相对稳定,通常无明显症状,所以本次研究对象选择非骨性联合患者。
3.2 跟距关节及毗邻结构的解剖 距骨从前往后分头、颈、体三部分,体部下面分别有前、中、后三个关节面,与跟骨前2/3上关节面对应,形成跟距关节,又称距下关节。跟骨内侧面中1/3有一扁平突起,称载距突,骨皮质厚而坚硬,与距骨内侧结节对应构成内侧承重柱,起到力量的传输和分散作用,其传输的力量从小腿到足。跟距骨联合多发生于此处。跟距关节内侧面构成了踝管外侧面,其内结构复杂,跟距关节从前内至后外依次毗邻胫后肌腱、趾长屈肌腱、胫神经足底内、外侧神经及踇长屈肌腱,并有脂肪组织填充[4]。
3.3 非骨性跟距骨联合MRI诊断及引起并发症的分析 非骨性联合分为纤维性和软骨性,冠状位脂肪抑制FSE T2WI是诊断非骨性联合最佳序列,跟骨载距突与距骨内侧结节不规则骨质增生,形成假关节,可表现载距突过度肥大、也可以表现为距骨内侧结节过度肥大或者两者相对均衡增生[5]。关节间隙不规则狭窄,呈裂隙状改变,软骨性联合FSE T1WI表现为低信号,脂肪抑制FSE T2WI表现为裂隙状高信号。而纤维性联合FSE T1WI、脂肪抑制FSE T2WI均表现为裂隙状低信号[6]。并且在关节面下可观察到不同程度骨髓水肿,压脂FSE T2WI表现为高信号,最好在横轴位,冠、矢状位下观察,可以大致判断骨髓水肿累及的范围,有利于手术方式的选择。作者认为骨性关节炎继发关节面下骨髓水肿是非骨性联合引起疼痛最常见的原因。
距、跟骨内侧面组成了踝管的外侧面,而内侧面由屈肌支持带围成,因此,踝管是一个纤维骨性管道,从内踝关节后方延伸至足底,管腔狭窄,管壁坚硬,伸缩性差,管道内由胫后肌腱、趾长屈肌腱和踇长屈肌腱、胫神经及其足底内侧和外侧分支,胫后动、静脉穿过。因此,非骨性联合尖锐的骨赘,易侵犯和损伤踝管内软组织结构。踇、趾长屈肌腱离跟距骨内侧缘最近,加上跟距关节反复、长期运动,导致其易受到撞击,轻者导致腱鞘炎,重者肌腱损伤,甚至肌腱撕裂[7]。腱鞘炎MRI表现为腱鞘肿胀、积液,且与关节腔内积液不呈比例,T2WI加权上环绕肌腱环形明显高信号。肌腱损伤表现为肌腱增粗、肿胀,并在T2WI加权上表现为不均质稍高信号,常与腱鞘炎并存。肌腱撕裂表现为肌腱纤维束中断,周围软组织肿胀。肌腱病变最常见于踇长屈肌腱,其次是趾长屈肌腱,胫后肌腱受影响可能性最小。本资料中,3例出现踇长屈肌腱鞘炎,1例出现趾长屈肌腱鞘炎,未发现肌腱损伤及撕裂。与肌腱受到撞击类似,胫后神经血管束,尤其是足底内侧神经,位于趾、踇长屈肌腱之间,并紧贴跟距骨内侧缘,易受到长期、慢性刺激,导致神经肿胀、卡压,引起踝管综合征[7],MRI表现为神经增粗、肿胀。横断位T1WI加压脂T2WI加权上可以较好显示踝管内软组织病变。此外,郝大鹏等[8]曾报道过7例TCC附近的腱鞘囊肿,并认为踝管内部分腱鞘囊肿是由非骨性联合反复刺激引起的。MRI表现为单房或多房囊性肿块,边界清,T2WI表现为明显高信号,囊壁及分隔菲薄,表现为明显低信号。本资料中,2例腱鞘囊肿,其中1例切除囊肿后复发,再次施行手术治疗,切除增生骨赘及囊肿,随访至今无复发,证明与文献报道发生机制一致。
距距骨联合严重限制跟距关节的运动,由于代偿或外侧韧带松弛,导致跗横关节活动范围增大,随着跟骨外翻的存在,腓骨在负重时可能与外侧跟骨壁接触,形成外踝的撞击[9]。另外,Song等[10]报道称,TCC向后内上过度增生,并向后延伸至内踝下方,可引起内踝撞击综合征。MRI冠状位压脂T2WI上可清晰的显示内外踝关节撞击引起骨髓水肿及软组织肿胀。另外,载距突与距骨内侧结节对应构成内侧承重柱,由于跟距关节活动受限,使压力无法得到正常的传输,长期的应力或者外伤,导致了骨折的发生,通常载距突骨折可能远高于距骨内侧结节[11]。MRI可以较好的显示骨折线及周围骨水肿。由于本次研究样本量小,本组病例未发现上述三种继发改变。MRI可以清晰的显示跟距关节周围的解剖结构,可以多方位观察非骨性跟距联合是否存在并发症可能。
综上所述,MRI具有良好的软组织分辨率,不仅可对非骨性联合做出明确诊断,还可准确评估周围软组织病理学改变,观察周围骨、神经及肌腱是否受到撞击,从而指导临床对非骨性联合的患者做出精准的治疗。
