关于绿色荧光蛋白发色团激发态动力学行为的实验设计与实践
2020-05-16郑海霞展凯云
赵 莉, 郑海霞, 展凯云, 刘 冰
(中国石油大学(华东)理学院,山东青岛266580)
0 引 言
“创新是一个民族进步的灵魂,是一个国家兴旺发达的不竭动力。”因此,培养卓越的创新型人才是我国加快建设创新型国家、深入实施人才强国战略的基础和关键[1]。高等院校作为人才培养的重地,必须深化教学改革,才能适应创新型人才培养的要求[2]。综合性创新实验是由教师引导学生进行自主学习的一种新型教学模式,有助于培养学生的知识运用能力、创新能力和动手实践能力,激发学生的求知欲与探索欲[3-5]。
高精度的量化计算手段结合动力学模拟的方法,是现阶段研究分子激发态动力学行为有效的理论手段。它是一门结合了经典力学、量子力学、量子化学以及物理化学知识的综合性技术。本项目依托于纵向科研项目,将最新的科研成果进行转化,结合分子动力学以及非绝热跃迁的研究热点与前沿,利用高精度的量化计算手段结合面跃迁的非绝热动力学模拟的方法,研究了绿色荧光蛋白发色团分子在独立于荧光蛋白结构时的激发态动力学行为。通过整个实验过程,让学生了解科学研究的过程,增强学生的科学素养、实践能力、创新能力、竞争能力和合作意识。
1 实验内容设计依据
1962年,日本科学家下村修[6]从维多利亚多管水母细胞中发现了绿色荧光蛋白。1992年,Prasher等[7]将其克隆出来并投入到应用中,这给分子生物学、药学以及细胞生物学等领域带来了革命性的突破。它可作为一种标记蛋白无创性的植入活细胞中监测基因表达、生物分子相互作用和蛋白质定位等生物学过程[8]。而这些应用主要来自于其内部发色团高强度的荧光特性,荧光量子产率达到了0.8[9]。科学家们试图从蛋白质中分离出发色团分子进行应用,却发现发色团在独立于荧光蛋白或在蛋白质失活的情况下会发生荧光淬灭现象,荧光量子产率降至10-3[10]。这种完全不同的光学行为强调了发色团与包裹在外面的蛋白质之间的联合作用。目前已经有大量的实验和理论研究试图揭示发色团在溶液和气相中的荧光淬灭机理[11-13]。在这些研究的基础上,科学家们认为一种由激发态分子扭转触发的内转换机制是导致荧光淬灭的关键原因[13],分子将通过激发态与基态的锥形交叉点退回到基态。实验中,人们发现该发色团分子的激发态寿命不随溶液的浓度发生变化,表明分子在退激发时是一种节省空间的构型变化,也就是单键和双键同时扭转的过程,称为hula扭转[14]。然而,通过时间分辨的荧光光谱实验却没有发现双键扭转的反式(trans)产物,也就是没有cis-trans对应的双键扭转产生的异构产物。由此,他们提出发色团分子是沿着单键扭转进行退激发的[15-16]。由此可见,发色团分子在退激发时到底是沿着双键、单键还是单双键同时扭转的机制依然不明确,而这对探究如何提高单独的发色团分子的荧光特性至关重要。因此,采用了静态的电子结构计算结合动力学模拟的方法来研究绿色荧光蛋白发色团分子的激发态动力学行为。
2 实验仪器
计算机、Molpro量化软件包中的CASSCF模块,Chemcraft及CYLview可视化软件、自主开发的基于面跳跃的非绝热动力学程序NAIMD-DICP、基态动力学模拟程序DFTB+以及Origin绘图软件和Fortran编程软件。
3 实验教学设计
3.1 实验预习
(1)实验开始之前,教师将Molpro使用手册、Origin绘图软件、Fortran编程软件、Chemcraft及CYLview可视化软件以及NAIMD-DICP和DFTB+动力学模拟程序的使用说明资料发给学生,让学生自主学习,了解量化计算软件Molpro中CASSCF计算方法以及动力学程序的理论基础。掌握输入文件的构建方法,CASSCF计算中活化空间的选择方法、线性插值法LIIC的应用和动力学模拟程序的计算流程、可视化软件的使用、后期的数据处理如何利用Fortran自主编程以及绘图程序Origin的使用。
(2)自主查阅文献了解分子在激发态的几种退激发过程,根据雅布隆斯基电子跃迁图掌握非绝热跃迁的理论基础以及锥形交叉点的相关知识。
(3)教师提前准备关于绿色荧光蛋白的激发态动力学理论研究的相关文献发给学生,让学生提前阅读,在此基础上学生自主查阅相关文献,找出研究空白,并了解文献中的理论分析方法。
(4)学生根据阅读自主查询的文献尝试设计实验。
3.2 实验操作
3.2.1 模型构建
在进行模拟计算之前,构建合适的计算模型至关重要。从维多利亚多管水母细胞中分离出来的野生型绿色荧光蛋白分子是由238个氨基酸残基组成,其晶体结构是11个β-折叠组成的桶状结构,在桶中央有一个α-螺旋,发色团分子就在α-螺旋上,其结构如图1所示。
考虑到绿色荧光蛋白的强荧光就来自于α-螺旋上的发色团分子,在野生绿色荧光蛋白中它是以阴离子的形式存在,因此在综合考虑实际模型、计算效率、计算精度等因素后,选择了一种广泛应用的结构对羟基苄基咪唑啉酮阴离子(HBI-)作为计算模型(见图2),该模型是把两个甲基取代基用两个氢原子取代,这种简化可以保证在不改变其性质的前提下降低计算成本。这种方法已经被很多理论计算文章使用过[13,17]。HBI-是顺式结构,标记为cis-1。由于重点在于研究发色团分子到底是单键还是双键扭转,为了区分,利用如图2所示的二面角进行标记,单键扭转为φ,双键扭转为τ。根据组合,一共可以有4种异构体,如图3所示。

图1 绿色荧光蛋白GFP的四级结构图

图2 绿色荧光蛋白发色团分子的计算模型
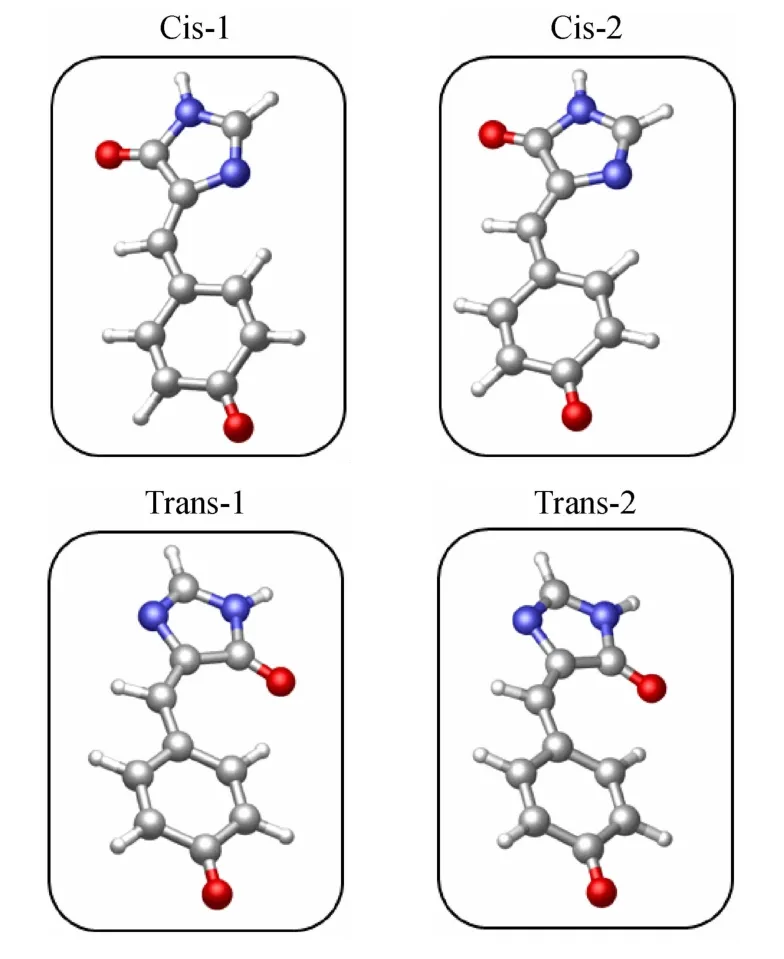
图3 绿色荧光蛋白发色团分子的4种异构体
3.2.2 计算方法
实验中发现更高能级的电子激发态对发色团分子的退激发行为影响甚微,因此在计算过程中只考虑了基态(S0)和第一电子激发态(S1)[18-19]。所有的电子结构计算都采用Molpro软件中的CASSCF方法。CASSCF计算中有两个具有相同比重的电子态参与态平均。值得一提的是,CASSCF的计算方法依赖于活化空间的选择,因此选择合适的活化空间至关重要。一般情况下,选择的活化空间越大,计算结果越准确,但是计算耗时也越长。所以在进行静态电子结构计算时,优先选择大的活化空间和基组以保障计算的准确度。但是对于动态的动力学模拟过程,选择大的活化空间和基组会消耗大量的计算机时,因此还需要在保证计算精度的前提下,选择计算耗时更短的小活化空间。为此,对比了不同活化空间(14e,12o)、(10e,8o)以及(6e,5o)和不同基组下(6-31G*和6-31G)优化的稳定构型和锥形交叉点的结构参数,如表1、2所示。通过数据可见,(6e,5o)的活化空间搭配6-31G的基组优化得到的构型参数与大活化空间(14e,12o)和6-31G*基组得到的相差不大。另外,由于分子的激发态行为取决于该分子激发态和基态势能面的拓扑结构,为了进一步确认(6e,5o)/6-31G计算的准确性,利用线性插值法LIIC得到了Franck-Condon点与锥形交叉点间的势能曲线,如图4所示。二者的拓扑结构一致,说明用(6e,5o)/6-31G进行动力学模拟得到的结果是可信的。

表1 在不同的计算水平下优化得到的HBI-分子在不同电子态的重要结构参数(键长单位为10-1pm,键角和二面角的单位为(°))

表2 在CASSCF(6e,5o)/6-31G,CASSCF(10e,8o)/6-31G*和CASSCF(14e,12o)/6-31G*计算水平下优化得到的4 个锥形交叉点的主要构型参数(键长单位为10-1pm,键角和二面角的单位为(°))

图4 在不同计算水平下利用线性插值法得到的基态和激发态的势能曲线
非绝热动力学部分采用的是自主开发的基于Zhu等[20]电子跃迁理论的动力学程序,具体的计算细节需要学生在实验预习阶段掌握。轨线的核运动方程采用Velocity-Verlet[21]算法进行数值积分,步长设为0.5 fs。由于在锥形交叉点处构型变化信息更加重要,因此将步长减少至0.1 fs。每一步对应的电子态能量,梯度以及电子态耦合系数都是通过调用外接的Molpro(http://www.molpronet)程序包进行。在运行动力学模拟之前,需要选取合适的初始坐标和速度。初始坐标和速度的选择方法有很多种,如基态的动力学模拟、玻尔兹曼分布、Winger分布、高斯分布等。先选择基于DFTB+的基态动力学模拟方法,在室温下计算500 ps,在分子达到平衡后,再在动力学结果中随机地选取构型和速度作为初始条件。计算的轨线数量由学生自主决定,一般数量越多,统计意义越明显。但一般认为计算结果达到收敛即可,经过计算30条轨线可满足要求。
4 结果与讨论
4.1 静态电子结构计算分析
静态的电子结构计算,采用的是SA2-CASSCF(14e,12o)方法来优化基态、第一激发态的稳定结构以及两个电子态之间的锥形交叉点。相应的结构参数已分别在表1、2中展示,锥形交叉点的构型如图5所示。如上所述,锥形交叉点作为分子从激发态到基态的反应通道,那么优化的这4个锥形交叉点是否全部参与到退激发过程中呢?为此,还需要接下来的动力学模拟来确定上述锥形交叉点的作用。

图5 在SA2-CASSCF(14e,12o)/6-31G*水平下优化得到的4个锥形交叉点
4.2 动力学模拟结果分析
对31条轨线进行分析,每条轨线以目标分子的弛豫过程从Franck-Condon点开始,最终生成稳定的基态产物为准。首先,统计了HBI-分子每条轨线的跃迁时间,并根据此画出基态和激发态随时间的布居数,如图6所示。这些分子的退激发时间从0.3 ps持续到1.4 ps,且主要集中在0.7~1.1 ps之间。平均跃迁时间为807.3 fs,这与实验上得到的激发态寿命吻合[22],再一次证明了所用模拟方法是可靠的。
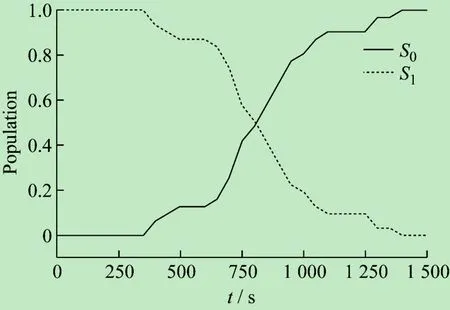
图6 基态和激发态随时间的布居曲线图
图7中总结了各条轨线的跃迁点与锥形交叉点之间的关系,可见,所有的跃迁点都围绕在4个锥形交叉点周围,说明这4个锥形交叉点都参与了发色团分子的退激发过程。值得一提的是,虽然这些跃迁点都围绕在锥形交叉点附近,但是仍然有一定的分布范围,表明分子在退激发时只要在锥形交叉区域内满足跃迁条件都可以发生跃迁。另外,所有的轨线最后只产生成了顺式的产物,并没有发现反式产物。也就是说由cis-trans对应的双键扭转在整个跃迁过程中并不存在,只有单键扭转产物产生。从优化得到的锥形交叉点可以看出,这4个锥形交叉点既包含单键扭转的过程,也包含双键的扭转。那么,为什么最终没有生成因双键扭转而产生的trans产物呢?为了解决这个问题,又扫描了分子在基态和激发态随CCCN和CCCC变化的二维势能面,如图8所示。可以发现,分子在被跃迁至激发态后,可以有两条路线退激发至基态,如图8中左箭头所示。到达基态后分子恰好落到势能面的“山脊”上,在弛豫过程中可无势垒的产生cis-1和cis-2。但是在生成trans产物的路径上存在势垒,因此阻止了trans产物的生成。
4.3 退激发机理总结
综上所述,总结了绿色荧光蛋白发色团的退激发机理。当分子被垂直激发到第1激发态后,会通过单双键协同扭转的形式(hula扭转)到达锥形交叉点附近,这可以解释实验中发现的发色团分子的激发态寿命与溶液黏度无关的现象。当分子通过锥形交叉点退激发至基态后,单键继续扭转生成新的顺式结构(cis-2)或反向扭转生成之前的反应物(cis-1)。但是此时的双键只会发生反向扭转,因此不会生成反式(trans)结构的产物,这与实验中只发现顺式产物的结果一致。

图7 以CCCC(纵坐标)和CCCN(横坐标)为变量做S1到S0跃迁点以及最终产物的散点图

图8 以CCCC和CCCN二面角为变量扫描得到的S1和S0态的势能面[23]。上面的星标分别表示激发态和基态的最稳定构型,箭头表示退激发反应进行的方向
4.4 实验内容拓展
本实验属于研究型实验,以野生绿色荧光蛋白的发色团分子为计算模型,采用高精度的量化计算手段以及非绝热动力学模拟的方法进行模拟计算,综合模拟结果进行理论分析揭示了绿色荧光蛋白发色团分子在独立于荧光蛋白之后发生荧光淬灭的内在机理。学生在教师的指导下完成了整个模拟过程,从科研选题、量子化学基础知识、计算模型的建立以及后期的数据分析等基本方法,激励学生由机械式学习到自主探究型学习,培养他们交叉学科知识的综合运用能力。考虑到课时量和不同学生的接受程度,对实验内容进行了充实与拓展,如图9所示。
首先是研究内容的拓展,随着科学技术的发展以及现实需求的增加,不同颜色的荧光蛋白已经被发现或通过基因克隆与变异技术发展出来。但是,与绿色荧光蛋白不同,不同颜色的荧光蛋白具有不同的激发态行为。因此,在本工作的基础上可以拓展以下的实验内容:
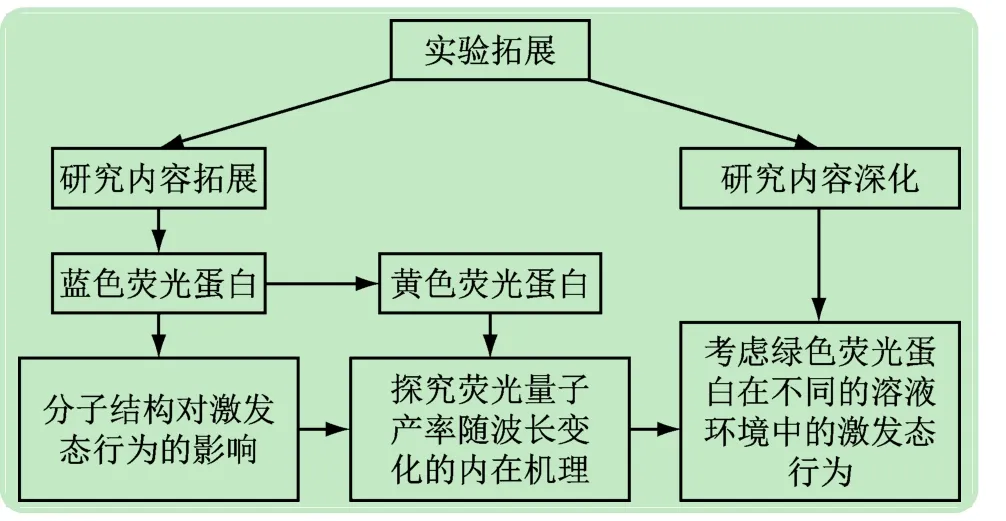
图9 试验拓展内容
(1)研究蓝色荧光蛋白的发色团在激发态的动力学行为,并与绿色荧光蛋白进行对比,分析不同的分子结构对激发态行为的影响。
(2)黄色荧光蛋白的激发态行为更加复杂,与蓝色、绿色荧光蛋白只有第1激发态参与不同,黄色荧光蛋白的激发态行为S2态也有参与,且它的荧光量子产率与激发波长有关,因此在计算时需要考虑3个电子态之间的耦合与跃迁,鼓励有能力的学生对现有的动力学模拟程序进行改善,使其能够处理3个电子态的跃迁行为。
其次是研究内容的深化,目前研究的绿色荧光蛋白分子是在气相环境中,没有考虑液相环境的影响。因此,在本工作的基础上,还可以考虑溶剂化效应,探索在不同溶液环境中绿色荧光蛋白发色团分子的激发态动力学行为,分析分子间氢键对其动力学行为的影响机制。拓展的内容工作量较大,教师可根据教学时长灵活地选取部分内容进行课堂教学,也可以作为有兴趣学生的创新研究内容。
4.5 撰写实验报告
实验课后,学生需要对计算模拟过程进行概括总结,分析静态的电子结构计算与动力学模拟的结果,并按照科研论文的格式撰写实验报告,分析总结计算过程中所遇到的问题及处理方式。对于进行实验内容扩展的学生研究报告,将由教师协助修改并向杂志社进行投稿。
5 结 语
本设计性实验通过高精度的电子结构计算和非绝热动力学模拟的手段,研究了绿色荧光蛋白发色团分子在被独立于荧光蛋白后发生荧光淬灭的内在机理。与之前的理论报道不同,提出了绿色荧光蛋白发色团分子在退激发时是以单键扭转为主,双键扭转为辅的退激发机理。
该设计性实验包含的理论知识复杂,涉及到数学、物理、化学、计算机编程等多个学科的交叉运用,有助于培养学生的科研创新能力,知识综合运用能力以及独立思考解决问题的能力。到目前为止,已经取得了很好的成绩,有6位本科生通过查阅文献,自己拟定题目并获批校级大学生创新项目,有4位已在杂志上公开发表科研论文。对于想继续读研究生的学生,可大大缩短他们融入科研团队的周期。
