MTT细胞毒性试验参数验证
2020-05-16药明康德医疗器械测试中心江苏苏州215124
药明康德医疗器械测试中心 (江苏 苏州 215124)
内容提要: MTT细胞毒性试验为常见的细胞毒性试验,其广泛地应用于国内外医疗器械生物相容性检测并为ISO10993所推荐。文章就该试验的几项参数细胞代数、加样时间、血清类型和阴性对照毒性范围等对该试验的影响进行了验证,以说明在该中心试验条件下该试验的稳定性,同时为标准实验操作提供参考。
医疗器械标准是医疗器械研发、生产和监督管理共同遵守的技术规范。随着医疗器械产业的蓬勃发展,医疗器械的安全检测对产品安全有效和推动产业发展的作用与日俱增,如何科学稳定地按照标准对医疗器械进行检测尤为重要。体外细胞毒性试验是医疗器械安全性检测的重要试验,而MTT法尤为广泛。
本试验通过检测暴露于供试品浸提液后的细胞新陈代谢活动的变化,进而获得其对细胞活力的影响。未被代谢的MTT(3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐)呈现黄色,当其被活细胞代谢消耗后变成难溶的蓝紫色甲瓒。用异丙醇溶解甲瓒并测量吸光度,活细胞的数量与颜色强度相关。活细胞数量的减少使其总体活力减少,这一减少与蓝紫色甲瓒的形成数量直接相关,变化大小可以通过测量光密度获得。本研究通过对MTT细胞毒性所涉及到的细胞代数,血清类型,给药时间以及阴性对照进行了确认和研究,为企业供试品生物相容性测试提供参考。
1.材料与方法
1.1 仪器、耗材与试剂
生物安全柜,高压蒸汽灭菌锅,MEM培养基,胎牛血清,小牛血清,酶标仪,高密度聚乙烯(HDPE)。

图1. L-929细胞(高密度)
1.2 细胞代数参数
L-929小鼠成纤维细胞为细胞毒性试验常用细胞系,为贴壁细胞,每传代一次需进行消化一次。本试验通过相差11代的细胞对同一供试品进行检测,并将数据进行对比,以验证随着细胞代数的增加,该细胞系的检测敏感度有所变化。
细胞系:L-929,美国模式培养物集存库(ATCC);细胞冻存:将细胞消化成单细胞悬液,将细胞密度调整为约1×106cells/mL;液氮长期储存(-196°C)细胞代数:P572和P561。细胞培养状态见图1。
1.3 给药时间参数
细胞接种后需要将细胞原培养基去除加入供试品浸提液/溶液,细胞的给药一般从左向右,而加样的速率和时间可能会对试验的结果产生影响,因此标准方法将空白对照加于左右两侧进行质控。本试验通过以不同的速率给药分别按照大约2、3、5、7、9、11、15和30min给完一个细胞板,从而判断细胞在原培养基去除之后因给药速率不同暴露时间不同而对试验结果的影响。
1.4 血清类型参数
胎牛血清取自剖腹产胎牛,小牛血清取自出生24h之内的新生牛。两种血清均可作为细胞培养基的重要添加成份,冷冻存放,使用前融化添加,而两者所含抗体、补体成分是存在一定差异的。本试验采用小牛血清和胎牛血清的培养基对不同的测试材料进行测试对比以期发现其对MTT细胞测试结果的影响。
1.5 阴性对照
医疗器械的MTT细胞毒性试验需要同时测试阴性材料,并且其结果应当保持稳定的阴性。本中心使用Hatano研究所食品药品安全中心获取的高密度聚乙烯材料(HDPE)并对其进行了约4个月的测试监控从而获得该阴性材料毒性历史值供参考。
2.结果与讨论
2.1 细胞代数参数
本设施通过浸提实验室手套并调整给药浓度以获得特定毒性浓度使用代数P572和P561的L-929细胞进行试验,细胞毒性结果见表1。
从表格数据以及对比可以发现20%试验手套浸提液在P561和P572细胞上表现出64.53%到76.74%的细胞活力,15%试验手套浸提液在P561和P562细胞上表现出85.09%到92.31%的细胞活力,10%试验手套浸提液在P561和P562细胞上表现出79.75%到87.18%的细胞活力,差异范围为-6.43%~7.22%,无显著性差异。细胞类型细胞毒性对比见图2。
2.2 给药时间参数
本试验通过浸提实验室手套获得毒性浸提液,并对其进行稀释以得到不同程度的细胞毒性反应。根据给药时间快慢,即细胞暴露时间不同数据总结见表2。
从数据总结表和曲线图(见图3)可以发现,10%的手套浸提液在2min给药情况下活力为87.35%,30min后给药活力为85.27%。15%的手套浸提液在2min给药情况下活力为75.70%,30min后给药活力为81.09%。20%的手套浸提液在2min给药情况下活力为39.51%,30min后给药活力为55.03%。25%的手套浸提液在2min给药情况下活力为21.81%,30min后给药活力为30.13%。总之,低中高浓度毒性的供试品浸提液的给药速度/给药等待时间在30min54s内无显著变化,可见细胞在空气中的暴露在0.5h内是不会影响MTT测试结果的。
2.3 血清类型参数
本参数验证使用两种培养基对三种材料,non-PVC膜袋,实验室手套,胶塞进行了浸提,浸提液稀释后按照一定的稀释比例进行MTT测试,具体数据见表3,对比柱状图见图4(FBS:胎牛血清;NBS:新生牛血清/小牛血清)。
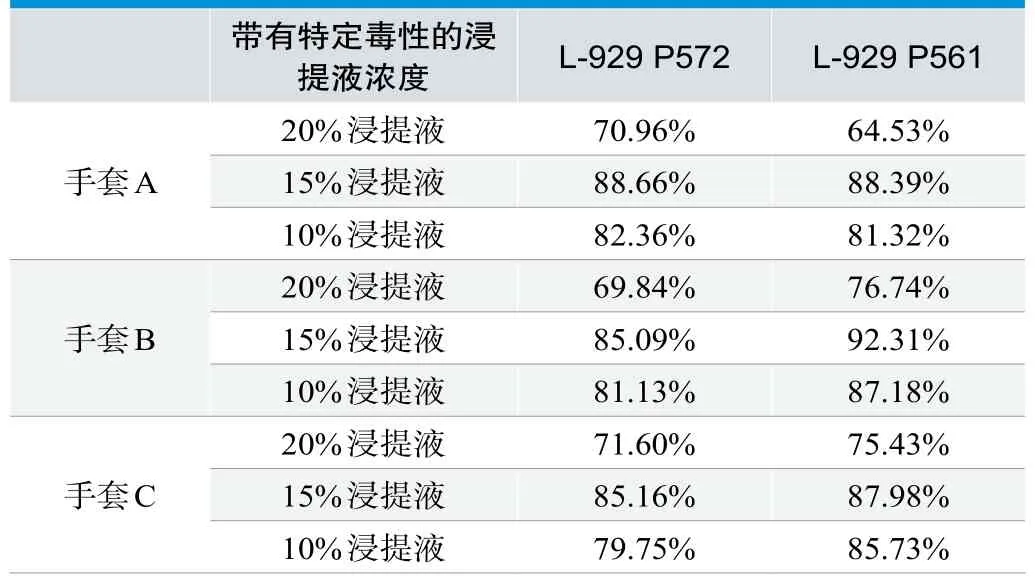
表1. 不同代数对同一给药制剂的细胞毒性表现
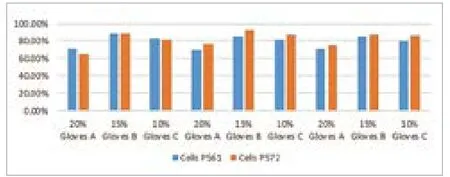
图2. 细胞类型细胞毒性对比柱状图
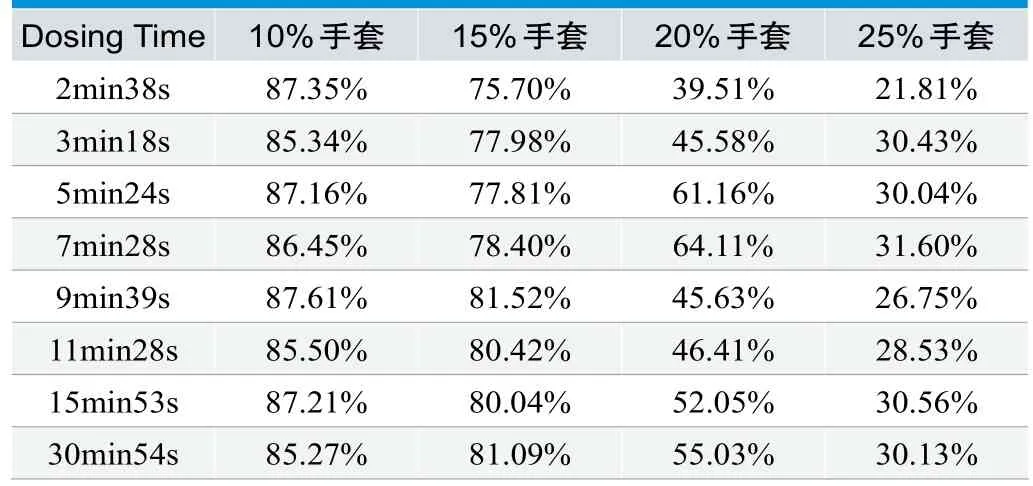
表2. 不同毒性浸提液在时间梯度延长时所表现出的细胞活力总结表
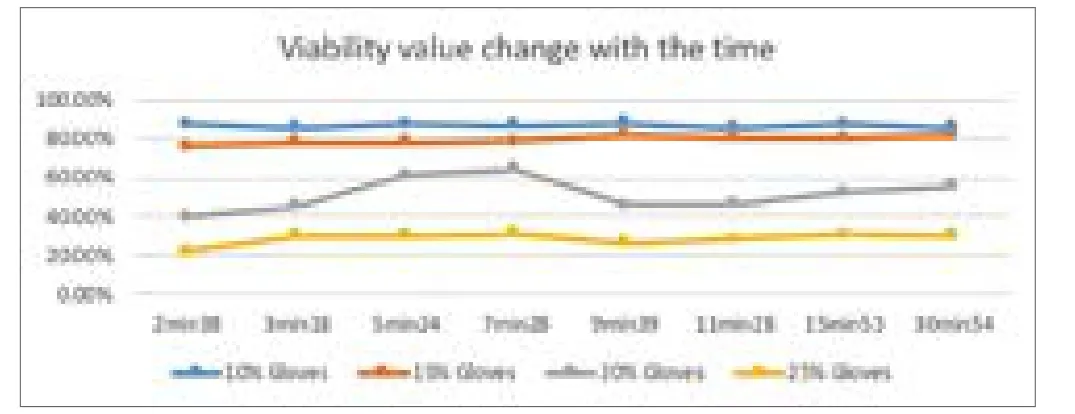
图3. 不同毒性浸提液在时间梯度延长时所表现出的细胞活力总结曲线图
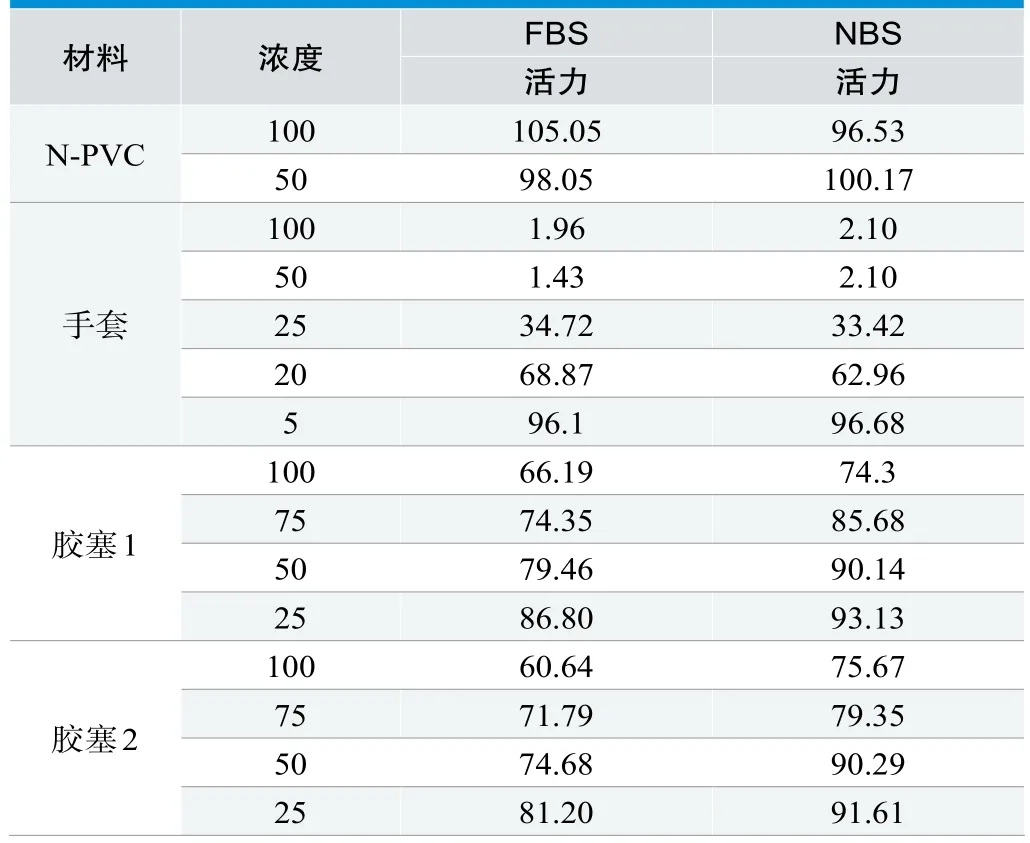
表3.胎牛血清培养基和小牛血清培养基作为浸提介质时在不同材料上的细胞活力表现(%)
所选Non-PVC膜袋为阴性结果,细胞活力分别为105.5%和96.53%。所选实验手套为显著毒性,活力分别为1.96和2.1%,所稀释梯度毒性无差异。在两种血清环境下未表现出显著不同。胶塞为中等毒性材料,在此材料上两种介质浸提液表现出了一定的差异性,如Plug1 50%浸提液活力分别为79.46和90.14%,相差约11%,Plug2 100%浸提中活力分别为60.64%和75.67%,相差约15%。并且所有Plug材料的毒性表现小牛血清高于胎牛血清。说明在本试验条件下某些特定材料可能会表现出活力差异,这一结论需要进一步的测试证明。
2.4 阴性对照
MTT细胞毒性试验的阴性对照需要保持70%以上,其毒性表现往往受到批次、制备等过程的影响。本实验室对该结果进行了连续4个月的监控,结果见图5。数据表明,绝大部分HDPE的活力范围在90%~100%,表明该试验在本实验室条件下具有很好的稳定性。
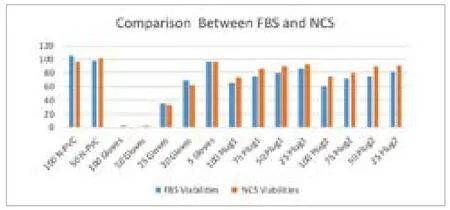
图4. 胎牛血清培养基和小牛血清培养基作为浸提介质时在不同材料上的细胞活力表现对比柱状图
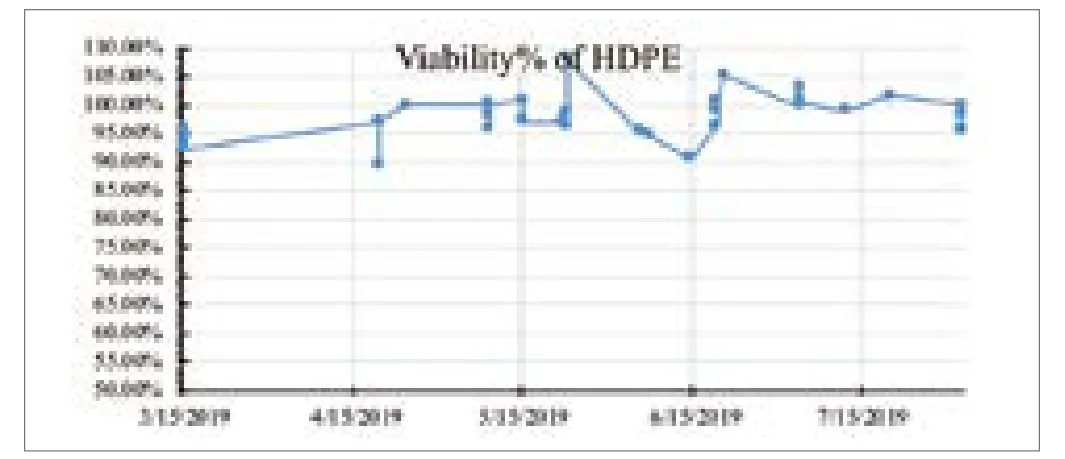
图5. MTT细胞毒性试验的阴性对照结果
3.小结
本研究中数据表明,MTT细胞毒性试验所采用的L-929细胞代数差异在11代以内不会引起测试结果的不同。原培养基移出后,给药时间在30min54s内对试验结果无显著影响,因此该给药时间控制在0.5h内完成不会对供试品活力产生影响。由于在培养基浸提介质中的胎牛血清和小牛血清在成分上存在一定差异,其在供试品毒性检测上略有差异,但非显著。购自Hatano研究所食品药品安全中心的阴性对照材料表现出了良好的阴性结果,并且在本实验室的重复测试中活力稳定。
