徐州地区无偿献血人群HTLV感染情况调查
2020-05-13赵艳梅
赵艳梅,刘 晶
(徐州市红十字血液中心,江苏 徐州 221006)
人类嗜T淋巴细胞病毒(HTLV)可以导致感染者出现成人T淋巴细胞白血病,热带痉挛性下肢轻瘫等疾病,该病毒主要经过母婴传播、性传播和输血传播,我国于1982年开始HTLV-1抗体调查,并在福建、广东、浙江和北方少数民族地区发现小流行区, 但仅发现10余例病人[1]。HTLV在我国大部分地区特别是城市确切的感染率尚不清楚,国家卫健委2016年在血站开展HTLV监测,掌握我国献血人群中HTLV感染情况,为制定血液管理相关政策提供决策依据,进一步提高我国血液安全水平。徐州市中心血站在2016年-2020年间共对126170份献血者标本进行了HTLV-1/2型抗体监测,现报告如下。
1 材料与方法
1.1 标本来源
徐州地区2016年3月28日至2020年9月15日采集的无偿献血者标本126170例。
1.2 试剂与仪器
人类T淋巴细胞白血病病毒抗体检测试剂盒(双抗原夹心酶联免疫法)(北京万泰,批号T20200503B)。STAR全自动加样仪(瑞士Hamilton公司),FAME全自动酶免分析仪(瑞士Hamilton公司)。
1.3 血液检测方法及判定规则
(1)使用双抗原夹心法ELISA试剂对126170份献血者标本进行抗- HTLV-1/2筛查,所有操作均严格按照试剂盒说明书要求进行。对初次检测S/Co值≥0.5的样本均做双孔复查,复查任1孔S/CO≥1判为筛查阳性样本,复查任1孔0.5≤S/CO<1判为筛查灰区样本。(2)将筛查阳性和灰区样本再次离心3000×g/min,10min,取全部血浆分装;再取白膜层1.0 mL分装,送国家卫健委临床检验中心进行核酸检测(PCR)和免疫印迹(WB)试验。(3)对WB证试验结果不确定的献血者追踪采集样本,再次送国家卫健委临床检验中心进行WB试验。
2 结 果
126170份献血者标本中共筛查出抗-HTLV-1/2阳性样本19份,灰区样本9份。筛查阳性率为0.015%(19/126170),灰区检出率为0.007%(9/126170);28份筛查阳性和灰区标本均送卫健委临检中心进行核酸检测(PCR)和免疫印迹试验(WB)。核酸检测结果均为阴性,免疫印迹试验结果为阳性0份,“不确定”2 份(2016年),其余为阴性。2016年对WB试验结果为不确定的2例献血者进行追踪采样,WB试验结果均为阴性。2016年至2020年无偿献血者HTLV-1/2检测结果统计分析,见表1。
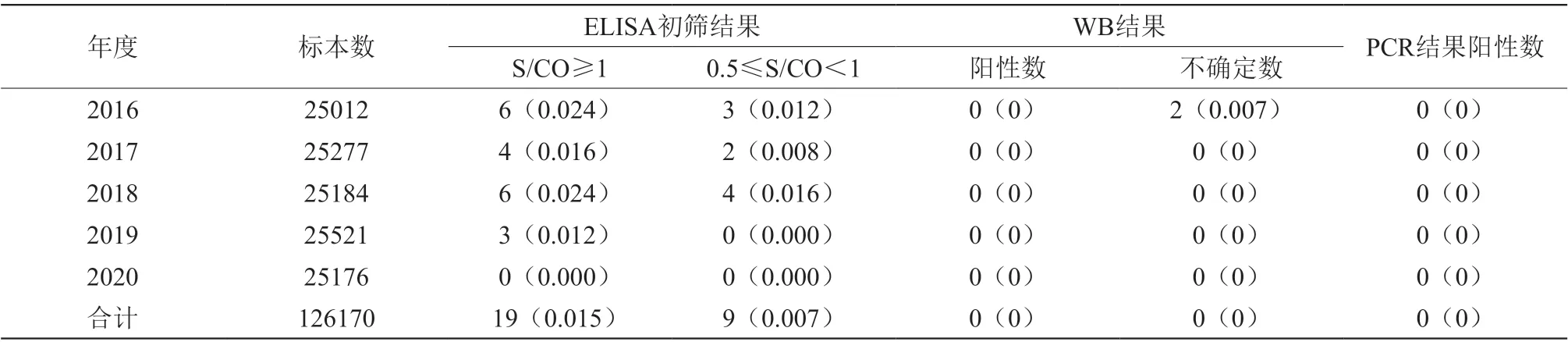
表1 2016年至2020年无偿献血者HTLV-1/2检测结果统计(n,%)
3 讨 论
HTLV是20世纪80年代初由美国 Poiesz等和日本 Miyo shi等分别从成人T细胞白血病患者和外周血培养的T细胞中分离出来的一种逆转录病毒,1983年在美国冷泉港的T淋巴细胞白血病病毒研讨会上将其命名为 HTLV-1,同时将1982年日本Kalyanarman报告的1例T细胞变异的多毛细胞白血病患者中与HTLV-1有血清学交叉反应的病毒命名为HTLV-2[2]。
自上世纪末季阳等首次发现福建地区存在HTLV流行后,我国已陆续报道了部分地区的HTLV流行率,高发区集中在东南沿海地区。而最近些年,随着中国社会、经济发展水平的快速发展而来的人口的频繁流动,势必造成当前各地区的HTLV在献血者中流行情况的变化。为获取HTLV在我国各地区献血者中的流行情况,国家卫生行政部门在全国范围内开展献血者HTLV筛查试点工作[3]。
本研究对徐州地区的无偿献血者HTLV-1/2感染情况进行了初步调查,采用ELISA法对126170例无偿献血者血液标本进行了HTLV-1/2抗体的检测,共检出阳性样本19例,灰区样本9例。28例样本送卫健委临床检验中心对抗体进行确证(WB试验)和PCR核酸检测,PCR检测结果全部为阴性,WB试验结果为17例阴性,2例不确定,对2例不确定的献血者进行追踪采样,再次进行WB试验,结果为阴性。徐州地区的初筛阳性率为0.015%(19/126170),与陈善华等报道的洛阳地区的初筛阳性率0.015%(5/34009)的结果一致[4]。与周学勇等报道的安徽地区的万泰试剂初筛阳性率0.059%(51/85948)有统计学差异(x2=29.06,P<0.01)[5]。分析原因可能是受实验室检测人员、检测环境、设备状况、标本内源性因素(如溶血、乳糜血、自身抗体等)和外源性因素、试剂批间差异等的影响。
综上所述,徐州地区为HTLV非流行地区,目前尚无开展HTLV-1/2常规检测的迫切性,但徐州地区是全国重要的交通枢纽,人口流动性高,对HTLV对输血安全的威胁不可掉以轻心,警惕流动人群中HTLV的传播,进行适时监测,了解HTLV的感染情况。因HTLV的致病性较强,且输入被HTLV污染的血液制品感染HTLV的可能性高达40%-60%[6]。现阶段可以采取白细胞过滤技术、病毒灭活技术与针对性血液筛查相结合的防控策略。
