经皮穿刺置管引流术联合通腑化瘀解毒方对急性重症胰腺炎并胰腺感染患者P物质、胰蛋白酶原激活肽水平的干预作用∗
2020-05-08张远军
张远军 汪 建 钟 建
(四川省资阳市第一人民医院,四川 资阳 641300)
急性重症胰腺炎(SAP)为临床多发急危重症,患者多存在不同程度腹胀、腹痛等,随病情进展可引发多器官功能障碍综合征、脓毒症、胰腺组织坏死感染等,其中胰腺感染较常见,对患者身心健康及生活质量影响极大[1-2]。经皮穿刺置管引流术(PCD)为临床治疗SAP合并胰腺感染的重要术式,具备创伤小、安全性高、术后恢复快等优势,在疾病治疗中发挥了重要作用[3-4]。近年来,中医在SAP中应用价值得到普遍关注。中医学认为,SAP发病多是因情志不舒、暴饮暴食、胆道阻塞致使热、湿、瘀藴结中焦,进而引起肝胆疏泄失职、腑气不通,故治疗应注重通腑行气、解毒化瘀等[5-6]。因此,为进一步提高SAP整体治疗效果,并结合上述病因病机,本研究自拟通腑化瘀解毒方,探讨其与PCD联合治疗在SAP合并感染患者应用价值。现报告如下。
1 资料与方法
1.1 病例选择 纳入标准:符合《慢性胰腺炎诊治指南(2014)》中SAP诊断标准[7];经细菌培养确定存在胰腺感染;年龄<65岁;患者及家属知晓本研究,签署同意书;经医院伦理委员会审批通过。排除标准:既往采取腹部手术治疗者;合并肾肝等脏器器质性病变者;过敏体质及对研究药物具有过敏史者;合并胰腺肿瘤者;合并消化道出血、胆道梗阻者;合并凝血功能异常者;休克者。剔除标准:主动要求退出及研究期间病死者。
1.2 临床资料 选取本院2017年10月至2019年5月SAP并胰腺感染患者82例,根据治疗方案分为研究组与对照组各41例。研究组男性24例,女性17例;年龄38~61岁,平均(49.23±5.03)岁;发病至治疗时间6.9~64 h,平均(35.22±14.02)h;急性生理和慢性健康量表(APACHEⅡ)评分9~17分,平均(13.06±1.38)分;构成因素为酒精性11例,胆源性25例,其他5例。对照组男性27例,女性14例;年龄37~64岁,平均(50.11±4.81)岁;发病至治疗时间7.6~65 h,平均(36.09±13.78)h;APACHEⅡ评分 9~18分,平均(13.20±1.41)分;构成因素为酒精性13例,胆源性24例,其他4例。两组性别、年龄、发病至治疗时间、病因构成、APACHEⅡ评分等临床资料差异无统计学意义(P>0.05)。
1.3 治疗方法 入院后给予两组常规干预,包括维持水/电解质平衡、营养支持、抑酸抗感染、胃肠减压及禁食等,在此基础上分别采取不同治疗方案。对照组给予PCD,平卧位,经腹部B超(探头频率设定至5 MHz)实施探查,明确坏死组织位置及范围、胰腺坏死组织区域中脏器和血管间关系,选取距腹壁最近、位置相对较低、积液较多处作穿刺点,经1%利多卡因实施局部麻醉,经超声导引刺入穿刺针,回抽有炎性坏死液体则提示穿刺成功,撤出针芯置入14 F引流管,抽出液体状坏死组织,以生理盐水清洗,连接无菌引流袋,引流管固定,每日观察引流液状况,待引流液培养无细菌、机体状况好转、引流液量<10 mL/24 h则可拔管。研究组在对照组基础上予通腑化瘀解毒方:白芷10 g,牡丹皮10 g,桃仁 15 g,赤芍 15 g,黄芩 12 g,柴胡 15 g,连翘15 g,金银花15 g,紫花地丁 g,蒲公英15 g,厚朴15 g,延胡索15 g,枳壳10 g,芒硝6 g,生大黄15 g。以水煎煮,每日1剂,收汁200 mL,早晚分2次经鼻肠管或胃管灌入,共治疗10 d。
1.4 观察项目 1)统计两组症状改善时间。2)抽取所有患者空腹静脉血4 mL,离心(3 000 r/min,10 min)取上清液,以美国Bio-RAD公司Bio-RAD550型酶标仪与配套试剂盒经酶联免疫吸附法测定P物质、前列环素I2(PGI2)及血浆血栓素2(TXA2)水平、炎性因子[白细胞介素-4(IL-4)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)],经竞争性酶联免疫吸附试验测定胰蛋白酶原激活肽(TAP)水平。3)统计两组治疗前后腹腔积液及腹内压,腹腔积液高度及腹内压经腹部B超检查测定。
1.5 疗效标准 参考文献[8]拟定。CT或B超检查提示腹腔积液及胰腺周边坏死组织消失,临床症状缓解为治愈;CT或B超检查提示腹腔积液及胰腺周边坏死组织减少≥50%,<100%,临床症状明显缓解为显效;CT或B超检查提示腹腔积液及胰腺周边坏死组织减少≥25%,<50%,临床症状有所改善为有效;未至上述标准为无效。总有效率=(治愈例数+显效例数+有效例数)/总例数×100%。
1.6 统计学处理 应用SPSS25.0统计软件。计量资料以(±s)表示,采用t检验,计数资料n(%)表示,χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组症状改善时间比较 见表1。研究组发热、腹内积液、呕吐恶心、腹胀、腹痛消失及恢复排便排气、肠鸣音恢复时间均短于对照组(P<0.05)。
表1 两组症状改善时间比较(d,±s)

表1 两组症状改善时间比较(d,±s)
与对照组比较,△P<0.05。下同
组别研究组对照组n 41 41发热消失9.11±2.71△12.05±2.87腹内积液消失9.35±2.01△12.26±2.39呕吐恶心消失5.61±1.18△7.56±1.73腹胀消失6.82±1.38△9.01±2.29腹痛消失6.55±1.53△8.35±2.08恢复排便排气1.74±0.56△2.21±0.69肠鸣音恢复1.66±0.45△2.18±0.54
2.2 两组临床疗效比较 见表2。研究组总有效率高于对照组(P<0.05)。

表2 两组临床疗效比较(n)
2.3 两组治疗前后P物质及TAP水平比较 见表3。治疗后两组P物质及TAP水平较治疗前降低,且研究组低于对照组(P<0.05)。
表3 两组治疗前后P物质及TAP水平比较(±s)

表3 两组治疗前后P物质及TAP水平比较(±s)
与本组治疗前比较,∗P<0.05;与对照组治疗后比较,△P<0.05。下同
组别研究组(n=41)对照组(n=41)时间治疗前治疗后治疗前治疗后P物质(pg/mL)637.62±102.67 359.72±89.36*△641.51±105.78 454.71±92.28*TAP(nmol/L)46.10±10.69 19.31±7.81*△44.96±11.12 25.63±8.08*
2.4 两组治疗前后PGI2及TXA2水平比较 见表4。治疗后两组PGI2水平均较治疗前增高、TXA2水平均较治疗前降低,且研究组PGI2水平高于对照组、TXA2水平低于对照组(P<0.05)。
表4 两组治疗前后PGI2及TXA2水平比较(pg/L,±s)
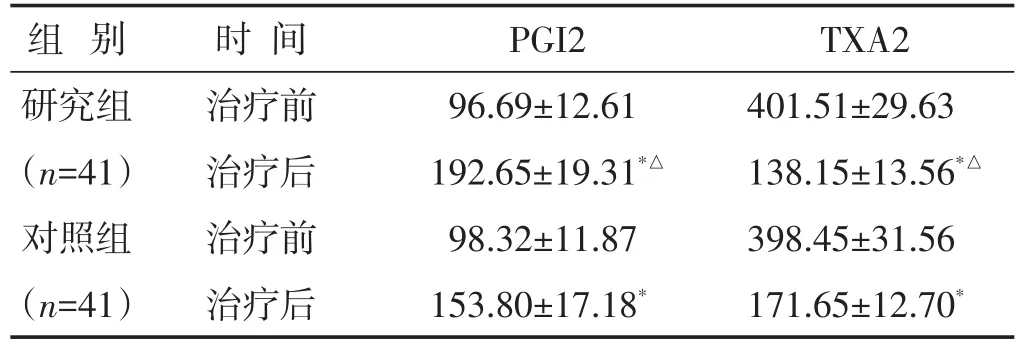
表4 两组治疗前后PGI2及TXA2水平比较(pg/L,±s)
组别研究组(n=41)对照组(n=41)时间治疗前治疗后治疗前治疗后PGI2 96.69±12.61 192.65±19.31*△98.32±11.87 153.80±17.18*TXA2 401.51±29.63 138.15±13.56*△398.45±31.56 171.65±12.70*
2.5 两组治疗前后炎性因子水平比较 见表5。治疗后两组IL-4水平均较治疗前增高,IL-6、TNF-α血清水平均较治疗前降低,且研究组IL-4水平高于对照组,IL-6、TNF-α血清水平低于对照组(P<0.05)。
2.6 两组治疗前后腹腔积液高度及腹内压比较 见表6。治疗后两组腹腔积液高度及腹内压较治疗前降低,且研究组低于对照组(P<0.05)。
表5 两组治疗前后炎性因子水平比较(ng/L,±s)
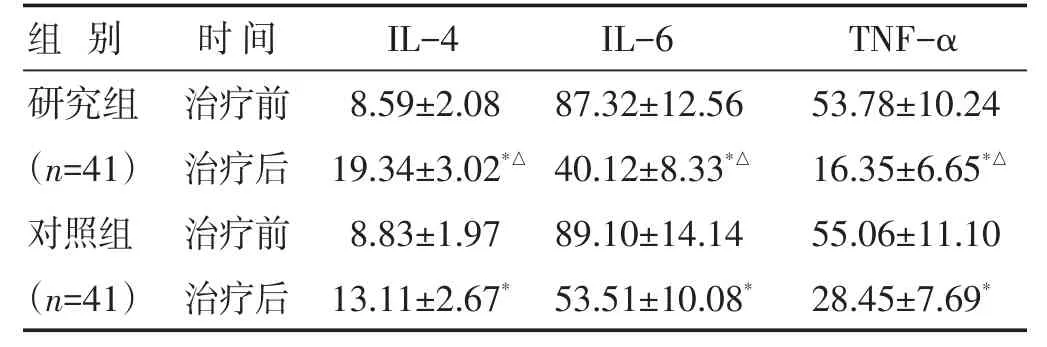
表5 两组治疗前后炎性因子水平比较(ng/L,±s)
研究组(n=41)对照组(n=41)治疗前治疗后治疗前治疗后8.59±2.08 19.34±3.02*△8.83±1.97 13.11±2.67*87.32±12.56 40.12±8.33*△89.10±14.14 53.51±10.08*53.78±10.24 16.35±6.65*△55.06±11.10 28.45±7.69*
表6 两组治疗前后腹腔积液高度及腹内压比较(±s)
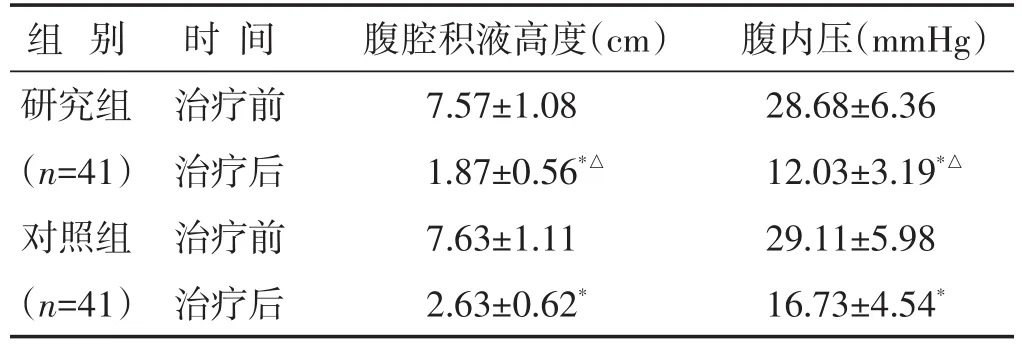
表6 两组治疗前后腹腔积液高度及腹内压比较(±s)
组别研究组(n=41)对照组(n=41)时间治疗前治疗后治疗前治疗后腹腔积液高度(cm)7.57±1.08 1.87±0.56*△7.63±1.11 2.63±0.62*腹内压(mmHg)28.68±6.36 12.03±3.19*△29.11±5.98 16.73±4.54*
3 讨 论
SAP为胰腺蛋白酶自身消化作用所致胰腺病变,具备病情重、进展迅速、发病急等特征,且发病后合并胰腺感染可进一步增加疾病转归难度[9-10]。因此,SAP合并胰腺感染发病后应及时实施有效治疗。
PCD为临床常用外科引流术,可有效引流出液化坏死组织,减小坏死组织及胸腹腔压力,阻止细菌毒素吸收,减轻体内炎性反应程度[11-12]。同时,PCD术中所用穿刺管可损坏组织引流,阻止病菌毒素吸收至血液循环,且术中根据B超实施操作,可避开肠管及大血管,避免细菌逆行至液体聚集区引发感染,调节全身与局部状态,保护部分可逆转性胰腺坏死组织[13-14]。但本研究中,仅采取PCD治疗的对照组患者总有效率仅为75.61%,仍存在一定提升空间。此外,近年来中医在多种疾病中的治疗优势及价值得到普遍关注。中医对SAP具有深刻认知,并根据其发病机制、病因病机将其归类于“腹痛”等范畴,认为疾病发生主要是因饮食不节,饮酒过度,过食肥甘辛辣,致使胃肠熟腐传导失司,肝胆疏泄失职;或外感六淫之邪,入里化热,里热炽盛,中焦积热,因热致瘀,造成肝气郁结、脾失健运,湿热邪毒壅积,腑气堵塞[15-16]。因此,疾病治疗应以清热解毒、活血化瘀、通里攻下等为基本原则。本研究所用通腑化瘀解毒方中,白芷可止痛排脓活血;牡丹皮、桃仁、赤芍擅消肿排脓、凉血解毒、活血化瘀;黄芩、柴胡能清热解郁、疏肝利胆;连翘、金银花、地丁、蒲公英功可清热解毒,解表宣肺强化大肠传导之功;延胡索、枳壳能活血散瘀、行气止痛;厚朴、芒硝、生大黄有行气逐瘀、通腑泄热功效;诸药联用共奏化瘀止痛、疏肝利胆、清热解毒、通腑理气之功。现代药理学研究证实,生大黄中芦荟大黄素、大黄酸、大黄酚、大黄泻素可刺激大肠,强化肠蠕动促使排便,且大黄蒽醌衍生物具备抗菌功效;芒硝有效成分为硫酸钠,其能阻止肠内水分吸收,增大肠内容体积,造成机械刺激,并促进肠蠕动;厚朴包含挥发油,其能兴奋肠管,抗菌谱广,能抑制痢疾杆菌、溶血性链球菌、金黄色葡萄球菌;枳壳包含黄酮类及挥发油成分,促进胃肠运动收缩节律增强[17]。本研究结果显示,治疗后研究组症状改善用时短于对照组,腹腔积液高度及腹内压低于对照组,IL-4、IL-6、TNF-α改善幅度较对照组更加显著,且总有效率显著高于对照组。IL-6、TNF-α为临床常见促炎细胞因子,可通过活化蛋白激酶C及酪氨酸激酶-2诱导胰腺细胞凋亡,并损坏胰腺组织微循环,加剧胰腺水肿及缺血坏死;IL-4则属于抗炎细胞因子,能有效对抗促炎因子所诱导炎性反应。因此上述结果可证实,PCD及通腑化瘀解毒方联合干预方案可更有效减轻SAP合并胰腺感染患者炎性反应,缓解临床症状,减小腹腔积液高度及腹内压,提高疾病治疗效果。
本研究结果还显示,治疗后研究组PGI2水平高于对照组、TXA2水平低于对照组。PGI2及TXA2具有血管舒张及收缩作用,可维持胰腺微循环平衡,其中TXA2能促使血小板聚集、收缩血管,致使凝血功能异常,直接损害血管内皮细胞;PGI2可拮抗TXA2,抑制血小板聚集与激活,保护血管内皮细胞,两者水平紊乱后可造成血栓形成、血小板聚集、微小动静脉痉挛收缩,最终引发微循环障碍,加剧病情[18]。故联合应用PCD及通腑化瘀解毒方可更有效地调节PGI2、TXA2含量,减轻SAP合并胰腺感染病情。此外,本研究还对SAP合并胰腺感染患者治疗前后P物质及TAP变化情况进行探究分析。TAP为处于脊椎动物胰蛋白酶原氨基末端激活肽,属胰蛋白酶原所激活降解产物,被胰蛋白酶原活化后可释放至血液循环、尿液及腹腔,而SAP发病机制在于胰蛋白酶原异常激活引发自身腺体消化,故检测其表达情况可评估病情及治疗效果[19]。而P物质为脑肠肽,其作为神经末梢所生成神经传递因子蛋白,可促使血浆外渗,参与SAP炎性反应,并和胰肠道损伤、胰腺微循环及外分泌[20]。研究结果显示,治疗后研究组P物质及TAP水平低于对照组,表明PCD及通腑化瘀解毒方联合治疗方案治疗SAP并胰腺感染,可显著降低P物质及TAP水平,进一步证实其能提高疾病治疗效果。
综上所述,联合采取PCD及通腑化瘀解毒方治疗SAP并胰腺感染,可有效缓解患者临床症状,降低腹腔积液高度及腹内压,提高疾病治疗效果,其原因可能与调节P物质及TAP、PGI2及TXA2含量、减轻炎性反应具有一定关联性。
