超高效液相色谱-串联质谱法检测动物源性食品中的β-受体激动剂类和喹诺酮类物质
2020-05-07刘新辉马小岭季秋红
刘新辉,马小岭,季秋红
(1.山东拜尔检测股份有限公司,山东 潍坊261000;2.山东匠造检测有限公司,山东 潍坊,261000)
β-受体激动剂属于苯乙醇胺类药物,是儿茶酚胺、肾上腺素和去甲肾上腺素的化学类似物,主要有克伦特罗、沙丁胺醇、莱克多巴胺、特布他林、非诺特罗、西布特罗、氯丙那林、西马特罗、马布特罗、马喷特罗、溴布特罗、喷布特罗等。这类药物对心脑血管疾病、糖尿病、冠心病、甲状腺功能亢进、青光眼、前列腺肥大者有不良影响;另外,孕妇中毒可导致癌变、胎儿致畸。我国现行标准GB 31650—2019“整顿办函〔2010〕50号”规定β-受体激动剂属于禁止用于所有食品动物的兽药。喹诺酮是以1,4-二氢-4-氧吡啶-3-羧酸为基本母环结构的化合物,是从萘啶酸或吡酮酸演化而来的合成抗菌药物,主要有洛美沙星、氟甲喹、环丙沙星、达氟沙星、伊诺沙星、氟罗沙星、诺氟沙星、氧氟沙星、培氟沙星、恩诺沙星、沙拉沙星等。动物性食品中残留较低浓度的药物容易诱导人类致病菌产生耐药性;在较高剂量下,出现站立不稳、烦躁不安、嗜睡等中枢神经系统症状。2015年农业农村部(原农业部)发布的第2292号公告中禁止将洛美沙星、培氟沙星、氧氟沙星、诺氟沙星等4种喹诺酮类抗菌药物用于食品动物。目前测定β-受体激动剂类和喹诺酮类药物的方法有光谱分析、免疫分析[1]、生物传感器技术、毛细管电泳法[2]、气相色谱法[3]、液相色谱法[4]、气相色谱串联质谱法、液相色谱串联质谱法等。现行国家标准β-受体激动剂类的色谱检测方法均需经过酶解,酶解时间需12 h以上[5-6],且萃取试剂较为复杂,重现性差。本研究采用酸水解法,前处理时间短,成本低,抗干扰能力强,可实现β-受体激动剂类和喹诺酮类药物的准确定性和定量。
1 材料与方法
1.1 材料与试剂
Cleanert LipoNo购自天津博纳艾杰尔科技有限公司;乙腈、甲醇、乙酸、乙酸铵、甲酸均为色谱纯,购自德国CNW公司;氯化钠为优级纯,购自中国国药集团化学试剂有限公司;克伦特罗(批号50223)、非诺特罗(批号40618AL)、洛美沙星(批号115068)、氟甲喹(批号40110)、环丙沙星(批号41006)、达氟沙星(批号40428)、伊诺沙星(批号30913)、氟罗沙星(批号40505)、诺氟沙星(批号41015)、氧氟沙星(批号21016)、培氟沙星(批号40716)购自德国Dr.Ehrensorfer标准品公司;西布特罗(批号271542)、西马特罗(批号292231)、马布特罗(批号120805)、诺氟沙星-D5(批号291528)、环丙沙星-D8(批号231722)购自德国WITEGA标准品公司;沙丁胺醇(批号170714)、莱克多巴胺(批号170303)、特布他林(批号B0002575)、氯丙那林(批号B0001425)、马喷特罗(批号160414)、溴布特罗(批号160414)、喷布特罗(批号24731)、克伦特罗-D9(批号160414)、莱克多巴胺-D6(批号170427)、沙丁胺醇-D3(批号170222)、氧氟沙星-D3(批号160713)购自北京曼哈格生物科技有限公司;恩诺沙星(批号A1808204)、沙拉沙星(批号A1806133)购自北京坛墨质检科技有限公司;恩诺沙星-D5(批号NY1701036a)购自农业部农产品质量标准研究中心。
1.2 仪器与设备
Agilent 1290Ⅱ-6460QQQ (配有电喷雾离子源(ESI)及Masshunter Quantitative B.08.00数据处理系统),美国Agilent公司;AS-E40UVT-R纯水仪,重庆奥思德仪器设备有限公司。
1.3 标准溶液配制
单一标准溶液,称取12种激动剂、11种喹诺酮及7种内标标准物质各10 mg(精确到0.01 mg)用甲醇溶解,定容至10 mL容量瓶中,配制成1.0 g/L的单一标准储备液,在-20 ℃下保存待用;混合标准溶液,从上述单一标准储备液中各吸取1 mL溶液于50 mL容量瓶中,以甲醇将其稀释定容为20 mg/L的混合储备液,吸取混合储备液250 μL于50 mL容量瓶中,以甲醇将其稀释定容为100 Hg/L的混合工作液,于4 ℃下避光保存;按同样方式将7种内标稀释为100 Hg/L的混合内标工作液,于4 ℃下避光保存。
1.4 方法
1.4.1 色谱条件
色谱柱:Agilent ZORBAX Eclipse Plus C18色谱柱(3.0×100 mm,1.8-Micron);流动相:A为5 mmol/L乙酸铵水溶液(含0.1%甲酸,质量分数),B为甲醇(含0.1%甲酸,质量分数);流速0.4 mL/min;柱温35 ℃;进样量2 μL;采用梯度洗脱程序:0~2 min,10%B;2~3 min,10%~60%B;3~4 min,60%B;4~5 min,60%~90%B;5~7 min,90%B;7~8 min,90%~10%B;8~10 min,10%B。
1.4.2 质谱条件
三重四级杆质谱仪,配有电喷雾离子源(ESI),干燥气温度为325 ℃,干燥气流速为9 L/min,鞘气温度为350 ℃,鞘气流速为10 L/min,雾化器压力为27.6 Pa。采用多反应监测(MRM)模式进行分析,正离子扫描,具体的质谱条件如表1所示。
表1 23种兽药及7种内标的质谱检测条件
Table 1 The mass spectrometric detection conditions for 23 veterinary drugs and seven internal standard materials
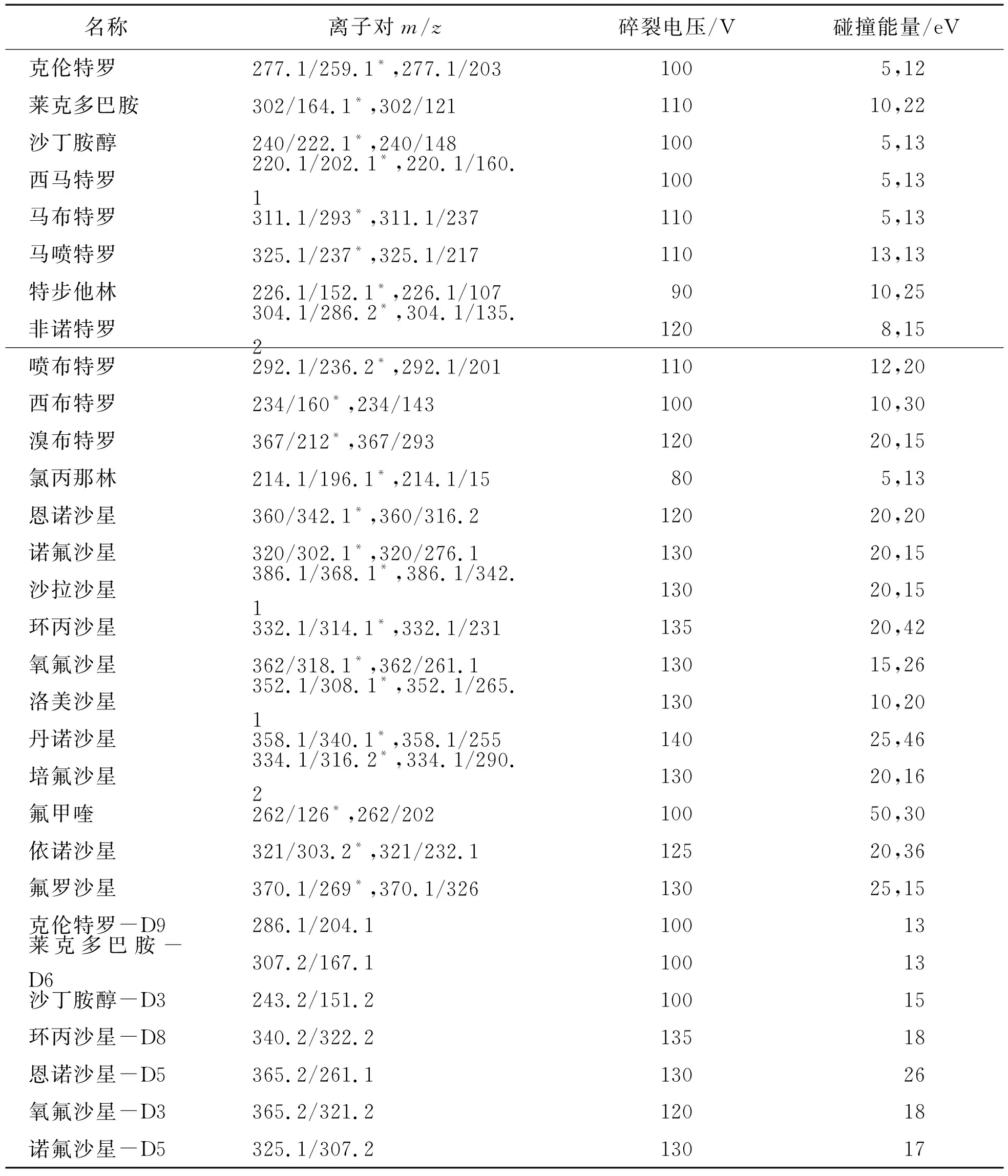
名称离子对m/z碎裂电压/V碰撞能量/eV克伦特罗 277.1/259.1*,277.1/2031005,12莱克多巴胺302/164.1*,302/12111010,22沙丁胺醇 240/222.1*,240/1481005,13西马特罗 220.1/202.1*,220.1/160.11005,13马布特罗 311.1/293*,311.1/2371105,13马喷特罗 325.1/237*,325.1/21711013,13特步他林 226.1/152.1*,226.1/1079010,25非诺特罗 304.1/286.2*,304.1/135.21208,15喷布特罗 292.1/236.2*,292.1/20111012,20西布特罗 234/160*,234/14310010,30溴布特罗 367/212*,367/29312020,15氯丙那林 214.1/196.1*,214.1/15805,13恩诺沙星 360/342.1*,360/316.212020,20诺氟沙星 320/302.1*,320/276.113020,15沙拉沙星 386.1/368.1*,386.1/342.113020,15环丙沙星 332.1/314.1*,332.1/23113520,42氧氟沙星 362/318.1*,362/261.113015,26洛美沙星 352.1/308.1*,352.1/265.113010,20丹诺沙星 358.1/340.1*,358.1/25514025,46培氟沙星 334.1/316.2*,334.1/290.213020,16氟甲喹 262/126*,262/20210050,30依诺沙星 321/303.2*,321/232.112520,36氟罗沙星 370.1/269*,370.1/32613025,15克伦特罗-D9286.1/204.110013莱克多巴胺-D6307.2/167.110013沙丁胺醇-D3243.2/151.210015环丙沙星-D8340.2/322.213518恩诺沙星-D5365.2/261.113026氧氟沙星-D3365.2/321.212018诺氟沙星-D5325.1/307.213017
注:碎片离子中标*为定量离子。
1.4.3 样品前处理
提取:准确称取5.0 g样品(精确至0.01 g)放入50 mL离心管中,加入5 mL 1%乙酸水溶液,加入内标工作溶液100 μL,旋涡混匀10 min。加入10 mL乙腈,于振荡器上剧烈震荡30 min,再加入2 g氯化钠,旋涡混匀2 min,在8 000 r/min条件下离心5 min。
净化:移取5 mL上清液于Cleanert LipoNo净化管中,旋涡混匀2 min,静置分层。移取2 mL上清液在50 ℃下氮气吹干,采用1 mL初始流动相复溶,过0.22 μm滤膜后待测定。
2 结果与分析
2.1 提取剂的选取
结合以往的研究经验,考察了1%乙酸水-乙腈、1%乙酸乙腈[7]、1%盐酸乙腈、乙腈4种提取溶剂,得到回收率及精密度。结果显示:通过1%乙酸水-乙腈作提取溶剂,样品分散效果最好,先加乙酸水后加乙腈的提取方式,避免了样品因蛋白质变性而发生凝结的现象[8],故回收率和精密度效果最好。乙腈的回收率和精密度最低,分析原因是缺少酸解,目标物无法从轭合物形态转化为游离态,且乙腈会导致蛋白质变性凝结,部分目标物无法充分释放;采用1%乙酸乙腈和1%盐酸乙腈提取,同样会发生凝结,回收率比乙腈稍高,但低于1%乙酸水-乙腈的提取方式。
2.2 净化方法的确定
比较了Cleanert LipoNo、C18和PSA[9]、乙腈饱和正己烷3种净化方式。Cleanert LipoNo为大颗粒填料,无需离心,操作进一步简化,对甘油一酯、甘油二酯、甘油三酯均有良好的吸附效果,比其他填料具有更好的去除脂类物质的性能;C18和PSA能吸附油脂和有机酸[10],但需要经过离心,且复溶液澄清度低,重现性差;因动物源性食品的提取液中含有大量油脂及蛋白,利用乙腈饱和正己烷净化,易发生乳化现象[11-12],无法进行后续检测。
2.3 色谱和质谱条件的优化
目标物经色谱分离时,流动相、进样介质及体系均会影响色谱峰型[13],使用甲醇-水作为流动相时,化合物色谱峰会展宽、拖尾、灵敏度降低,在水相中加入乙酸铵和甲酸后可改善目标物的峰型[14],促进目标物的离子化[15],因此,选择5 mmol/L乙酸铵水溶液(含0.1%甲酸)-甲醇(含0.1%甲酸)为最佳流动相[16]。23种目标物及7种内标物质检测在10 min内完成,结果显示在既定时间内所有目标化合物均出现峰值,且峰型尖锐对称,进样分析时间短,分离度满足要求[17-18]。
2.4 方法学考察
线性范围与定量限:完成前处理与仪器测定的优化后,可据此配制混合工作液进行后续实验分析,X轴设定为质量浓度,Y轴设定为峰面积,由此完成标准曲线的绘制并进行线性回归。所得结果表明23种兽药的质量浓度范围为0.5~20 Hg/L时,线性关系良好,相关系数R取值范围为0.996 2~0.999 9,具备实验的可行性;同时,以S/N≥10(信噪比≥10)确定方法的定量限质量分数为(0.43~1.02)μg/kg,具体结果如表2所示。
方法的准确度与精密度:选取阴性样品基质,将配制的质量分数为0.5,1.0和2.5 μg/kg的混合标准溶液加入其中,按照确定的提取、净化方法在选定的仪器条件下进行测定,每个浓度水平重复测定6次,计算所得平均回收率为80.2%~106.0%,相对标准偏差RSD为0.52%~9.52%,满足了复杂样品基质中高通量痕量残留检测需求[19]。
表2 23种兽药的相关系数、定量限与回收率
Table 2 Related coefficient,quantitative limit and recovery rate of 10 veterinary drugs

名称RLOQ/(μg/kg)加标量0.5 μg/kg回收率/%RSD/%加标量1.0 μg/kg回收率/%RSD/%加标量2.5 μg/kg回收率/%RSD/%克伦特罗0.998 90.4395.62.0695.33.3391.95.11莱克多巴胺0.996 90.4894.81.2299.62.9897.41.29沙丁胺醇0.997 40.4896.52.0598.77.15102.65.02西马特罗0.998 10.4989.38.0789.60.5295.23.96马布特罗0.996 70.5090.19.0786.92.8789.98.20马喷特罗0.997 50.5080.25.5190.73.8591.63.40特布他林0.998 00.4883.66.0088.71.5988.55.26非诺特罗0.998 60.49105.18.4193.24.9890.63.21喷布特罗0.996 80.5092.94.4584.65.2689.91.09西布特罗0.999 10.4888.56.0290.87.5190.52.22溴布特罗0.998 70.5097.33.4182.95.8294.82.56氯丙那林0.997 60.5096.21.5892.86.4191.73.65恩诺沙星0.997 60.80100.22.2995.62.8596.90.95诺氟沙星0.999 01.0298.63.8594.81.9198.71.23沙拉沙星0.997 31.00109.24.47105.77.6296.96.54环丙沙星0.991 40.80101.36.0994.31.0196.52.25氧氟沙星0.987 10.8590.65.8888.82.0597.63.96洛美沙星0.991 90.9088.27.0684.18.7590.35.62丹诺沙星0.980 51.0085.32.4190.26.9591.82.65培氟沙星0.986 31.0092.76.8591.84.1888.87.41氟甲喹0.969 71.0087.25.4192.63.9693.94.98依诺沙星0.981 71.0091.63.9593.15.8198.63.85氟罗沙星0.986 51.0093.54.82106.03.4090.59.52
2.5 实际样品测定
随机购买10种不同的动物源性食品,根据上述方法对其进行UHPLC-MS/MS测定,检出项目结果如表3所示,鸡肉、鸭肉、鲫鱼、草鱼等4种动物源性食品中均含有恩诺沙星,根据GB 31650—2019的相关规定,恩诺沙星(以恩诺沙星与环丙沙星之和计)在动物肌肉中的限量质量分数为100 μg/kg,而实测结果显示鲫鱼、草鱼中恩诺沙星的残留量分别为132,103 μg/kg,均超出最大残留限量;克伦特罗为禁止检出的药物,依据现有标准定量限在0.5 μg/kg,但检测结果该种兽药在羊肉中的残留量为0.92 μg/kg,也存有超标现象。这说明在水产养殖的过程中应控制相应喹诺酮类药物的使用量;而克伦特罗属于农业农村部明文规定禁止用于所有食品动物的兽药,在养殖过程中应禁止添加β-受体激动剂的药物。标准品、鸡肉样品、羊肉样品的总离子流图(TIC)分别如图1~3所示;西马特罗、特布他林、沙丁胺醇、西布特罗、非诺特罗、氟罗沙星、氧氟沙星、培氟沙星、依诺沙星、诺氟沙星、莱克多巴胺、环丙沙星、恩诺沙星、丹诺沙星、洛美沙星、氯丙那林、沙拉沙星、克伦特罗、溴布特罗、马布特罗、马喷特罗、氟甲喹、喷布特罗的色谱图及质谱图如图4所示。

表3 10种样品的UHPLC-MS/MS检出项目的检测结果Table 3 UHPLC-MS/MS test results of 10 samples μg/kg
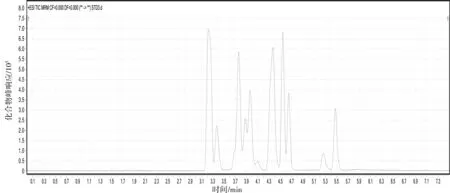
图1 标准品总离子流图Fig.1 TIC of standard products

图2 鸡肉样品总离子流图Fig.2 TIC of chicken sample

图3 羊肉样品总离子流图Fig.3 TIC of mutton sample
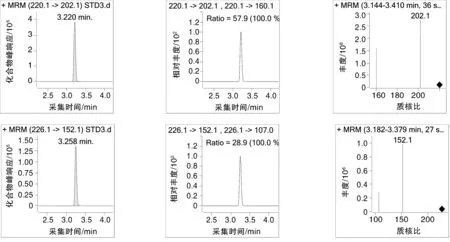
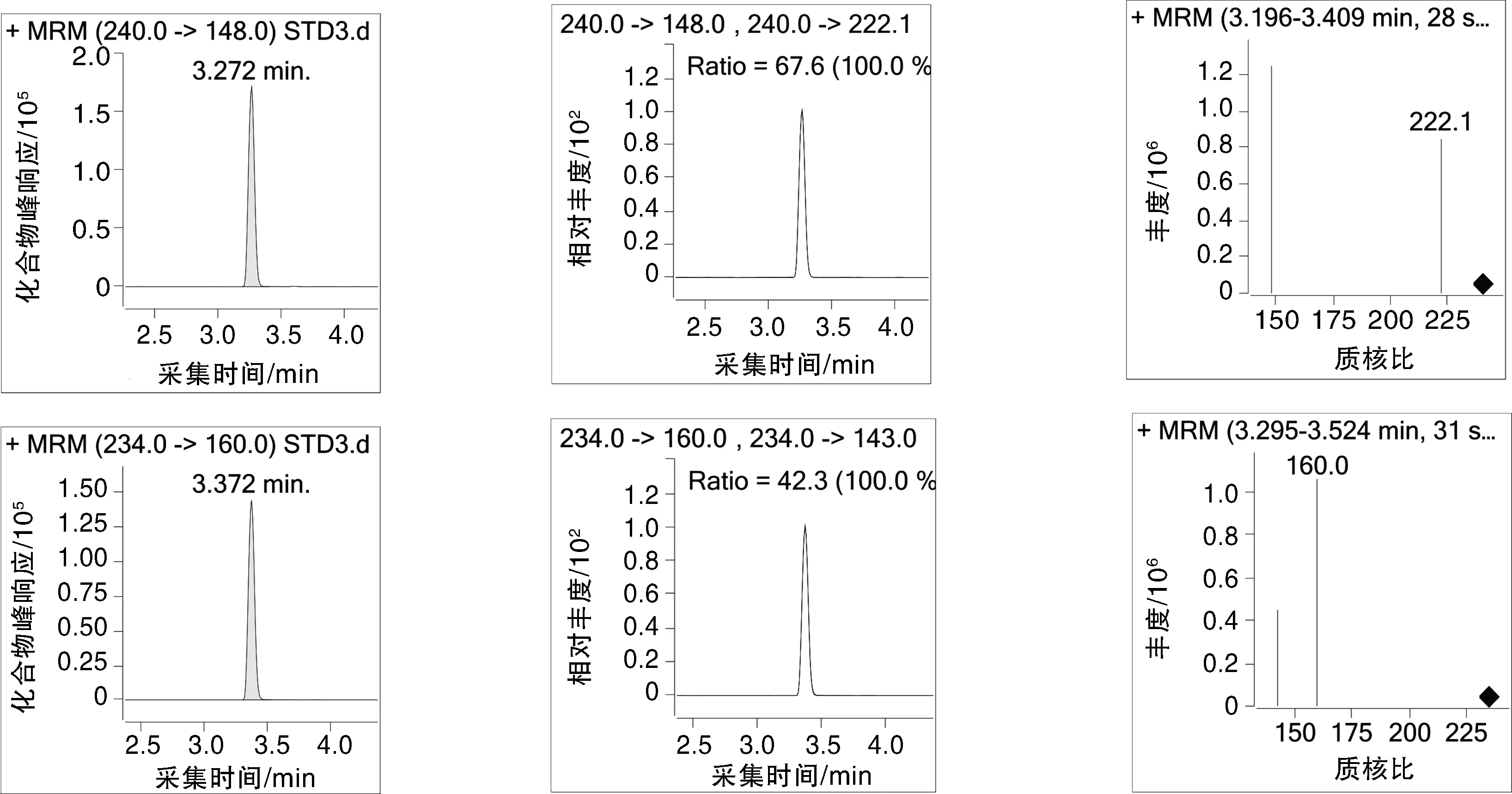
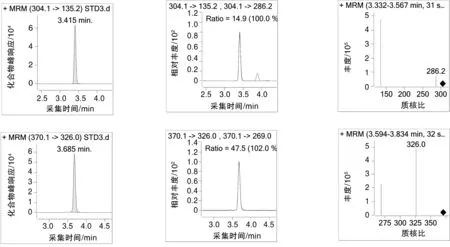
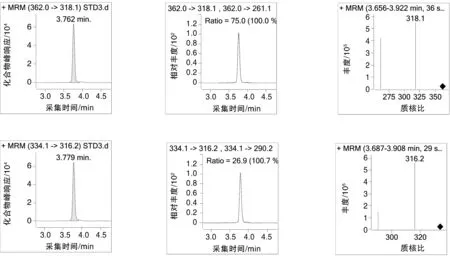
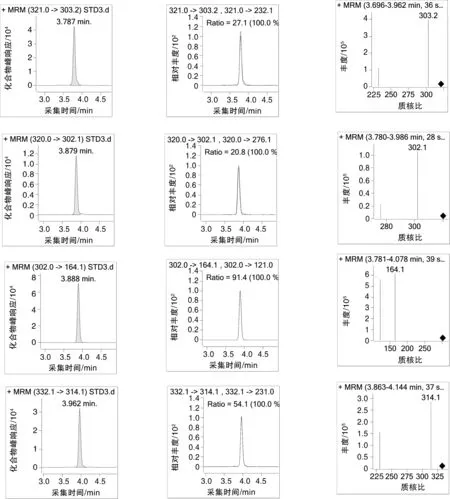
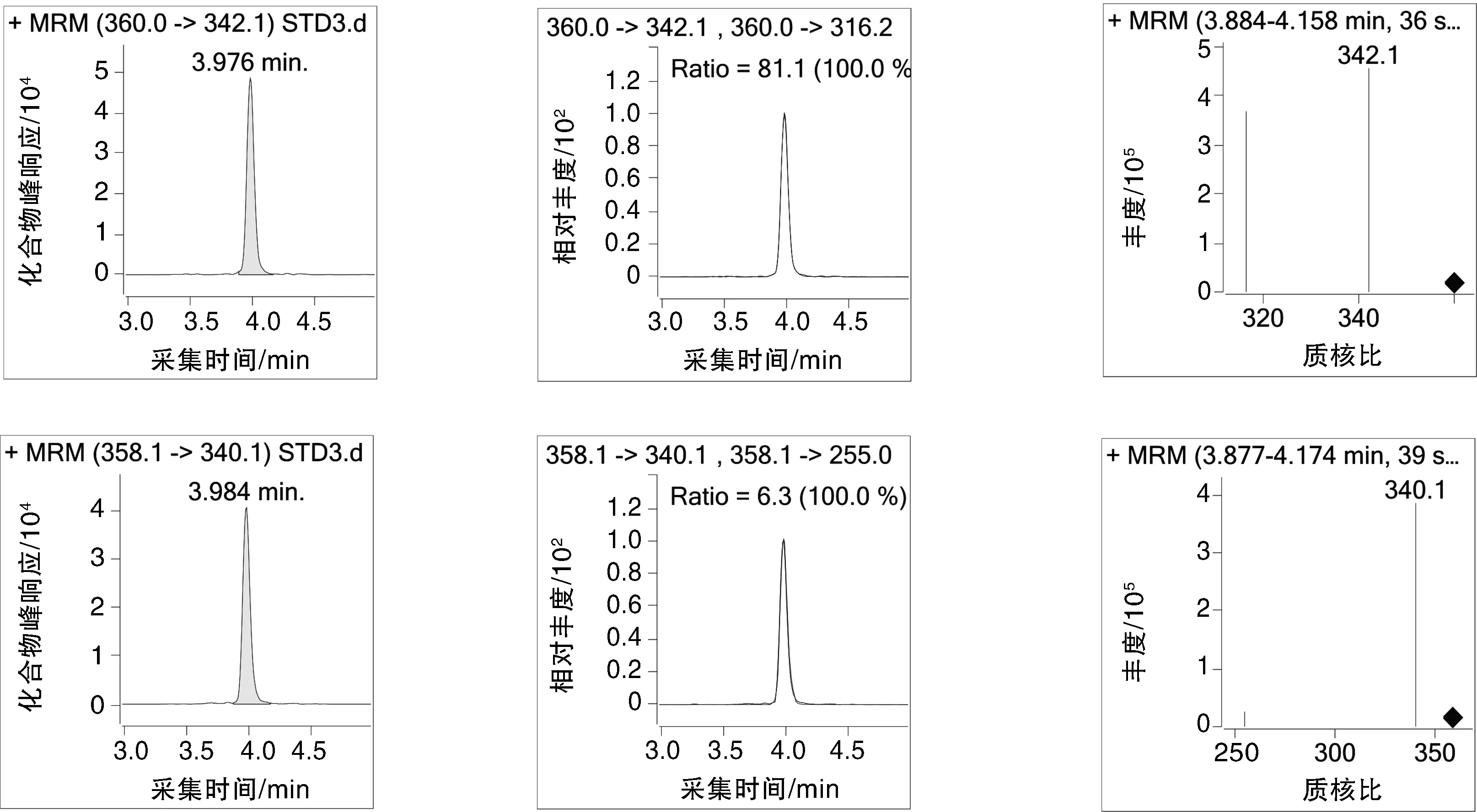
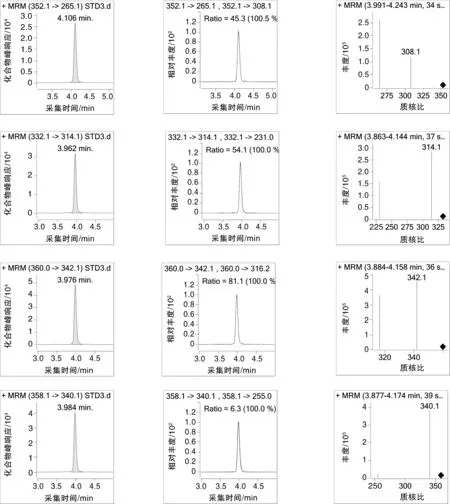
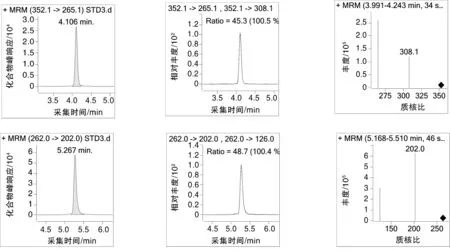
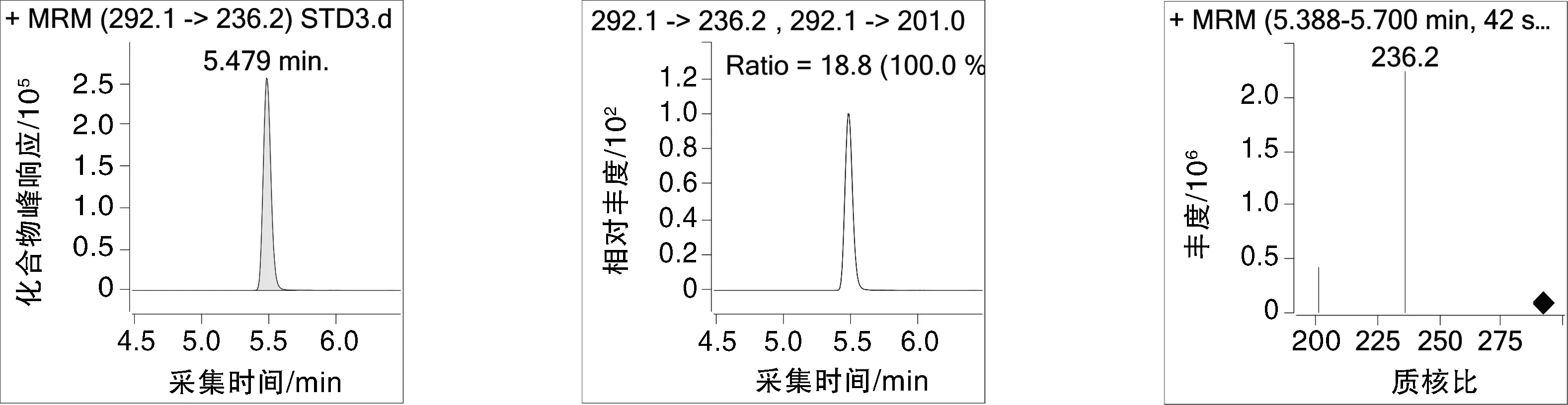
图4 23种兽药的色谱图及质谱图Fig.4 Chromatography and mass spectrograph of 23 veterinary drugs
3 结论
通过优化提取溶剂、净化方法和流动相条件,建立了动物源性食品中的12种β-受体激动剂类和11种喹诺酮类物质的液相色谱-串联质谱检测方法。本方法与国家标准方法比较,操作简便,成本低,抗干扰能力强,重现性高,灵敏度高,选择性强。
