替吉奥与卡培他滨同步放疗治疗复发性结直肠癌疗效与安全性的Meta分析
2020-05-06郭雪石学军
郭雪 石学军

摘要:目的 对替吉奥与卡培他滨同步放疗在复发性结直肠癌的疗效及安全性進行Meta分析。方法 2017年9月~2019年12月计算机检索PubMed、The Cochrane Library、Embase、VIP、CKNI、万方数据库,按照纳入和排除标准筛选文献和提取资料后,采用RevMan 5.3 软件进行Meta分析。结果 最终纳入8篇文献,包括706例患者。Meta分析结果显示,替吉奥同步放疗较卡培他滨能有效改善复发性结直肠癌的客观缓解率,差异有统计学意义[OR=2.23,95%CI(1.59,3.13)],P<0.00001];替吉奥同步放疗较卡培他滨能有效改善复发性结直肠癌的疾病控制率,差异有统计学意义[OR=3.63,95%CI(2.00,6.57),P<0.0001];第1、第2、第3年生存率比较,差异有统计学意义[OR=3.48,95%CI(1.98,6.13),P<0.0001]、[OR=2.35,95%CI(1.55,3.55),P<0.0001]、[OR=1.94,95%CI(1.30,2.90),P=0.001]。替吉奥同步放疗手足综合征发生率低于卡培他滨同步放疗,差异有统计学意义[OR=0.33,95%CI(0.13,0.81),P=0.02];恶心、呕吐等消化道反应[OR= 0.74,95%CI(0.5,1.10),P=0.14]、放射性直肠炎[OR=0.72,95%CI(0.42,1.24),P=0.24]与对照组比较,差异无统计学意义。结论 在治疗复发性结直肠癌方面,替吉奥同步放疗与卡培他滨同步放疗比较,前者能有效改善客观缓解率,在手足综合征方面具有更良好的安全性。
关键词:替吉奥;卡培他滨;放疗;结直肠癌;Meta 分析
Abstract:Objective To conduct a meta-analysis on the efficacy and safety of simultaneous radiotherapy of Tegafur and capecitabine in recurrent colorectal cancer.Methods The computer searched PubMed, The Cochrane Library, Embase, VIP, CKNI, Wanfang databases, after screening literature and extracting data according to the inclusion and exclusion criteria, using RevMan 5.3 software for Meta analysis from September 2017 to December 2019.Results 8 articles were finally included, including 706 patients. Meta analysis results showed that Tegafur simultaneous radiotherapy can effectively improve the objective remission rate of recurrent colorectal cancer compared with capecitabine, the difference was statistically significant [OR=2.23,95%CI (1.59, 3.13)],P<0.00001];Tegafur simultaneous radiotherapy can effectively improve the disease control rate of recurrent colorectal cancer compared with capecitabine, the difference was statistically significant[OR=3.63,95%CI (2.00,6.57),P<0.0001];Comparison of survival rates in the first, second, and third years respectively, the difference was statistically significant [OR=3.48,95%CI (1.98,6.13),P<0.0001], [OR=2.35,95%CI (1.55,3.55),P<0.0001],[OR =1.94,95%CI(1.30,2.90),P=0.001].The incidence of hand-foot syndrome was lower than capecitabine in simultaneous radiotherapy for Tegafur,the difference was statistically significant[OR=0.33,95%CI (0.13, 0.81),P=0.02]; nausea, vomiting and other gastrointestinal reactions [OR=0.74,95%CI (0.5,1.10),P=0.14], radiation proctitis[OR=0.72,95%CI(0.42,1.24),P=0.24] compared with the control group, the difference was not statistically significant.Conclusion In the treatment of recurrent colorectal cancer, compared with synchronous radiotherapy of Tegafur and capecitabine, the former can effectively improve the objective remission rate and has better safety in hand-foot syndrome.
结直肠癌(colorectal cancer)是危害公众健康的严重疾病之一,目前其发病率在不断上升。有资料显示[1],2018年全球结直肠癌新发病例达到180多万,仅次于肺癌和乳腺癌,居于第3位,比2012年增加了32.6%。我国结直肠癌发病率也在上升阶段,2015年新发病例有38万多,亦位居第3位,位于肺癌和胃癌之后,比2012年增加了17.2%[2,3]。外科治疗被认为是复发性直肠癌的主要治疗方法[4]。然而,因肿瘤扩展到或固定在其他骨盆结构上,只有50%的患者能够再次接受手术治疗[5],因此放、化疗等保守治疗方式是较为适合的治疗手段。目前,卡培他滨或替吉奥均是治疗晚期结直肠癌常用的化疗药物。这两种口服化疗药物因给药方便、毒副反应小等特点在结直肠癌的治疗中具有很大优势[6]。替吉奥是第四代口服氟嘧啶衍生物,单药治疗复发性恶性肿瘤有效率约为40%,同时其具有放疗增敏作用,可以为不能手术治疗的恶性肿瘤患者治疗带来希望[7]。关于替吉奥与卡培他滨单药或联合化疗治疗复发性结直肠癌已有大量研究报道,但相关研究系统评价两者同步放疗的治疗效果报道较少。本研究旨在比较替吉奥与卡培他滨同步放疗治疗复发性结直肠癌的疗效和不良反应,为临床实践提供参考依据。
1资料与方法
1.1文献检索 于2017年9月~2019年12月计算机检索PubMed、The Cochrane Library、Embase、CNKI、VIP、万方数据库,搜索替吉奥与卡培他滨同步放疗在复发性结直肠癌中的随机对照临床试验,英文检索词包括“S-1”“Tegafur”“Capecitabine”“radiotherapy”“colorectal cancer”;中文检索词包括“替吉奥”“卡培他滨”“放疗”“结直肠癌”,并根据入选文献的参考文献进一步扩大检索,检索时限均为各数据库建库起至2019年10月。
1.2纳入标准
1.2.1研究类型 国内外公开发表的随机对照临床试验,语种限制为中文和英文。
1.2.2研究对象 ①确诊为复发性结直肠癌的患者;②患者身体条件可耐受放化疗;③种族、年龄、性別不限。
1.2.3干预措施 试验组为替吉奥联合三维适形放疗,对照组为卡培他滨联合三维适形放疗。
1.2.4结局指标及疗效判定结局指标 ①客观缓解率(ORR);②疾病控制率(DCR);③不良反应:依据实体肿瘤的疗效评价标准1.1 版(Response E-valuation Criteria in Solid Tumors,RECIST Version1.1)进行疗效判定。
1.3排除标准 ①个案报告、综述等;②结果不完整、无法提取数据或未找到全文的文献;③重复研究:同一团队重复报道;④非中、英文文献。
1.4文献数据提取及质量评价 由2名研究人员独立进行文献筛选和数据提取,并进行交叉核对,若遇分歧则由双方讨论并请第三方裁定。数据提取的内容包括:①每篇文章的一般资料,如文献题目、作者、发表年限、临床试验的分期和文献来源等;②研究设计的信息,如研究对象的一般情况、随机化方案、干预措施、盲法、分配隐藏等;③ORR、DCR、不良反应发生率。由2名研究者按Cochrane系统评价手册5.1.0质量评价标准从随机分配方法、分配隐藏、盲法、不完整数据报告、选择性发表及其他偏倚来源等6个方面对纳入文献交叉进行质量评价。对每一项研究结果,分别按照上述6条内容做出“是”(低风险)、“否”(高风险)和“不清楚”(风险未知)的判断。完全满足上述6条质量标准,其发生各种偏倚的可能性最小,质量为A级;≥上述1条描述不清楚者,有发生相应偏倚的中度可能性,质量为B级;≥上述1条未描述者有发生相应偏倚的高度可能性,质量为C级。
1.5统计学方法 采用RevMan 5.3 软件进行Meta 分析。以比值比(OR)及其95%可信区间(CI)为效应量。首先分析各纳入研究的临床异质性,然后采用?字2检验分析其统计学异质性。P>0.1,I2<50%时可认为多个同类研究间具有同质性,选用固定效应模型进行分析;当P<0.1,且I2>50%时,选用随机效应模型合并分析,P<0.05表示差异有统计学意义。
2结果
2.1纳入文献结果 初检出文献552篇,经逐层筛除最终纳入8篇文献,共计706例患者。筛选流程见图1,纳入研究基本信息见表1,偏倚风险见图2。
2.2 Meta分析结果
2.2.1两组ORR比较 纳入8项[8-15]研究均比较了ORR,共706例患者,各研究间异质性检验结果为P=0.37,I2=7%,采用固定效应模型分析。Meta分析结果显示,替吉奥联合放疗组ORR高于对照组,差异有统计学意义[OR=2.23,95%CI(1.59,3.13),P<0.00001],见图3。
2.2.2两组DCR比较 纳入8项[8-15]研究均比较了DCR,共706例患者,各研究间异质性检验结果为P=0.57,I2=0%,采用固定效应模型分析。Meta分析结果显示,替吉奥联合放疗组DCR高于对照组,差异有统计学意义[OR=3.63,95%CI(2.00,6.57),P<0.0001],见图4。
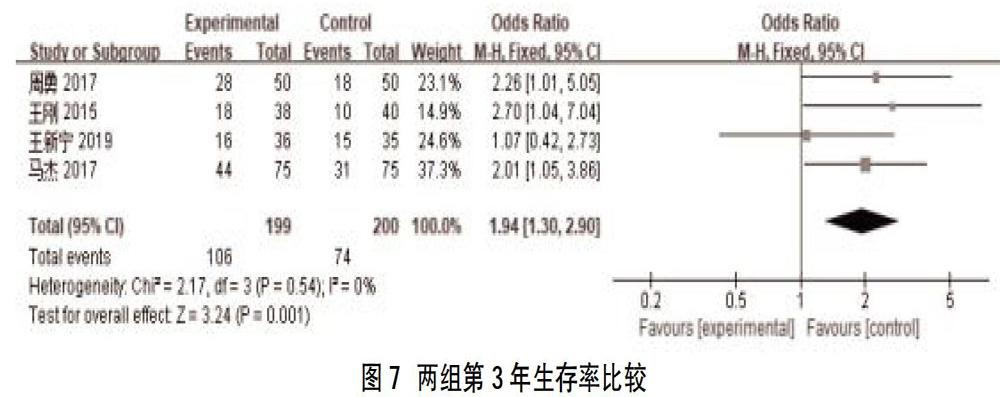
2.2.3两组第1、2、3年生存率比较 均纳入了4项[10,12,14,15]研究,共399例患者,结果显示两组第1、2、3年生存率比较,差异均有统计学意义[OR=3.48,95%CI(1.98,6.13),P<0.0001],[OR=2.35,95%CI(1.55,3.55),P<0.0001],[OR=1.94,95%CI(1.30,2.90),P=0.001],见图5~图7。
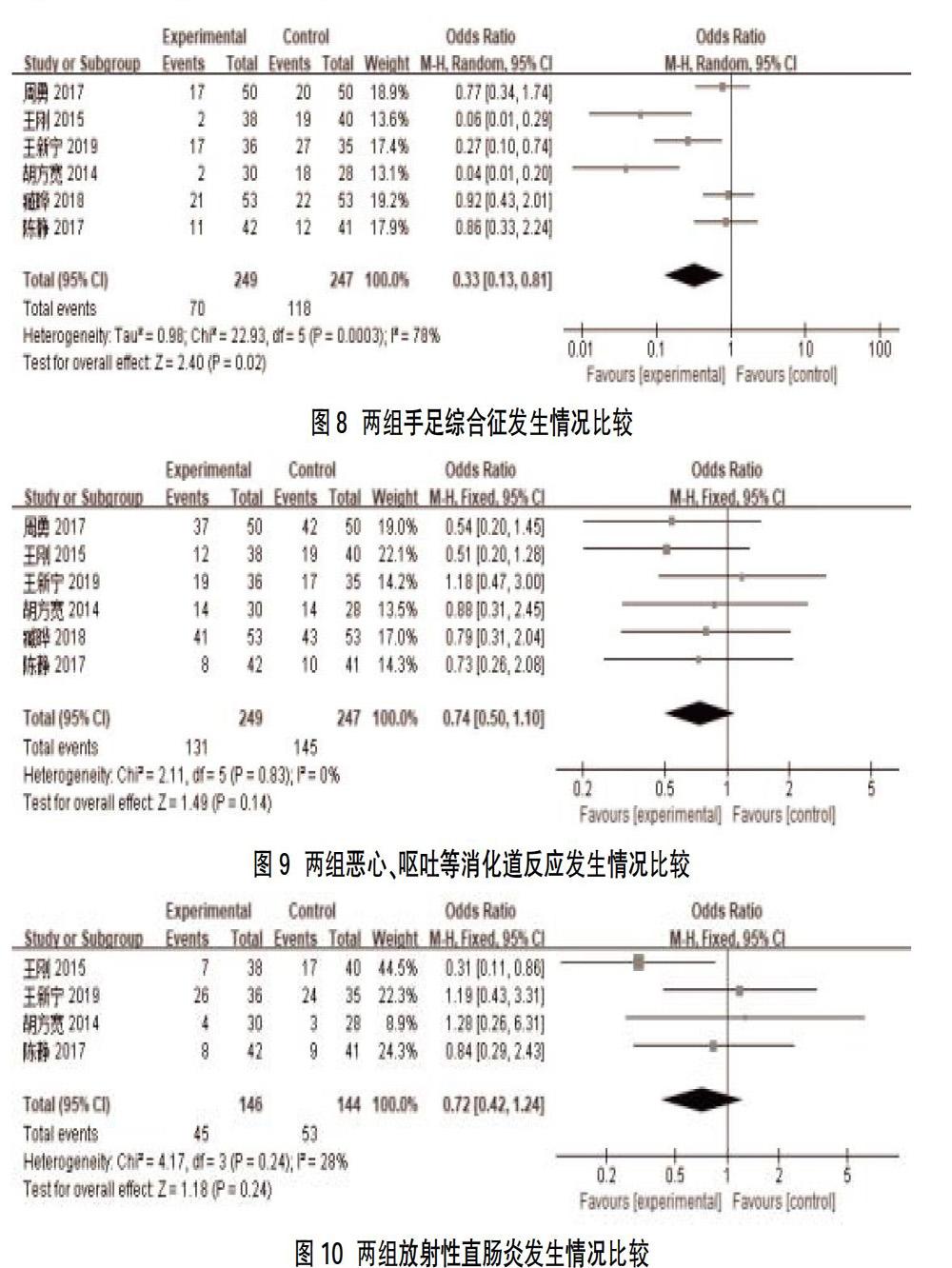
2.2.4两组不良反应发生情况比较 ①手足综合症:共纳入6项[8-10,12-14]研究,496例患者,结果显示两组间比较,差异有统计学意义[OR=0.33,95%CI(0.13,0.81),P=0.02],见图8;②恶心、呕吐等消化道反应:共纳入6项[8-10,12-14]研究,496例患者,两组间比较,差异无统计学意义[OR= 0.74,95%CI(0.5,1.10),P=0.14],见图9。③放射性直肠炎:共纳入4项[8,10,13,14]研究,290例患者,两组比较,差异无统计学意义[OR= 0.72,95%CI(0.42,1.24),P=0.24],见图10。
3讨论
晚期结直肠癌患者治疗主要行姑息性化疗,目前,卡培他滨或替吉奥因给药方便、毒副反应小等特点成为治疗晚期结直肠癌常用的化疗药物[6]。但单纯化疗有效率低,效果欠佳[16],而调强放疗可以最大程度减少放疗所致的毒副作用,是晚期恶性肿瘤的可靠治疗手段之一[17-19]。故采用放化疗同步治疗手段从而提高疗效。卡培他滨是一种抗代谢类药物,其原型无细胞毒性,口服进入人体肿瘤细胞后,形成活性成分5-Fu,5-Fu可以结合进入肿瘤细胞DNA内,干扰增殖復制过程,从而达到抗肿瘤细胞作用[20]。替吉奥是由替加氟、吉美嘧啶、奥替拉西钾组成的复合制剂。替加氟为5-FU的前体药物,可在体内活化为5-FU从而发挥抗肿瘤作用 ;吉美嘧啶抑制5-FU的分解,从而使肿瘤组织中5-FU浓度增加;奥替拉西钾可以阻断5-FU磷酸化从而降低其毒性[21-23]。有研究表明[24],替吉奥一线治疗转移性结直肠癌的有效率可高达55.3%。穆毅等[25]研究发现,复发性直肠癌患者调强放疗联合替吉奥治疗,不但可以提高患者的近期疗效,也可降低血清肿瘤标志物及血管新生标志物水平。
本研究Meta分析结果表明,与卡培他滨相比,替吉奥同步放疗在复发性结直肠癌中能有效提高客观缓解率、疾病控制率及第1、2、3年生存率,可见替吉奥同步放射治疗可有效用于复发性结直肠癌的治疗。安全性方面,替吉奥同步放疗治疗组在手足综合征发生情况比对照组明显降低,差异有统计学意义(P<0.05),考虑替吉奥联合放疗在手足综合征方面具有更良好的安全性。两组治疗在恶心、呕吐等消化道反应及放射性直肠炎方面,差异均无统计学意义(P>0.05)。本研究的局限性在于纳入的文献较少,样本量不多;多数研究未描述随机方法、是否采取盲法及是否对分配方案进行隐藏,存在偏倚可能性较大;本研究集中于亚洲患者,可能存在人种局限性。因此,仍需要更多大样本、多中心的临床随机对照试验来证实。
参考文献:
[1]Bray F,Ferlay J,Soerjomataram I,et al.Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J].CA,2018,68(6):394-424.
[2]郑荣寿,孙可欣,张思维,等.2015中国恶性肿瘤流行情况分析[J].中华肿瘤杂志,2019,41(1):19-28.
[3]陈万青,郑荣寿,张思维,等.2012年中国恶性肿瘤发病和死亡分析[J].中国肿瘤,2016,25(1):1-8.
[4]Moriya Y.Treatment strategy for locally recurrent rectal cancer[J].Jpn J Clin Oncol,2006(36):127-131.
[5]Nielsen MB,Laurberg S,Holm T.Current management of locally recurrent rectal cancer[J].Colorectal Dis,2011(13):732-742. [6]Caceres M,Pascual M,Alonso S,et al.Treatment of colorectal cancer with unresectable metastasis with chemotherapy without primary tumor resection:analysis of tumor-related complications[J].Cir Esp,2014,92(1):30-37.
[7]Nakagawa R,Inoue Y,Ohki T,et al.Erratum to: Efficacy and short-term outcomes of preoperative chemoradiotherapy with intermittent oral tegafur-uracil plus leucovorin in Japanese rectal cancer patients:a single center experience retrospective analysis[J].World J Surg Oncol,2017,15(1):171.
[8]胡方宽,王亚楠,邓业巍,等.替吉奥或卡培他滨同步三维适形放疗治疗中老年复发直肠癌疗效[J].世界华人消化杂志,2014,22(3):439-443.
[9]臧晔.替吉奥化疗同步三维适形放疗治疗复发性结直肠癌的疗效与安全性研究[J].吉林医学,2018,39(5):906-907.
[10]王新宁,赖德星,杜月群,等.调强放疗同步替吉奥化疗治疗局部晚期或复发性直肠癌的临床研究[J].临床医学工程,2019, 26(3):320-322.
[11]顾立强.替吉奥化疗联合三维适形放疗治疗复发性结直肠癌的疗效分析[J].吉林医学,2015,36(5):840.
[12]周勇,杨勇.两种同步放化疗方案对复发性结直肠癌患者生存时间及不良反应的影响[J].检验医学与临床,2017(1411):1565-1567.
[13]陈静.替吉奥或卡培他滨同步三维适形放疗治疗中老年复发直肠癌的临床疗效分析[J].现代诊断与治疗,2017,28(7):1221-1222.
[14]王刚,郝勤玲,刘旭,等.替吉奥或卡培他滨同步三维适形放疗治疗中老年复发直肠癌的临床疗效[J].中国老年学杂志,2015,35(2):344-346.
[15]马杰,姚林果,刘世君,等.替吉奥与卡培他滨同步放疗用于结肠癌根治术后复发患者的效果比较[J].中国药房,2017,28(26):3691-3693.
[16]Andre T,Gramont AD,Vernerey D,et al.Adjuvant Fluorouracil,Leucovorin,and Oxaliplatin in Stage II to III ColonCancer:Updated 10-Year Survival and Outcomes According to BRAF Mutation and Mismatch Repair Status of the MOSAIC Study[J].J Clin Oncol,2015,33(35):4176-4187.
[17]But-Hadzic J,Anderluh F,Brecelj E,et al.Acute Toxicity and Tumor Response in Locally Advanced Rectal Cancer After Preoperative Chemoradiation Therapy With Shortening of the Overall Treatment Time Using Intensity-Modulated Radiation Therapy With Simultaneous Integrated Boost:A Phase 2 Trial[J].Int J Radiat Oncol Biol Phys,2016,96(5):1003-1010.
[18]Sun Z,Adam MA,Kim J,et al.Intensity-Modulated Radiation Therapy Is Not Associated with Perioperative or Survival Benefit over 3D-Conformal Radiotherapy for Rectal Cancer[J].J Gastrointest Surg,2017,21(1):106-111.
[19]Zhu XG,Li YH,Li XF,et al.Intensity-modulated radiation therapy for pelvic oligo-recurrence from rectal cancer: longterm results from a single institution[J].Am J Transl Res,2016,8(2): 1265-1272.
[20]Tanaka H.Effect of capecitabine therapy on the blood levels of antiepi leptic drugs:report of two cases[J].Gan To Kagaku Ryoho,2014,41(4):527-530.
[21]Nakagawa R,Inoue Y,Ohki T,et al.Efficacy and shortterm outcomes of preoperative chemoradiotherapy with intermittent oral tegafur-uracil plus leucovorin in Japanese rectal cancer patients: a single center experience retrospective analysis[J].World J Surg Oncol,2017,15(1):112.
[22]Sadahiro S,Suzuki T,Tanaka A,et al.Gene expression levels of gamma-glutamyl hydrolase in tumor tissues may be a useful biomarker for the proper use of S-1 and tegafur-uracil/leucovorin in preoperative chemoradiotherapy for patients with rectal cancer[J].Cancer Chemother Pharmacol,2017,79(6):1077-1085.
[23]Tahara M,Kiyota N,Mizusawa J,et al.Phase Ⅱ trial ofchemoradiotherapy with S-1 plus cisplatin for unresectable locallyadvanced head and neck cancer(JCOG0706)[J].Cancer Sci,2015,106(6):726-733.
[24]Yamazaki K, Kuwano H, Ojima H,et al.A randomized phase Ⅱstudy of combination therapy with S-1, oral leucovorin, and oxaliplatin (SOL) and mFOLFOX6 in patients with previously untreated metastatic colorectal cancer[J].Cancer Chemotherapy and Pharmacology,2015,75(3):569-577.
[25]穆毅,譚昊,王茜,等.替吉奥联合调强放疗治疗复发性直肠癌的疗效分析[J].肿瘤药学,2018,8(6):927-930.
收稿日期:2020-01-02;修回日期:2020-02-03
编辑/肖婷婷
