从低品位含铝矿石酸浸液中回收铝
2020-05-06高利坤马方通沈海榕
蒋 朋 高利坤 马方通 饶 兵 沈海榕
(1.昆明理工大学 复杂有色金属资源清洁利用国家重点实验室,昆明 650093;2.昆明理工大学 国土资源工程学院,昆明 650093)
我国铝土矿储量约10 亿t,居世界第5位,其中,中低品位铝土矿占80%以上[1-2]。由于我国生产氧化铝的主要原料是Al2O3含量在40%以上的优质铝土矿,导致我国大量进口铝土矿[3]。据统计,2017年我国进口铝土矿6 855 万t,同比增长32.4%[4]。我国非铝土矿铝资源中的粉煤灰、煤矸石以及其它矿物共伴生铝等都是丰富的低品位铝资源。因此,如何经济高效综合利用低品位含铝资源中的Al2O3,为我国铝资源的增储和缓解铝土矿资源短缺且依赖进口的局面具有重要的现实意义。
低品位含铝矿石普遍含铁高,嵌布粒度细,难以单体解离,常规选矿手段很难实现铝铁的有效分离,采用湿法化学浸出则是较为有效的处理手段。当采用酸浸法处理含铝物料时,铝、铁等有价金属也随之进入溶液[5]。因此,经济合理地从高铝铁的酸性溶液中有效分离铝铁成为低品位含铝资源制备高纯氧化铝的关键,同时也是含铝矿石湿法综合利用的难题。
溶液中铝铁分离的方法主要有萃取法[6]、高锰酸钾/二氧化锰沉淀法[7-12]、铁氰化钾与亚铁氰化钾沉淀法[13]、黄钾铁矾/黄铵铁矾沉淀法[14-15]、有机络合沉淀法[16-20]、磷酸盐沉淀法[21]和结晶法[22-25]。以上提到的方法中除结晶是用来回收铝外,其他几种方法均是用来重点回收铁的。采用回收铁的方法处理高铝铁的酸溶液,成本高,且工艺操作复杂。相对来讲,在基本不改变原溶液主要性质条件下,采用结晶法回收铝具有成本低、工艺操作简单等优点。但采用结晶手段从高铝铁的酸性溶液回收铝的研究鲜有报道,基于此,本文以硫酸浸出低品位含铝锐钛矿原矿得到的高铝铁浸出溶液为研究对象,在回收钪、钛等过程中,不改变原溶液主要性质条件下,采用硫酸铝铵结晶法高效回收酸液中的铝,并进行制备高纯氧化铝的试验研究。
1 试验
1.1 原料
以硫酸浸出低品位含铝锐钛矿原矿得到的高铝铁的浸出溶液为原料。锐钛矿原矿主要化学成分见表1。该锐钛矿主要为风化蚀变矿物,嵌布粒度小于10 μm,相互浸染分布,很难单体解离,常规选矿难以富集,因此,采用硫酸浸出钪钛等有效组分,在浸出过程中99%的铝和铁都随进入溶液,得到含Sc3+0.19×10-3mol/L、Ti4+0.10 mol/L、Al3+0.70 mol/L、Fe3+/Fe2+0.465 mol/L、H2SO42.40 mol/L的浸出溶液。

表1 锐钛矿主要化学成分Table 1 Main chemical components of the anatase /%
1.2 试验原理与方法
图1是硫酸铵、硫酸铝、硫酸铝铵三种物质在水中的溶解度随溶液温度变化的曲线。从图1可以看出,三种物质相比,硫酸铝铵的溶解度受温度影响最大,温度大于80 ℃时,三者的溶解度从大到小的顺序依次是硫酸铵、硫酸铝铵、硫酸铝,温度在10~80 ℃时,硫酸铝铵的溶解度最低,且随着温度的降低,其溶解度降低幅度最大,当温度降到10 ℃时,其溶解度仅为4.77 g。由于锐钛矿的浸出一般在90 ℃及以上进行,因此三种硫酸盐相比,硫酸铝铵是结晶法提取铝试剂的最佳选择,可采用在浸出时向溶液中加入(NH4)2SO4试剂,使溶液中的SO42-、Al3+和NH4+在溶液降温过程中形成NH4Al(SO4)2复合盐结晶的方式回收溶液中的铝。

图1 硫酸铵、硫酸铝、硫酸铝铵溶解度随温度变化的曲线Fig.1 Solubility curves of ammonium sulfate,aluminum sulfate and aluminum ammonium sulfate varying with temperature
试验采用硫酸铝铵结晶法—两次重结晶—树脂吸附—焙烧联合工艺从酸液中回收铝。首先,向锐钛矿浸出后得到的高铝铁浸出溶液中加入一定比例的硫酸铵,搅拌使其充分溶解并使溶液中的SO42-、Al3+和NH4+三种离子的浓度按NH4Al(SO4)2·12H2O晶体组成比例达到过饱和;然后,将溶液温度降低至最终结晶温度并使溶液中的离子结晶一段时间,获得NH4Al(SO4)2·12H2O粗产品,研究结晶过程中铝离子初始浓度、NH4+/Al3+摩尔比、结晶终点温度以及结晶时间对铝回收的影响;最后,将结晶得到的NH4Al(SO4)2·12H2O粗产品进行两次重结晶和一次树脂吸附除铁后得到的高纯NH4Al(SO4)2·12H2O在1 300 ℃下焙烧,最终获得高纯氧化铝产品。
该工艺结晶尾液均可返回流程中循环使用,树脂为可再生,焙烧尾气中的NH3、SO3均可通过回收再利用。
2 结果与讨论
2.1 十二水硫酸铝铵结晶法回收铝
2.1.1 铝离子初始浓度对铝回收的影响
在NH4+/Al3+摩尔比1.2、结晶终点温度20 ℃条件下,以300 r/min的速度搅拌30 min,通过浓缩或稀释浸出溶液控制铝离子初始浓度在0.5~0.9 mol/L,对应的铁离子浓度在0.33~0.60 mol/L,研究浸出液铝离子初始浓度对铝回收和铁夹杂的影响,结果如图3所示。
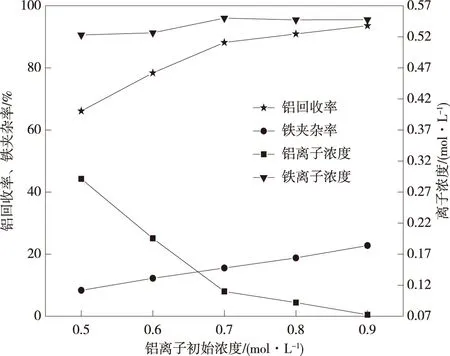
图3 铝离子初始浓度对铝回收和铁夹杂的影响Fig.3 Effect of initial concentration of aluminum ion on aluminum recovery and iron inclusion
从图3可以看出,铝离子初始浓度从0.5 mol/L浓缩到0.7 mol/L时,结晶尾液中的铝离子浓度从0.29 mol/L迅速降到0.11 mol/L,结晶尾液中的铁离子浓度变化不大,在0.523~0.545 mol/L,铝的回收率从66.10%迅速升高到88.19%,铁的夹杂率从8.36%缓慢升高到15.56%;铝离子初始浓度从0.7 mol/L浓缩到0.9 mol/L时,结晶尾液中的铝离子浓度从0.11 mol/L缓慢降到0.07 mol/L,结晶尾液中的铁离子浓度变化不大,在0.545~0.548 mol/L,铝的回收率从88.19%缓慢升高到93.58%,铁的夹杂率从15.56%迅速升高到27.00%;结晶铝离子初始浓度越高,越有利于铝离子的结晶,进而有利于铝的回收,但铝离子过高,硫酸铝铵结晶越快,夹杂的铁也越多,而铁在后续过程较难处理,不利于获得高纯氧化铝,因此初始铝离子浓度不宜太高。从图3可以看出,适宜的初始铝离子浓度为0.7 mol/L,此时,铝的回收率为88.19%,铁的夹杂率为15.56%,结晶尾液中的铝离子浓度为0.11 mol/L,铁离子浓度为0.545 mol/L。
2.1.2 NH4+/Al3+摩尔比对铝回收的影响
在铝离子初始浓度0.7 mol/L、结晶终点温度20 ℃条件下,以300 r/min的速度搅拌30 min,向溶液中加入硫酸铵,控制NH4+/Al3+摩尔比在1.0~1.4,研究NH4+/Al3+摩尔比对铝回收和铁夹杂的影响,结果如图4所示。
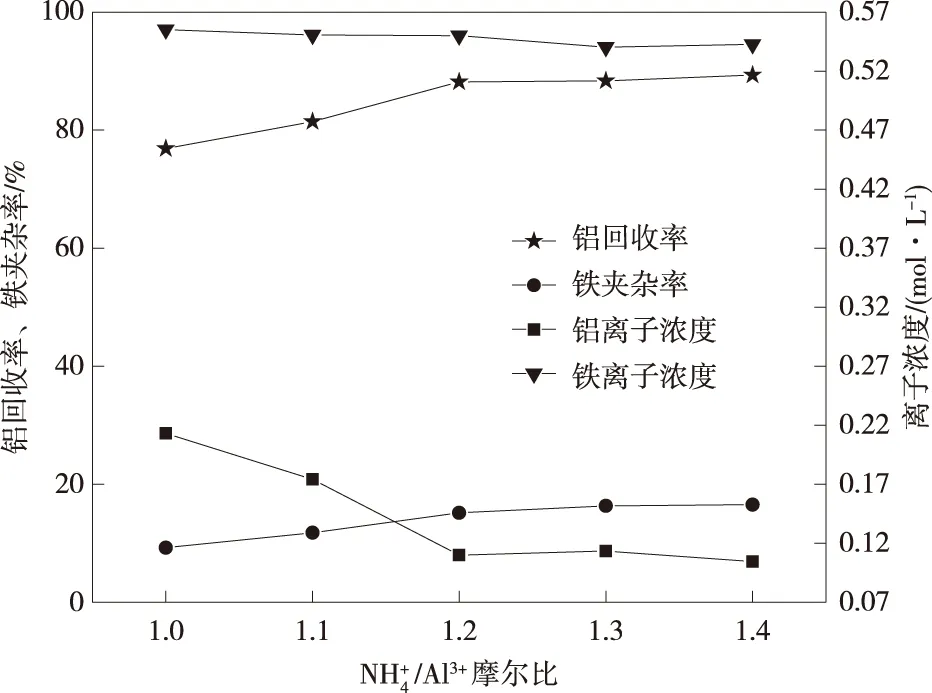
图4 NH4+/Al3+摩尔比对铝回收和铁夹杂的影响Fig.4 Effect of NH4+/Al3+ molar ratio on aluminum recovery and iron inclusion
从图4可以看出,NH4+/Al3+摩尔比从1.0增加到1.2时,结晶尾液中铝离子浓度从0.21 mol/L迅速降低到0.11 mol/L,结晶尾液中的铁离子浓度变化不大,在0.555~0.545 mol/L,铝的回收率从76.86%迅速升高到88.19%,铁的夹杂率从9.25%缓慢升高到15.56%;NH4+/Al3+摩尔比从1.2增加到1.4时,结晶尾液中的铝离子浓度变化不大,在0.10~0.11 mol/L,结晶尾液中的铁离子浓度变化不大,在0.545~0.543 mol/L,铝的回收率变化不大,在88.19%~89.33%,铁的夹杂率变化不大,在15.56%~16.55%;NH4+/Al3+摩尔比越大,越有利于铝离子结晶和铝的回收,但与此同时,铁的夹杂率随之升高,NH4+/Al3+最佳摩尔比为1.2,此时,铝的回收率为88.19%,铁的夹杂率为15.56%,结晶尾液中的铝离子浓度为0.11 mol/L,铁离子浓度为0.545 mol/L。
2.1.3 结晶终点温度对回收铝的影响
在铝离子初始浓度0.7 mol/L、NH4+/Al3+摩尔比1.2条件下,以300 r/min的速度搅拌30 min,控制结晶终点温度在15~35 ℃,研究结晶终点温度对铝回收和铁夹杂的影响,结果如图5所示。
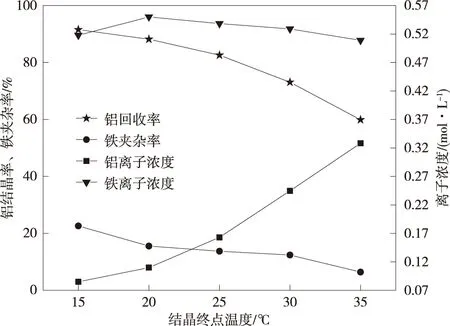
图5 结晶终点温度对铝回收率和铁夹杂率的影响Fig.5 Effect of crystallization end temperature on aluminum recovery and iron inclusion
从图5可以看出,结晶终点温度从15 ℃升高到20 ℃时,结晶尾液中铝离子浓度变化不大,在0.09~0.11 mol/L,结晶尾液中的铁离子浓度从0.518 mol/L缓慢升高到0.545 mol/L,铝的回收率从91.56%缓慢降低到88.19%,铁的夹杂率从22.61%缓慢降低到15.56%;结晶终点温度从15 ℃升高到35 ℃时,结晶尾液中的铝离子浓度从0.11 mol/L迅速升高到0.33 mol/L,结晶尾液中的铁离子浓度从0.545 mol/L缓慢降低到0.509 mol/L,铝的回收率从88.19%迅速降低到59.90%,铁的夹杂率从15.56%缓慢降低到6.41%。综合考虑铝的回收率、产品纯度和实验操作条件的易实现程度等,结晶终点温度选择接近室温20 ℃较为合适,此时,铝的回收率为88.19%,铁的夹杂率为15.56%,结晶尾液中铝离子浓度为0.11 mol/L,铁离子浓度为0.545 mol/L。
2.1.4 结晶时间对铝回收的影响
在铝离子初始浓度0.7 mol/L、结晶终点温度20 ℃、NH4+/Al3+摩尔比1.2条件下,以300 r/min的速度搅拌,控制结晶时间在0~45 min,研究结晶时间对铝回收和铁夹杂的影响,结果如图6所示。

图6 结晶时间对铝回收率和铁夹杂率的影响Fig.6 Effect of crystallization time on aluminum recovery and iron inclusion
从图6可以看出,结晶时间从0增加到30 min时,结晶尾液中的铝离子浓度变化不大,在0.11~0.12 mol/L,结晶尾液中的铁离子浓度从0.519 mol/L缓慢升高到0.545 mol/L,铝的回收率变化不大,在87.57%~88.19%,铁的夹杂率从19.71%缓慢降到15.56%;结晶时间从30 min增加到45 min时,结晶尾液中的铝离子浓度变化不大,在0.11~0.12 mol/L,结晶尾液中的铁离子浓度从0.545 mol/L平缓升高到0.550 mol/L,铝的回收率变化不大,在87.64%~88.19%,铁的夹杂率从15.56%缓慢降到14.77%;适宜的结晶时间可选择为30 min,此时,铝的回收率为88.19%,铁的夹杂率为15.56%,结晶尾液中铝离子浓度为0.11 mol/L,铁离子浓度为0.545 mol/L。
综上,硫酸铝铵结晶试验在铝离子初始浓度为0.70 mol/L、NH4+/Al3+摩尔比为1.2、结晶终点温度为20 ℃的条件下,以300 r/min的速度搅拌30 min,获得的十二水硫酸铝铵粗产品中晶体纯度为95.31%,铝的回收率达到88.19%,夹杂铁的含量为1.39%,硫酸铝铵结晶法可以从含高铝铁的酸性浸溶液中有效回收铝。
2.2 重结晶法提纯NH4Al(SO4)2·12H2O
NH4Al(SO4)2·12H2O粗产品中主要杂质为铁、硅、钠等元素,通过重结晶可以有效提纯NH4Al(SO4)2·12H2O。重点研究了重结晶过程中,液固比、终点结晶温度和结晶时间对提纯效果的影响。
2.2.1 重结晶液固比对NH4Al(SO4)2·12H2O提纯的影响
在重结晶终点温度25 ℃条件下,以300 r/min的速度搅拌30 min,控制液固比(mL/g)为1.1~1.9,研究液固比对铝回收和铁去除的影响,结果如图7所示。

图7 重结晶液固比对铝回收率和铁去除率的影响Fig.7 Effect of liquid-solid ratio of recrystallization on aluminum recovery and iron removal
从图7可以看出,液固比从1.1增加到1.3时,结晶尾液中的铝离子浓度从0.21 mol/L缓慢升高到0.26 mol/L,铁离子浓度从0.174 mol/L缓慢升高到0.181 mol/L,铝的回收率从86.05%缓慢降到82.85%,铁去除率从90.40%小幅升高到93.16%;重结晶液固比从1.3增加到1.9时,结晶尾液中的铝离子浓度从0.26 mol/L缓慢升高到0.45 mol/L,铁离子浓度从0.181 mol/L缓慢升高到0.194 mol/L,铝的回收率从82.85%缓慢降到71.72%,铁去除率变化不大,在93.16%~94.76%。由于重结晶液固比越高,溶液浓度越低,相应铝离子的结晶率也越低,因此,NH4Al(SO4)2·12H2O重结晶过程中铝的回收率降低,铁去除率升高。综上所述,液固比为1.3 mL/g时,NH4Al(SO4)2·12H2O的提纯效果最佳,此时,铝回收率为82.85%,铁去除率为93.16%,结晶尾液中的铝离子浓度为0.26 mol/L,铁离子浓度为0.18 mol/L。
2.2.2 重结晶终点温度对NH4Al(SO4)2·12H2O提纯的影响
在液固比1.3 mL/g条件下,以300 r/min的速度搅拌30 min,控制重结晶终点温度在15~35 ℃,研究重结晶终点温度对铝回收和铁去除的影响,结果如图8所示。
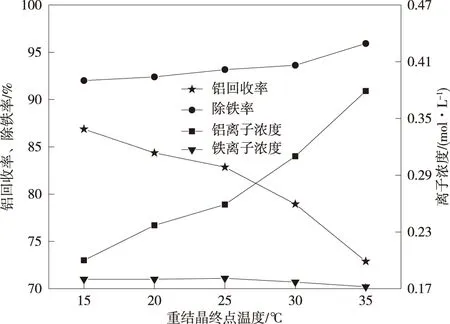
图8 重结晶终点温度对铝回收率和铁去除率的影响Fig.8 Effect of recrystallization end temperature on aluminum recovery and iron removal
从图8可以看出,重结晶终点温度从15 ℃升高到25 ℃时,结晶尾液中铝离子浓度从0.20 mol/L缓慢升高到0.26 mol/L,结晶尾液中的铁离子浓度变化不大,在0.180~0.181 mol/L,铝的回收率从86.87%缓慢降到82.85%,铁去除率从92.00%缓慢升高到93.16%;重结晶终点温度从25 ℃升高到35 ℃时,结晶尾液中的铝离子浓度从0.26 mol/L缓慢升高到0.38 mol/L,结晶尾液中的铁离子浓度变化不大,在0.181~0.172 mol/L,铝的回收率从82.85%迅速降到72.89%,铁去除率从93.16%缓慢升高到95.92%。
由于溶液温度越高,硫酸铝铵的溶解度越大,因此升高溶液温度不利于铝离子的结晶转化会造成NH4Al(SO4)2·12H2O重结晶过程中铝的回收率降低,结晶终点温度选择25 ℃较为合适,此时,铝的回收率为82.85%,铁去除率为93.16%,结晶尾液中的铝离子浓度为0.26 mol/L,铁离子浓度为0.18 mol/L。
2.2.2 重结晶时间对NH4Al(SO4)2·12H2O提纯的影响
在重结晶终点温度25 ℃、液固比为1.3 mL/g、搅拌速度300 r/min条件下,控制重结晶时间在0~45 min,研究重结晶时间对铝回收和铁去除的影响,结果如图9所示。
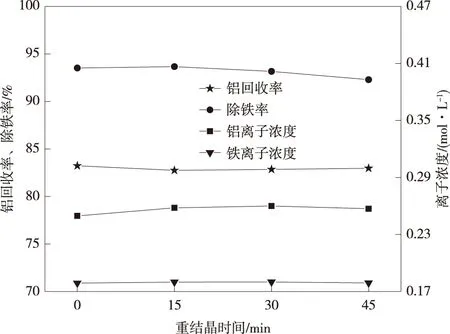
图9 重结晶时间对铝回收率和铁去除率的影响Fig.9 Effects of recrystallization time on aluminum recovery and iron removal
从图9可以看出,重结晶时间从0增加到30 min时,结晶尾液中的铝离子浓度变化不大,但略微升高,结晶尾液中的铁离子浓度略微升高,铝的回收率变化不大,在82.85%~83.23%,铁去除率变化不大,在93.16%~93.52%;重结晶时间从30 min增加到45 min时,结晶尾液中的铝铁离子浓度变化不大但略微降低,铝的回收率基本不变,铁去除率变化不大,在92.29%~93.16%;最佳结晶时间为30 min,此时铝的回收率为82.85%,铁去除率为93.16%,结晶尾液中的铝离子浓度为0.26 mol/L,铁离子浓度为0.18 mol/L。
综上,在搅拌转速为300 r/min时,最佳硫酸铝铵重结晶试验条件为:液固比1.3、重结晶终点温度25 ℃、搅拌时间30 min,在此条件下所得NH4Al(SO4)2·12H2O重结晶产品纯度高,铝回收率可达到82.85%,夹杂铁的含量可降到0.10%,硫酸铝铵重结晶法可以有效提纯NH4Al(SO4)2·12H2O。
2.3 NH4Al(SO4)2·12H2O深度除铁以及制备高纯氧化铝
2.3.1 NH4Al(SO4)2·12H2O深度除铁
重结晶获得的NH4Al(SO4)2·12H2O产品进行二次重结晶深度除铁。试验条件为:液固比1.3、结晶终点温度25 ℃、搅拌转速300 r/min、搅拌时间30 min,在此条件下所获NH4Al(SO4)2·12H2O二次重结晶产品中夹杂的铁含量降到0.007%。
采用HYC-100氨基羧酸螯合树脂对NH4Al(SO4)2·12H2O二次重结晶产品进行深度除铁,具体方法是将NH4Al(SO4)2·12H2O用水溶解,控制硫酸铝铵溶液浓度为0.70 mol/L,将硫酸铵溶液在温度65 ℃条件下以13 mL/min的速度通过HYC-100树脂,最终所获高纯NH4Al(SO4)2·12H2O产品中夹杂的铁含量为0.000 016%。
2.3.2 高纯氧化铝制备
将深度除铁后所得高纯NH4Al(SO4)2·12H2O在高温条件下热解,热解温度1 300 ℃、时间2 h,所得氧化铝产品的比表面积为7.844 m2/g,化学分析见表2,XRD图如图10所示,扫描电镜图像(SEM)照片如图11所示。从表2和图10可以看出,最终所得氧化铝产品杂质含量低,且结晶好。图11产品的微观形貌也证明氧化铝产品结晶度好,且粒度均匀,进一步说明采用本文所用工艺可获得品质高的氧化铝产品。

表2 氧化铝产品化学成分Table 2 Chemical composition of the alumina product /%
3 结论
1)对铝含量22%左右、铁含量17%左右的含铝铁低品位难处理含铝矿物,采用酸浸—结晶—两次重结晶—树脂吸附—焙烧工艺可回收矿物中的铝,获得高纯氧化铝产品。
2)针对含高铝铁的酸性溶液,可采用硫酸铝铵结晶法回收溶液中的铝。在铝离子初始浓度0.70 mol/L、NH4+/Al3+摩尔比1.2、结晶终点温度20 ℃条件下,铝的回收率可达到88.19%,同时晶体中的铁夹杂率为15.56%,结晶尾液中的铁离子浓度为 0.545 mol/L、铝离子浓度为0.11 mol/L,所得NH4Al(SO4)2·12H2O粗产品晶体纯度为95.31%,铁含量为1.39%。对该粗结晶产品采用重结晶法进一步提纯,一次重结晶铝的回收率可达到82.85%,同时铁去除率可达93.16%,NH4Al(SO4)2·12H2O晶体中的杂质铁含量可降到0.10%,两次重结晶后所得NH4Al(SO4)2·12H2O晶体中的杂质铁含量可进一步降到0.007%。采用树脂吸附法进一步提纯二次重结晶产品可获得杂质铁含量为0.000 016%的高纯NH4Al(SO4)2·12H2O晶体产品。高纯NH4Al(SO4)2·12H2O晶体在1 300 ℃条件下焙烧2 h后即可获得纯度为99.99%的高纯Al2O3。
3)酸浸—结晶—两次重结晶—树脂吸附—焙烧工艺流程合理,基本不改变溶液主要性质,可有效回收溶液中的有价组分,具有操作简单、高效、低成本的特点。研究结果对该类酸浸工艺综合回收有价组分具有重要的参考价值,可为低品位铝的资源化及高值化应用奠定一定的技术基础,为我国铝资源增储以及缓解铝土矿资源短缺、依赖进口的局面具有重要的现实意义。
