2024铝合金氧化陶瓷膜的制备与性能
2020-05-05马国峰刘志扬贺春林
马国峰, 刘志扬, 贺春林
(沈阳大学 辽宁省先进材料制备技术重点实验室, 辽宁 沈阳 110044)
铝是地球中含量最丰富的金属元素,铝及其合金具有比强度高、可加工性好、导热导电性好、耐腐蚀性能优良的特点,是一种优秀的有色金属.铝合金是仅次于钢铁的使用量第二大的金属材料,广泛地应用于建筑材料、汽车制造、航空航天、国防工业、电子产品等领域[1-3].但是,铝合金的耐磨性较差,硬度较低,在实际使用中往往不能满足需要.因此,铝合金的表面处理是一个重要的研究方向[4-7].
阳极氧化技术是铝合金应用最广的表面处理技术.阳极氧化技术的工艺简单,制备出的氧化膜硬度及耐腐蚀性均有很大提高.但是在单一的硫酸、草酸、磷酸或者其他传统单电解质中制成的铝合金阳极氧化陶瓷膜,硬度通常都比较低,综合机械性能不高,不能满足工业生产要求[8-11].
表1为2024铝合金各成分质量分数.研究结果显示,2024铝合金中高含量的Cu容易在阳极氧化反应中形成含铜相,如CuAl2和Al2CuMg.当2024铝合金发生阳极氧化时,含铜相CuAl2和Al2CuMg的存在将加速阳极氧化陶瓷膜的溶解速率,导致溶解速率大于氧化陶瓷膜生成速率,从而增大了阳极氧化的困难程度.将一定量的有机弱酸(例如柠檬酸、酒石酸、硼酸等)添加到普通硫酸类的电解液中,可以解决因含铜相CuAl2和Al2CuMg的存在而导致的溶解速率过快的问题,并且提高氧化陶瓷膜的成膜速率,拓宽氧化陶瓷膜生成的温度范围,提高氧化陶瓷膜的性能[6,12-14].
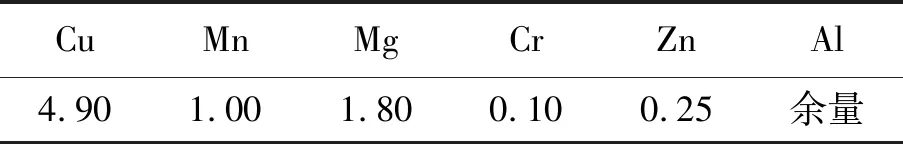
表1 2024铝合金各成分质量分数Table 1 Mass fraction of each componentof 2024 aluminum alloy %
传统的阳极氧化处理通常使用直流电源与交流电源,本文使用脉冲电源进行实验.相对于传统电源,脉冲电源具有节能环保,成膜速度快,膜层不易烧蚀,膜层质量好等优点[15].使用脉冲电源的阳极氧化反应呈周期性变化,相对应的瞬间电压低,电流密度高,而且由于负向周期的存在能够充分分散氧化陶瓷膜生成时产生的热量,同时可以降低电解液中的酸性物质对铝合金基体的溶解速率.使用脉冲电源对制成的氧化陶瓷膜的显微硬度、耐腐蚀性、耐磨性等都有一定程度的提高.此外,由于脉冲电源具有高脉冲频率、低脉冲周期、低脉冲能量和低电流密度等特点,能够使氧化反应时间缩短,氧化陶瓷膜的增长速率加快[16-17].通过调整占空比,能够使氧化反应生成的高温Al2O3充分冷却,避免烧蚀,从而形成均匀的氧化陶瓷膜.
1 材料与方法
实验在硫酸-草酸体系下进行,草酸质量浓度为20 g·L-1,硫酸质量浓度为220、250和280 g·L-1.实验所用药品均使用分析纯试剂与去离子水配置.实验装置如图1所示,正极为2024铝合金试件,负极使用不锈钢材料,电解槽使用烧杯代替.使用电动搅拌装置和低温恒温槽控制反应容器内的温度,电动搅拌装置的搅拌速率为300 r·min-1,低温恒温槽的温度为10 ℃.反应时间分别为40、50、60和70 min.
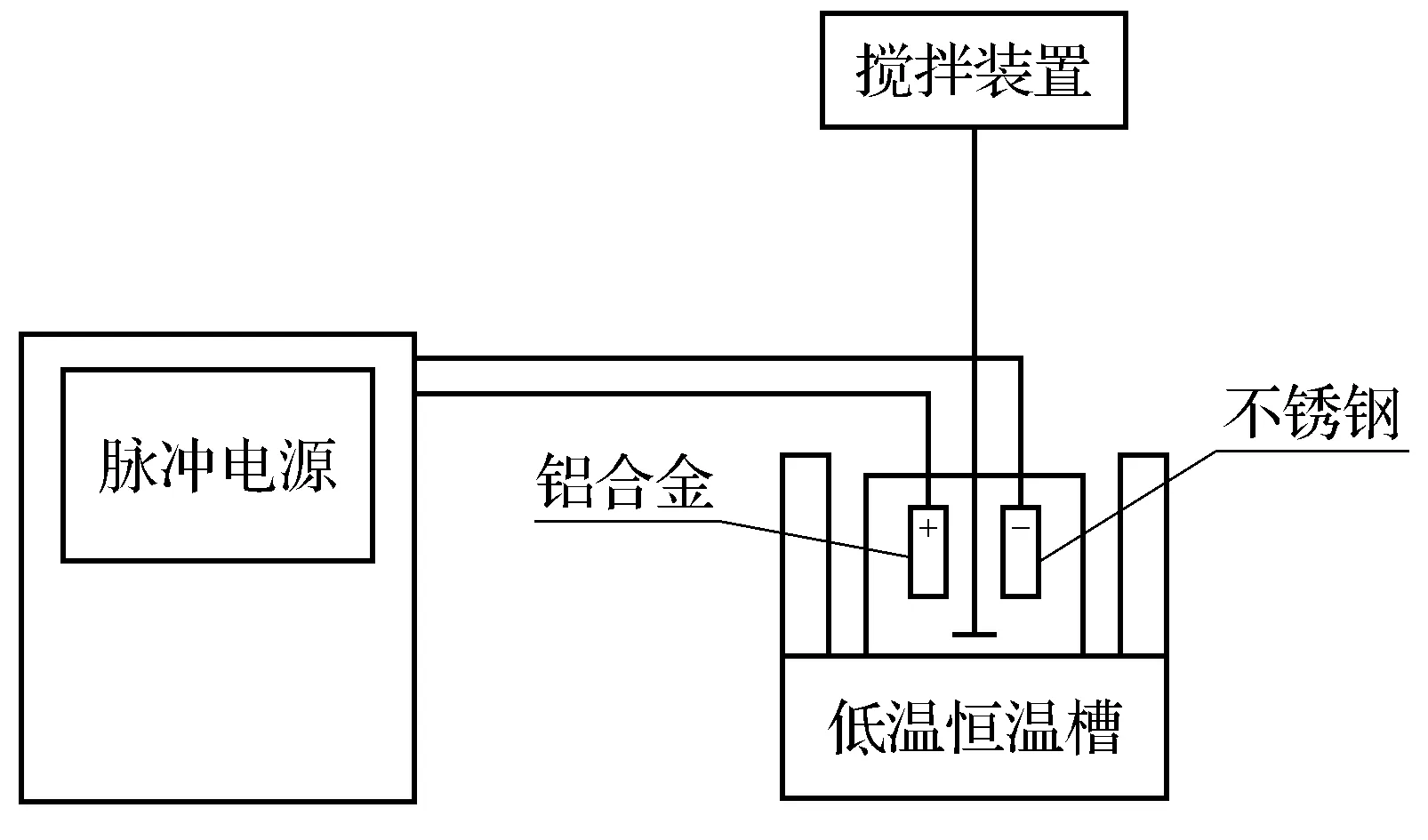
图1 实验装置示意图Fig.1 Schematic diagram of experimental device
试样的材料使用2024铝合金, 试样使用线切割,统一切割成大小为25 mm×20 mm的矩形. 在试样的正上方打孔用以连接导线.实验开始前要对试样进行预处理. 首先对试样进行机械打磨, 使用水性砂纸从400#打磨至1500#, 完成后使用超声波清洗仪清洗20 min, 拿出后使用吹风机吹干. 然后放入质量分数为5%的NaOH溶液中碱蚀4 min, 清洗后吹干. 碱蚀过程的反应方程式为

(1)
即铝溶解生成可溶性的NaAlO2,铝表面在空气中自然形成的氧化膜与NaOH反应,化学方程式如下:

(2)
最后放入质量分数为30%的硫酸中进行除灰处理4 min,清洗后吹干.连接导线,导线与试样的连接处使用石蜡密封,密封后使用万用表检测导线与试样接触是否良好.
本实验所使用的脉冲电源为恒流模式,电压可调节范围为0~60 V.实验使用的电流密度为3、4、5、6 A·dm-2.脉冲电源导通与截止时间如表2所示.

表2 脉冲电源导通与截止时间Table 2 Remaining parameters of pulsepower supply ms
实验使用日立S4800扫描电镜观察氧化陶瓷膜的表面形貌. 耐腐蚀性能测试使用上海辰华牌CHI660e电化学工作站,电化学实验采用三电极体系,工作电极为2024铝合金试样, 参比电极为饱和甘汞电极, 辅助电极为石墨电极, 测试溶液为室温下质量分数为3.5%的NaCl溶液, 初始电位为-1.2 V,终点电位为-0.2 V, 扫描段数为1, 终止电位的保持时间为0,扫描速度为1 mV·s-1,测试面积为10 cm2, 非测试部分使用石蜡进行密封. 陶瓷膜厚度使用德国EPK MiniTest 720涂层测厚仪测量, 在试样表面取5个点取平均值.
2 结果与讨论
2.1 氧化陶瓷膜生长机理
氧化膜生长电位-时间曲线如图2所示.在氧化反应开始的一瞬间,电压急剧提高,并且电流密度越大,电压升高的速率越快.当壁垒层生成后出现拐点,电压升高速率降低,开始缓慢增长.氧化反应过程可以分为4个阶段,如图3所示.在反应初期铝合金基体表面生成一层厚度很小的壁垒层,如图3(a)所示.随着反应继续进行,电压持续升高,壁垒层的厚度也继续增加,电解液中的硫酸和草酸开始对壁垒层进行溶解,壁垒层表面开始出现微米级的孔洞,如图3(b)所示.由于微孔的产生,表面变得不均匀,电流分布也变得不均匀.电流密度较高处反应继续进行,电流密度低处反应停止,开始形成多孔状的氧化膜,如图3(c)所示.随着反应时间的增加,多孔结构开始均匀,并且形成阻挡层,如图3(d)所示.电流密度越大,电压越高,阻挡层越厚.
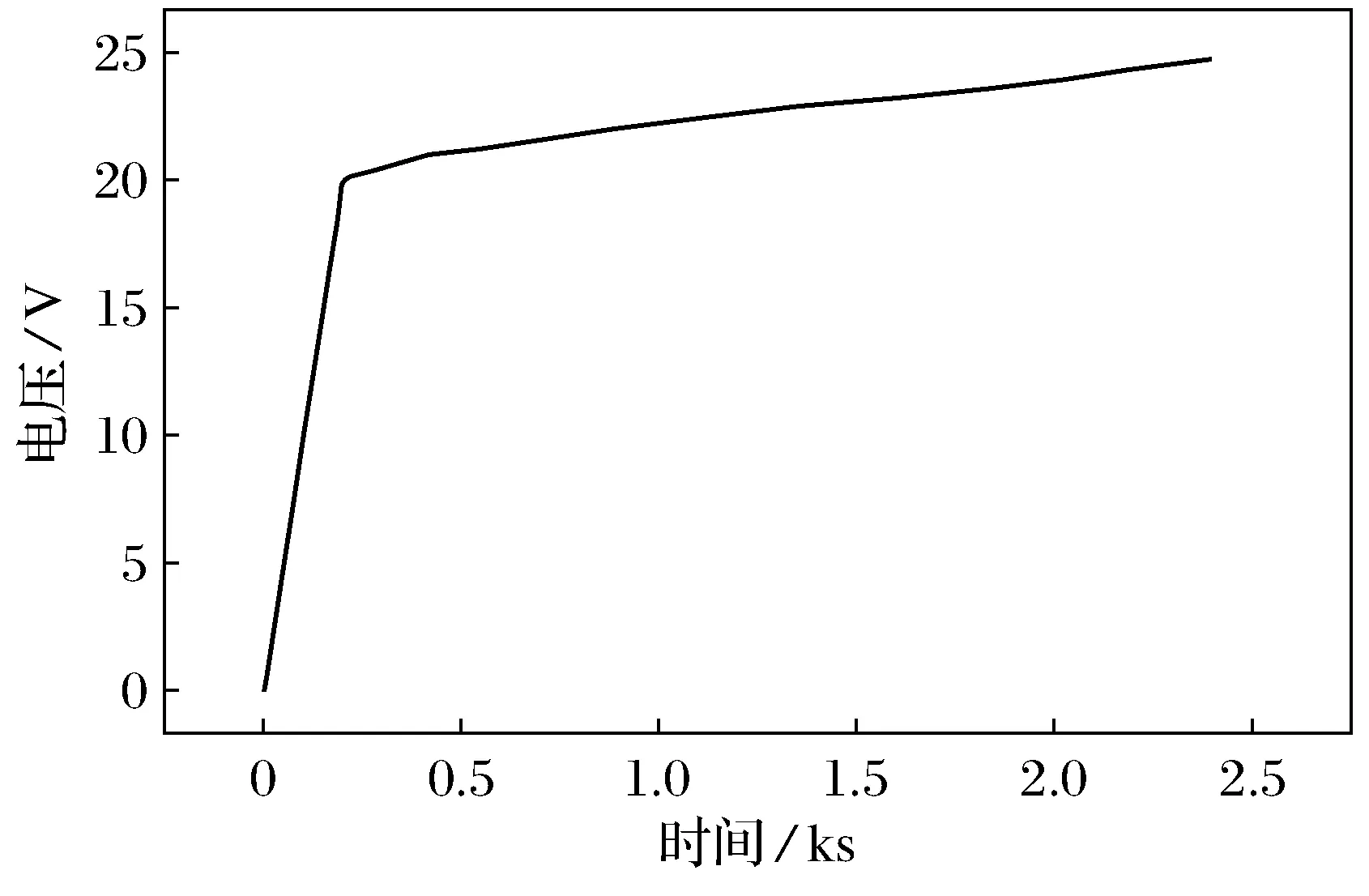
图2 电位-时间曲线Fig.2 Potential-time curve
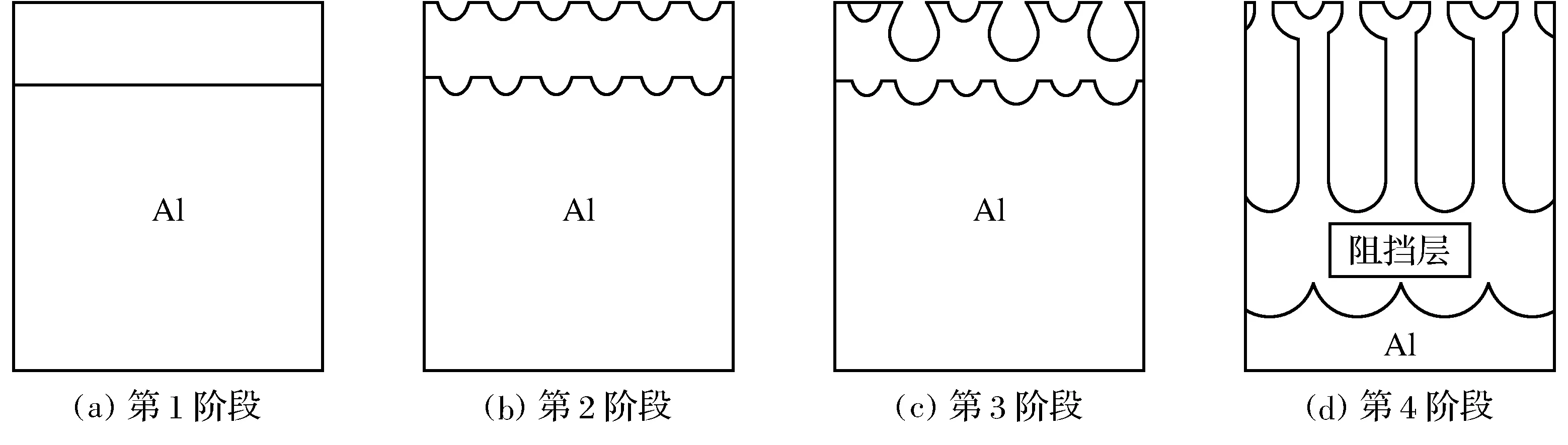
图3 膜层生长示意图Fig.3 Schematic diagram of film layer growth
2.2 氧化反应时间对氧化陶瓷膜的影响
氧化反应时间是一种非常重要的影响因素.图4显示了在不同氧化反应时间下氧化陶瓷膜的SEM图.氧化铝膜通常由2层组成:一层是薄的无孔层,也称为阻挡层,紧邻金属基材;另一层是与金属基材分离的厚度较大的多孔外层.在图4中,已经在2024铝合金的基材表面上形成了氧化陶瓷膜.由于反应是在硫酸体系中进行的,所以形成多孔型氧化陶瓷膜,氧化陶瓷膜表面呈现出明显的小而致密的多孔状结构.膜表面起伏不平,是由于电解液中的草酸和硫酸溶解铝合金氧化陶瓷膜造成的.当反应时间为40 min时,孔径为1.80 μm;当反应时间为50 min时,孔径为1.00 μm;当反应时间为60 min时,孔径基本保持不变;当反应时间为70 min时,孔径为2 μm.氧化陶瓷膜的表面孔隙率和微孔数量明显增加.这时氧化反应发生在微孔的底部.当氧化反应时间增加时,热量难以从内部扩散到外部.因此,热量将累积,导致孔底部的温度升高并且孔径增加.孔径越大,微孔数量越多,氧化陶瓷膜越容易被腐蚀.

图4 不同氧化时间下氧化陶瓷膜的SEM图Fig.4 SEM diagram of oxide ceramic film at different oxidation time
图5为氧化陶瓷膜在不同氧化时间下的动电位极化曲线,由图5可以得出,通过进行氧化反应,氧化陶瓷膜耐腐蚀性能对比2024铝合金基体有着显著的提高,而且由于氧化时间的不同, 耐腐蚀性能也有显著差别.随着反应时间的增加,自腐蚀电位先正移后负移,在反应时间为60 min时自腐蚀电位最大.根据Tafel外推法通过使用Origin软件对极化曲线拟合,表3为不同反应时间下极化曲线的拟合结果,其中腐蚀速率使用式(3)计算得出.
v=3.27×10-3·J·M/nρ
(3)
式中:v为腐蚀速率,mm·a-1;J为自腐蚀电流密度,μA·cm-2;M为相对原子质量;n为化合价;ρ为密度[18],g·cm-3.其中相对原子质量取Al相对原子质量27,化合价取Al化合价+3,密度取Al的密度2.74 g·cm-3.
由表3可以看出随着时间的增长腐蚀速率先减小后增大,反应时间为60 min时腐蚀速率最低,为0.28 μm·a-1,与极化曲线分析结果相吻合.表4为不同反应时间下氧化陶瓷膜的厚度,可以看出反应时间为60 min的氧化陶瓷膜厚度值最高,与耐腐蚀性分析结果相吻合.

表3 不同反应时间下极化曲线的拟合结果Table 3 The fitting results of polarization curve under different reaction time
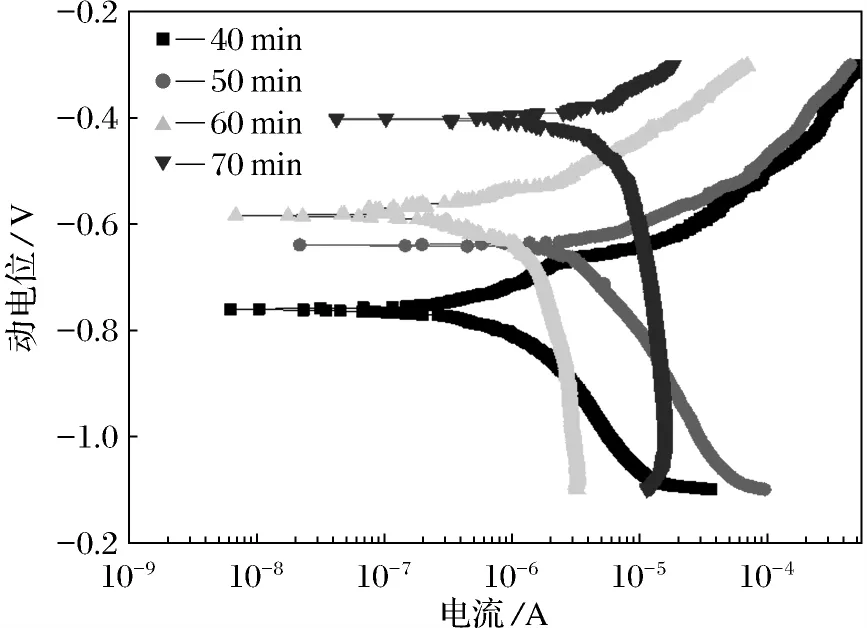
图5 氧化陶瓷膜在不同氧化时间下的动电位极化曲线
Fig.5 Dynamic potential polarization curves under different oxidation time

表4 不同反应时间下氧化陶瓷膜的厚度Table 4 Thickness of oxide ceramic filmsat different reaction time
2.3 电流密度对氧化陶瓷膜的影响
电流密度对铝合金氧化陶瓷膜的生长过程、微观结构、元素成分、相组成和耐蚀性都有重要的影响.图6为不同电流密度下氧化陶瓷膜的SEM图. 由SEM图可以看出,氧化陶瓷膜的表面形貌随着电流密度的增大趋于致密和均匀,当电流密度为3 A·dm-2时, 氧化陶瓷膜表面较粗糙; 当电流密度为4 A·dm-2时, 氧化陶瓷膜的表面形貌最为均匀, 且孔洞大小趋于一致; 当电流密度达到6 A·dm-2时, 氧化陶瓷膜表面的均匀性变差, 微孔的分布变得不规则且致密度也明显下降. 电流密度对氧化陶瓷膜表面形貌的影响主要是由氧化反应过程中的放热引起的. 当电流密度过小时,氧化反应的速率较慢, 电压上升的速率慢, 而且膜的表面均匀性差,孔洞分布不均,表面粗糙. 当氧化电流密度过大时, 电压上升的速率过快, 氧化反应过程中放出的热量大量累积,且快速聚集在膜的表面, 导致电解液局部温度显著升高, 膜孔内的温度也显著增大, 氧化陶瓷膜因温度过高溶解的速率大于生成的速率, 致使氧化陶瓷膜中出现缺陷, 氧化陶瓷膜表面变得粗糙,均匀性变差. 由此可见, 合适的电流密度应选择在4 A·dm-2左右.

图6 不同电流密度下氧化陶瓷膜的SEM图Fig.6 SEM diagrams of oxide ceramic film at different current densities
图7为氧化陶瓷膜在不同电流密度下的动电位极化曲线.由图可知不同电流密度下的氧化陶瓷膜的耐腐蚀性也不同.随着电流密度的增加,自腐蚀电位先正移后负移,在电流密度为4 A·dm-2时,自腐蚀电位最大.根据Tafel外推法通过使用Origin软件对极化曲线拟合,表5为不同电流密度下极化曲线的拟合结果,其中腐蚀速率使用式(3)计算得出.
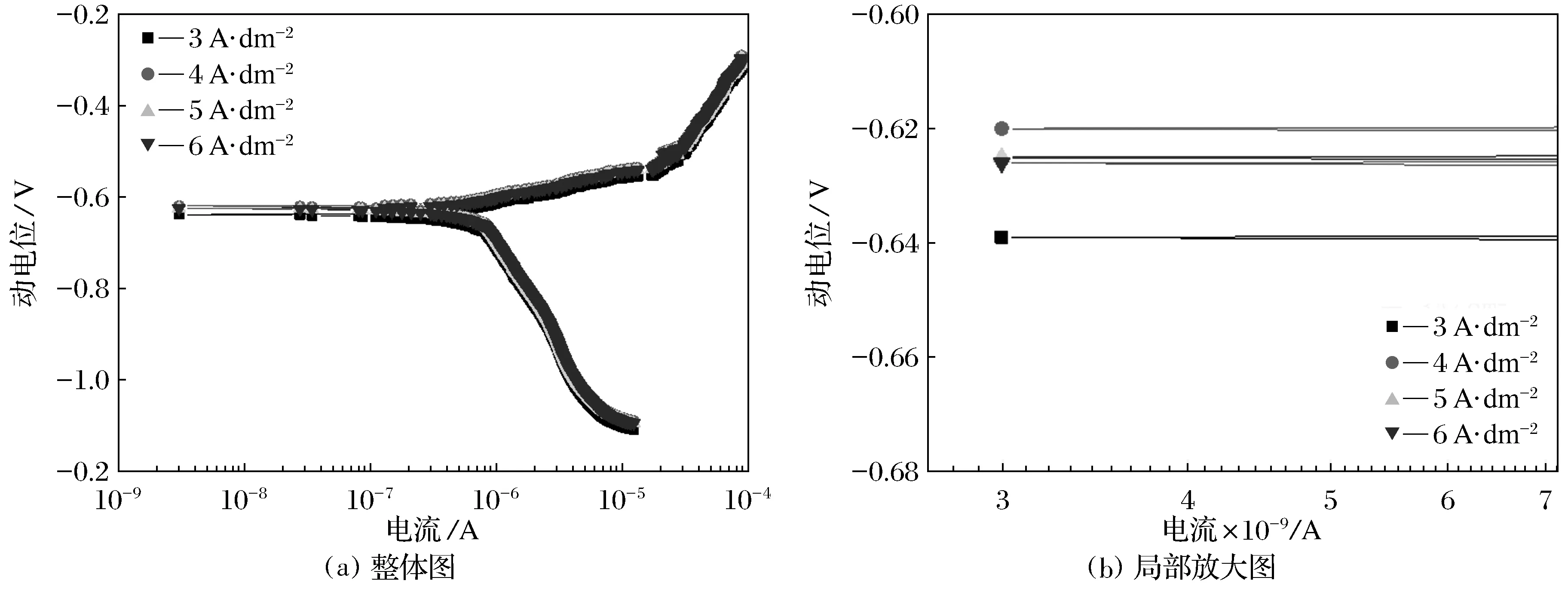
图7 氧化陶瓷膜不同电流密度下的动电位极化曲线Fig.7 Dynamic potential polarization curves of oxide ceramic film at different current densities of ocide ceramic film
表5 不同电流密度下极化曲线的拟合结果
Table 5 Results of polarization curve fitting under different current densities
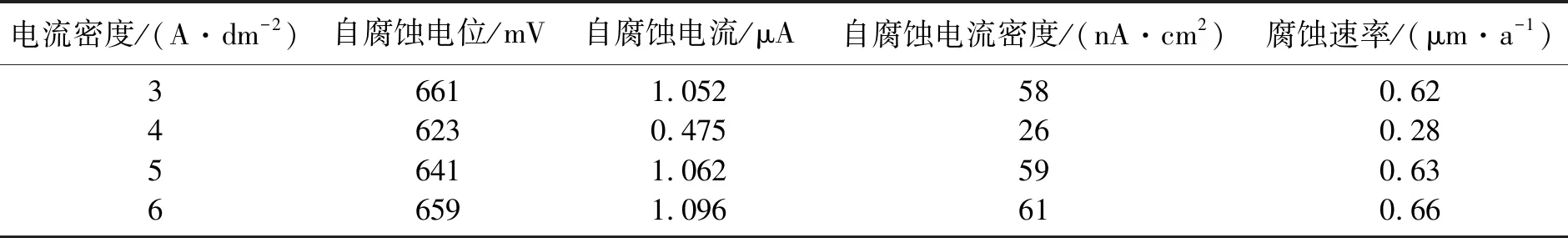
电流密度/(A·dm-2)自腐蚀电位/mV自腐蚀电流/μA自腐蚀电流密度/(nA·cm2)腐蚀速率/(μm·a-1)36611.052580.6246230.475260.2856411.062590.6366591.096610.66
由表5可以看出随着电流密度的增大,蚀速率先减小后增大,电流密度为4 A·dm-2时腐蚀速率最低为0.28 μm·a-1,与极化曲线分析结果相吻合.表6为不同电流密度下氧化陶瓷膜的厚度,可以看出电流密度为4 A·dm-2时,氧化陶瓷膜厚度值最高,与耐腐蚀性分析结果相吻合.

表6 不同电流密度下氧化陶瓷膜的厚度Table 6 Thickness of oxide ceramic films at different current densities
2.4 硫酸浓度对氧化陶瓷膜的影响
对使用不同质量浓度硫酸制成的氧化陶瓷膜进行耐腐蚀性测试.图8为不同硫酸质量浓度下的动电位极化曲线,在硫酸质量浓度为250 g·L-1时,氧化陶瓷膜自腐蚀电位最大.根据
图8 不同硫酸质量浓度下的动电位极化曲线
Fig.8 Dynamic potential polarization curves at different sulfuric acid concentrations
Tafel外推法通过使用Origin软件对极化曲线拟合,表7为不同硫酸质量浓度下极化曲线的拟合结果,其中腐蚀速率使用式(3)计算得出.

表7 不同硫酸质量浓度下极化曲线的拟合结果Table 7 The fitting results of polarization curves under different sulfuric acid concentrations
由表7可知,硫酸质量浓度为250 g·L-1,氧化陶瓷膜腐蚀速率最低,耐腐蚀性能最好.表8为不同硫酸质量浓度下氧化陶瓷膜的厚度,可以看出硫酸质量浓度为250 g·L-1时,氧化陶瓷膜厚度值最高,与耐腐蚀性分析结果相吻合.

表8 不同硫酸质量浓度下氧化陶瓷膜的厚度Table 8 Thickness of oxide ceramic films at differentmass concentrations of sulfuric acid
2.5 氧化陶瓷膜成分与结构分析
对不同氧化时间的氧化陶瓷膜进行SEM-EDS能谱分析如图9所示.从图中可以看到,不同氧化时间陶瓷膜的能谱分析取点皆在相对光滑的表面.能谱图中显示主要有3个峰,表示氧化陶瓷膜的成分均含有Al、O、S元素,其中Al和O元素的峰较高,说明氧化陶瓷膜的主要成分为Al和O元素.表9为不同氧化时间下氧化陶瓷膜各元素原子数分数,是图9各元素含量的具体数值,不同反应时间的产物各元素的质量分级有差距,但是差距不大.氧化陶瓷膜主要由Al元素和O元
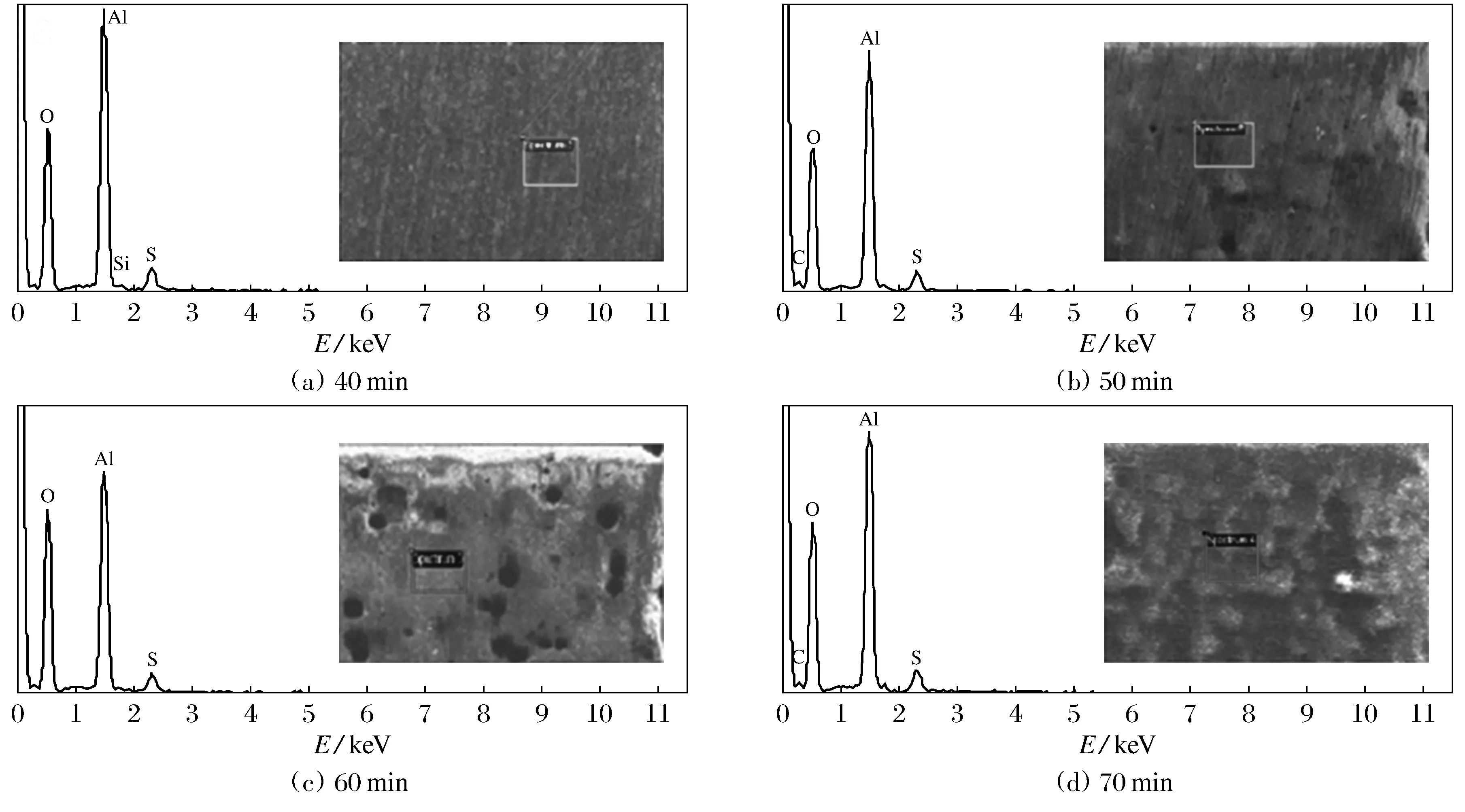
图9 不同氧化时间下的SEM-EDS能谱图Fig.9 Energy spectrum of different oxidation time
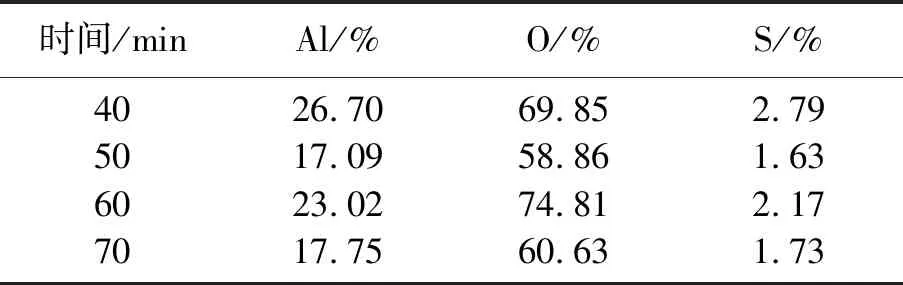
表9 不同氧化时间下氧化陶瓷膜主要元素原子数分数Table 9 Mass fraction of main elements in oxide ceramic film under different oxidation time
素构成.Al元素来自于铝基体,所以峰值最高.电解过程中产生的O元素与基体中的Al元素生成Al2O3是氧化陶瓷膜的主要成分.图中的S元素来自于电解液,Si元素与C元素为氧化陶瓷膜表面的污染物所致.
图10为氧化陶瓷膜的XRD谱图.图中可见有4个Al衍射峰,这是由于氧化陶瓷膜过薄,X射线直接打到铝合金基体所致.在2θ为20°~40°之间出现宽化的衍射峰,说明膜层的结构为非晶态的Al2O3.
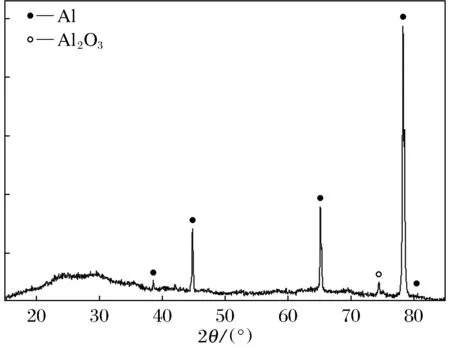
图10 氧化陶瓷膜的XRD谱图Fig.10 XRD pattern of oxide ceramic film
3 结 论
1) 2024铝合金氧化在硫酸-草酸体系中,使用脉冲电源制备出的氧化陶瓷膜以非晶态的Al2O3为主要成分,且不随工艺参数的变化而改变.
2) 2024铝合金氧化陶瓷膜的厚度随着工艺参数的变化而变化.电流密度超过4 A·dm-2,氧化时间超过60 min,硫酸质量浓度超过250 g·L-1时,氧化陶瓷膜的厚度开始显著减小.
3) 2024铝合金氧化陶瓷膜的耐腐蚀性能受氧化时间、电流密度和硫酸质量浓度的影响很大,在硫酸-草酸体系中,电流密度应控制在4 A·dm-2,氧化时间应控制在60 min,硫酸质量浓度应控制在250 g·L-1,耐腐蚀性能较好.
