肿瘤甲基化抑制剂5-氮杂-2′-脱氧胞苷抑制人皮静脉内皮细胞及生长因子受体2
2020-04-29陈涵李鼎鹏郑先丽
陈涵 李鼎鹏 郑先丽
(1甘肃省康复中心医院,甘肃 兰州 730030;2甘肃省中医药研究院;3甘肃中医药大学附属医院)
目前认为恶性肿瘤的发生是由多种因素导致的,这些自身基因和外在因素共同作用使人体细胞的DNA遭受非凋亡性损害,此过程会使潜在的致癌和抑制肿瘤灭活基因被激发,此时正常基因也会起到干预和阻滞作用,但在这过程中正常细胞逐渐发生癌性改变。我国恶性肿瘤每10万人发生人数为285.91人,其中总体发病人群60岁以上超过3/5,城市发病率比农村高20%,而农村的死亡率却比城市高8%〔1,2〕。
国家癌症中心最新发布的包含了全国所有癌症登记点的数据中指出,患病男性主要暴露因素为生活习惯、职业环境、各种压力等相关因素〔3〕。而对于肿瘤的研究,诸多研究者发现血管生成与其缓慢发展和逐渐扩散关系非常紧密,当周径<2 mm时,肿瘤只有原发部位的浸润,呈潜伏性;当肿瘤>2 mm时,血管会逐渐形成,并伴随转移发生,新生血管的数目和增长速度决定了肿瘤的生长和扩散转移程度,可见新生血管形成对其的重要性〔4〕。基于上述理论,目前对肿瘤治疗药物的研究热点主要聚集在新生血管抑制剂上,肿瘤新生血管系统是由多种细胞参与的综合复杂过程,但这个过程最初的形成是由血管内皮细胞(EC)进行的,因此对其进行最初的阻断是阻止肿瘤生长的最初环节〔5〕。5-氮杂-2′-脱氧胞苷(5-Aza-CdR)可以与DNA甲基转移酶结合,依靠活性降低来抑制甲基化基因,调节其表观调控,抑制新生血管发生和分化,以此抑制肿瘤〔6〕。本研究从肿瘤扩散转移的新生血管出发,通过发挥5-Aza-CdR去甲基化功能抑制其最初始的血管EC来防治肿瘤发生。
1 材料与方法
1.1试剂 人脐静脉内皮细胞(HUVEC,货号:120704491600)购于赛默飞世尔生物化学制品(上海)有限公司美国。DMEM高糖培养基(货号:26406.02)、胎牛血清(货号:F7305)、基质胶(货号:526234)、胰蛋白酶(货号:SH35042.01)购自GIBCO;磷酸盐缓冲液(PBS)购自武汉博士德生物科技有限公司(货号:SH30256.01);噻唑蓝(MTT)粉(货号:88417)、Transwell小室(货号:CLS3583)和5-Aza-CdR(货号:HPBIO163803)购自SIGMA公司;聚偏氟乙烯(PVDF)膜(thermo fisher公司,货号:T2234);十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)蛋白上样缓冲液(货号:WB0135)和超敏化学发光(ECL)试剂盒(货号:WB0164)购自上海维奥生物科技有限公司。二喹啉甲酸(BCA)蛋白浓度测定试剂盒购自必拓生物(货号:K12001S)。
1.2仪器 实验室级纯水系统(millipore,Milli-Q Integral);超净工作台(苏州亿博,SZY3-12);高速低温冷冻离心机(GE,5804R);CO2细胞培养箱(SANYO,SY-25);-80℃超低温冰箱(Eppendorf,M450);光学显微镜(OLMPUS,BX60);电热数显恒温水浴锅(北京长风仪器仪表公司,HH-8);低速台式离心机(北京医用离心机厂,DS-2A);垂直电泳仪(美仑,MH0430);电转移装置(国药集团化学试剂有限公司,SE600)。
1.3细胞培养 将HUVEC从液氮中取出放入提前预热至37℃的水浴钵中,匀速晃动,直至完全溶解后放置于超净工作台进行操作。将废液弃去,胰酶消化后,培养基吹打后,接种于培养瓶,用含有10%胎牛血清的DMEM培养基培养,置于37℃,5% CO2的培养箱,72 h换液1次。在显微镜下观察细胞活性,在无污染的情况下,当细胞铺满瓶壁时进行传代,传代时弃去废液,吸取胰酶消化细胞,细胞皱缩快要脱落时弃去胰酶,加入DMEM培养基反复吹打,当细胞全部悬浮后分装到各培养瓶中,再加入含有10%胎牛血清的DMEM培养基进行培养。培养环境不变。各实验均将细胞分为空白对照组、1、5、10 μmol/L 5-Aza-CdR药物组(低、中、高剂量组)。
1.4MTT法检测5-Aza-CdR对HUVEC细胞的增殖作用 当细胞传至第3代时,取对数生长期HUVEC,按照传代步骤消化后吹打成细胞悬液,在离心机中1 000 r/min离心5 min,弃上清,加入DMEM培养基使HUVEC重悬,在细胞计数板中吸取10 μl细胞悬液,在倒置相差显微镜下观察计数,将其浓度调整为1×105个/ml后在96孔板中接种,每孔吸入200 μl的悬液,每孔为2×104个,设置调零孔,检测组每组10孔。每孔加入单纯的含10%胎牛血清的DMEM培养液,为减少培养液的蒸发,在周围孔每孔加入100 μl PBS。将96孔板置于CO2培养箱中过夜,然后弃上清,第1列含HUVEC培养孔和调零组的每孔加入无5-Aza-CdR的含10%胎牛血清的培养液。第2~4列孔中每孔分别加入5-Aza-CdR浓度为1、5、10 μmol/L的培养液100 μl。再次将96孔板置于培养箱中培养72 h,在24、48、72 h时各取出样本检测1次,弃废液,PBS洗涤后,加入完全DMEM培养基,每孔再加入 10 μl MTT,浓度为5 mg/ml,孵育4 h,弃去每孔液体,再加入200 μl二甲基亚砜(DMSO),以1 500频率震荡10 min,融解结晶,在酶标仪上调零后,检测各孔的吸光度值(A490值)。
1.5Transwell检测5-Aza-CdR对HUVEC细胞的迁移作用 传至第3代的细胞铺满培养瓶底时,用胰酶消化后加入完全DMEM培养基,混悬细胞,以1×105个/cm2密度接种于24孔的Transwell板上层培养小室中,每孔200 μl,在Transwell孔板下层培养小室中分别加入空白对照组完全培养液、1%含5-Aza-CdR的血清培养液、5%含5-Aza-CdR的血清培养液、10%含5-Aza-CdR的血清培养液,然后将其仍置于培养箱中,分别在24、48、72 h测细胞迁移。
1.65-Aza-CdR对HUVEC细胞管样结构的形成作用 实验检测前1 d在超净工作台中铺基质胶,从-20℃冰箱中取出冷冻的冰袋,紫外线消毒15 min,基质胶与DMEM培养基以1∶3的比例混匀后,以50 μl/孔加入96孔板,96孔板置于冰袋上,将其放入37℃恒温箱中4 h后,转至4℃冰箱中过夜。取对数生长期HUVEC,弃废液,加入PBS冲洗1次后胰酶消化细胞,消化后加入完全培养基终止消化,吹打制备单细胞悬液并用细胞计数板分别计数。加入DMEM培养基将细胞稀释为浓度2×104个/cm2,将细胞吸取加入到之前铺好基质胶的96孔板中,置于37℃恒温箱培养30 min后,分别加入10 μl含有5-Aza-CdR浓度为1、5、10 μmol/L的培养液,继续放入培养箱中6 h后观察小管形成并拍照。
1.7Western印迹检测5-Aza-CdR对血管内皮生长因子受体(VEGFR)2的表达作用 细胞换液时各个培养瓶中分别加入含1、5、10 μmol/L 5-Aza-CdR的培养液,放入培养箱过夜后在检测孔中加入2 ml 4℃的PBS后晃动洗涤1 min,弃去废液后置于冰上,每孔加入裂解液100 μl,均匀来回摇动,裂解完成后用细胞刮刀收集,用移液器转移至1.5 ml离心管中反复吹打。高速低温冷冻离心机预冷4℃下离心10 min(12 000 r/min)后收集上清,-20℃保存备用。将裂解液A与裂解液B以50∶1比例混匀后加入BCA工作液,37℃恒温箱过夜稳定。余步骤按照说明书操作后在酶联免疫检测仪(562 nm)检测吸光值,计算出样品中的蛋白浓度。据目标蛋白浓度,加入双蒸水和5×上样缓冲液后100℃灭活10 min,得到最终的蛋白样品,配制的10%分离胶灌胶至绿带中间线高度时即可,待浓缩胶凝固后加入电泳液,上样量计算依据为检测蛋白含量中含30 μg蛋白,同时加入蛋白Marker作为标记,以连续系统中上层浓缩胶的电泳电压为恒压90 V,分离胶电泳电压为恒压160 V进行电泳,完成后,在冰水中放入转膜装置并在295 mA条件下电泳1.5 h进行转膜。加入抗体稀释液的稀释磷酸化兔抗人VEGFR2(1∶1 000),封口,4℃摇动孵育过夜进行孵育抗体杂交,然后进行发光显色。室温孵育3 min后进行压片曝光,扫描胶片后通过图象处理系统分析目标带净光密度值。
1.8统计学分析 采用SPSS21.0软件进行Q检验、单因素方差分析、LSD检验、DunnettT检验。
2 结 果
2.15-Aza-CdR对HUVEC增殖的影响 高剂量组各时间点HUVEC的吸光度值显著低于空白对照组和低剂量组(P<0.01)。低、中剂量组48、72 h的吸光度值显著低于空白对照组(P<0.05),且中剂量组72 h的吸光度值显著低于低剂量组(P<0.05);见表1。提示在时间程度上,时间长短与HUVEC的抑制程度呈正相关,而且在最大时间限度内药物浓度越大对HUVEC的抑制作用越明显。
2.25-Aza-CdR对HUVEC迁移的影响 不同浓度5-Aza-CdR在不同时间段能抑制HUVEC迁移,以高剂量组抑制效果最明显。低、中、高剂量各时间点的HUVEC迁移均显著小于空白对照组(P<0.01)。中、高剂量组各时间点的HUVEC迁移均显著小于低剂量组(P<0.05,P<0.01),见图1,表2。
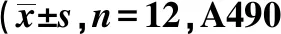
表1 培养不同时间点各组HUVEC增殖值)
与空白对照组比较:1)P<0.05,2)P<0.01;与低剂量组比较:3)P<0.05,4)P<0.01;下表同

图1 孵育24、48、72 h各组HUVEC迁移情况(台盼蓝染色,×200)

表2 不同培养时间各组HUVEC迁移
2.35-Aza-CdR对HUVEC细胞管样结构形成的作用 不同浓度5-Aza-CdR在一定时间段内对HUVEC细胞小管形成影响不同,小管形成能力随5-Aza-CdR浓度的降低而增加(图2)。细胞接种6 h后在基质胶上排列形成类似于毛细血管的完整管腔。在不同浓度5-Aza-CdR作用下,HUVEC细胞成团聚集,基质胶上完整的管腔结构与空白对照组相比显著减少。与空白对照组比较,各剂量组小管形成完整的管腔结构显著减少;低剂量组6 h后管腔结构被破坏,不时有断裂出现,呈现一种不完整的、稀疏的网状结构;中剂量组细胞管腔结构破坏严重,断裂扩大,细胞不再聚集开始分散,网状结构明显;高剂量组几乎没有发现完整闭合的管腔形成,5-Aza-CdR对HUVEC细胞形成管腔能力的抑制作用则更明显。提示,不同浓度5-Aza-CdR均可降低HUVEC小管形成能力,使小管周径变小、成环率降低,高剂量组抑制作用最明显。

图2 各组HUVEC细胞管样结构生成活性(Brdu,×200)
2.45-Aza-CdR对细胞VEGFR2表达的作用 随含药浓度增加,细胞内VEGFR2蛋白表达降低,见图3。5-Aza-CdR可以明显抑制VEGFR2蛋白表达,并与剂量浓度大小有正相关关系,浓度越大其抑制蛋白表达的作用也越明显。

图3 5-Aza-CdR干预HUVEC 24 h后VEGFR2表达
3 讨 论
血管生成是肿瘤血管形成的经典方式,它是原有血管在肿瘤细胞分泌的各种促血管生长因子的作用下,经过一系列降解、EC增殖迁移导致形成新生血管的过程。虽然部分肿瘤的发生可以不伴有血管形成,但是因为其最初的原位癌有潜在漫长的休眠期,此时期肿瘤体积很小只有几立方毫米,但当足够数量的细胞从休眠表型转变为血管化表型时,便会快速生长并会有转移〔7〕。Folkman等〔8〕首次提出血管生成对于肿瘤生长和转移的重要性,并由此推断抑制肿瘤生长的有效措施可以是阻断血管生成,在此机制中把肿瘤生长发生的机制归结为肿瘤本身和依存的环境致使血管生成,主要是EC被刺激活化使拮抗因子平衡失调导致的过程,尤其会导致加速扩散增殖。此策略观点被后来的学者接受,并一致认为肿瘤血管生成中EC的不断增殖和迁移是极为重要的环节,并针对此机制研发了抑制EC的药物,以此抑制肿瘤血管的生成。烟曲霉类似物TNP-470便是典型的肿瘤血管抑制剂,在临床各种实体恶性肿瘤的迁移验证中取得了较好的疗效〔9〕。研究证明EC通过增加自身的血管生成或增加肿瘤细胞迁移到细胞外基质的侵袭能力来调节肿瘤细胞的侵袭能力〔10〕。而且研究已充分证明此种以EC为靶点来抵抗血管新生来抑制肿瘤细胞增殖是可行性极高的方式〔11〕。其主要表现为首先在肿瘤细胞刺激下的EC功能变化引起相关生化指标的变化可通过血液系统获得直接体现,有利于肿瘤的早期预测;其次,EC也是肿瘤药物治疗时最先到达的靶细胞。
研究发现,非小细胞肺癌化疗时采用5-Aza-CdR进行辅助可以改善药敏降低,使细胞受到抑制和凋亡〔12〕。肿瘤血管的发生从单一细胞增殖开始逐渐发展为大量细胞增殖,新生血管会在原有基础上快速增殖,通过细胞的不断增殖来为HUVEC提供源源不断的营养,而HUVEC反过来又会分泌多种物质来促进这个过程的加快,因此,抗血管生成首先就要抑制细胞增殖〔13〕。本研究提示,5-Aza-CdR在参与抑制血管生成过程的机制之一可能是抑制细胞增殖而起作用。
以含药血清干预HUVEC来抑制其增殖和迁移使血管难以或者延迟生成,是依靠EC的黏附力降低以使EC损伤加快诱发肿瘤血管新生和转移〔14,15〕。由此可见,肿瘤的发生和转移中血管生成起到很大的作用,抑制此过程将是治疗的一个有效措施。本研究提示5-Aza-CdR可能是抑制细胞迁移而阻滞血管生成来防治肿瘤的发生。
肿瘤的血管形成过程是增殖-迁移-血管形成〔8〕。血管生成的过程虽然复杂,但是其主要途径之一便是EC的活化、增殖和迁移,最后形成管样结构,在管样结构形成的基础上,再由多个血管芽相互连接形成血管网状结构〔16〕。因此,抑制血管形成中的管样结构,使其难以形成网状结构是阻滞肿瘤发生的重要步骤。本研究表明,5-Aza-CdR可显著抑制HUVEC的管腔形成。
不论是原发性还是转移性的肿瘤均有内部因子失控的发生〔17〕。肿瘤在快速生长和侵袭周围环境时需要较多的营养和有氧化条件,当所在血管不能满足发展时会激发肿瘤细胞生成促进血管新生的因子,来改变局部环境利于其生长。在此过程中因为这些分泌的因子,EC会快速增殖、芽生,迅速形成管腔,以此建立连接功能性血供网为肿瘤提供充足的养分〔18〕。EC在新生血管的前端持续迁移以便于竞争顶端细胞,而这种趋势需要细胞内环境信号的依赖〔19〕。通过肿瘤血管中EC前期研究,发现促进EC迁移是多种因子作用的结果,这些因子与其相应的受体及靶细胞结合以此促进迁移,来诱导血管新生,使肿瘤发生转移,其中血管内皮生长因子(VEGF)便是影响EC迁移最重要的因子〔20〕。VEGF通过激活细胞外信号调节激酶和丝裂原活化蛋白激酶信号转导途径引起EC增殖和迁移。内皮顶端细胞在胞外VEGF诱导下,高表达的VEGFR2促使HUVEC更易于占据顶端位置〔21〕。而5-Aza-CdR还能干扰VEGFR2降低细胞能动性,使作为血管生成因子在肿瘤血管生成中具有强大调节性的最活跃和最强特异性的VEGF受到阻滞,抑制肿瘤的形成、转移。本研究发现VEGFR2蛋白表达量显著下降,其蛋白下降的程度与药物浓度呈正比。
本课题组在前期研究的基础发现5-Aza-CdR作为一种特异性甲基转移酶抑制剂能够抑制血液恶性肿瘤和多种实体肿瘤细胞,有着广谱抗肿瘤的作用〔22〕。因此,充分利用其抗肿瘤的广谱性质和去甲基化的作用,结合分子生物学研究药物途径抑制HUVEC的增殖、迁移、小管形成和血管因子受体蛋白的作用和表达,达到有效、安全、快速抑制恶性肿瘤细胞和治疗肿瘤的目的,在目前的医疗水平阶段有重要意义,是一种应用前景良好且有效的抗肿瘤药物。
