影响新生儿毛细血管渗漏综合征预后的危险因素
2020-04-27张忠垚李禄全
韦 欢 张忠垚 李禄全
重庆医科大学附属儿童医院新生儿诊治中心 儿科学重庆市重点实验室 儿童发育疾病研究教育部重点实验室 国家儿童健康与疾病临床医学研究中心 儿童发育重大疾病国家国际科技合作基地(重庆 400014)
毛细血管渗漏综合征(capillary leak syndrome,CLS)是以毛细血管内皮细胞损伤,血管通透性增加,大量血浆蛋白渗漏到组织间隙为特征,可能导致全身性水肿和多发性器官衰竭甚至休克为临床表现的危重疾病[1-2]。其主要的临床表现包括进行性的全身性水肿、低蛋白血症、低血压、体质量增加、血液浓缩,严重时发生多器官功能障碍综合征等。新生儿CLS发病率为1.62%,病死率高达30.6%[3],引起新生儿CLS的病因多样,包括败血症、呼吸窘迫综合征、寒冷损伤综合征、高血糖等[3-4]。
以成人为对象的临床研究表明,影响CLS预后的危险因素包括感染加重、组织灌注进一步恶化、脓毒性休克难以纠正、内环境紊乱、严重低蛋白血症、氧合指数低以及多器官功能障碍综合征等[5-6]。探讨影响新生儿CLS预后的危险因素少有报道,国内有文献报道,15例CLS新生儿死亡原因包括多器官功能障碍9例、肺出血3 例、休克2 例和脓毒症1 例[3]。为改善新生儿CLS 预后、提高新生儿生存率,本研究分析影响新生儿CLS预后的因素。
1 对象与方法
1.1 研究对象
本研究为回顾性研究。以2010 年10 月—2019 年7月在重庆医科大学附属儿童医院明确诊断为CLS的新生儿为研究对象,入组标准:①入院日龄≤28 天;②符合CLS诊断标准[7]。排除入院日龄>28天、住院时间<48小时、临床资料不全者。
根据研究对象的治疗结局分为存活组及死亡组。
1.2 方法
1.2.1 临床资料收集 回顾性收集两组患儿母孕期基本特征(包括是否合并妊娠期高血压、妊娠期糖尿病、妊娠期胆汁淤积、胎膜早破、羊水污染),两组患儿入院时的基本情况(包括胎龄、出生体质量、性别、入院日龄等)以及住院期间发生的合并症、主要治疗方案及住院天数、结局等。
1.2.2 CLS诊断标准 临床上满足以下1~5条中1条,必须满足第6 条:①原发病无法解释的血压、中心静脉压下降;②全身水肿,伴有胸腔、腹腔或心包积液;③氧合指数<300 mmHg;④胸片提示有间质性渗出改变;⑤血清白蛋白显著降低(<25 g/L),红细胞比容降低不明显;⑥排除心源性、肾源性、肝源性水肿及遗传代谢性疾病引起的水肿。
1.2.3 复杂性先天性心脏病 指生后1 年内需要内科介入或外科治疗的先天性心脏病[8]。本文特指主动脉缩窄、肺动脉闭锁、肺静脉异位引流、完全型大动脉转位和主动脉弓发育不良。
1.3 统计学分析
采用SPSS 21.0统计软件进行数据处理。符合正态分布的计量资料采用均数±标准差表示,组间比较采用两独立样本t检验;非正态分布以中位数(四分位数范围)表示,组间比较采用非参数检验。计数资料以百分比表示,组间比较采用χ2检验。采用二元logistic回归分析影响毛细血管渗漏综合征预后的独立危险因素。以P<0.05表示差异有统计学意义。
2 结果
2.1 基线资料
本研究纳入临床明确诊断CLS患儿66例,其中男45例、女21例,平均胎龄(38.14±4.27)周,平均出生体质量(2 775.00±958.95)g,入院日龄5.50天(1~12天)。66 例患儿中37 例有复杂性先天性心脏病。主动脉缩窄11例,其中2例合并主动脉弓发育不良、1例合并肺静脉异位引流;肺动脉闭锁2 例;肺静脉异位引流14例,其中1例合并主动脉缩窄,1例合并主动脉弓发育不良;完全型大动脉转位10例;主动脉弓发育不良4例,其中2 例合并主动脉缩窄、1 例合并肺静脉异位引流。均进行外科手术治疗。
CLS新生儿入院后均予呼吸机辅助呼吸,积极治疗原发病,输注白蛋白、丙种球蛋白,利尿,限制补液量等治疗,复杂先天性心脏病患儿均采取外科手术治疗。最终,存活46例(存活组),死亡20例(死亡组)。
存活组低出生体质量儿的比例低于死亡组,出生体质量高于死亡组,差异有统计学意义(P<0.05)。两组患儿在性别、胎龄、入院日龄,孕母妊娠期高血压、妊娠期糖尿病、妊娠期胆汁淤积、羊水污染及胎膜早破发生率方面比较,差异均无统计学意义(P>0.05)。存活组住院时间长于死亡组,两组比较差异有统计学意义(P<0.001)。见表1。
2.2 影响CLS预后的单因素分析
CLS 患儿可存在多种并发症,包括呼吸衰竭(66.7%)、低蛋白血症(63.6%)、凝血功能障碍(54.5%)、低心排综合征(53%)、肾脏损害(48.5%)、心力衰竭(24.2%)及肺出血(22.7%)等。死亡组患儿肺出血、消化道出血、高血糖、高钾血症的发生率明显高于存活组,差异有统计学意义(P<0.05)。两组患儿的复杂先天性心脏病、低心排综合征、肺动脉高压、呼吸衰竭、心力衰竭、肾脏损害、凝血功能障碍、新生儿败血症、休克、呼吸窘迫综合征、异常出血、血小板减少症、低蛋白血症、贫血发生率比较,差异无统计学意义(P>0.05)。见表2。
2.3 CLS预后的独立危险因素
将影响CLS 预后的危险因素,如低出生体质量、肺出血、消化道出血、高血糖、高钾血症纳入二元logistic 回归分析(向前逐步回归法),发现肺出血(β=2.104,Wald χ2=10.432,OR=8.200,95%CI:2.287~29.399,P=0.001)是影响CLS预后的独立危险因素。
3 讨论
CLS 主要是由于血管内皮细胞的损伤、凋亡、收缩变形等引起内皮细胞功能失调,最终引起微血管渗漏性增加,使细胞内富含蛋白质的液体流向组织间隙,导致全身性水肿为突出表现的危重症[9]。严重CLS 患者往往并发多器官功能障碍综合征[2]。本组CLS患儿主要的严重并发症包括低心排综合征、呼吸衰竭、肺动脉高压、肺出血、呼吸窘迫综合征、心力衰竭、休克等。目前关于影响CLS新生儿预后相关危险因素报道极少,未见探讨影响其预后危险因素的病例对照研究或队列研究。分析影响其预后的危险因素有助于临床采取预防性措施,改善患儿预后。
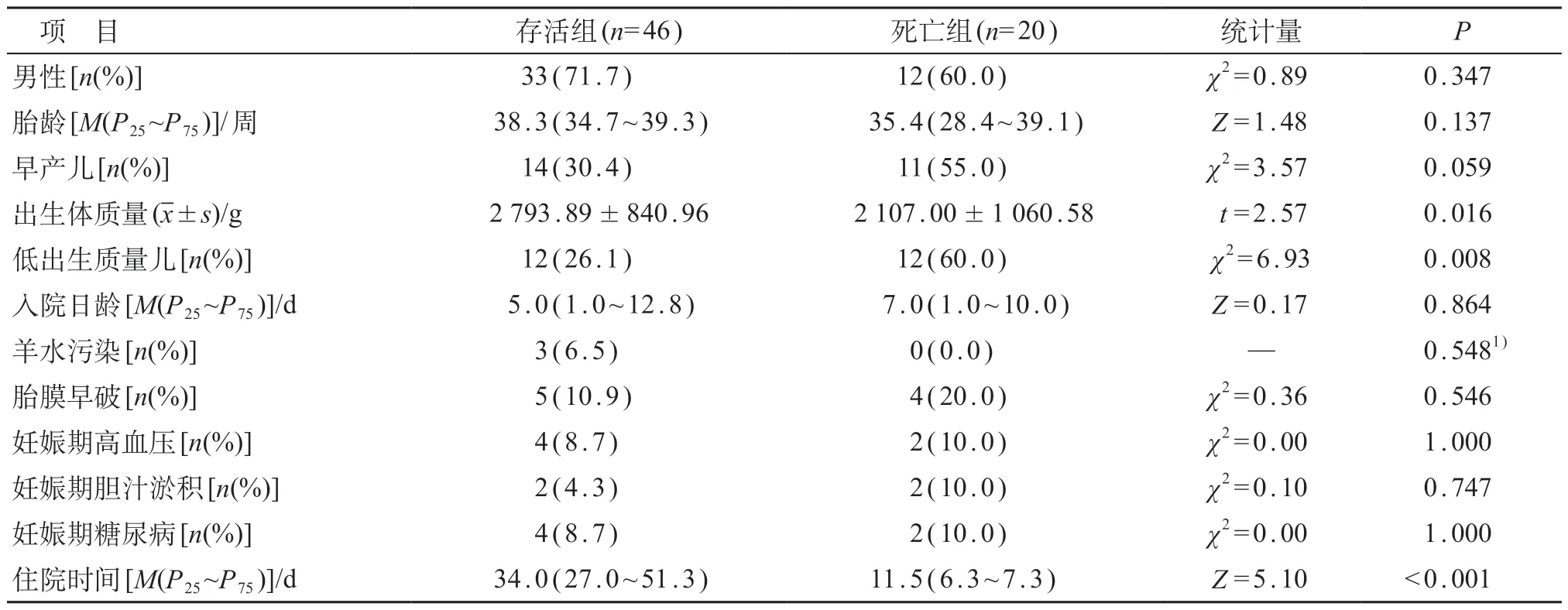
表1 两组患儿一般情况比较
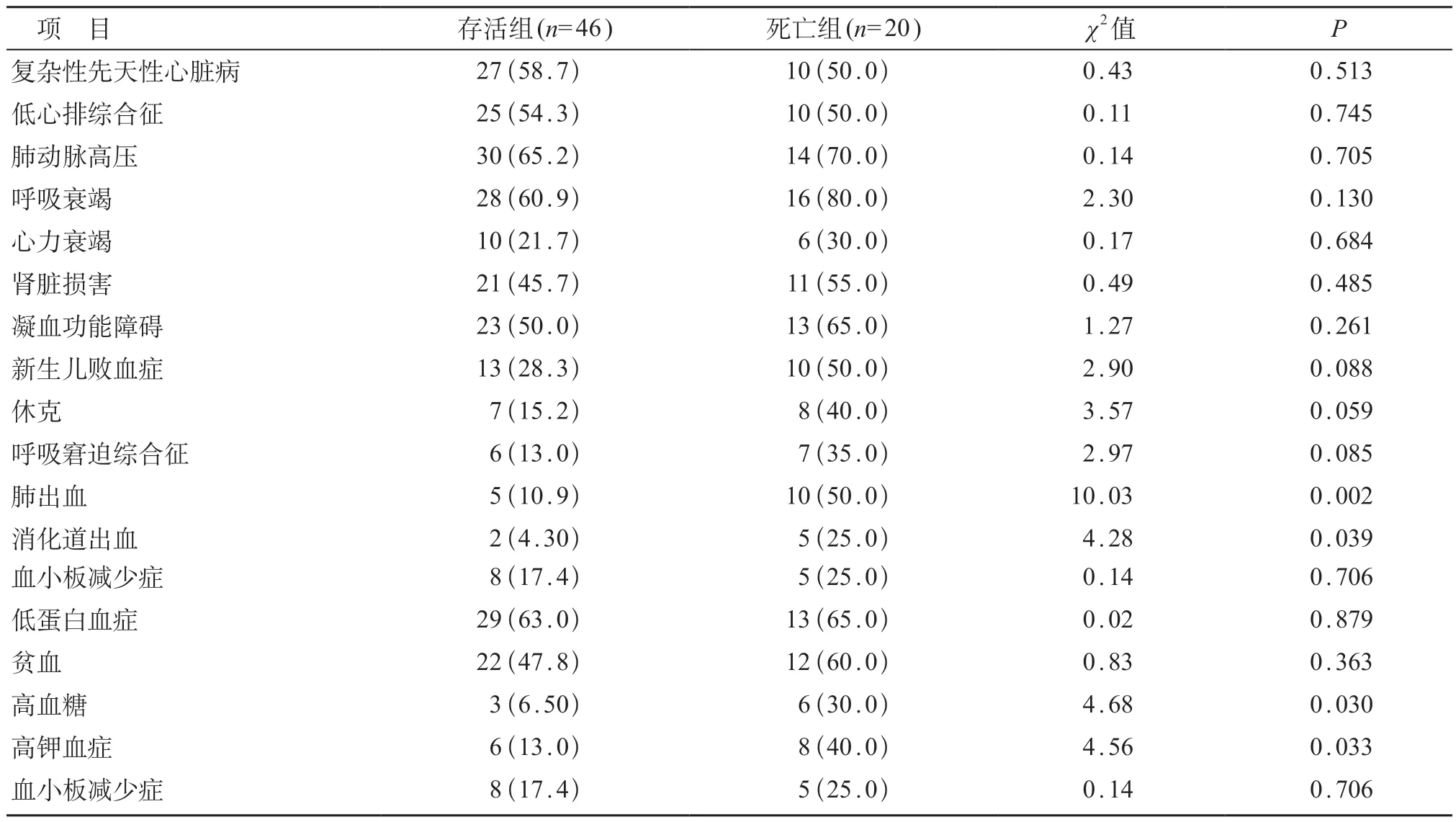
表2 影响CLS预后的单因素分析 [n(%)]
本研究经多因素分析发现,肺出血显著增加CLS新生儿病死率。肺出血是引起新生儿死亡的严重疾病之一[10],其发生的危险因素有早产、低出生体质量、感染、围生期缺氧缺血性损伤、低体温、凝血功能障碍、急性左心衰竭等[11-13]。在CLS 渗漏期,患儿全身毛细血管通透性增加,大量体液渗漏至肺间质,使肺顺应性降低,换气率降低,可导致严重的低氧血症,增加肺出血发生风险[14]。肺出血发生后显著增加患儿病死率[10,12]。本研究发现病死组肺出血患病率高达50%,即使在存活组也有10%的患儿存在肺出血。因此,积极防治肺出血可能改善CLS患儿的预后。
本研究单因素分析发现低出生体质量对CLS 预后有影响。存活组患儿低出生体质量显著低于死亡组。推测这与低出生质量儿本身免疫力弱,器官功能发育不完善,危重状态下病情更容易恶化,从而导致预后不良有关。本研究中CLS患儿消化道出血、高血糖、高钾血症患病率分别为10.6%、13.6%、21.2%。考虑这主要与CLS患儿在应激状态下,容易并发消化道出血及内环境紊乱有关。进一步单因素分析发现死亡组消化道出血、高血糖、高钾血症患病率明显高于存活组(P<0.05)。高钾血症可增加心跳骤停的发生风险,诸多研究也表明高血糖症与新生儿预后不良密切相关[15-17]。本研究中,7例发生消化道出血的患儿(存活组2 例,死亡组5 例)均存在肺出血,且并未合并消化道畸形或坏死性小肠结肠炎等严重肠道疾病。因此考虑消化道出血为伴随症状而非独立危险因素。
本研究的局限性在于存在回顾性研究的缺陷及偏倚。且本研究样本量较小,有待继续进一步扩大样本量并进行多中心大样本量的研究提供更多临床数据,以提高CLS新生儿存活率及改善后期生活质量。
综上所述,本研究提示肺出血是新生儿CLS预后的独立危险因素,采取针对肺出血为主的综合性防控措施可能对降低新生儿CLS死亡率有促进作用。
