纳米粒子给药系统在内耳靶向给药的研究进展
2020-04-27安晓刚查定军
安晓刚 查定军
空军军医大学西京医院耳鼻咽喉头颈外科(西安710032)
听力损失已成为世界上最常见的感觉障碍性疾病[1]。世界卫生组织(WHO)网站最新数据,听力损失人口已超过4.66亿人,其中3400万是儿童;11亿年轻人(12-35岁)由于暴露于娱乐环境的噪音中,从而面临着听力损失的风险;全球每年用于听力损失的花费高达7500亿美元。据WHO估计,到2050年,超过9亿人将丧失听力[2]。
由于内耳某些特殊的生理和解剖学特征严重阻碍药物对耳蜗靶细胞的供应和吸收[3,4],临床上对感音神经性听力损失疾病的治疗方案有限。内耳特殊的生理特征决定不同给药途径及疗效。给药过程中,许多药物的血浆半衰期短,随着身体新陈代谢的变化,个体间存在很大差异[1,5],上述因素都会影响药物的有效输送和吸收,如何解决这些问题成为治疗听力损失的关键。
近些年,伴随纳米技术的发展,兴起的纳米给药系统能够解决上述难题,靶向给药和治疗内耳疾病具有极大的潜在希望,通过可降解、无毒的纳米粒子将药物装载、构建靶向特异识别配体、递送到达靶组织器官及细胞,可实现靶向给药及治疗,且无毒副作用,成为研究热点。
1 内耳解剖生理特点及内耳给药途径
1.1 内耳解剖生理特点
内耳深隐于颞骨之中,Corti器位置较隐蔽,体积小且结构精细,内部充满内、外淋巴液,壶腹嵴、椭圆囊斑和球囊斑浸泡于内淋巴液中。内耳给药途径存在多个屏障,其中血-迷路屏障的存在使得内耳与身体其他部分隔离,使药物不能迅速到达整个耳蜗[1,6,7]。特殊的生理和解剖学特征比较适合于局部药物递送,但是圆窗膜(round window membrane,RWM)和卵圆窗(oval window,OW)的选择透过性在很大程度上限制了内耳局部给药的应用。
1.2 内耳不同给药途径及优缺点
内耳给药途径主要包括全身给药、经中耳鼓室给药和内耳内直接给药。全身给药主要通过口服、静脉注射、肌肉注射等方式给药。Fowler率先研究证实静脉注射链霉素可有效控制耳源性眩晕[8],后来发展应用氨基糖苷类抗生素治疗梅尼埃病[9]。临床广泛采用皮质类固醇激素治疗突发性感音神经性聋[5,6]和自身免疫性内耳疾病[10]。由于内耳血-迷路屏障阻碍药物向内耳的弥散分布,使得局部药物浓度难以达到理想状态。虽然经全身给药治疗内耳疾病应用广泛,但靶向性差、局部药物浓度低及分布不均匀、全身副作用大等缺点。
相比全身给药,内耳特殊的生理和解剖学特征更适合于局部药物递送。局部药物递送可绕过血-迷路屏障,使得较低剂量的药物能够更直接地实现预期目标,副作用最小化。目前,比较适用于局部药物输送到内耳的给药方式有两种[1,3,7],分别为中耳鼓室给药和内耳直接给药。中耳鼓室给药主要有经鼓膜、乳突两种给药途径,通过将药物置于中耳鼓室,随后药物通过RWM进入内耳鼓阶外淋巴液并扩散分布到内耳各个部位;也可通过OW进入前庭阶,再扩散分到内耳其他部位[3,11]。
1957年,Schuknecht等[12]首次尝试中耳鼓室内注射庆大霉素治疗梅尼埃病,并获得成功。发展至今,中耳鼓室内注射药物已成为梅尼埃病和突发性耳聋的标准治疗方法的一部分。然而,不足的是中耳鼓室给药,渗透到达内耳中的药物浓度仍然相对较低。
内耳直接给药途径包括内耳耳蜗内或前庭内直接给药[1,7]。内耳直接给药相比全身给药和经中耳鼓室给药,药物递送更直接、更容易到达靶目标。另外,随着纳米技术发展起来的纳米粒子药物递送系统使得内耳直接给药效果更好,不仅可解决上述难题,而且实现高效靶向治疗。
2 纳米粒子给药系统
纳米粒子是指粒度在1-100 nm之间的粒子。“纳米”的最初概念是由诺贝尔物理学奖获得者Richard P.Feynman首次提出[13],并引起科技人员的关注。直到1999年,才开始称为“纳米粒”,将粒径大小处于纳米级范围的给药系统统称为纳米给药系统(Nanoparticulate drug delivery systems)。1965年,脂质体纳米材料诞生[14],科技人员将其用于药物递送研究[13-15],纳米粒被广泛用作药物载体用于药物递送[16-18]。药物递送目标和功能的实现需要借助药物递送系统或称给药系统[13]。后来的研究中,学界给予纳米给药系统高度关注和深入的研究,随着纳米材料的发展,现已发展成为研究药物体内外活性常规技术[13]。
2.1 纳米粒子给药系统的优点
纳米粒子给药系统可以弥补药物溶解度低、易降解、半衰期短和不稳定等缺点,并能提高递送效率,减少内耳疾病治疗中出现与药物相关的副作用[1,19]。同时,纳米粒子可以提高生物相容性、体内稳定性和靶向特异性。纳米粒子给药在临床应用前首要考虑的问题是材料的可降解性和安全性。新型的纳米水凝胶给药系统可完美的解决该问题[20-23]。通过纳米粒子封装治疗药物,可增加细胞/组织对药物的摄取和内化,从而大大减少所需剂量、减少副作用。这种独特的性能组合使纳米粒子成为一种新的药物递送载体,比较适用于内耳药物递送[7]。
2.2 纳米粒子给药系统适用于局部药物递送
纳米粒子给药系统适用于内耳局部药物递送的优点已被研究证实[1,7,24]。从理论上讲,纳米粒子载体给药可以提高内耳的药物利用率,并持续释放药物[25,26]。纳米载体携带基因或药物成为内耳疾病治疗研究新的工具[27],可将目的基因导入内耳实现基因治疗[27-29]。
局部给药治疗内耳疾病的研究越来越受到重视,通过纳米医学策略将药物递送到内耳有望成为治疗内耳疾病(包括听觉和平衡障碍)的有效方法。但是,在全面临床应用前亟须解决的问题之一是开发用于药物靶点和内耳控释的智能给药系统[7],针对内耳特殊的解剖生理特点,正确选择合适的内耳给药途径至为关键。
3 纳米粒子给药系统内耳靶向给药及应用研究
鼓室内注射已被用作递送氨基糖苷类,类固醇和其他治疗药物、实现内耳治疗的方法[30,31]。但当药物经中耳鼓室内注射后,药物必须通过RWM或OW到达内耳才能被吸收利用[25]。鼓室内应用的NPs或药物主要通过RWM[32-35]扩散进入内耳外淋巴,RWM的渗透性已得到广泛研究,并被视为主导途径[36]。然而,由于镫骨足板被环状韧带包围封闭,通过OW进入前庭的通道(即OW)被长期忽视。研究发现药物既可通过RWM,也可通过OW进入内耳,OW可能性更高[37]。对于内耳最佳直接给药途径是RWM还是OW途径,目前尚无统一定论。
3.1 内耳直接给药最佳途径的探究
Tanaka K等人[38]使用辣根过氧化物酶作为示踪剂,通过电子显微镜证实了OW的渗透性。此后的研究证明离子标记物三甲基苯基铵直接进入镫骨临近的前庭[39],有研究发现钆和庆大霉素进入内耳的过程中,OW途径比RWM更容易[40-42]。然而,OW能否有效促进NPs向内耳的传输仍不清楚,OW和RWM哪个途径更有利于内耳药物输送,尚无统一结论。
2018年,陈钢[37]等人设计了荧光可追踪壳聚糖纳米粒子(CS-NPs),研究NPs在耳蜗和前庭器官中的分布,并评估了RWM和OW途径对NPs转运的有效性。豚鼠体内实验结果表明,CS-NPs可通过RWM和OW进入内耳,但OW在向前庭呈递NPs中具有控制作用。基于上述发现,他们首次提出将OW作为内耳给药“Royal Gate”的观点,认为能够方便和有效的促进CS-NPs进入内耳,降低耳蜗毛细胞病理相关的听力损失风险。然而,这一新的观点还有待更多的学者对不同材料纳米粒子载药系统及负载药物进一步验证后,方可定论。
3.2 纳米粒子给药系统用于内耳靶向给药及治疗研究进展
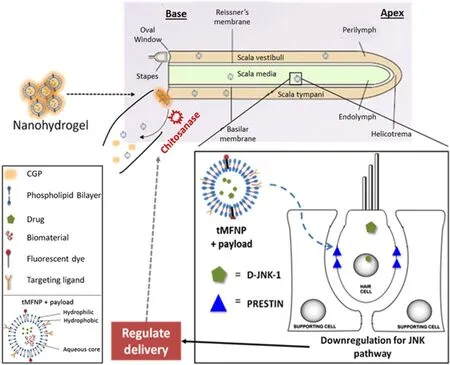
图1 纳米水凝胶药物递送系统靶向治疗噪声性听力损失示意图(图片引自文献[23])Fig.1 Schematic diagram of nano-hydrogel drug delivery system targeted therapy for noise-induced hearing loss(Image taken from the literature[23])
近些年,对纳米粒子载药系统的研究重点不再是简单地研究纳米粒子渗透到内耳中,而是研究如何将药物加载到纳米粒子上并将其转移到内耳以观察功能变化[43,44]。Sun[44]等人使用聚乙二醇-聚乳酸(PEG-PLA)纳米粒子包裹药物递送,在用负载地塞米松的纳米粒子进行鼓室内预处理后,注射顺铂使豚鼠耳聋。这项研究表明,施用负载地塞米松的纳米粒子可保护频率在4 kHz和8 kHz的听觉功能。另一项顺铂诱导的听力损失研究表明,使用α生育酚衍生物将6a-甲基强的松龙装载到纳米粒子上,可保护10 kHz,14 kHz和16 kHz频率的听觉功能[43]。以上研究表明,通过纳米粒子递送药物可直接观察到听力的实际变化,这对听力损失的治疗具有重要意义。然而,这些研究缺乏有关纳米粒子适用于内部药物递送的适当表面特性的信息,也缺乏与临床使用的药物的比较研究[25]。因此,优化纳米粒子的表征,明确纳米粒子在内耳的分布,对于螺旋神经节和耳蜗毛细胞靶向性药物载体的开发至关重要。
2010年,Sakamoto等人[31]以临床应用材料为基础,对三种内耳给药系统进行了评价。与小鼠体内应用倍他米松相比,隐形纳米粒子封装倍他米松的的全身应用为治疗噪声诱发的听力损失提供了更好的治疗效果。利用生物可降解聚合物(PLGA)包覆利多卡因制成的微粒,将其置于豚鼠RWM上,使得耳蜗内药物浓度合理,且无严重不良反应。此外,他们进行并完成了I/IIa期临床试验,将明胶水凝胶与重组人IGF-1(rhIGF-1)结合并置于RWM上,对平均听力水平和不良事件随访24周,未观察到严重的相关不良事件。结果表明:使用这种方法,平均听力水平与高压氧治疗相当,高压氧治疗通常在全身性类固醇治疗失败后用作挽救治疗。这项纳米粒子药物输送的临床研究有望为未来临床内耳疾病的治疗提供理论依据,并促进对内耳药物输送的进一步研究。
Li等人一直致力于内耳给药系统的研究[45-48]。2015年,他们开发了一种微创纳米水凝胶给药系统。最近,他们基于先前开发的药物递送系统,进行功能修饰,并引入一种特异性识别prestin的靶向肽。经RWM途径注射,该系统通过靶向纳米粒子可将JNK抑制剂(D-JNKi-1)靶向递送到OHCs,可以改善对噪声性听力损失的保护(图1)[23],该研究是首次使用一种新型、微创、安全可控的内耳给药系统对NIHL进行保护。值得借鉴的是,该系统具备将生物材料递送到特定内耳细胞类型的潜力,减少由非靶向递送系统引起的潜在副作用。该靶向纳米水凝胶递送系统有望成为未来临床应用的治疗平台基础,对内耳疾病的治疗具有极大的发展潜力。
近些年,纳米粒子给药系统领域的研究趋势充分体现了多学科间的相互交叉融合,生物学家、化学家及临床研究者之间的协同合作、创新。基于纳米粒子的靶向给药系统为临床疾病的治疗研究提供了更好的技术支撑。
4 结语
听力损失是一个重要的临床问题,目前缺乏有效的预防或治疗手段。纳米给药系统为近年来内耳给药研究热点,已成为一种有效的药物释放控制内耳给药策略,被用于靶向给药和治疗听力损失,并在动物实验中取得了理想的治疗效果[23,25]。但目前,关于纳米粒子给药系统的研究仍多为实验阶段,仅少数进入临床试验。在纳米粒子药物递送系统用于临床治疗前仍然存在许多亟待解决的问题,如圆窗膜或卵圆窗途径药物输送的安全性和风险需要更深入的评估和验证,如何实现靶向给药依然是研究难点。
技术的发展是为了更好地服务于应用,只有当技术的发展永远走在应用的前面,才能更好地服务于应用。尽管纳米粒子给药系统的研究多为临床前阶段,但随着后续研究的不断深入和技术的不断进步、完善,相信纳米粒子药物递送系统应用于临床靶向治疗听力损失等疾病的前景是美好的。
