曲妥珠单抗联合新辅助化疗治疗HER-2过表达乳腺癌的临床研究
2020-04-22沈永康张美华陈文婷
沈永康 张美华 陈文婷
广东省佛山市禅城区中心医院药剂科,广东佛山 528000
分子靶向治疗区别于传统的单纯化疗,极大程度上改变了靶点不明确毒副作用大的缺点[1-3]。曲妥珠单抗作为一种靶向治疗药物,其安全性、作用机制和远近期疗效均为人们所普遍关注的问题[4]。在前大量体外实验和动物实验对曲妥珠单抗治疗HER-2过表达乳腺癌的作用机制进行了报道[5-7],然而曲妥珠单抗联合新辅助化疗治疗HER-2过表达乳腺癌远期疗效报道尚少。本研究旨在探讨曲妥珠单抗联合新辅助化疗治疗HER-2过表达乳腺癌的疗效和安全性,为临床治疗HER-2过表达乳腺癌提供科学依据。
1 资料与方法
1.1 一般资料
选取2013年1月~2018年12月我院新诊断HER-2过表达乳腺癌患者100例,按不同治疗方案分为观察组和对照组,每组50例。观察组均为女性;年龄24~65岁,平均(46.2±6.5)岁;受体情况:ER阳性21例,PR阳性18例;TNM分期:Ⅱb 4例,Ⅲa 29例,Ⅲb 17例;病理情况:浸润小叶癌19例,浸润性导管癌31例;腋淋巴结转移情况:阴性6例,阳性44例;乳腺术式:乳腺癌改良根治术13例,扩大根治术37例;辅助内分泌治疗:是34例,否16例。对照组均为女性;年龄22~64岁,平均(46.3±6.3)岁;受体情况:ER阳性22例,PR阳性19例;TNM分期:Ⅱb 3例,Ⅲa 31例,Ⅲb 16例;病理情况:浸润小叶癌20例,浸润性导管癌30例;腋淋巴结转移情况:阴性5例,阳性45例;乳腺术式:乳腺癌改良根治术12例,扩大根治术38例;辅助内分泌治疗:是35例,否15例。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准
参照美国国立综合癌症网络公布的《NCCN乳腺癌筛查和诊断临床实践指南》中乳腺癌的诊断标准并且HER-2过表达[8]。
1.3 纳入与排除标准
1.3.1 纳入标准 年龄18~65岁;无化疗禁忌证;具有完整病历资料;功能状态评分≥60分;预计生存期≥3个月;知情并签署知情同意书。
1.3.2 排除标准 哺乳期或妊娠期妇女;心肝肾功能不全者;伴有自身免疫性疾病。
1.4 治疗方法
对照组给予TCH方案新辅助化疗,包括每个周期第1天给予75 mg/m2多西他赛(江苏奥赛康药业股份有限公司,H20080443)静脉滴注,每个周期第1天给予6mg/(mL·min) 卡铂(齐鲁制药有限公司,H20020180)静脉滴注,21d为1个周期,连续治疗6个周期。观察组在此基础上给予曲妥珠单抗(上海罗氏制药有限公司,J20180073)静脉滴注,第1周4mg/kg,之后每周2 mg/kg,连续治疗17周。TCH方案新辅助化疗完成后接受既定手术,包括乳腺癌改良根治术或扩大根治术。
1.5 观察指标
两组患者均获得为期5年的随访,中位随访时间为5.36年(5.00~6.18)年,随访途径包括电话、短信及复诊,随访期间跟踪两组患者安全性和长期生存情况。无病生存率(dis-ease-free survival,DFS)定义为从手术后即刻至因疾病进展为主要原因引起死亡的时间。总生存率(overall survival,OS)定义为从手术后即刻至因任何原因引起死亡的时间。采用不良事件评价标准(Common terminology criteria for adverse events,CTCAE)4.0版对不良事件进行评价[9]。
1.6 临床疗效判定标准
参照实体瘤客观疗效评价标准(response evaluation criteria in solid tumors,RECIST) 将HER-2过表达乳腺癌患者预后分为4个等级[10]:完 全 缓 解(completere-sponse,cCR)、部 分 缓 解(partial response,PR)、疾 病 稳 定(stabledisease,SD)、疾病进展(progressive disease,PD)。总有效率=(cCR+PR)例数/总例数×100%。
1.7 统计学方法
所有数据均经SPSS20.0统计学软件进行统计学处理,计量资料若呈正态分布,组间比较采用独立样本t检验,以()的形式表示;计数资料采用χ2检验,以[n(%)]的形式表示;检验水准α=0.05。P<0.05为差异有统计学意义。
2 结果
2.1 6个周期治疗后两组临床疗效比较
6个周期治疗后,观察组cCR、OR显著高于对照组,观察组PR显著高于对照组,差异有统计学意义(P<0.05);6个周期治疗后,两组SD、PD比较,差异无统计学意义(P>0.05)。见表1。

表1 6个周期治疗后两组临床疗效比较[n(%)]
2.2 两组长期生存情况比较
观察组5年DFS、OS显著高于对照组,差异有统计学意义(P<0.05)。见表2。
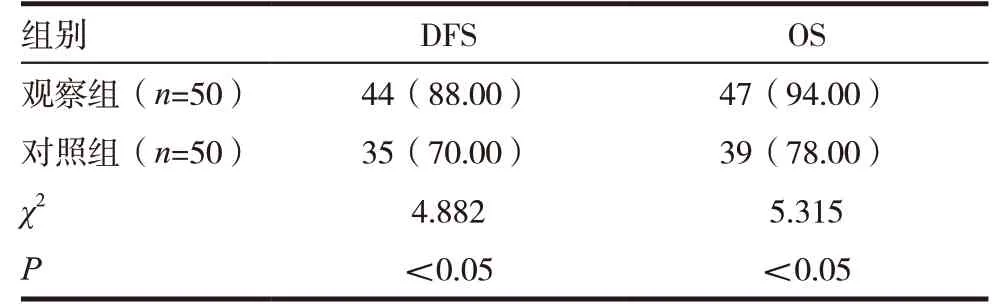
表2 两组手术后长期生存情况比较[n(%)]
2.3 两组不良反应发生情况比较
观察组皮疹发生率、心脏毒性发生率、骨髓抑制发生率和末梢神经毒性发生率显著高于对照组,差异有统计学意义(P<0.05);两组发热发生率、脱发发生率、肝功能损害发生率和胃肠道反应发生率比较,差异无统计学意义(P>0.05)。见表3。
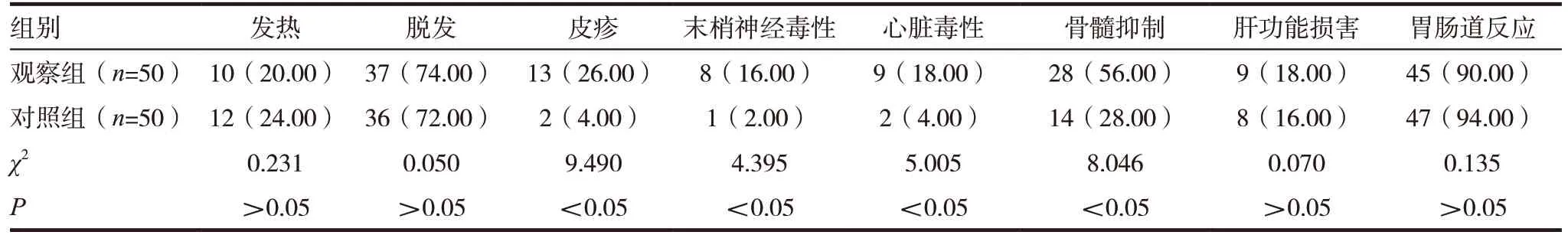
表3 两组不良反应发生情况比较[n(%)]
3 讨论
新辅助化疗能杀灭乳腺癌亚临床播散病灶,使原发病灶和区域淋巴结降期,在局部晚期乳腺癌外科治疗中的地位已经被临床确立[11-12]。TCH方案新辅助化疗具有适应证广泛和心脏毒性低的特点已经成为HER-2过表达乳腺癌新辅助化疗的一线方案[13]。本研究经过多方面考量,最终选取已被临床广泛用于治疗HER-2过表达乳腺癌的TCH方案新辅助化疗,与曲妥珠单抗作对照。
生长因子及其受体在细胞生长、分化方面起到至关重要的作用。许多受体具有内在的酪氨酸激酶活性,并被受体和其同源配体相互作用催化。HER-2与乳腺癌进展和生存密切相关,并且成为了HER-2过表达乳腺癌靶向治疗的线索[14]。曲妥珠单抗是一种人源化抗HER-2单克隆抗体或HER-2/neu受体拮抗剂,其通过特异性地与HER-2的细胞外区结合,起到增加化疗药物的细胞毒性、介导抗体依赖细胞和补体依赖性细胞介导的细胞毒反应、拮抗HER-2家族促肿瘤细胞增长以及抑制HER-2过表达的肿瘤细胞的增殖等作用[15]。因此,曲妥珠单抗丰富了HER-2过表达乳腺癌的治疗措施;曲妥珠单抗联合新辅助化疗治疗HER-2过表达乳腺癌或能改善患者临床疗效,使患者长期生存获益。
为了客观地验证曲妥珠单抗联合新辅助化疗治疗HER-2过表达乳腺癌的疗效和安全性,采用χ2检验比较了两组临床疗效、长期生存情况和不良反应发生情况。结果显示,6个周期治疗后,观察组cCR、OR比对照组高,观察组PR比对照组高,差异有统计学意义;6个周期治疗后,两组SD、PD比较,差异无统计学意义;观察组5年DFS、OS比对照组高,差异有统计学意义。提示,与单纯TCH方案新辅助化疗相比,在此基础上联用曲妥珠单抗能改善HER-2过表达乳腺癌患者预后,提高HER-2过表达乳腺癌患者cCR、OR,提高HER-2过表达乳腺癌患者5年DFS、OS。结果显示,观察组皮疹发生率、心脏毒性发生率、骨髓抑制发生率和末梢神经毒性发生率比对照组高,差异有统计学意义;两组发热发生率、脱发发生率、肝功能损害发生率和胃肠道反应发生率比较,差异无统计学意义。提示与单纯TCH方案新辅助化疗相比,在此基础上联用曲妥珠单抗会增加HER-2过表达乳腺癌患者皮疹、心脏毒性、骨髓抑制和末梢神经毒性等不良反应的发生率,而不良反应均为可逆性,未发生心力衰竭等严重不良反应。
综上所述,本研究探讨了曲妥珠单抗联合新辅助化疗治疗HER-2过表达乳腺癌的疗效和安全性。
