病毒是什么?——人类发现首个病毒的过程考察
2020-04-16周程
周 程
“直面新型冠状病毒肺炎:重大疫情防控的跨学科研究”专刊
病毒是什么?——人类发现首个病毒的过程考察
周 程1,2
(1. 北京大学 哲学系,北京 100871;2. 北京大学 医学人文学院,北京 100191)
在细菌致病学说盛行的时代,在电子显微镜尚未问世的情况下,病毒是怎样被发现的?病毒的概念又是怎样被构建起来的?基于科学思想史视角,对人类发现第一个病毒——烟草花叶病毒过程中的如下8个关键节点进行了考察:(1)麦尔发现烟草患花叶病后其病叶汁液具有传染性;(2)伊万诺夫斯基发现烟草花叶病致病因子具有滤过性;(3)贝杰林克发现烟草花叶病致病因子是“传染性活流质”;(4)吕夫勒和菲洛施发现牛口蹄疫致病因子是“极小生物”;(5)伊万诺夫斯基认为烟草花叶病致病因子不是活流质;(6)杜加尔认为烟草花叶病致病因子是可在细胞内增殖的微粒;(7)斯坦利基于结晶实验提出烟草花叶病毒是一种蛋白质;(8)烟草花叶病毒原来是杆状核酸蛋白质复合体。在此基础上,还针对科学研究的局限性和科学认知的渐进性问题进行了探讨。
细菌致病学;烟草花叶病毒;科学发现;科学概念;科学精神
自武汉爆发新型冠状病毒肺炎以来,病毒这个专业术语在国内迅速普及,可以说如今已成为家喻户晓、妇孺皆知的日常用语了。不过,对于国际病毒分类委员会为什么会在这次的新型冠状病毒命名问题上产生意见分歧,很多人未必有很深刻的理解。
按照美国主流教科书《现代病毒学导论》给出的解释,病毒是亚微观的寄生性的含有蛋白质衣壳的遗传物质颗粒[1]。说得更具体一点,病毒与细菌不同,是一类极小的非细胞生物;其体积小到可以通过细菌过滤器,人们只能借助电子显微镜才能看到它;病毒的结构非常简单,通常由蛋白质衣壳和核酸内芯组成(图1)。
人类最早发现的病毒是烟草花叶病毒(图2)(Tobacco Mosaic Virus,缩写为TMV)。这种亚微观的病毒究竟是怎样被发现的?其概念又是怎样被构建起来的?不同时期、不同国别、不同专业的学者在此过程中扮演了什么样的角色?
荷兰林堡大学健康伦理与哲学系的赫尔沃特(Ton van Helvoort)博士曾于1991年发表长文讨论过这些问题[2],日本东京大学理学部名誉教授冈田吉美甚至在2004年出版专著详细梳理了烟草花叶病毒研究百年史[3]。尽管二人的研究已有些年头,但仍具有重要参考价值。笔者拟基于他们的研究和新近问世的相关论著,并尽可能对照当年研究烟草花叶病毒的学者发表的原始论文或报告,从科学思想史视角就上述问题做些粗浅的考察,以期能为国内的科学史和科学哲学研究提供一些素材,并为中国当下的科学技术治理提供一些借鉴。
图1 形形色色的病毒
需要指出的是,本文在深描烟草花叶病毒的发现过程时,重点关注的是跨时代、跨国别和跨专业的病毒研究人员持续性的、反思性的“集体学习”行动。这种研究接力,揭示了有别于传统的知识生产模式。其中,每位后来者扮演的都不是简单的“反对者”角色,而是在扬弃的基础上调度更多的研究资源,以形成更具鲁棒性的科学共识。
1 麦尔发现烟草患花叶病后其病叶汁液具有传染性
因率先成功制备烟草花叶病毒蛋白质结晶而分享1946年诺贝尔化学奖的美国生物化学家斯坦利(Wendell Meredith Stanley,1904-1971),在1944年发表的一篇文章中指出:有相当多的理由将俄国的植物生理学家伊万诺夫斯基(Dmitrii Ivanovsky,1864-1920)视作新兴的病毒学学科之父[4]。尽管如此,讨论首个病毒的发现经纬时,仍不能不从德国农业化学家麦尔(Adolf Eduard Mayer,1843-1942)谈起。
麦尔于1843年生于德国西北部的奥尔登堡。他1860年进入卡尔斯鲁厄理工学院学习数学和化学,1862年又进入著名的海德堡大学深造,并于1864年获得该校的博士学位。在海德堡大学讲授一段时间的发酵学和化学工程之后[5]13,麦尔于1876年赴荷兰担任瓦格宁根农业试验站主任[6]。当时,很多种植烟草的农民都遇到了一个困惑,那就是,烟草长出的深绿色叶子上会莫名其妙地出现浅绿色斑纹,致使烟叶的产量和质量都受到严重的影响(图3)。为探明该烟草疾病的产生原因,麦尔自1879年开始对烟草的种植展开了长时间的观察与实验研究,并于1882年将这种烟草疾病命名为“烟草花叶病”(mozaik ziekte van de tabak,即Tobacco Mosaic Disease)[3]22(图4)。

图3 烟草花叶病症状
麦尔曾研究过种子对烟草花叶病的影响,但他排除了这一影响的存在。因为同一批种子种植在不同的地方,并没有都出现花叶病。麦尔还研究过气温、光照对烟草花叶病的影响,他发现烟草花叶病与气候并没有直接的关联,因为不同地区、不同时节的烟草都会得花叶病。于是,麦尔将研究的重点集中到土壤的影响上。
1840年,德国的化学家李比希(Justus von Liebig,1803-1873)公开出版了《化学在农业和生理学中的应用》一书,揭开了近代农业化学革命的序幕[7]。1862 年,李比希把它增补成两厚册作为第7版出版时,麦尔正在海德堡大学攻读与化学有关的学位。因此,这本名著不可避免地对他产生了影响。按照李比希在该书中提出的物质补偿法则,麦尔推测,烟草花叶病很有可能是因为土壤中缺少某种或某些元素导致烟草营养不良造成的。为此,他对患病烟草和健康烟草的叶子所含有的化学成分以及患病烟草和健康烟草根茎周围的土壤成分进行了对比分析,但他并没有找到导致烟草患花叶病的原因[8]。
1881年夏季的某一天,麦尔漫无目的地来到瓦格宁根农业试验站的实验苗圃。他发现苗圃中种植的好几个外国品种的烟草都没有患花叶病,但附近农家种植的本国品种烟草都不同程度地得了花叶病[5]13。麦尔由此意识到烟草花叶病不太可能是由土壤成分的差异造成的。这些烟田互相毗邻,土壤成分不可能有太大的差异。既然烟草花叶病不可能是营养不良症,那么它又是由什么因素造成的呢?
当时,德国细菌学家科赫(Robert Koch,1843-1910)虽然尚未因发现结核杆菌而成为家喻户晓的英雄人物,但他1876年在《植物生物学通讯》上发表的论文“炭疽热病因:基于炭疽杆菌的发展过程”已在学术界产生了广泛的影响[9]。尽管人们已普遍接受动物罹患的一些疾病是因感染了某种特定的细菌造成的这一细菌致病理论(germ theory)[10],但是没有任何证据表明某些植物疾病也是因细菌感染造成的。
处于穷途末路的麦尔决定模仿科赫的研究看看烟草花叶病是不是也会通过病原体传染。于是,他将患有花叶病的烟草叶子捣碎、将从中提取的汁液用玻璃毛细管注入多株健康烟草的叶脉中。他发现,这些烟草已经长出的叶子并没有出现花叶病症,但大约10天后新长出来的嫩叶几乎都出现了花叶病症。而且,将从患有花叶病的烟草叶子中提取的汁液加热到摄氏80度后,这些汁液都会失去上述特性[3]23。因此,麦尔怀疑患病烟草叶子的汁液中含有可传染花叶病的细菌。但他使用当时最先进的光学显微镜也未观察到这种假想的细菌。而且,用培养皿进行培养后也没有培养出任何可传染烟草花叶病的细菌。

图4 麦尔(Adolf Eduard Mayer,1843-1942)拍摄的感染上花叶病的烟草叶子
于是,麦尔开始给健康烟草接种各种各样的已知细菌,看看导致烟草感染花叶病的细菌是不是其中的一种。未果后,他又给健康烟草接种一些动物和人的粪肥,以及磨碎了的过期奶酪和腐败了的豆制品,看看烟草花叶病会不会是像酵母那样的真菌作用的结果,因为当时基于李比希的发酵和腐败学说建立起来的发酵致病理论(zymotic theory)仍然相当流行[11]61-69。当然,所有这些努力都未能帮助麦尔找到烟草花叶病的致病因子[8]。
麦尔后来又做了一系列实验。他发现,用单层滤纸过滤患病烟草叶子的汁液时,致病因子是能够通过滤纸的。但他还发现,使用双层滤纸过滤时,提取液会变成“透明滤液”,而且这种滤液不具有传染性。由此,麦尔推定,烟草感染花叶病不可能是由真菌引起的,因为即使是酵母这样的微小真菌也穿越不了滤纸,也就是说它们在第一次过滤时就会被滤除。麦尔认为,烟草花叶病也不会是酶参与作用的结果,因为酶之类化学物质不仅不能自我繁殖,而且即使是使用多层滤纸过滤也不至于被滤除。
麦尔最终给出的结论是,(1)烟草感染花叶病与细菌有关;(2)患有花叶病的烟草叶子污染土壤后容易引起花叶病,因此不能将病变烟叶放置在烟田里。尽管麦尔并没有真正找到烟草花叶病的致病因子,但他1886年还是公开发表了上述研究结论[12]。
实际上,烟草花叶病是由病毒而非细菌引起的。由于病毒远小于细菌,使用光学显微镜根本就看不到,所以麦尔当时找不到烟草花叶病的致病因子并不奇怪。问题是病毒是可滤过的,即便使用多层滤纸过滤,滤液都应该具有传染性。是故,麦尔提出的非滤过性的细菌是导致烟草患花叶病的病原这个观点并不成立,它经受不住重复实验的检验。但毋容置疑的是,麦尔乃史上第一个发现烟草花叶病是一种植物传染病的科学家。
麦尔开启了烟草花叶病致病因子的研究先河。他的研究结果对正在撰写与烟草花叶病有关的学位论文的俄国学生伊万诺夫斯基以及当时也在瓦格宁根工作的荷兰同行贝杰林克(Martinus Beijerinck,1851-1931)产生了很大的影响,并为他们取得研究突破奠定了重要的基础。
2 伊万诺夫斯基发现烟草花叶病致病因子具有滤过性
伊万诺夫斯基1864年11月9日生于圣彼得堡附近的一个乡村,其父乃西伯利亚的一名地主,幼年丧父后,随家人搬迁至圣彼得堡的一个贫民区,并在那里上完了中学。1888年,伊万诺夫斯基提交的学位论文“论烟草的两种疾病”通过审查,被圣彼得堡大学授予理学士学位。刚毕业时,他继续待在圣彼得堡大学,一边准备申请教职,一边在植物学实验室工作。此后,他转赴圣彼得堡科学院的法明茨恩(Andrei Sergeevich Famintsyn,1835-1918)实验室担任助手。伊万诺夫斯基于1895年完成论文“对酒精发酵的一项调查”的写作,并因此获得硕士学位。之后,他又因在烟草花叶病研究方面卓有建树而于1903年被授予博士学位[13]。同年,伊万诺夫斯基获聘担任波兰的华沙大学植物学系教授。
伊万诺夫斯基在圣彼得堡大学学习期间,曾于1887年和1890年两度接受俄罗斯农业部的委托赴乌克兰和克里米亚调查烟草疾病的形成原因。在搜集有关烟草疾病的先行研究文献过程中,他获悉德国学者麦尔此前已对烟草花叶病展开过深入细致的研究[13]。不过,伊万诺夫斯基在重复麦尔的实验时发现,使用两层滤纸对患有花叶病的烟草叶子的汁液进行过滤后,所获得的滤液仍然具有传染性,这与麦尔的实验结果明显不符。于是,他又使用一种当时最为先进的生产无菌纯净水用过滤器——尚柏朗(Charles Chamberland,1851-1908)氏过滤器对患有花叶病的烟草叶子的汁液进行了过滤(图5)。结果,所获得的滤液同样具有传染性。这使伊万诺夫斯基感到非常纳闷[5]14。

图5 尚柏朗(Charles Chamberland,1851-1908)氏烛形陶瓷滤芯过滤器
在伊万诺夫斯基看来,只有两种可能性可以解释这种现象。一是这种过滤器存在质量不稳定问题,以致具有传染性的细菌通过了通常根本无法通过的微小滤孔。二是滤液中的致病因子是一种和自己两年前发现的毒素类似的物质,这种毒素有可能是细菌在加压过滤过程中分泌出来的。不论是前者还是后者,归根结底,汁液的传染性都是由细菌导致的。由此可见年轻的伊万诺夫斯基当时对巴斯德(Louis Pasteur,1822-1895)和科赫的细菌致病说的盲信程度。正因为如此,他未能对该项实验结果所揭示的意义进行深入的思考和探究。他虽然率先发现通过细菌过滤器的滤液仍然具有传染性这一现象,但却未能明确提出滤过性病原体这一概念[5]14。
其实,即使是在当时的实验条件下,要排除毒素引起花叶病这种可能也并不困难。譬如说,可以使用玻璃毛细管将少量通过尚柏朗氏过滤器的汁液稀释后接种至健康烟草的叶脉中,待该烟草的叶子出现花叶病症状后,再提取该患病叶子的汁液,并将其稀释后接种至其他健康烟草的叶脉中。如果传染是由毒素类化学物质引起的,此时汁液中的毒素的浓度会大为降低,因此传染性会明显减弱。这样重复做几轮实验后,被接种的健康烟草应该不会再出现花叶病症状。如果仍然出现,那就意味着汁液中的致病因子具有增殖性,不太可能是毒素类化学物质引起的。
当然,伊万诺夫斯基也可以多购置几个过滤器再做几次重复实验。如果更换多个甚至是多个型号的过滤器后,所获得的滤液都具有传染性,那么就应该意识到,即使这种滤过性病原体是“细菌”,那它也非通常意义上的细菌,而是一种体度远小于常见细菌的致病因子。但是,伊万诺夫斯基并没有这么做。
伊万诺夫斯基1892年向圣彼得堡科学院提交了一篇题为“关于烟草花叶病”的论文,介绍了上述研究发现[14]。因此,后来很多学者,尤其是俄国学者据此认为,伊万诺夫斯基是滤过性病原体、亦即病毒的发现者。为纪念伊万诺夫斯基的上述研究业绩,前苏联《微生物学》杂志曾在1942年出了一个纪念专辑[15]。1964年,在伊万诺夫斯基诞辰100 周年之际,前苏联还将其视作为病毒学的创始人特意为其发行了一枚纪念邮票[16](图6)。1992年,普林斯顿大学分子生物学系的卢斯蒂格(Alice Lustig)和莱文(Arnold J. Levine)在题为《病毒学100年》的评论中高度评价了伊万诺夫斯基百年前的研究,认为该项研究迈出了病毒发现的第一步[13]。
但是很多欧美学者认为,虽然伊万诺夫斯基1892年发表的论文值得在病毒学史中大书特书,但将其视作为病毒的发现者未必合适。例如,1998年,英国皇家学会召开了“烟草花叶病毒:一个世纪的开创性研究”专题研讨会,该会的组织者就倾向于认为荷兰的微生物学家贝杰林克才是病毒学学科的创始人[6]。

图6 前苏联发行的伊万诺夫斯基(D. Ivanovsky, 1864-1920)纪念邮票
3 贝杰林克发现烟草花叶病致病因子是“传染性活流质”
贝杰林克1851年生于阿姆斯特丹,1872年毕业于代尔夫特理工学院化学系,1877年获莱顿大学理学博士学位。1876年,他赴新创立的瓦格宁根农业学校担任植物学教师。同年,麦尔也来到了瓦格宁根。由于研究领域相近,二人在瓦格宁根交往甚密,所以贝杰林克从麦尔那里获得了不少有关烟草花叶病的研究信息[17]。1885年,贝杰林克从瓦格宁根搬迁到代尔夫特,在一家生产酵母和酒精的工厂担任细菌学实验室负责人。1895年,他又来到代尔夫特理工学院担任细菌学教授[16]。
1897年,新的细菌学实验室和温室一经建成,贝杰林克便急切地重新开启了烟草花叶病研究。1898年,他发表了一篇著名论文,提出了“传染性活流质()”的概念(图7)。1900年,他又将这篇论文翻译成了法文,引起了广泛的关注[16]。
从贝杰林克1898年发表的论文中可以看出,他和伊万诺夫斯基一样使用尚柏朗氏过滤器对从患有花叶病的烟草叶子中提取的汁液进行了过滤,并发现滤液具有传染性[18](图8)。不过,贝杰林克在上述论文中并没有引用伊万诺夫斯基1892年写的论文。这很可能是因为他当时的确没有看到该论文。
尚柏朗氏过滤器使用无釉陶瓷做滤芯,滤芯上的滤孔直径在0.1~1微米,因此即使是非常微小的细菌也无法通过滤芯上的滤孔进入滤液。现在从患有花叶病的烟草叶液中提取的滤液居然有传染性,如何解释?问题是使用最先进的光学显微镜也无法从滤液中找到致病因子;而且,无论是在有氧的环境下,还是在无氧的环境下,对滤液进行培养后,都显示滤液中没有任何细菌。不过,贝杰林克并没有裹足不前。
贝杰林克对滤液进行大剂量稀释后做了一组对比实验,他发现大剂量稀释后的滤液和未经稀释的滤液对健康烟草产生感染的程度几乎没有差别。而且,受稀释滤液感染的烟草叶子的汁液仍然具有很强的感染性,健康烟草接种其汁液后仍然都会出现花叶病症状。于是,贝杰林克推定滤液的感染性不是由无生命的化学物质引起的。

图7 贝杰林克(M. Beijerinck,1851-1931)1898年论文中的接种实验插图
如果滤液中存在有生命的致病因子,那么这种致病因子是如何增殖的呢?贝杰林克又做了一组对比实验。他像过滤患病烟草叶子的汁液一样,用尚柏朗氏过滤器对健康烟草叶子的汁液进行了过滤,并获得了一批滤液。他将这种滤液加入到有传染性的滤液中之后,再给健康烟草进行接种。他发现健康烟草感染后的病症表现程度与他用同体积的蒸馏水稀释后的带有传染性的滤液的情况一样。这意味着致病因子并没有在健康烟草叶子汁液的滤液中发生增殖。它表明,致病因子只有在有细胞的条件下才有可能发生增殖。
尽管滤液中的致病因子无法用光学显微镜观察到,但并不能排除它是比细胞还要小的超显微颗粒的可能。于是,贝杰林克又使用琼脂凝胶层析的方法做了一组实验。他将从患病烟草叶子的汁液中提取的滤液滴到琼脂凝胶上,然后将其抹匀,并定期加注纯净水,以方便滤液扩散。贝杰林克认为,如果滤液中的致病因子具有可溶性,那它就会渗透到琼脂凝胶内部;如果致病因子具有颗粒性,那它就不会扩散。结果显示,滤液10日后能够向琼脂凝胶内部至少扩散2毫米。而且,扩散至琼脂凝胶内部的滤液仍然具有传染性。贝杰林克据此推定,烟草花叶病的致病因子是一种液体或者是可溶的,也就是说不是颗粒状的。
为了弄清烟草花叶病致病因子是如何感染烟草组织的,贝杰林克进行了一系列观察。他发现,健康烟草接种病变叶子汁液的滤液后,总是在新长出来的嫩叶上出现花叶病斑,已经完全成熟的烟草叶子上并不会出现花叶病斑。叶子在生长过程中,总是在叶尖部位出现花叶病斑,在叶尖下部并不会出现花叶病斑。由于土壤中的致病因子是由根部进入烟草体内的,因此,贝杰林克推定,致病因子先进入烟草茎部,然后再感染正在进行细胞分裂的组织——叶芽或叶尖。致病因子只会在细胞组织分裂、生长时才增殖,且不会在不再分裂的成熟的细胞组织中增殖,但却可以通过其传播扩散。
贝杰林克还对烟草花叶病致病因子的活性进行了深入研究。他发现,滤液保存三个月之后,其传染能力并没有出现任何变化。而且,在摄氏40度的条件下将在病叶汁液中浸泡过的滤纸烘干后,仍能使健康烟草出现花叶病症;将自然干燥后的病叶放置在植物标本箱里保存两年后,同样能使健康烟草感染花叶病。不过在这两种情况下,致病因子的感染能力都会有所减弱。此外,将病叶汁液的滤液加热到摄氏90度后,滤液将会完全失去活性,不再具有传染性。

图8 贝杰林克的烟草花叶病实验记录
贝杰林克还做了一项有关烟草花叶病致病因子的越冬性实验。他在秋季终止给患有花叶病的盆栽烟草浇水,等其枯死后再拔出烟草,并将粘在烟草根部的土放回盆中。第二年春天,他在干放了一个冬季的盆子里栽了几颗健康烟草。他发现,这些健康烟草最终都不同程度地患了花叶病。贝杰林克由此推定,烟草花叶病的致病因子即使在干燥的土壤中也能越冬,而且这些致病因子在春天会经由新栽培的烟草根部、茎部,感染烟草叶子,使其出现花叶病斑。
尽管当时的实验条件和对细胞的认识有限,但贝杰林克的上述推论和假设有不少后来被证明与事实相当吻合。
4 吕夫勒和菲洛施发现牛口蹄疫致病因子是“极小生物”
值得注意的是,贝杰林克只在论文题目和两个小节的标题中使用了“传染性活流质”()这一术语,在论文的正文中,贝杰林克提及该因子时,都用“contagium”(触染物)或“virus”(病毒)表示,后者更为常见[16]。
根据《牛津英语词典》的解释,“Virus”一词源自于拉丁语,其字面意思是“粘稠的液体,毒素”,在中世纪晚期的英语中主要指“蛇的毒液”。实际上,“Virus”的含义在贝杰林克1898年发表上述文章之前一直没有发生过太大的变化。因此,在十九世纪后期,人们在表达生物体内增殖的“poison”(毒素)之意时,会根据自己的喜好选择“contagion”(触染物)、“germs(病菌)”、“bacteria”(细菌)、或“virus”[11]126。它表明,这一时期“virus”仍未被赋予滤过性病原体的含义,它和“触染物”、“病菌”、“细菌”可以互换使用。
1890年,微生物学之父巴斯德提出著名的论断:“tout virus est un microbe”(所有的病毒都是微生物)。[16]但是,时过八年之后,贝杰林克就将“virus”用来指代“传染性活流质”。贝杰林克的“传染性活流质”的概念包含这几层含义:(1)能通过细菌过滤器;(2)具有传染性;(3)能在生物体内增殖,但不能在体外生长。简言之,病毒是一种滤过性病原体。
很明显,贝杰林克1898年时已经确立了存在一种自主的亚微观(亚细胞)生命形式的信念。于是,“所有的病毒都是微生物”变成了“病毒不是微生物”。贝杰林克对病毒概念如此进行形塑与德国的细菌学家、科赫的弟子吕夫勒(Friedrich Loeffler,1852-1915)和菲洛施(Paul Frosch,1860-1928)的工作有着一定的关联。
1882年,科赫在柏林生理学学会上宣布,他找到了结核病的病原体,这是一种若不用特殊染料进行染色,用光学显微镜根本看不见;而且生长十分缓慢,即使在特殊培养基上培养两周后也只能形成很小菌落的新型杆菌[9]。科赫的这一重大发现在学界掀起了一波寻找疑难病病原菌的热潮[10]。科赫的助手吕夫勒同年就发现了类鼻疽杆菌,1884年又培养出了白喉杆菌[19]。积累了丰富的细菌学研究经验后,吕夫勒又和菲洛施合作于1897年在科赫担任所长的普鲁士皇家传染病研究所(现罗伯特·科赫研究所,RKI)启动了牛口蹄疫病原体的探究(图9)。如前所述,贝杰林克也是在同年启动了对烟草花叶病的研究。
牛口蹄疫是一种传染病,其典型症状是牛口腔、乳房和蹄部出现水泡和溃烂,犊牛患病后死亡率相当高(图10)。吕夫勒和菲洛施研究后发现,牛患口蹄疫后,其淋巴液中含有能通过细菌过滤器的传染性物质,而且这种口蹄疫致病因子小到无法通过光学显微镜观察到,也无法在培养基上培养。还有,病牛淋巴液的滤液经过高度稀释后,仍然具有传染性,因此可排除其为化学毒素的可能性[20]。这项发现和伊万诺夫斯基1892年研究烟草花叶病时的发现有着很多相似之处,不同的是,后者当时没有用实验排除致病因子是化学毒素的可能。
吕夫勒曾长期在科赫身边工作,他对科赫确立的细菌致病理论深信不疑。因此,尽管牛口蹄疫的病原体具有滤过性,但他仍然不愿意全面修正细菌致病理论。吕夫勒和菲洛施认为,牛口蹄疫病原体虽然能够通过连最小的细菌都无法通过的过滤器滤孔,但它仍是一种微粒(corpuscular)。人类和动物罹患的很多其他传染病,例如天花、牛痘、猩红热、麻疹、伤寒和牛瘟等,其病原体也都是这种类型的“极小生物体”()。很明显,在吕夫勒和菲洛施看来,究极而言牛口蹄疫病原体是一种微生物,只不过其体度极小罢了。

图9 吕夫勒(Friedrich Loeffler,1852-1915)1897年所在的皇家传染病研究所
吕夫勒和菲洛施将上述研究成果整理成了4份研究报告,第1份报告的落款日期为1897年4月17日,因此被认为有可能在当年就已经公开发表了。不过,可以确定的是吕夫勒和菲洛施于1897年9月发表了一份德文的研究摘要,可能是因为没有过滤实验记录,所以没有引起贝杰林克的关注。贝杰林克在1898年的论文中只提到了吕夫勒1898年独立发表的第4份研究报告[16]。毋容置疑,贝杰林克在研究烟草花叶病过程中受到了吕夫勒对牛口蹄疫病原体的研究影响。但是,二人在滤过性病原体究竟是微粒还是流质一事上看法截然不同。因此,贝杰林克在1898年的论文中批评了吕夫勒的滤过性病原体微粒说。
要而言之,贝杰林克发现烟草花叶病病原体的时间点与吕夫勒和菲洛施发现牛口蹄疫病原体的时间点几乎没有差异,而且他们都用实验表明滤过性病原体是一种客观存在。只是双方对实验结果的解释不同,贝杰林克认为这种新病原体是“传染性活流质”,不是细菌;吕夫勒和菲洛施认为这种新病原体乃迄今为止从未遇到过的一种极其细小的微粒,但它仍属于微生物,除体度外和细菌没有太大的差异。因此,将贝杰林克视作病毒概念的提出者似乎更有说服力。但是,若将滤过性病原体的发现等同于病毒的发现,那么将病毒发现者的荣冠戴在贝杰林克的头上还不如戴在吕夫勒和菲洛施的头上更合适。实际上,伊万诺夫斯基早在1892年就已发现了滤过性病原体,只是他对当时观察到的实验现象没有进行深究罢了。
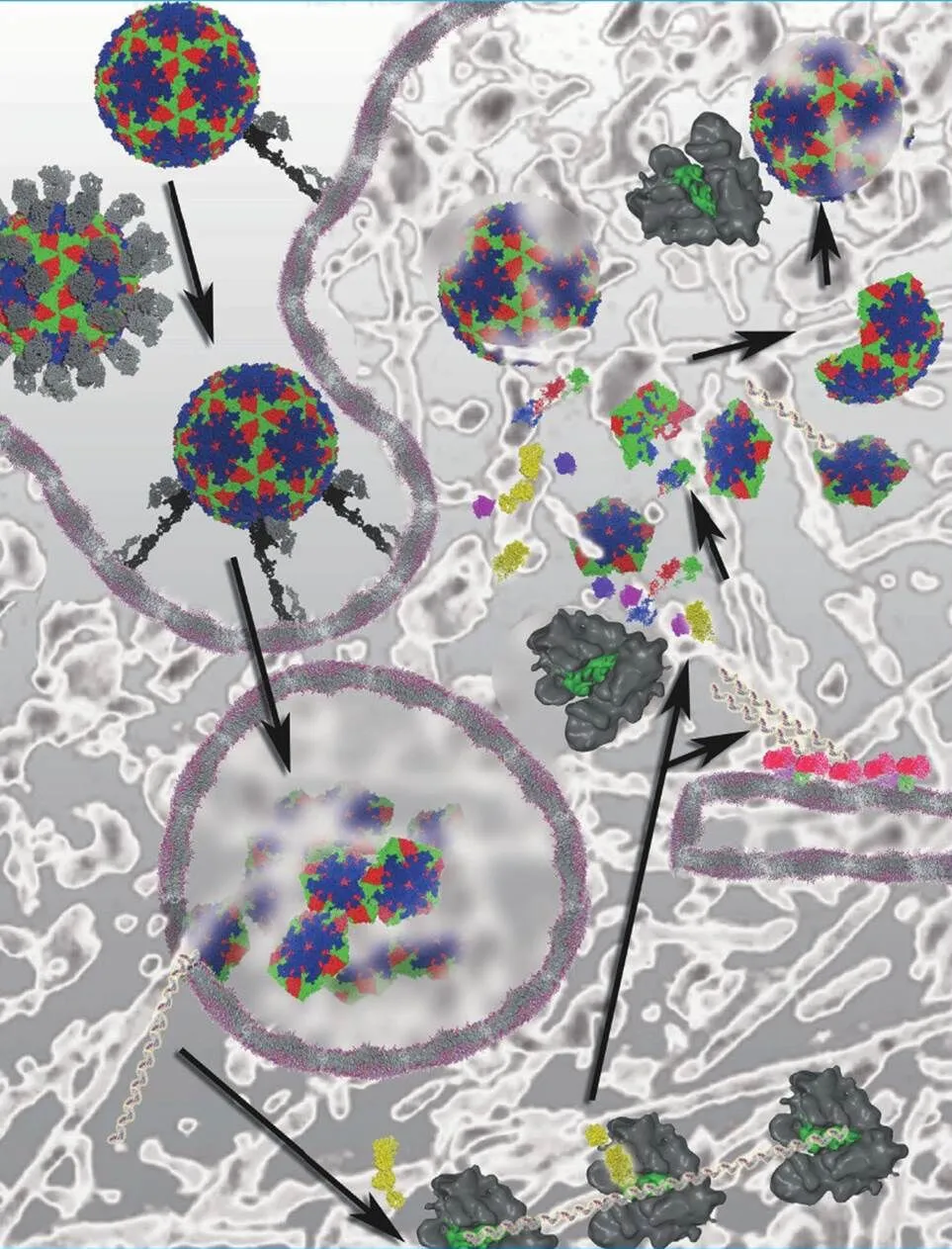
图10 现已解明的口蹄疫病毒生命周期示意图
5 伊万诺夫斯基认为烟草花叶病致病因子不是活流质
1899年,贝杰林克将自己1898年发表的上述论文翻译成了德文。这篇德文论文很快就引起了伊万诺夫斯基的关注。伊万诺夫斯基当年就写了一篇论文回应道:自己早在1892年就已发现滤过性病原体,因此滤过性病原体的发现者应该是他,而不是别人[3]23。通过贝杰林克的论文,伊万诺夫斯基获悉贝杰林克和吕夫勒对滤过性病原体是微粒还是流质存在严重的意见分歧。伊万诺夫斯基难以接受贝杰林克的活流质说,他更倾向于支持吕夫勒的微粒说。于是,伊万诺夫斯基开始对贝杰林克基于实验提出的诸多观点进行了追试[5]16-17。
伊万诺夫斯基也使用尚柏朗氏过滤器对患花叶病的烟草叶子的汁液进行了过滤(图11)。不过,伊万诺夫斯基过滤时没有给汁液加压,而且分三个时段进行了采样。他发现,健康烟草接种这些滤液试样后发病情况存在明显差异。具体而言,最初采集的滤液确实具有传染性,会使健康烟草出现花叶病症。但是,过滤12小时后采集的滤液试样和过滤36小时后采集的滤液试样都不具有传染性。因此,他认为贝杰林克的活流质说不成立。
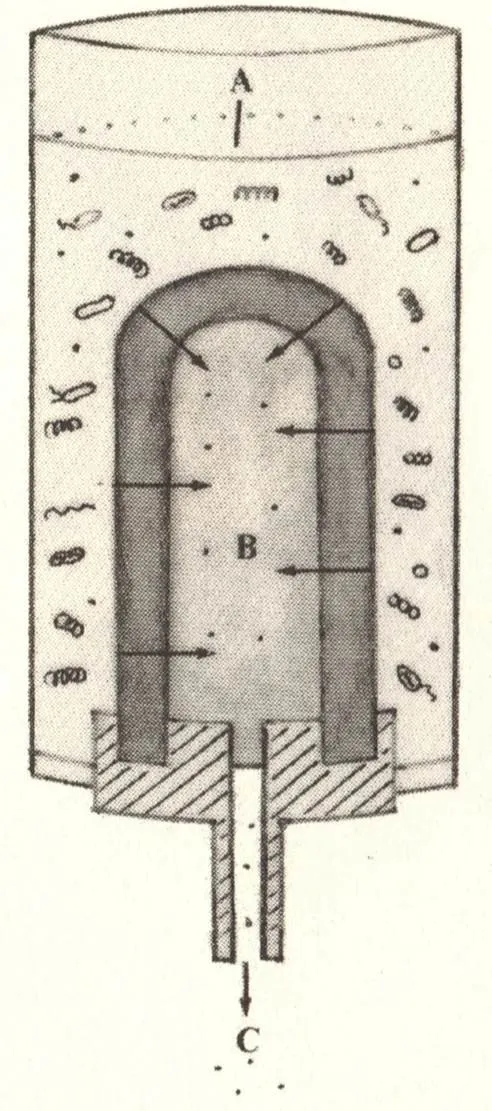
图11 烛形陶瓷滤芯过滤原理示意图
在伊万诺夫斯基看来,如果烟草花叶病病原体是液体,或者是可溶的,那么不论是在哪个时段采集的滤液都应具有传染性,只有当烟草花叶病病原体是微粒时才会出现滤液的传染性随时间不断降低的情况。其原因是,在不加压的情况下,微粒形态的病原体会逐渐淤积在过滤器的微小滤孔中,使得病原体越来越难以通过滤孔,当达到一定的时间值后,只有液体才能通过过滤器的滤孔,由于此时微粒形态的病原体也不再能够通过滤孔,所以滤液不再具有传染性。
伊万诺夫斯基对贝杰林克的琼脂凝胶层析实验也进行了追试。不过,伊万诺夫斯基使用的是刚刚凝固成形的新鲜琼脂凝胶。他发现,患有花叶病的烟草叶汁的滤液根本就不会在这种新鲜琼脂凝胶中扩散,而且做对比实验用的颜料墨水溶液也不会在这种新鲜琼脂凝胶中扩散。但是,如果使用放置数日的陈旧琼脂凝胶做实验,那么烟草叶汁的滤液和颜料墨水溶液都会在琼脂凝胶中扩散。
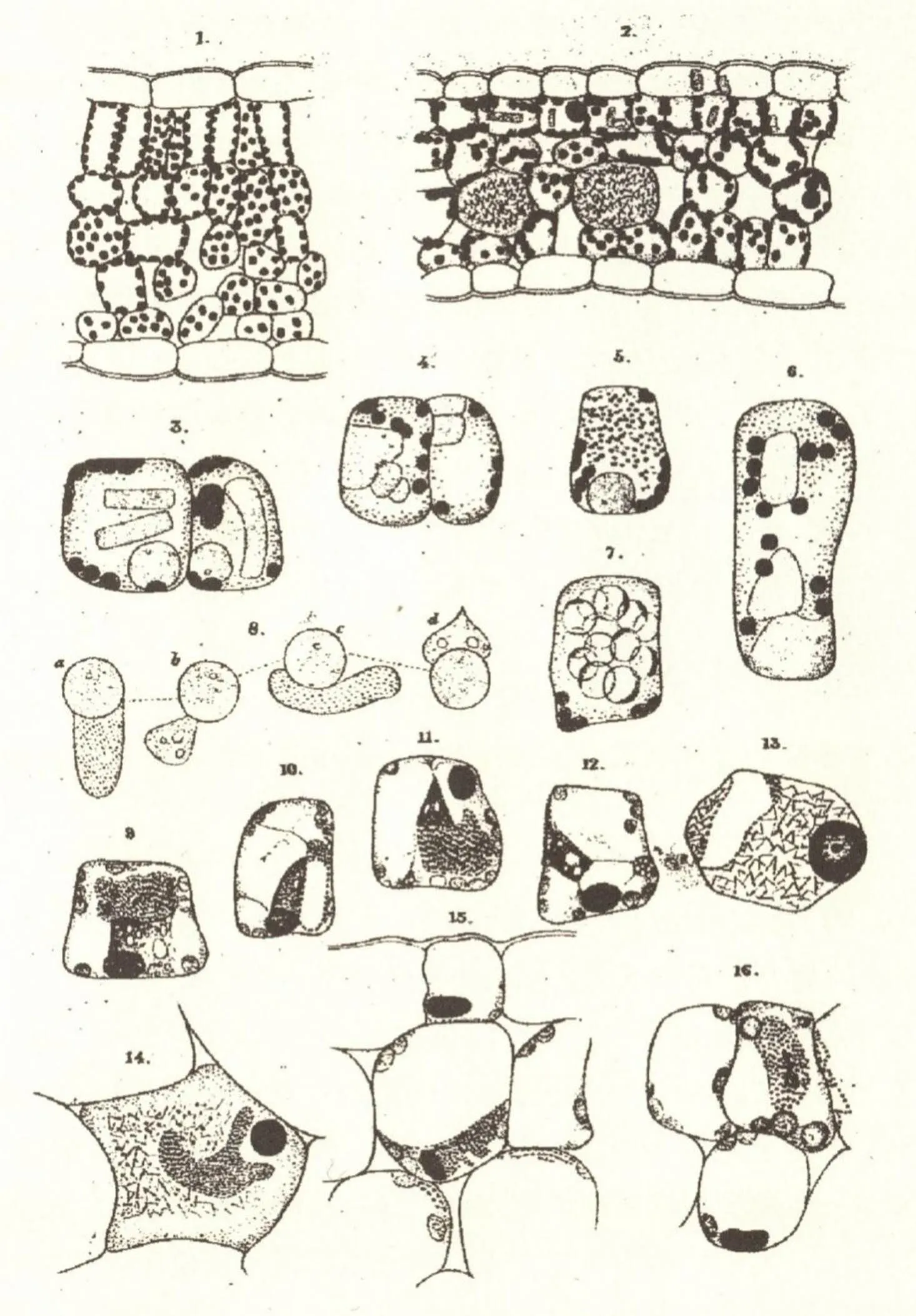
图12 伊万诺夫斯基1903年论文中的病叶光学显微镜观察图
伊万诺夫斯基的解释是,琼脂凝胶放置一段时间后内部会出现细微裂纹,从而使烟草叶汁的滤液和颜料墨水溶液能够渗透到其内部。颜料墨水溶液能够在陈旧琼脂凝胶中扩散,说明陈旧琼脂凝胶中的裂纹已经相当之大。因此,贝杰林克观察到的烟草叶汁的滤液在琼脂凝胶中扩散的现象不足以证明烟草花叶病的滤过性病原体是流质的观点。
既然烟草花叶病的病原体不是液体或可溶的,那它是什么?是一种细菌,还是一种异常原生质? 伊万诺夫斯基认为,它应该是一种极其微小的细菌。
只要烟草花叶病的病原体是细菌,不论它的体度小到何种程度,都应该能够进行体外培养。因此,伊万诺夫斯基尝试着对烟草花叶病的病原体进行了体外培养。他发现,健康烟草接种培养液后出现花叶病的个体数量比对比组的要多,这个现象似乎只能用病原体在体外培养时发生了增殖来进行解释。因此,伊万诺夫斯基最终还是倾向于认定,烟草花叶病病原体是一种极其特殊的细菌(microbe),而非人们通常所讲的细菌。不过,他在1903年公开发表的论文的结尾处提到,有关烟草花叶病病原体的人工培养问题需留待将来继续研究(图12)。
伊万诺夫斯基对贝杰林克的流质说进行了有力的反驳,但他并没有用实验充分证明烟草花叶病病原体就是微粒。因此,进入20世纪后,学术界围绕滤过性病原体,亦即贝杰林克所说的病毒是否是微粒问题展开了新一轮的研究竞争。
6 杜加尔认为烟草花叶病致病因子是可在细胞内增殖的微粒
迈入20世纪后,跻身烟草花叶病毒研究领域的学者越来越多。因电子显微镜的普及是1939年以后的事,故20世纪初期人们对烟草花叶病毒的研究只能是各显神通。当时,人们讨论得最多的问题是,烟草花叶病毒究竟是不是微粒?它是不是微生物?
1899年,美国农业部植物产业局专家伍兹(Albert F. Woods,1866-1948) 在研究叶绿素变色问题时意识到树叶入秋后由绿变黄可能是叶内的氧化酶的作用结果。他由此推测某些植物病变,譬如烟草花叶病有可能是因叶内的氧化酶或过氧化酶活性增强所致[2]。这意味着烟草花叶病有可能不是外源性疾病,而是植物本身出了问题。1902年,他深入研究后发现患花叶病的烟草叶子的汁液中的确含有大量的氧化酶。他据此断定,烟草花叶病是因氧化酶的新陈代谢发生紊乱引起的[21]。这样,毒素说又开始抬头。稍后进入美国农业部植物产业局担任专家的奥拉德(Harry A. Allard,1880-1963)对毒素说表示怀疑。他1916年在对伍兹的实验研究进行追试后指出,氧化酶不是引发烟草患花叶病的原因,而是烟草患花叶病导致的结果[22]。
当时第一次世界大战正酣,奥拉德无法从德、法等国买到尚柏朗氏过滤器。正巧利文斯通(Burton. E. Livingstone)1908年发明了一种用于监测土壤水分变化情况的装置(图13)。该装置带有一个埋在土壤中的、主要用云母制成的多孔杯。于是,奥拉德就用这种现成的多孔杯来替代尚柏朗氏过滤器进行过滤。他发现,患花叶病的烟草叶子的汁液用这种多孔杯过滤后,滤液中确实含有高活性的氧化酶,但这种滤液几乎没有传染性。它表明烟草花叶病病原体已被多孔杯过滤掉了。尽管这是一项偶然发现,但它却很好地证明了氧化酶并非烟草花叶病的病原体,同时还证明了烟草花叶病病原体是可被云母吸附的颗粒。
奥拉德还发现,烟草花叶病病原体不仅能够被云母吸附,而且使用高浓度的乙醇对其进行处理后病原体还会失去活性。不过,使用45%~50%的乙醇对其进行处理后,病原体仍然会保持较强的活性,同时还会出现沉淀。
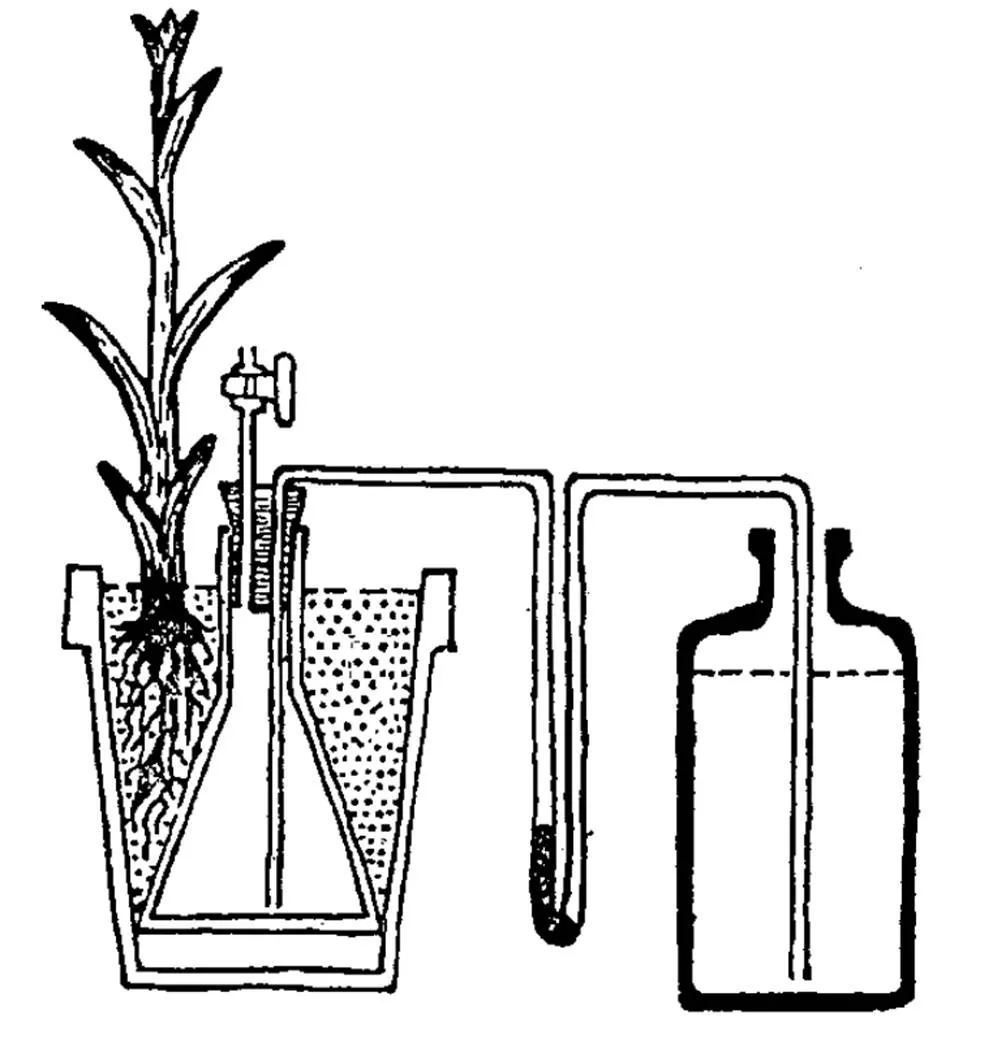
图13 利文斯通(B. E. Livingstone)1908年发明的带有多孔杯的土壤水分监测仪
奥拉德的上述研究引起了美国著名的植物生理学家、植物病理学拓荒者杜加尔(Benjamin M. Duggar,1872-1956)的注意。杜加尔1898年在康奈尔大学取得博士学位后,曾赴美国农业部担任过一年的植物生理学专家。1912年,他来到圣路易斯担任华盛顿大学的植物生理学教授和密苏里植物园的生理学专家,开始涉足烟草花叶病研究[23]。
杜加尔和其研究助理使用奥拉德的方法制得烟草花叶病病原体的沉淀物后,通过与已知物质颗粒的大小进行比对,于1921年推定,烟草花叶病致病因子的大小与血红蛋白相近,直径大约为30纳米,体积大约是一般细菌的1/37000[24]。当时,测定血红蛋白、明胶这类胶体的分子大小时都是先让它们在溶液中充分扩散,然后用孔径不同的超细过滤器进行过滤,根据其不能通过的最大孔径来推定该分子的大小取值范围。
杜加尔在研究过程中还发现,用45%~50%的乙醇处理后获得的烟草花叶病致病因子好几天后仍具有传染性。此前,有研究表明,枯草菌的芽孢对高浓度的乙醇也具有耐受性。两者的性质似乎没有本质上的差异。杜加尔感到很好奇,于是和其研究助理对烟草花叶病致病因子和枯草菌的芽孢展开了比较研究。结果,枯草菌的芽孢在玛瑙研钵中研磨3小时后就失去活性,而烟草花叶病致病因子研磨9个小时后仍然具有一定的传染性[25](图14)。杜加尔给出的解释是,枯草菌的芽孢在研磨过程中由于细胞结构被破坏了所以才失去活性,烟草花叶病致病因子的体积只有枯草菌芽孢的1/37000,由于不可能拥有枯草菌芽孢那样的细胞结构,所以长时间研磨后仍未失去传染性。这意味着烟草花叶病致病因子乃有别于细菌的微粒。

图14 电动玛瑙研钵主要部件
杜加尔在1923年的上述论文中指出:目前,认为烟草花叶病致病因子是细菌的观点可能是完全错误的;被广泛接受的观点是烟草花叶病致病因子乃“病毒”。这种病毒在细胞内具有非同寻常的活性,但脱离细胞后,和任何没有细胞结构的胶体粒子一样没有活性。总体看来,花叶病毒的行为更像是生物胶体,但它具有复制力。在该文的末尾,他写道:“花叶病的致病因子可能是宿主细胞的间歇性产物,但不是像酶那样简单的产物,更像是构成染色质的颗粒或具有某种遗传结构,譬如基因那样的颗粒。也就是说,它摆脱了宿主细胞中各种调节机制的束缚,并被赋予了自我复制的能力。”[25]至于颗粒状的烟草花叶病致病因子自身究竟有没有生命?杜加尔并没有回答。
由上可知,一战结束之初,美国的烟草花叶病毒研究水准就已超过欧洲。此时,在一些美国学者看来,致使烟草患花叶病的病毒乃滤过性病原体,但它既不是“传染性活流质”,也不像具有细胞结构的“极小生物”,而是可在细胞内进行自我复制的超显微颗粒。问题是这种颗粒状的病毒究竟是什么?
7 斯坦利基于结晶实验提出烟草花叶病毒是一种蛋白质
19世纪末期的烟草花叶病毒研究虽然只是小荷才露尖尖角,但却带动了20世纪早期的病毒研究的快速发展。不过,“20世纪早期的病毒研究主要在病毒病,而不在病毒的本质,因为识别某些传染病比识别病原体要容易些。”[26]
一战后初期,在烟草花叶病毒研究领域表现最为突出的研究团队当属博伊斯汤普森植物研究所的昆克尔实验室。昆克尔(Louis O. Kunkel,1884-1960)早年曾在美国农业部植物产业局研究过土豆病毒病,1920年去夏威夷工作后主要研究甘蔗病毒病,1923年他接受新成立的汤普森植物研究所的聘请来到纽约,负责组建植物病毒学实验室[27]。该实验室很快就吸引来了一批对烟草花叶病毒研究抱有浓厚兴趣的学者。其中的代表人物有普尔蒂(H.A.Purdy)、霍姆斯(F.O.Holmes)和文森(C.G.Vinson)[3]41-46。
普尔蒂在研究过程中发现,患有花叶病的烟草叶汁中存在一种健康烟草叶汁中没有的特殊物质,而且用烟草花叶病毒感染同为茄科的番茄、矮牵牛、辣椒等植物后,其叶汁中同样含有这种物质,但在受其他病毒感染的烟草叶汁中并没有找到这种物质。实验表明,将该特殊物质与使用兔子制备的抗烟草花叶病毒血清混合后,其感染性会被中和。很明显,这种具有抗原性的特殊物质源自于烟草花叶病毒。由于已有研究表明,具有抗原性的物质通常都是蛋白质,所以普尔蒂在1928年推定烟草花叶病毒中含有蛋白质。
霍姆斯在阅读与烟草花叶病有关的研究文献时注意到,有多篇文章提及将患有花叶病的烟草叶汁接种到某些烟草属植物的叶子上之后,该片叶子上会出现局部病斑。于是,他给17种烟草属植物接种了患有花叶病的烟草叶汁,结果,其中5种植物的叶子上出现了局部病斑(图15)。霍姆斯确认这些局部病斑都是由烟草花叶病毒感染引起的。他认为可以用受感染叶子上的局部病斑数量来检测所接种的烟草花叶病毒的浓度。于是,他于1929年开发出了使用心叶烟草定量检测烟草花叶病毒浓度的新方法。这种方法不仅耗时短、精度高,而且简单易行。此项研究为烟草花叶病毒的提纯带来了极大的便利。
文森在处理被烟草花叶病毒感染的烟草病叶提取液时发现,添加藏红、丙酮、乙醇等沉淀剂后,传染性物质会发生沉淀。而且,添加藏红后沉淀的那些被认为是病毒的传染性物质,不再具有传染性,但去除其中的藏红后,又会恢复传染性。文森认为这可能是传染性物质与藏红发生反应造成的,换言之,病毒可能是一种化学物质。他于1931年推定这种化学物质与酶类似。此外,文森还注意到,用丙酮处理烟草病叶提取液时,会有结晶析出。不过,这种结晶的传染性不强,而且含有不少杂质。尽管他试图用结晶的方式提取分离烟草花叶病毒,但一直没有成功。

图15 烟草花叶病毒诱发的烟叶局部病斑
从烟草病叶的提取液中成功分离出烟草花叶病毒晶体的是美国洛克菲勒医学研究所的生物化学家斯坦利。
1932年,在时任所长西蒙·弗莱克斯纳(Simon Flexner,1863-1946)的主导下,洛克菲勒医学研究所将位于普林斯顿的动物病理学部扩充为动物与植物病理学部。鉴于昆克尔在汤普森植物研究所组织开展植物病理学研究卓有成效,弗莱克斯纳决定聘请他担任新设立的植物病理学部门主任。昆克尔到任后,除了将霍姆斯等一批老部下带到新单位之外,还将刚满28岁的斯坦利纳入自己的麾下。
斯坦利曾在伊利诺伊大学跟随在美国科学界和工业界享有盛誉的著名化学家罗杰·亚当斯(Roger Adams,1889-1971)教授学习有机化学,并于1929年在那里获得博士学位。之后,他又赴德国慕尼黑跟随1927年的诺贝尔化学奖得主海因里希·维兰德(Heinrich Wieland,1877-1957)教授做了一段时间与天然物化学有关的博士后研究。[28]在这两个有机化学顶尖研究室受到的学术训练为他进入科研经费充裕的洛克菲勒医学研究所开展烟草花叶病毒结晶研究奠定了重要的基础。
斯坦利1933年启动烟草花叶病毒结晶研究可以说是恰逢其时。(1)已有研究表明,烟草花叶病毒可能含有蛋白质;(2)提纯所需的快速测定烟草花叶病毒浓度的方法已经确立;(3)从溶液中制备高纯度晶体蛋白酶已有成功先例。关于第(3)点,需要再做些补充说明。
1926年康奈尔大学生物化学助理教授萨姆纳(James B. Sumner,1887-1955)成功地从刀豆中提取分离出晶体脲酶,这是生物化学史上首次获得的晶体酶。受其鼓舞,洛克菲勒医学研究所研究员诺斯罗普(John H. Northrop,1891-1987)重启了胃蛋白酶的研究与制备工作,并于1930年从一种商业胃蛋白酶制剂中分离出了晶体胃蛋白酶。此后,他又与人合作分离出了多种蛋白酶及其前体,从而使“酶是蛋白质”这一发现成为学界共识,并且积累了丰富的制备晶体蛋白酶的经验[29]。
斯坦利的烟草花叶病毒结晶研究是从重复文森等人的实验开始的。由于烟草病叶的提取液中除含有烟草花叶病毒外,还含有很多其他成分,所以需要采用盐析法和层析法进行提纯。关键是使用盐析法进行分级沉淀时,需要对变量进行严格控制。斯坦利是学有机化学出身的,而且必要时还可以请所里的同事诺斯罗普提供帮助。这些有利条件都是文森所不具备的。而且,在浓缩病毒过程中,还需要频繁地使用局部斑纹定量检测法来确认沉淀物或上清液有无传染性。由于霍姆斯已成为同事,所以必要时也可以随时请教。总之,斯坦利很快就获得了高浓度的烟草花叶病毒提取物。
斯坦利发现,胰蛋白酶虽然能抑制这种烟草花叶病毒提取物的传染性,但其传染性仍能恢复,而胃蛋白酶则能使其水解,从而彻底失去传染性。据此,他1934年得出结论:烟草花叶病毒是一种蛋白质,或与某种蛋白质密切相关。其后,对烟草花叶病毒在不同氢离子浓度下的灭活速率的研究也同样支撑这一结论[30]。这一结论无疑有助于斯坦利将目标直接锁定蛋白质结晶的制备来设计接下来的浓缩与纯化烟草花叶病毒的研究进路。
由于方向明确、路线正确、条件优越,斯坦利1935年就从烟草病叶的提取液中成功地浓缩、分离出了高纯度的烟草花叶病毒结晶(图16)。该结晶即使稀释10亿倍或重复结晶10次仍然具有传染性。而且,给动物注射这种结晶后获得的抗血清能够抑制烟草花叶病毒的传染性。斯坦利随即就将这项研究结论发表在当年的《科学》杂志上。他在这篇文章中明确指出:“烟草花叶病毒被认为是一种自催化蛋白质,就目前而言,它的增殖可能需要活细胞的存在。”“该蛋白质的分子量,大约是几百万。”[31]
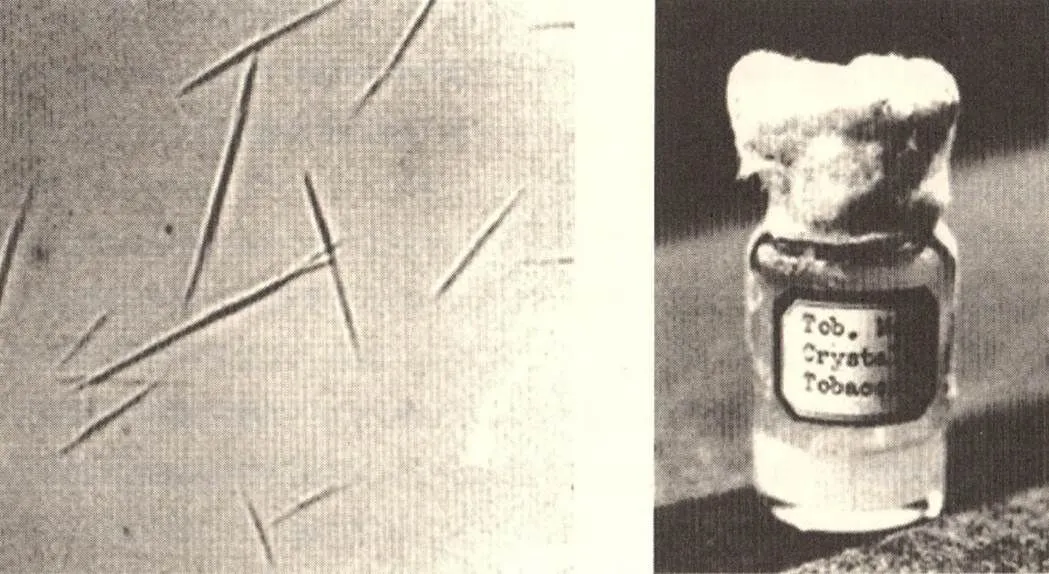
图16 斯坦利(W. M. Stanley,1904-1971)1935年制备的TMV结晶
在西门子公司于1939年首次推出实用电子显微镜之前,科学家们虽然有足够的证据断定烟草花叶病毒是一种不同于细菌的微粒,但一直无法借助光学显微镜观察到病毒。在根本看不到病毒的情况下,要将病毒分离出来进行培养,进而对其本质展开深入探究,无异于缘木求鱼。斯坦利独辟蹊径,采用化学方法从患有花叶病的烟草叶子的提取液中成功分离出烟草花叶病毒结晶,使烟草花叶病毒变成一种既“看得见”又“摸得着”的蛋白质颗粒。这一贡献无疑推动了人们从分子水平去进一步认识病毒的本质,促进了生物学与化学以及生物学与物理学的交叉融合,并为分子生物学的诞生奠定了重要基础。斯坦利因在病毒蛋白质的分离、纯化与结晶方面贡献突出,1946年与萨姆纳、诺斯罗普一道被授予诺贝尔化学奖。这是病毒研究领域的第一个诺贝尔奖。
8 烟草花叶病毒原来是杆状核酸蛋白质复合体
斯坦利从患有花叶病的烟草叶子的提取液中浓缩、分离出蛋白质结晶,并用实验证明这种蛋白质结晶具有传染性,亦即能够进行自我增殖。自我增殖乃生物才具有的属性,如果像蛋白质这样的化学物质的确具有自我增殖能力,那么生命和物质之间的界限岂不需要重新划分?面对年轻的化学家提出的挑战,生物学家不可能无动于衷。那些坚信病毒是生物,晶体蛋白质不是生物,因而不可能是病毒的生物学家最初的反应是对斯坦利的研究结论表示怀疑[2]。
理论上讲,病原体的确定必须遵循生物学家公认的“科赫四原则”[32]。具体到烟草花叶病毒就是以下情况。(1)所有烟草病叶中都应含有烟草花叶病毒,但健康的烟草叶子中不能有。在这种情况下,我们并不知道烟草花叶病毒是导致烟草叶子受感染的原因,还是烟草叶子受感染后出现的结果。(2)从烟草病叶中分离出烟草花叶病毒,并进行纯培养或纯化处理。如果不能获得无杂质的纯粹烟草花叶病毒,根本就无法做单一要素可控实验。而非单一要素实验,对其结果无法进行明确归因。(3)用纯烟草花叶病毒给健康烟叶接种,健康烟叶都会发生相同病变。如果健康烟叶接种烟草花叶病毒后并没有都发生病变,那意味着导致病变的并不只是烟草花叶病毒,可能还有其他未知因素参与作用。(4)从接种后发生病变的烟草叶子中仍能分离出烟草花叶病毒,而且分离出的病毒与抗烟草花叶病毒血清混合后会发生中和,亦即特异性应答。如果发生病变的烟草叶子中未必都确定有烟草花叶病毒,那么烟草花叶病的病原体究竟是什么,仍然不能完全断定。
斯坦利1935年在《科学》杂志上发表的那篇论文不足2页,由于写得过于简练,引起一些质疑在所难免。但他在1936年发表的一篇论文中详细地介绍了自己的具体研究过程和所获得的数据[33]。从中可以看出,他的烟草花叶病毒结晶研究从整体上讲符合“科赫四原则”的基本精神。
比起生物学家,化学家对斯坦利的质疑则要尖锐得多。当时,化学家提出的主要问题是,烟草花叶病毒结晶的纯度如何?它果真只是蛋白质?
从1935年的论文中可以看出,斯坦利从烟草花叶病毒结晶中并没有测出磷,只是说测出了1%的灰分,而且测出的含氮量高达20%,与已知的蛋白质含氮量不符。这意味着他在使用硫酸铵盐析法和硅藻土过滤法制备烟草花叶病毒结晶过程中很有可能没有完全去除硫酸铵。在1936年的论文中,他虽然更正了含氮量的数值,但仍然没有测出含磷量。
1936年,英国洛桑农业实验站植物病理部门的鲍顿(F. C. Bawden)和剑桥大学病理系的皮里(N. W. Pirie)合作对自己混合使用硫酸铵盐析法和等电点沉淀法精制出的烟草花叶病毒结晶进行检测后发现,结晶中的含氮量为16.7%,含磷量为0.5%,含糖量为2.5%。他们深入研究后指出:烟草花叶病毒大约是由95%的蛋白质和5%的核糖核酸(RNA)组成的核酸蛋白质复合体。而且,他们还基于烟草花叶病毒溶液具有各向异性推定烟草花叶病毒颗粒呈杆状[34]。这意味着病毒并不像人们通常想象的那样是非常小的细菌,而是一种完全不同的实体。
鲍顿和皮里虽然证明了烟草花叶病毒中含有RNA,但是他们当时并没有发现RNA作为基因组携带着重要的遗传信息。“RNA具有增殖能力,亦即传染性”直到1956年才被德国科学家吉尔(A. Gierer)和施拉姆(G. Schramm)发现。1956年,吉尔和施拉姆将烟草花叶病毒放在水和苯酚中震荡,使RNA与蛋白质分离后,再用提纯过的RNA去给烟草接种,结果烟草叶子上出现了典型的花叶病斑。而当用核糖核酸酶对RNA进行处理后,再给烟草接种,烟草叶子上并不会出现病斑。经过一系列实验验证之后,吉尔和施拉姆指出,RNA是一种遗传物质,烟草花叶病毒的RNA成分在接种后的烟草叶片中能够诱导合成出新的烟草花叶病毒。1957年,佛兰科尔-康拉特(H. Fraenkel-Conrat)和辛格尔(B. Singer)通过病毒的重建进一步证实了吉尔和施拉姆的上述结论[3]81-84。
鲍顿的弟子哈里森(B. D. Harrison)曾在文章中谈到,鲍登和皮里当时曾就RNA是否具有传染性的问题进行过实验研究,可能是由于两人的实验室相距有50英里,等皮里把分离出的RNA运送给鲍登时RNA已经失活,所以鲍登和皮里未能发现RNA的传染性[35]。
尽管鲍登和皮里推定烟草花叶病毒颗粒呈杆状结构,但是直到1939年才被柏林帝国生物学研究所的生物化学家古斯塔夫·阿道夫·考舍(Gustav Adolf Kausche,1901-1960)等人确认。如众所知,1933年,两位德国年轻人恩斯特·鲁斯卡(Ernst Ruska,1906-1988)与波多·冯·波里斯(Bodo von Borries,1905-1956)合作,成功地研制出了全球第一台分辨率超过光学显微镜的电子显微镜。但这台电子显微镜结构比较简单,实用性不强。1938年,二人在西门子公司的支持下又合作研制出2台结构更加合理、功能更为齐全、放大率可达3万倍的实用电子显微镜试制品,其中1台旋即交给了恩斯特·鲁斯卡的胞弟,同时也是波多·波里斯的妻兄哈尔墨特·鲁斯卡(Helmut Ruska,1908-1973)测试使用(图17)。在此基础上,西门子公司于1939年正式推出第1台商用电子显微镜[36]。哈尔墨特·鲁斯卡当时正在柏林大学查理特医学院实习,他坚信电子显微镜有助于促进医学和生物学的发展,因此1938年拿到电子显微镜后就开始尝试着用它来观察多种亚微观生物。1939年他又协助考舍等人使用电子显微镜成功地观察到了烟草花叶病毒[37](图18)。
考舍等人为了增加影像的对比度,将烟草花叶病毒与胶体金混合,不仅在电子显微镜中观察到了烟草花叶病毒,而且还获得了第一张烟草花叶病毒的电镜照片。根据考舍等人的观察,“烟草花叶病毒分子”呈杆状,其直径大约为15纳米,长度为150或300纳米。斯坦利等人1941年也使用电子显微镜对晶体烟草花叶病毒进行了观察,这两个团队的观察结果高度吻合。
这样,自贝杰林克1898年使用“病毒”一词特指滤过性病原体以来,人们终于用自己的眼睛看到了病毒颗粒,并确认它是含有RNA成分、具有传染性的核酸蛋白质复合体。只是后来随着电子显微镜技术的不断发展,人们对杆状烟草花叶病毒体度和结构的把握更加精准罢了。
9 结语
19世纪末20世纪初,巴斯德、科赫等人提出的细菌致病学说正处于鼎盛时期。受这种学说的启迪,德国农业化学家麦尔发现烟草花叶病是一种植物传染病,但他未能证明烟草花叶病的致病因子是一种滤过性病原体。首先在实验过程中意识到烟草花叶病的致病因子是一种滤过性病原体的是俄国的伊万诺夫斯基,但他当时并未意识到这种滤过性病原体是一种有别于细菌的新型病原体。

图17 哈尔墨特·鲁斯卡(H. Ruska,1908-1973)1938年用过的电子显微镜
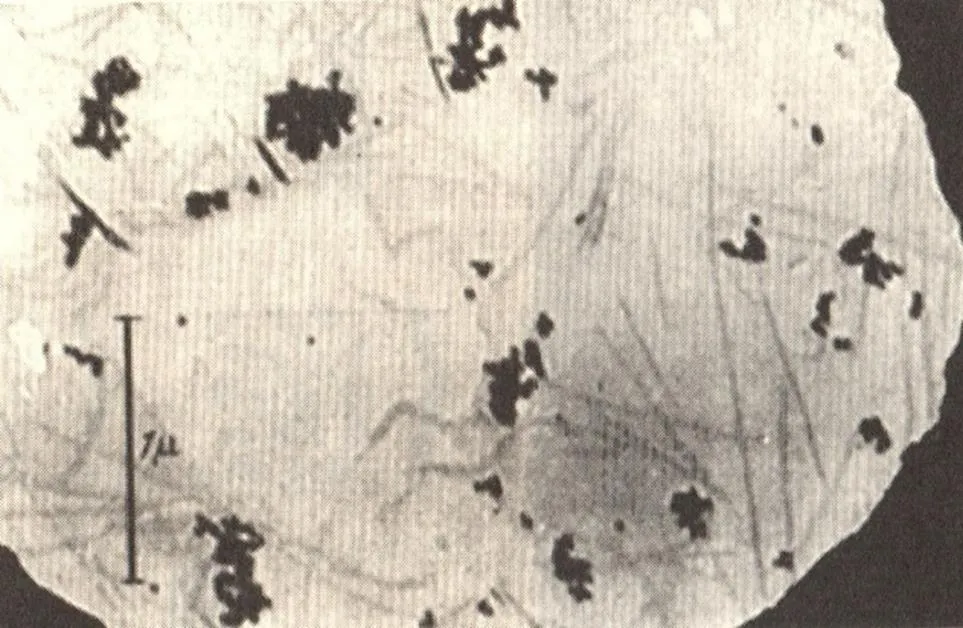
图18 考舍(G. A. Kausche,1901-1960)1939年拍摄的TMV电镜照片
由于传染病皆由细菌或其毒素引起的观点获得了广泛认同,因此当可以通过细菌过滤器的新型病原体——口蹄疫病毒被“发现”之后,德国的吕夫勒和菲洛施等人仍然不愿意抛弃既有的理论和概念,继续将这种新型病原体视作一种细菌。荷兰学者贝杰林克虽然改造了传统的“病毒”概念,并赋予其全新的涵义——“传染性活流质”,但很少有人能够接受这一观念,因为根据以往的经验人们很难想象非颗粒形态的流质也像单细胞细菌那样具有生命力。
一战结束后不久,美国植物病理学家杜加尔基于自己的实验研究将“病毒”的概念发展成为可在细胞内自我增殖的微粒,但他既没有见到这种微粒形态的病毒,也不知道它究竟是什么。因此,当美国生物化学家斯坦利借助当时最先进的酶蛋白质结晶技术于1935年制得烟草花叶病毒结晶,并指出“病毒”是一种蛋白质时,在学术界引起了热议,因为这种“病毒”概念颠覆了很多人对生命和物质的认知。自我增殖被认为是只有生命才具有的属性,如果作为化学物质的蛋白质确实具有这种属性,那么生物与非生物的界限在哪里?
尽管对斯坦利的研究表示怀疑的人有很多,但很快就用事实修正斯坦利的研究结论的唯有英国的鲍登和皮里。鲍登和皮里1936年用无可争辩的实验数据证明,烟草花叶病毒中除含有大量的蛋白质外,还含有少量的RNA,只是他们当时并没有意识到这种RNA才是病毒的遗传物质。鲍登和皮里还从这种核酸蛋白质复合体具有各向异性推出,烟草花叶病毒应该是杆状颗粒,而不是球状颗粒。在电子显微镜的发明人、1986年诺贝尔物理学奖得主恩斯特·鲁斯卡的弟弟哈尔墨特·鲁斯卡的协助下,德国生物化学家考舍于1939年终于直接观察到了烟草花叶病毒,并确认其为杆状颗粒。不过,考舍给出的烟草花叶病毒的大小尺寸并不准确。
从最初断定烟草花叶病毒为滤过性病原体,到终于看到这种滤过性病原体为一种亚微观颗粒,人类整整用了41年。在这段时间里,很多科学家都为人类加深对病毒的理解做出了重要的贡献。不可否认的是,这些科学家虽然在研究烟草花叶病毒的过程中都得出了一些符合事实的、有价值的结论,但是他们的论文或报告中也都存在着这样或那样的错误,要么实验结果不完全符合事实,要么构建的病毒概念不完全正确。简言之,没有一篇论文或报告没有错误,没有一位科学家说得完全正确。至于没有为加深对病毒的理解做贡献,甚至对病毒概念的形成产生严重误导的论文或报告则不计其数。如果当时的人们对这些论文或报告推崇备至,甚至将这些论文或报告的作者奉若神明,不仅不利于病毒概念的形塑,甚至会阻碍科学的发展。
倘若历史上的绝大多数论文与报告都会或多或少地存在一些错误,每一位科学家都会不可避免地存在一些认识误区,那么今人该如何看待科学认知,如何对待科学家?尤其是,今天的科学家会不会像100年前的科学家那样,即使在自己的专业领域内也会频频出错?显然,迷信科学和盲从科学家并不能使我们更加接近真理,也无助于我们解决当下所面临的诸多科技难题。怀疑的世界真理多,盲信的社会谬误多。科学始于疑问,过去是如此,现在也应该是这样。
通过回顾烟草花叶病毒的发现过程,我们还可以看到,科学的发展是累积性的,即使是重大发现通常也是由很多人共同完成的。因此,有必要在科学共同体内部建立平等对话和合作交流的机制。
只有充分发扬学术民主,建立平等对话的机制,才有可能使每一位科学家的真知灼见都不至于被埋没,同时确保任何权威的认知盲点都不至于成为阻碍科学发展的绊脚石。真理越辩越明,在科学共同体内部,批评错误观点和理论的方法不是压制这种观点和理论的传播,而是提出一个更有竞争力的观点和理论。
要建立合作交流机制,首先需要建立一套大家都能理解的话语体系,不能各说各话;其次需要搭建一批方便各国学者高效沟通的平台,不能画地为牢。可以说,无论是德国学者、俄国学者,还是美国学者、英国学者,如果大家在研究烟草花叶病毒过程中,不是基于普遍主义立场行动,就不可能建立起那么庞大的“行动者网络”,因而也就不可能形成那么强大的如实表征病毒本质的能力。
致谢
在成稿过程中,康奈尔大学科学技术论系胡万亨博士曾帮助搜集部分研究资料,北京大学生命科学学院昌增益教授曾提出很多中肯的修改建议,特此一并致谢!
[1] Dimmock N J, Easton A J, Leppard K N.[M]Hoboken, NJ: Wiley-Blackwell, 2006.
[2] Helvoort T. What is a Virus? The Case of Tobacco Mosaic Disease[J].,1991,22(4): 557-588.
[3] 岡田吉美. タバコモザイクウイルス研究の100年[M]. 東京: 東京大学出版会, 2004.
[4] Stanley W M. Soviet studies on viruses., 1944,81: 644-645.
[5] 鳥山重光. 黎明期のウイルス研究:野口英世と同時代の研究者たちの苦闘[M].東京:創風社,2008.
[6] Harrison B D, Wilson T M A. Milestones in the research on tobacco mosaic virus[J]., 1999,354(1383): 521-529.
[7] 董恺忱. 李比希的农学思想[J]. 世界农业,1981,(9): 21-27.
[8] Zaitlin M. The Discovery of the Causal Agent of the Tobacco Mosaic Disease[C]// Kung S D, Yang S F.. Hong Kong: World Publishing Co., Ltd.,1998: 105-110.
[9] 夏 钊. 从“范式”的视角看结核杆菌的发现[J]. 自然辩证法通讯, 2018, 40(11): 134-141.
[10] 周 程. 19世纪前后西方微生物学的发展——纪念恩格斯《自然辩证法》发表90周年[J]. 科学与管理, 2015, (6): 3-9.
[11] 小川真理子. 病原体と国家:ヴィクトリア時代の衛生・科学・技術[M]. 名古屋: 名古屋大学出版会, 2016.
[12] Mayer A. Concerning the mosaic disease of tobacco[C]//. St. Paul, MN: American Phytopathological Society Press, 1942: 11-24.
[13] Lustig A, Levine A J. One Hundred Years of Virology[J]., 1992, 66(8): 4629-4631.
[14] Ivanovsky D. Concerning the mosaic disease of the tobacco plant[C]//. St. Paul, MN: American Phytopathological Society Press, 1942: 27-30.
[15] 高尚荫. 伊文诺史基(Iwanowski)与病毒[J]. 科学, 1950,(3): 68.
[16] Bos L. Beijerinck’s work on tobacco mosaic virus: historical context and legacy[J]., 1999, 354(1383): 675-685.
[17] Martinus Willem Beijerinck:1851-1931[C]//. St. Paul, MN: American Phytopathological Society Press, 1942: 31-32.
[18] Beijerinck M W. Concerning aas cause of the spot disease of tobacco leaves[C]//. St. Paul, MN: American Phytopathological Society Press, 1942: 33-54.
[19] Blevins S, Bronze M. Robert Koch and the “golden age” of bacteriology[J].2010(14): e744-e751
[20] Loeffler F, Frosch P. Report of the commission for research on the foot-and-mouth Disease[C]//Hahon N., Englewood Cliffs, NJ: Prentice-Hall, 1964: 64-68.
[21] Woods A F. Observations on the Mosaic Disease of Tobacco[R]. Washington D C: Bureau of Plant Industry, USDA., 1902.
[22] Allard H A. Some properties of the virus of the mosaic disease of tobacco[J]., 1916, 6: 649-674.
[23] Walker J C. Pioneer Leaders in Plant Pathology: Benjamin Minge Duggar[J]., 1982, 20: 33-39.
[24] Duggar B M, Karrer J L. The sizes of the infective particles in the mosaic disease of bobacco[J]., 1921, 8(4): 343-356.
[25] Duggar B M, Karrer-Armstrong J. Indications respecting the nature of the infective particles in the mosaic of bobacco[J]., 1923, 10(3): 191-212.
[26] 高尚荫. 20世纪病毒概念的发展[J]. 病毒学杂志, 1986, 1(1): 1-7.
[27] Stanley W M. A Biographical Memoir: Louis Otto Kunkel, 1884–1960[R]. Washington D C: National Academy of Sciences,1965.
[28] Manchester K L. The crystallization of enzymes and virus proteins: laying to rest the colloidal concept of living systems[J].,2004,28(1): 25-29.
[29] Northrop J. The preparation of pure enzymes and virus proteins, Nobel Lecture, December 12, 1946[OL]. [2020-02-02]. https://www.nobelprize.org/prizes/ chemistry/1946/northrop/lecture/.
[30] Stanley W M. The isolation and properties of crystalline tobacco mosaic virus,Nobel Lecture, December 12, 1946[OL]. [2020-02-02]. https://www.nobelprize.org/ prizes/chemistry/1946/Stanley/lecture/.
[31] Stanley W M. Isolation of a crystalline protein possessing the properties of tobacco-mosaic virus[J]., 1935, 81(2113): 644-645.
[32] 冯 薇. 科赫:医学微生物学的奠基人[J]. 中国医院, 2004, 8(5): 76-77.
[33] Stanley W M. Chemical studies on the virus of tobacco mosaic Ⅵ. The isolation from diseased Turkish tobacco plants of a crystalline protein possessing the properties of tobacco mosaic virus[J]., 1936, 26: 305-320.
[34] BawdenF C, Pirie N W, Bernal J D, Fankuchen I. Liquid crystalline substances from virus-infected plant[J]., 1936, 138: 1051-1052.
[35] HarrisonB D. Frederick Charles Bawden: Plant Pathologist and Pioneer in Plant Virus Research[J]., 1994, 32: 39-47.
[36] 西门纪业, 弗·棱茨. 两位电子显微镜卓越的先驱者——鲁斯卡和波里斯90周年诞辰纪念[J]. 电子显微学报, 1995, (3): 235-242.
[37] Kruger D H, Schneck P, Gelderblom H R. Helmut Ruska and the visualisation of viruses[J]., 2000, 355: 1713-1717.
What is Virus: A Historical Review of Discovery of the Tobacco Mosaic Virus
Zhou Cheng1, 2
(1. Department of Philosophy, Peking University, Beijing 100871, China;2. School of Health Humanities, Peking University, Beijing 100191, China)
In the years before the advent of electron microscopy, where the “germ”, as in the dominating germ theory of disease, was confined to bacteria, how did virus, which remained invisible, come to be known? How did people manage to identify something as “virus”? This article approached these issues by studying the intellectual history of science in the discovery of the tobacco mosaic virus (TMV), while remaining fully aware that scientific research has its limitations and that knowledge resulting from it could be wrong. Specifically, this article reviews eight milestone discoveries that gradually revealed the TMV: 1) tobacco mosaic disease was transmissible by inoculating healthy plants with sap from the leaves of diseased plants (Adolf Mayer); 2) the agent that causes the disease was filterable (Dmitri Ivanowsky); 3) the agent was(Martinus Beijerinck); 4) foot-and-mouth disease in cattle was caused by the “minutest organisms” (Friedrich Loeffler & Paul Frosch); 5) the infective entity of the tobacco mosaic disease was not(Ivanowsky); 6) the disease was caused by some particle that could multiply itself in cells (Benjamin M. Duggar); 7) crystallization showed TMV as a protein (Wendell Meredith Stanley); and 8) TMV turned out to be a rod-shaped aggregate of protein containing RNA.
Germ theory; TMV; scientific discovery; scientific concept; scientific spirit
2020–02–01;
2020–02–17
中国科学院学部咨询项目( 2017ZWH016A–040)
周 程(1964–),男,博士,教授,研究方向为科学社会史、科学实践哲学、创新管理与科技政策。E-mail: zhoucheng@pku.edu.cn
10.3724/SP.J.1224.2020.00092
N09
A
1674-4969(2020)01-0092-21
