PEG-400/H2O中无配体条件下卤代芳烃与芳基硼酸交叉偶联反应的研究
2020-04-15匡仁云张振兴沈玉君谢宝星唐伯孝
匡仁云,张振兴,黄 翔,沈玉君,邹 红,谢宝星,唐伯孝
PEG-400/H2O中无配体条件下卤代芳烃与芳基硼酸交叉偶联反应的研究
匡仁云1,2,张振兴1,黄 翔1,沈玉君1,邹 红1,谢宝星1,*唐伯孝1,2
(1. 井冈山大学化学化工学院,江西,吉安 343009;2. 江西省配位化学重点实验室应用化学研究所,江西,吉安 343009)
在无配体条件下,以聚乙二醇(PEG-400)和水为反应介质,醋酸钯为催化剂,卤代代芳烃和芳基硼酸通过交叉偶联反应合成一系列联苯类化合物(3a~3h), 其结构经1H NMR和13C NMR表征,交叉偶联产率为30%~99%。PEG和水作为反应溶剂减少了对环境污染,实现了偶联反应的绿色化。
PEG/H2O;无配体;Suzuki-Miyaura偶联;绿色化学
0 引言
过渡金属催化构建C-C键已成为有机合成的有效手段之一,在现代有机反应中扮演着重要角色[1-2]。在这些研究方法中,Suzuki-Miyaura反应因为良好的选择性和偶联收率,已经发展成为一种具有实际应用价值的合成方法[3-4]。大多数Suzuki-Miyaura偶联反应研究方向主要集中在配体、有机溶剂等方面[5-8]。例如,Karami 等研究人员,以膦配体和氯化钯为催化体系,在温和条件下实现了Suzuki-Miyaura偶联反应[9]。随着学者对原子经济性和环保的认知不断提高,绿色介质使用、催化剂循环已经成为该领域的研究热点[10-15]。Korolev 研究小组发现,以纯水为反应介质,PdCl2-EDTA 催化体系,K2CO3为碱,碘代芳烃的Suzuki-Miyaura偶联收率还不错,但溴代芳烃的偶联反应活性要差一些[16]。总之,Suzuki-Miyaura偶联反应在配体、催化剂循环和绿色化学方面已取得较好的研究成果,但在某些方面仍然存在一些瑕疵,比如,催化体系复杂且昂贵、反应底物局限性等,这些问题都会影响Suzuki-Miyaura偶联的实际应用价值。因此,发现一些简单、经济、绿色的催化体系,仍然是这一研究领域的良好策略。
聚乙二醇(PEG)高温下稳定而不易挥发,并且可生物降解和无毒副作用,它是一类对环境友好的反应介质[17]。我们研究小组一直致力于绿色介质中偶联反应的研究,也取得了一些研究成果[18-19]。最近的研究发现,在无配体的条件下,以PEG /H2O为反应介质,Pd(OAc)2能够有效催化溴代和氯代芳烃的Suzuki-Miyaura反应, 并能够得到30%~99%的偶联收率。
1 实验部分
1.1 试剂和仪器
芳基苯硼酸、卤代烃、Pd2(OAc)2等试剂从百灵威化学公司购买(分析纯),K2CO3、EtN3、KOAC、NaOH、PEG、石油醚等从国药集团公司购买(化学纯),以上试剂未经纯化直接使用。核磁共振仪:AVANCE Ⅲ HD 400(厂家:Bruker)。
1.2 Suzuki-Miyaura偶联反应及产物表征
在反应管中依次加入卤代芳烃(0.5 mmol),芳基硼酸(0.6 mmol),醋酸钯(0.015 mmol),NaHCO3(1.0 mmol),PEG-400(0.5 g)和H2O(0.5 g),在100 ℃油浴下反应,TLC跟踪反应,反应完成后,冷却降至室温,加入饱和食盐水15 mL,用乙酸乙酯萃取(10 mL×3),分液,有机相用无水MgSO4干燥,过滤后减压蒸去乙酸乙酯得到粗产物,经柱色谱分离得到偶联产物3。
4-甲基-4'-甲氧基联苯(3a):1H NMR (400 MHz, CDCl3) δ 7.50 (d,= 8.6 Hz, 2H), 7.44 (d,= 8.0 Hz, 2H), 7.21 (d,= 8.0 Hz, 2H), 6.95 (d,= 8.6 Hz, 2H), 3.82 (s, 3H), 2.37 (s, 3H);13C NMR (100 MHz, CDCl3) δ 158.89, 137.92, 136.31, 133.70, 129.41, 127.91, 126.54, 114.12, 55.29, 21.02.
4-硝基联苯(3b):1H NMR (400 MHz, CDCl3) δ 8.27 (d,= 8.8 Hz, 2H), 7.71 (d,= 8.8 Hz, 2H), 7.61 (d,= 6.8 Hz, 2H), 7.51 – 7.41 (m, 3H);13C NMR (100 MHz, CDCl3) δ 147.51, 146.98, 138.64, 129.07, 128.85, 127.69, 127.29, 124.00.
4-乙酰基联苯(3c):1H NMR (400 MHz, CDCl3) δ 8.01 (d,= 8.4 Hz, 2H), 7.66 (d,= 8.4 Hz, 2H), 7.61 (d,= 7.0 Hz, 2H), 7.47 – 7.24 (m, 3H), 2.62 (s, 1H);13C NMR (100 MHz, CDCl3) δ 197.67, 145.67, 139.76, 135.75, 128.88, 128.83, 128.16, 127.18, 127.12, 26.56.
4-甲氧基联苯(3d):1H NMR (400 MHz, CDCl3) δ 7.55 – 7.50 (m, 4H), 7.39 (t,= 7.6 Hz, 2H), 7.28 (t,= 7.4 Hz, 1H), 6.96 (d,= 8.8 Hz, 2H), 3.82 (s, 3H);13C NMR (100 MHz, CDCl3) δ 159.11, 140.78, 133.72,128.68, 128.10, 126.69, 126.61, 114.17, 55.27.
2-甲基-4'-甲氧基联苯(3e):1H NMR (400 MHz, CDCl3) δ 7.25– 7.17 (m, 6H), 6.93 (d,= 8.6 Hz, 2H), 3.82 (s, 3H), 2.26 (s, 3H);13C NMR (100 MHz, CDCl3) δ 158.47, 141.50, 135.41, 134.33, 130.25, 130.20, 129.85, 126.92, 125.71, 113.44, 55.19, 20.49.
3-甲基-4'-甲氧基联苯(3f):1H NMR (400 MHz, CDCl3) δ 7.50 (d,= 8.8 Hz, 2H), 7.35 – 7.27 (m, 3H), 7.11 (d,= 7.2 Hz, 1H), 6.95 (d,= 8.8 Hz, 2H), 3.82 (s, 3H), 2.39 (s, 3H);13C NMR (100 MHz, CDCl3) δ 159.04, 140.77, 138.22, 133.85, 128.59, 128.11, 127.51, 127.38, 123.81, 114.10, 55.26, 21.51.
1-(4-甲氧基苯基)萘(3g):1H NMR (400 MHz, CDCl3) δ 7.92 (d,= 8.2 Hz, 1H), 7.87 (d,= 7.8 Hz, 1H), 7.81 (d,= 8.2 Hz, 1H), 7.50 – 7.37 (m, 6H), 7.00 (d,= 8.8 Hz, 2H), 3.85 (s, 3H);13C NMR (100 MHz, CDCl3) δ 158.91, 139.87, 133.81, 133.08, 131.80, 131.07, 128.22, 127.29, 126.87, 126.03, 125.88, 125.66, 125.37, 113.68, 55.28.
4-甲氧基-4'-氯联苯(3h):1H NMR (400 MHz, CDCl3) δ 7.47 – 7.43 (m, 4H), 7.35 (d,= 8.6 Hz, 2H), 6.95 (d,= 8.8 Hz, 2H), 3.82 (s, 3H);13C NMR (100 MHz, CDCl3) δ 159.32, 139.21, 132.61, 132.41, 128.79, 127.96, 127.87, 114.27, 55.29.
2 实验结果与讨论
2.1 Suzuki-Miyaura偶联反应条件优化
以4-甲基溴苯(1a)与4-甲氧基苯硼酸(2a)交叉偶联反应为模板, 在无配体条件下,以Pd(OAc)2作为催化剂,研究了聚乙二醇的种类、不同碱和反应温度对交叉偶联反应的影响(如表1所示)。首先,考察了PEG类型对交叉偶联反应的影响,其中PEG-400/H2O反应体系表现出最好的反应活性, 其他PEG/H2O反应体系的反应活性较差, 交叉偶联产率较低(entries 1-4)。我们考察了不同碱对交叉偶联反应的影响,实验结果表明NaHCO3的交叉偶联产率最高,NaOH的交叉偶联产率最低(entries 5-8)。最后考察了不同温度对交叉偶联反应的影响,当反应温度是90℃和110℃时,交叉偶联产率都有所下降,分别为82%和70%(entries 9, 10)。
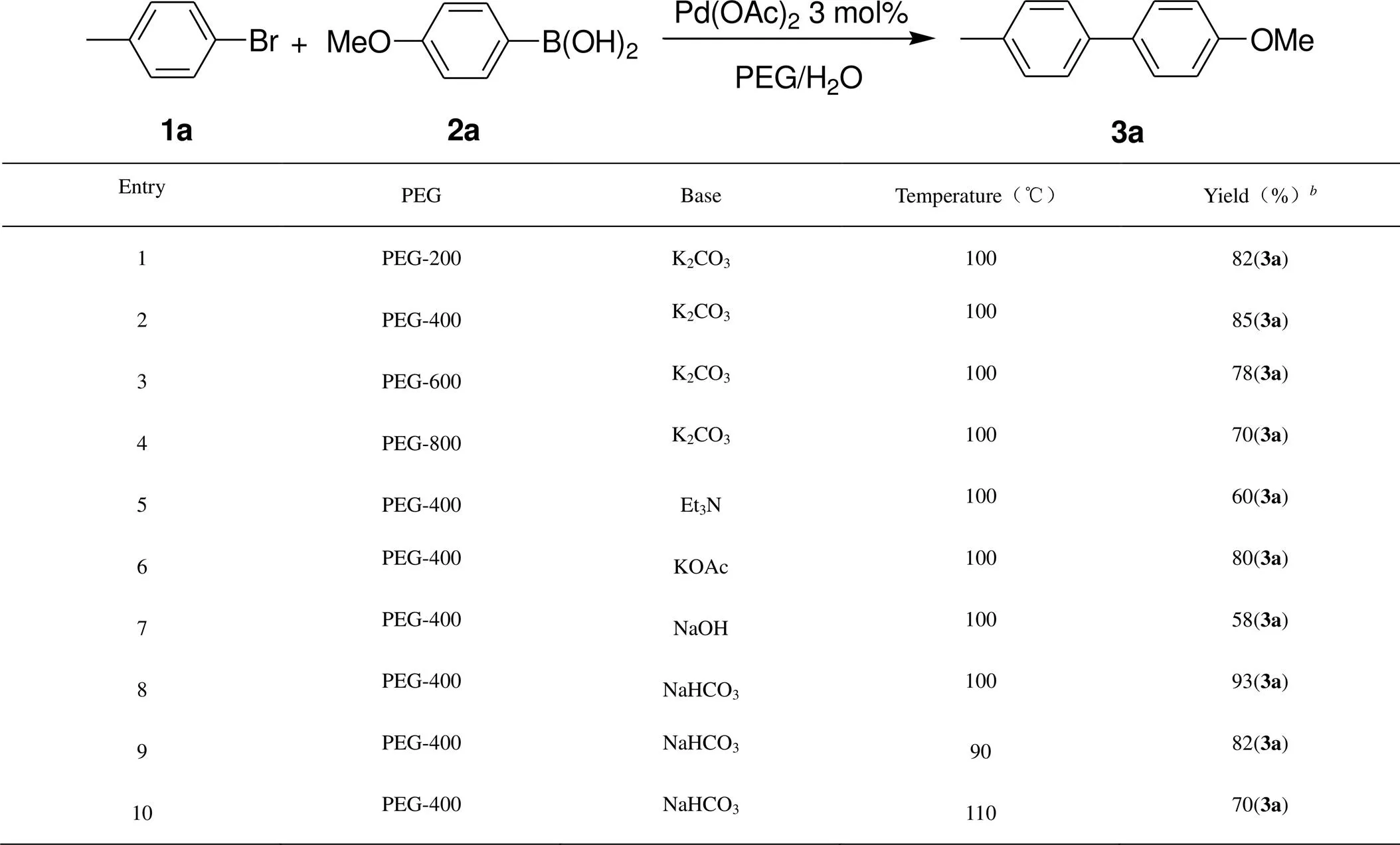
表1 4-甲基溴苯和4-甲氧基苯硼酸交叉偶联反应条件的筛选a
Reaction condition: 1a (0.5 mmol), 2a (0.6 mmol), Pd(OAc)2(0.015 mmol), base (1.0 mmol), water (0.5 g), PEG (0.5 g), 100 °C, air and 10 h;Isolated yield
2.2 Suzuki-Miyaura偶联反应底物拓展
在最佳的反应体系PEG-400/H2O中,选择了一系列溴、氯代芳烃与芳基硼酸进行交叉偶联反应,实验结果见表2。在无配体的条件下,含有吸电子基团卤代芳烃的反应活性比含有给电子基团芳烃要好(entries 1-6)。例如,当溴代芳烃上含有硝基时,交叉偶联产率可达99%。但是,当溴代芳烃上含有甲氧基时,其产率下降到84%(entries 1,4)。由于C-Cl键比C-Br键牢固,不容易断裂,在交叉偶联反应中,氯代芳烃的反应活性比溴代芳烃要差,而且交叉偶联反应条件也要苛刻(entries 5,6)。然后选取4-甲氧基溴苯与不同芳基硼酸反应,实验结果表明不同芳基硼酸的反应活性相差不大,都能够得到85%以上交叉偶联收率(entries 7-12)。实验发现,当用邻、间、对位有甲基的芳基硼酸分别进行交叉偶联反应时,它们的交叉偶联产率相差无几,这一实验结果说明位阻效应对交叉偶联反应影响不大(entries 8-10)。
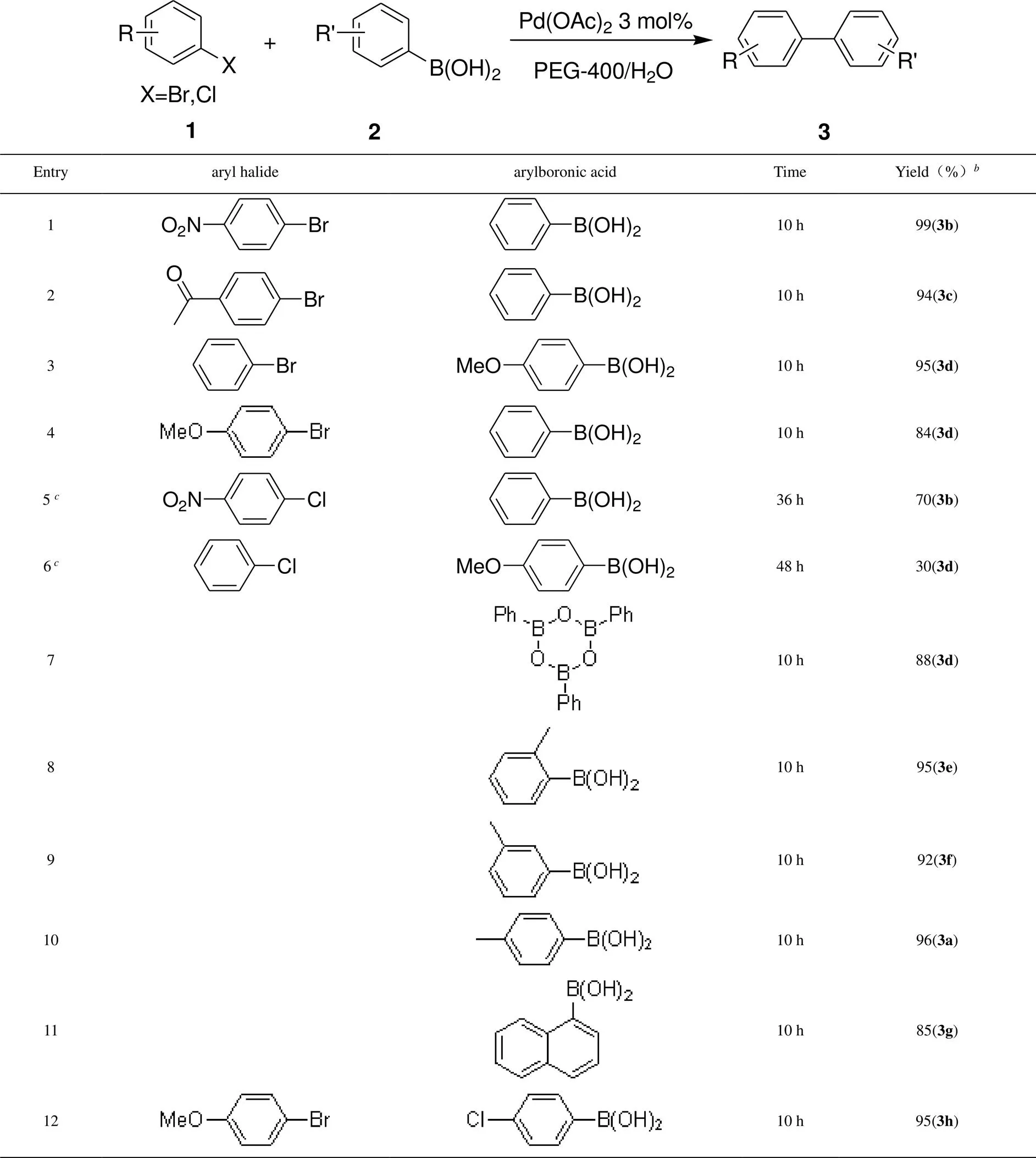
表2 不同反应底物的Suzuki-Miyaura偶联a
Reaction condition: 1 (0.5 mmol), 2 (0.6 mmol), Pd(OAc)2(0.015 mmol), NaHCO3(1.0 mmol), water (0.5 g), PEG-400 (0.5 g), 100 °C and air;Isolated yield;1 (0.5 mmol), 2 (0.75 mmol), Pd(OAc)2(0.02 mmol), NaHCO3(1.0 mmol), water (0.4 g), PEG-400 (0.6 g), 100 °C and air
3 小结
在Pd(OAc)2(0.015 mmol)为催化剂,NaHCO3(1.0 mmol)为碱,PEG-400 (0.5 g)/H2O (0.5 g)为反应介质,无需任何配体的条件下,发展了一种溴、氯代芳烃与芳基硼酸交叉偶联的新方法,交叉偶联产率30%~99%。同时,PEG的难挥发性、可降解、无毒等优点与传统有机溶剂相比,减少了对环境的污染,实现了Suzuki-Miyaura偶联反应的绿色化。
[1] Nájera C, Beletskaya I P, Yus M. Metal-catalyzed regiodivergent organic reactions, Chemical Society Reviews [J]. 2019, 48(16): 4515-4618.
[2] Cherney A H, Kadunce N T, Reisman S E. Enantioselective and enantiospecific transition-metal- catalyzed cross-Coupling reactions of organometallic reagents to construct C-C bonds [J]. Chemical Reviews, 2015, 115(17): 9587-9652.
[3] Miyaura N, Suzuki A. Palladium-catalyzed cross- coupling reactions of organoboron compounds [J]. Chemical Reviews, 1995, 95(7): 2457-2483.
[4] Han F S. Transition-metal-catalyzed Suzuki–Miyaura cross-coupling reactions: a remarkable advance from palladium to nickel catalysts [J]. Chemical Society Reviews, 2013, 42(12): 5270-5298.
[5] Schaarschmidt D, Lang H P. O-Ferrocenes in Suzuki- Miyaura C-C couplings [J]. ACS Catalysis, 2011, 1(4): 411-416.
[6] Chung K H, So C M, Wong S M, et al. An efficient palladium-benzimidazolyl phosphine complex for the Suzuki-Miyaura coupling of aryls mesylates: facile ligand synthesis and metal complex characterization [J]. Chemical Communications, 2012, 48(14): 1967-1969.
[7] Fleckenstein C A, Plenio H. Sterically demanding trialkylphosphines for palladium-catalyzed cross coupling reactions-alternatives to PtBu3[J]. Chemical Society Reviews, 2010, 39(2): 694-711.
[8] 蓝倩,元洋洋,李美,等. 非膦钯催化Suzuki偶联反应[J].井冈山大学学报:自然科学版,2017,38(6):30-34.
[9] Karami K, Rizzoli C, Salah M M. Synthesis and application of ortho-palladated complex of ( 4-phenylbenzoyl-methylene) triphenylphosphorane as a highly active catalyst in the Suzuki cross-coupling reaction [J]. Journal of Organometallic Chemistry, 2011, 696(4): 940-945.
[10] Da Conceição Silva A, Senra J D, Aguiar L C S, et al. Ligand-free Suzuki-Miyaura reactions in PEG-300 [J]. Tetrahedron Letters, 2010, 51(30): 3883-3885.
[11] Yamada Y M A, Maeda Y, Uozumi Y. Nnovel 3D coordination palladium- network complex: a highly active and recyclable catalyst [J]. Organic Letters, 2006, 8(19): 4259 -4262.
[12] Tang B-X, Fang X-N, Kuang R-Y, et al. Carrier-free and recyclable PdCl2-catalyzed Suzuki-Miyaura and Mizoroki-Heck reactions in water/ionic liquid media [J]. Chinese Journal of Organic Chemistry, 2017, 37(11): 2956-2961.
[13] Fu Q, Meng Y, Fang Z, et al. Boron nitride nanosheetnnchored Pd-Fe core-shell nanoparticles as highly efficient catalysts for suzuki-miyaura coupling reactions [J]. ACS Applied Materials & Interfaces, 2017, 9(3): 2469-2476.
[14] Park J C, Heo E, Kim A, et al. Extremely active Pd@pSiO2yolk-shell nanocatalysts for Suzuki coupling reactions of arylhalides [J]. The Journal of Physical Chemistry C, 2011, 115(32): 15772-15777.
[15] Baran N Y, Baran T, Mente A, et al. Highly effective and recoverable Pd ( II) catalyst immobilized on thermally stable Schiff base polymer containing phenol group: Production,characterization and application in suzuki coupling reactions [J]. Journal of Organometallic Chemistry, 2018, 866(1): 87-94.
[16] Korolev D N, Bumagin N A. Pd-EDTA as an efficient catalyst for Suzuki-Miyaura reactions in water [J]. Tetrahedron Letters, 2005, 46(34): 5751-5754.
[17] Clarke C J, Tu W-C, Levers O, et al. Green and sustainable solvents in chemical processes [J]. Chemical Reviews, 2018, 118(2): 747-800.
[18] Tang B-X, Fang X-N, Kuang R-Y, et al. Ligand-free PdCl2-catalyzed heck reaction of arylboronic acids and olefins under reusable TBAB/H2O conditions [J]. Synthesis, 2013, 45(21): 2971-2976.
[19] Tang B-X, Kuang R-Y, Wen J-W, et al. A carrier-free and recyclable protocol for the cross-coupling of terminal alkynes with arylboronic acids in H2O/TBAB [J]. Tetrahedron Letters, 2019, 60(30): 1975-1977.
LIGAND-FREE CROSS-COUPLING REACTIONS OF ARYL HALIDES WITH ARYLBORONIC ACIDS IN PEG-400/H2O
KUANG Ren-yun1,2, ZHANG Zhen-xing1, HUANG Xiang1, SHEN Yu-jun1, ZOU Hong1, XIE Bao-xin1,*TANG Bo-xiao1,2
(1. School of Chemistry and Chemical Engineering, Ji’an,Jiangxi 343009, China; 2. The key Laboratory of Coordination Chemistry of Jiangxi Province, and Institute of Applied Chemistry, Jinggangshan University, Ji’an, Jiangxi 343009, China)
Using PEG-400/H2O as the reaction medium and Pd(OAc)2as the catalyst, a series of biphenyl compounds (3a~3h) were synthesized by the cross-coupling reactions of aryl halides with arylboronic acids under ligand-free conditions. The structures were characterized by1H NMR and13C NMR, and the yield of the cross-coupling were 30%~99%. PEG/H2O as reaction solvent can reduce environmental pollution and realize green coupling reaction.
PEG/H2O; ligand-free; Suzuki-Miyaura coupling; green chemistry
1674-8085(2020)01-00025-05
O645.11
A
10.3969/j.issn.1674-8085.2020.01.006
2019-09-12;
2019-11-27
国家自然科学基金项目(21563015);江西省教育厅科技计划项目(GJJ170656);国家级大学生创新创业训练计划项目(201910419008)
匡仁云(1974-),男,江西吉安人,高级实验师,硕士,主要从事有机合成方法学的研究 (E-mail: kuagrenyun@163.com);
张振兴(1998-),男,江西鹰潭人,井冈山大学化学化工学院化学工程与工艺专业2016级本科生(E-mail:1258405442@qq.com);
黄 翔(1998-),男,江西萍乡人,井冈山大学化学化工学院材料化学专业2016级本科生(E-mail:1203574208@qq.com);
沈玉君(1998-),女,福建诏安人,井冈山大学化学化工学院应用化学专业2016级本科生(E-mail:1305691795@qq.com);
邹 红(1998-),女,江西吉安人,井冈山大学化学化工学院化学(师范)2017级本科生(E-mail:1409055828@qq.com);
谢宝星(1998-),男,江西赣州人,井冈山大学化学化工学院化学(师范)专业2017级本科生(E-mail:892374607@qq.com);
*唐伯孝(1975-),男,湖南邵阳人,副教授,博士,主要从事绿色偶联反应的研究(E-mail:520tangboxiao@163.com).
