用LC-MS 法测定人血浆中顺式阿曲库铵的浓度
2020-04-13万丽丽刘金变上海交通大学附属第六人民医院药剂科麻醉科上海200233
辛 博,万丽丽,王 婧,刘金变,霍 炎,郭 澄 (上海交通大学附属第六人民医院:.药剂科, .麻醉科,上海 200233)
顺式阿曲库铵(cisatracurium, CA)是一种新型中时效非去极化肌松药,其结构式如图1,因其代谢方式(Hofmann elimination,霍夫曼降解)独特,同时释放较低水平的组胺,在临床麻醉过程中被广泛应用。因与其他非去极化肌松药一样,存在术后肌松残留作用[1],且已成为麻醉后呼吸系统不良事件的主要原因。因此,为保证患者围术期安全,对顺式阿曲库铵进行血药浓度监测十分必要。
CA 的稳定性主要受温度和pH 影响,温度和pH 升高可加快其消除,因此离体后的生物样本稳定性是血药浓度监测方法建立的一个难点。国内外文献报道测定人血浆中CA 浓度的方法主要为高效液相色谱荧光检测法(HPLC-FD)及高效液相色谱串联质谱法(LC-MS)[2-6],但样本前处理方法较为复杂。本研究在既往文献报道的基础上,建立了一种更加简便、准确、快速、稳定的LC-MS 方法,适用于人血浆中CA 的血药浓度测定。
1 仪器与试药
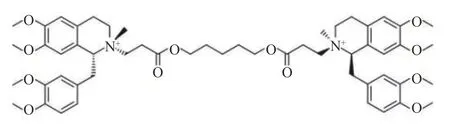
图 1 顺式阿曲库铵的结构式
高效液相色谱仪(Agilent 6410,美国Agilent 公司);Triple Quad 三重四极杆质谱仪,配电喷雾(ESI)离子源(美国Agilent 公司);纯水机(Millipore);分析天平(BP211D,德国Sartorius 公司)。对照品顺式阿曲库铵(cisatracurium,CA,批号:C496700,纯 度 90%,Toronto Reasearch Chemicals Inc 公司);对照品盐酸普罗帕酮(propafenone hydrochloride,PPF,批 号:101190-201101,纯度99.9%,中国药品食品检定研究院);乙腈、甲酸均为质谱纯(美国TEDIA 公司);水为自制超纯水。
2 方法与结果
2.1 分析条件
2.1.1 色谱条件
Agilent SB-C18色谱柱(2.1 mm×50 mm, 3 μm),柱温35 ℃;流动相A 为0.1%甲酸水溶液,B 为0.1%甲酸乙腈溶液。线性梯度洗脱:0 ~1 min,20% B;1~3 min,50% B;3 ~5 min,20% B; 5 ~10 min,20% B。流速0.3 ml/min;进样量2 μl。
2.1.2 质谱条件
采用正离子工作模式;离子源为ESI 源;多反应监测(multiple reaction monitoring, MRM)。毛细管电压4 000 V;干燥器温度350 ℃;干燥气流速12 L/min;雾化器压力35 psi。MRM 监测离子对,离子驻留时间、碰撞诱导解离电压及碰撞能量等参数见表1。典型质谱图见图2。

表 1 质谱条件

图 2 HPLC-MS 色谱图
2.2 对照品及内标溶液配制
CA 标准储备液:精密称取CA 10 mg 置10 ml容量瓶,加入2%甲酸甲醇溶液至刻度,溶解混匀,配制成相当于CA 质量浓度为1 mg/ml 的储备液,于冰箱(4 ℃)备用。
CA 标准工作液:精密吸取CA 储备液适量,用50%甲醇水溶液配制成系列浓度的工作溶液,其中,CA 质量浓度分别为5 000、2 500、1 000、500、250、100、20 ng/ml。
PPF 标准储备液:精密称取PPF 0.4 mg 置2 ml容量瓶,加甲醇至刻度,溶解混匀,配制成相当于PPF质量浓度为0.2 mg/ml 的储备液,于冰箱(4 ℃)备用。
PPF 标准工作液:精密吸取PPF 储备液适量,配制成200 ng/ml 的含内标乙腈溶液。
2.3 血浆样品处理
精密吸取血浆30 μl,加入2%甲酸水溶液30 μl,振摇10 s,再加50 μl 含内标乙腈溶液后旋涡振荡10 s,12 000 r/ min 离心10 min,转移上清液置进样瓶,进样。
2.4 标准曲线及最低定量限
取空白人血浆,精密加入不同浓度的对照品溶液,配制成CA 浓度为500、250、100、50、25、10、2 ng/ml 的血浆标准品。以浓度为X 轴,样品峰与内标峰的比值为Y 轴,进行线性回归,经“1/X”权重得回归方程分别为:Y = 7.43×10-3+ 1.99 × 10-2X(r = 0.996 5)。结果表明,CA 在2~500 ng/ml 内,线性关系良好。本方法CA 的定量下限为2 ng/ml。
2.5 系统精密度与准确度(回收率)
配制CA 浓度分别为8、80、400 ng/ml 的血浆样品,日内误差以3 个浓度各5 个样品的测定结果表示;日间误差以3 个浓度样品分别3 个批次结果表示。人空白血浆分别加入不同浓度CA 工作溶液,按照“2.3”项下方法提取后,相同色谱条件进行浓度测定。同时测定用流动相稀释为相应浓度的无基质溶液的峰面积,以计算绝对回收率。结果如表2 所示。
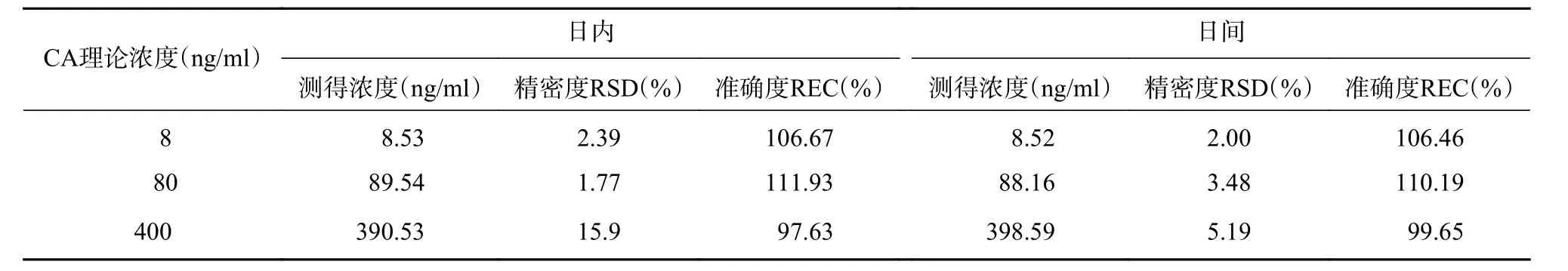
表 2 CA 人血浆样品的系统精密度与准确度(回收率)
2.6 稳定性试验
空白血浆分别配制成8、80、400 ng/ml 的样品,每批次各3 个,分别考察其①室温下放置4 h;②处理后室温放置24 h;③-80 ℃放置14 d 的稳定性。结果如表3 所示。
2.7 基质效应
取6 个不同来源的人空白血浆30 μl,除不加内标外,其余按“2.3”项下操作,取上清液,分别制备成CA 浓度为31.25 和1 000 ng/ml;PPF 浓度为200 ng/ml 的溶液,进样测定,记录峰面积。另用流动相将CA 稀释成31.25 和1 000 ng/ml;PPF 浓度为200 ng/ml 浓度的溶液,进样测定,记录峰面积。
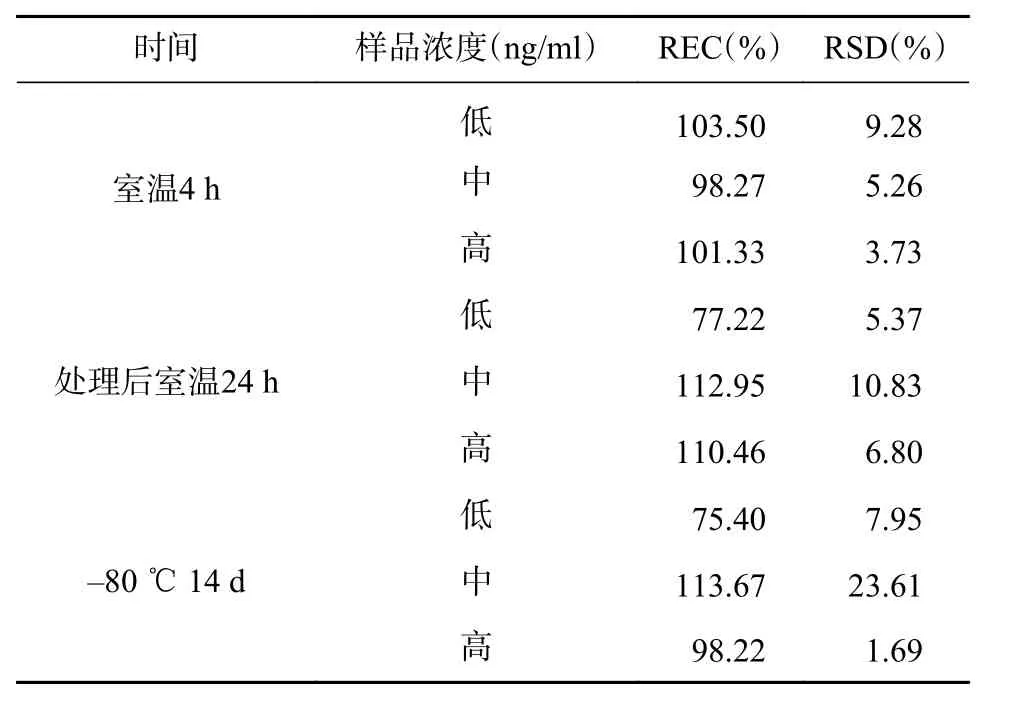
表 3 CA 人血浆样品不同条件下的稳定性
基质效应=(空白基质中添加工作溶液峰面积/重组溶液中添加工作溶液峰面积)×100%
CA 的基质效应为52%(RSD 2.09%~15.33%)。PPF 的基质效应为96.71%(RSD4.6%)。
2.8 方法在治疗药物监测中的应用
采用肌松仪监测患者注射苯磺顺式阿曲库铵后神经肌肉阻滞程度。给予4 个成串刺激(train of four stimulation,TOF),给药后,T4 最先发生衰减,T1 最后衰减。当T1 消失即仪器显示为0 时,肌肉阻滞程度最大,随后逐渐恢复。分别在T0(T1 消失至0)、TOFr 50(恢复至50%)、TOFr 90(恢复至90%)时采集输液对侧动脉血3 ml,并及时保存于4 ℃冰箱中。采用建立的方法测定样本血药浓度,结果见表4。同时记录T0(给药结束到T1 消失至0)、TOFr50(给药结束到恢复至50%)、TOFr90(给药结束到恢复至90%)发生所需时间,结果见表5、表6。
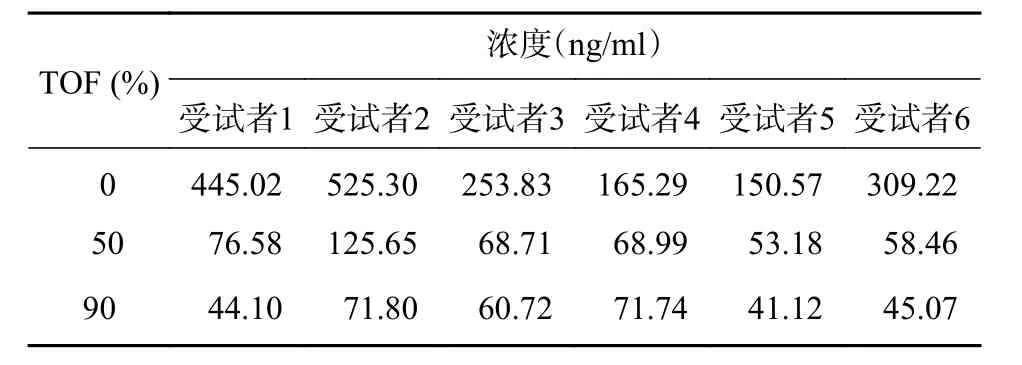
表 4 6 例受试者血浆中CA 血药浓度测定结果

表 5 6 例受试者临床资料

表 6 6 例受试者达到各TOF 值的时间
3 讨论
CA 的代谢途径主要为Hoffman 消除[7],Hoffman消除受温度和pH 值的影响。有研究显示[8],将苯磺顺阿曲库铵注射液稀释于20%的甲醇中,室温下,10~15 min 即可检测到大量降解产物N-甲基四氢罂粟碱和单季丙烯酸酯。血浆的pH 值在7.4 左右。我们发现,在CA 血浆样本前处理过程中,如果不加入酸调节pH 值,即使在-80 ℃的储存条件下,CA 仍然会很快降解(结果未在文中体现)。为此,我们考察了不同比例的甲酸,最终确定了在样本前处理过程中加入2%的甲酸能够保证血浆中CA 的稳定性。在既往报道中,多是加入一定浓度的硫酸来调控pH 值[2-6]。硫酸为有机酸,对测定仪器尤其是质谱仪的离子源损害很大。同时,加入硫酸并不能保证室温条件下样本的长时间稳定(<4 h)[9]。本研究结果显示,加入2%的甲酸,室温下样本稳定性可保持在24 h 以上。此外,我们的样本前处理过程并不需要经过离心-上清液真空浓缩或氮吹浓缩-复溶-离心取上清液等[2-6,9]复杂过程,更为省时、省力。经验证,本研究建立的方法测定CA 血浆样本的精密度、准确度和稳定性均符合方法学要求。该方法更加简便、准确、快速、稳定,可应用于临床CA 治疗药物浓度的监测。
