CalliSpheres 载药微球联合碘化油治疗大肝癌14 例
2020-04-11徐燕能张向琼马小燕斯光晏
张 训,徐燕能,张向琼,胡 伟,袁 罡,马小燕,斯光晏
原发性肝癌(PLC)是全球最常见的恶性肿瘤之一,中国是高发地区之一,全球每年新增的肝癌患者中约50%为中国人[1]。手术切除、消融治疗、肝移植是早期肝癌的一线治疗方法,且提供了治愈的可能[2]。但对于中晚期肝癌,特别是体积较大的肝癌,往往恶性程度高、并发症多,发现时多已失去了手术切除的机会, TACE 疗效确切,现已成为不能手术切除的PLC 的首选治疗方法[3-4]。随着新型载药微球CalliSpheres 在临床上的逐步推广使用,近期有多项研究指出,应用CalliSpheres 载药微球行TACE(DEB-TACE)治疗PLC 较传统TACE(cTACE)有更高的肿瘤反应率和更好的安全性[5-6]。但载药微球价格昂贵,单用载药微球治疗体积较大的肝癌往往需要多瓶载药微球才能达到栓塞终点,单次DEB-TACE 治疗的经济成本相对较高。刘金等[7]尝试将载药微球与碘化油联合使用治疗肝癌并取得了较好的疗效。本研究以临床上常见的大肝癌患者为研究对象,旨在探讨CalliSpheres 载药微球联合碘化油治疗大肝癌的近期疗效和安全性。
1 材料与方法
1.1 临床资料
选取2017 年7 月至2018 年6 月我院收治的14 例大肝癌患者,所有病例均符合《原发性肝癌诊疗规范(2017 年版)》诊断标准,经病理组织学或临床诊断为原发性肝癌。其中男12 例,女2 例,年龄38 ~79 岁,中位年龄53 岁。患者术前均签署手术知情同意书,术前基本资料见表1。
1.1.1 纳入标准 ①患者不能或不愿意接受外科手术切除治疗,5 cm <肿瘤直径≤10 cm,且占肝脏体积的70%以下;②巴塞罗那分期为B 期、C 期患者;③肝功能Child-Pugh 分级为A 级或B 级;④不伴有其他影响生存期的严重疾病且预计生存期>3 个月⑤ECOG 评分≤2 分。
1.1.2 排除标准 ①恶病质或全身多脏器功能衰竭患者;②严重肝功能不全,Child-PughC 级;③难以纠正的凝血功能损害;④存在肝动脉-门静脉瘘(或肝动脉-肝静脉瘘)⑤门静脉主干完全阻塞且无侧支循环形成;⑥合并不能控制的严重感染;⑦肾功能障碍:肌酐>176.8 μmol/L 或者肌酐清除率<30 mL/min。

表1 患者基础资料
1.2 方法
1.2.1 手术操作 采用Seldinger 技术穿刺右侧股动脉成功后,首先插入5 F-RH 导管进行腹腔干动脉及其他肿瘤供血动脉造影以评估肿瘤供血特点、门静脉通畅情况以及是否存在动静脉瘘,然后超选择插入2.7 F 微导管至肿瘤供血动脉内。先用碘化油乳剂(碘化油与阿霉素水溶液按体积2∶1 比例配制)缓慢注入肿瘤靶血管内,见血流减慢后脉冲式注入粒径为100~300 μm 的CalliSpheres 载药微球(1 瓶载药微球加载60~80 mg 阿霉素),注射速度1~2 mL/min。碘化油单次用量不超过20 mL,阿霉素剂量根据患者体表面积和肿瘤大小换算。栓塞终点为肿瘤实质染色消失,微导管尖端对比剂滞留或供血动脉主干呈“干树枝”状,等待5 min 后再次造影,如肿瘤实质染色仍可见则追加同样大小的空白微球(8 Spheres)栓塞,直至靶血管血流中断或肿瘤染色完全消失。
1.2.2 术后处理 围手术期对伴有HBsAg 阳性患者给予抗病毒治疗,患者介入术后常规给予保肝、止吐、镇痛等支持治疗,酌情予抗感染治疗,针对术后出现的常见不良反应(疼痛、发热、恶心、呕吐等)予以对症处理。记录患者术后的不良反应及其它并发症(肝肾功能衰竭、肝脓肿、胆汁瘤、肝破裂、消化道出血、骨髓抑制等)的发生情况。
1.2.3 随访 术后7 d、1 个月复查肝功能(AST、ALT、ALB、TBIL)和AFP 并与术前比较,术后1、3和6 个月复查腹部增强CT(或MRI),采用改良实体瘤疗效评价标准(mRECIST)对肿瘤病灶进行评价,具体分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD),根据CR+PR 计算疾病缓解率,根据CR+PR+SD 计算疾病控制率。根据肿瘤复查结果并结合患者全身状况决定是否再次行TACE 治疗或联合其他标准治疗以及下次随访间隔时间。
1.3 统计学分析
采用SPSS17.0 统计学软件进行数据分析。计量资料采用±s 表示,术前、术后肝功能指标及AFP 比较采用配对t 检验或Wilcoxon 符号秩检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 技术资料
本组14 例患者均成功接受CalliSpheres 载药微球联合碘化油TACE 治疗,技术成功率100%。碘化油的平均用量为(12.21±4.17)mL,载药微球平均用量为(0.86±0.16)g,其中11 例患者使用不超过1 瓶载药微球即达到栓塞终点,3 例患者使用1 瓶载药微球后未能达到栓塞终点,后加用同样大小的空白微球行补充栓塞治疗。从患者第1 次TACE 手术后随访至少6 个月以上,末次随访时间2018 年12 月31 日,随访期间有2 例患者术后肿瘤复发,其中1 例患者术后6 个月随访时肝内新发2枚病灶,另1 例患者术后肿瘤全身多处转移(肝内、肺、腰椎),在术后8 个月时因多脏器功能衰竭死亡,13 例患者生存。
2.2 临床疗效
采用mRECIST 标准对患者术后的影像资料进行评价,14 例患者术后疾病缓解率和控制率见表2。

表2 患者术后疗效评价(mRECIST 标准) 例数(%)
2.3 治疗前后肝功能及AFP 变化
14 例患者术后7 d、术后1 个月AFP 均有不同程度下降,术后1 个月的AFP 值与术前比较差异具有统计学意义(P <0.05),其中有3 例术前AFP >200 μg/L 在术后1 个月时AFP 已恢复正常。术后7 d 患者ALT、AST 及总胆红素(TBIL)明显升高,白蛋白(ALB)有所下降,ALT、TBIL、ALB 与术前比较差异有统计学意义(P <0.05),但AST 与术前比较差异无统计学意义(P>0.05)。术后1 个月时,ALT、AST、TBIL、ALB 基本恢复至术前基线水平,与术前比较差异无统计学意义(P >0.05)(详见表3)。
2.4 术后不良反应及并发症发生情况
患者术后生命体征均平稳,术后不良反应主要有轻度腹痛8 例(57.1%)、低热4 例(28.6%)、恶心6 例(42.9%)、呕吐5 例(35.7%),持续时间约1 周左右,经对症处理后均得到缓解。术后均未出现肝功能衰竭、胆囊及胃肠道穿孔、消化道大出血、肝脓肿、肝癌破裂出血、骨髓抑制等严重并发症。患者术后影像改变见图1、2。
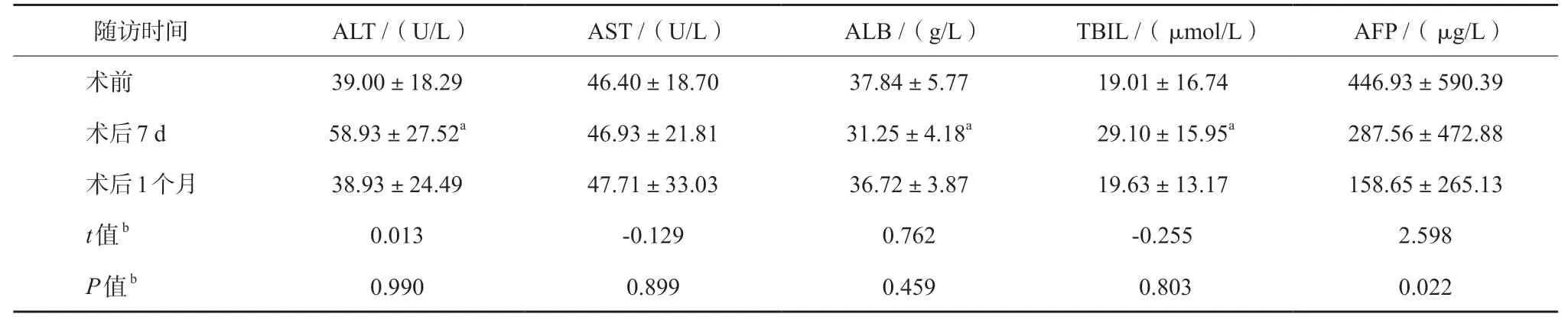
表3 患者术前与术后相关临床资料比较 x±s
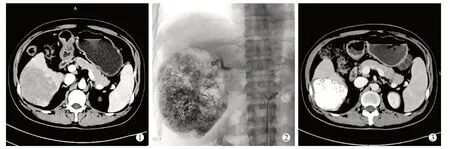
图1 典型病例增强CT 及术中造影影像
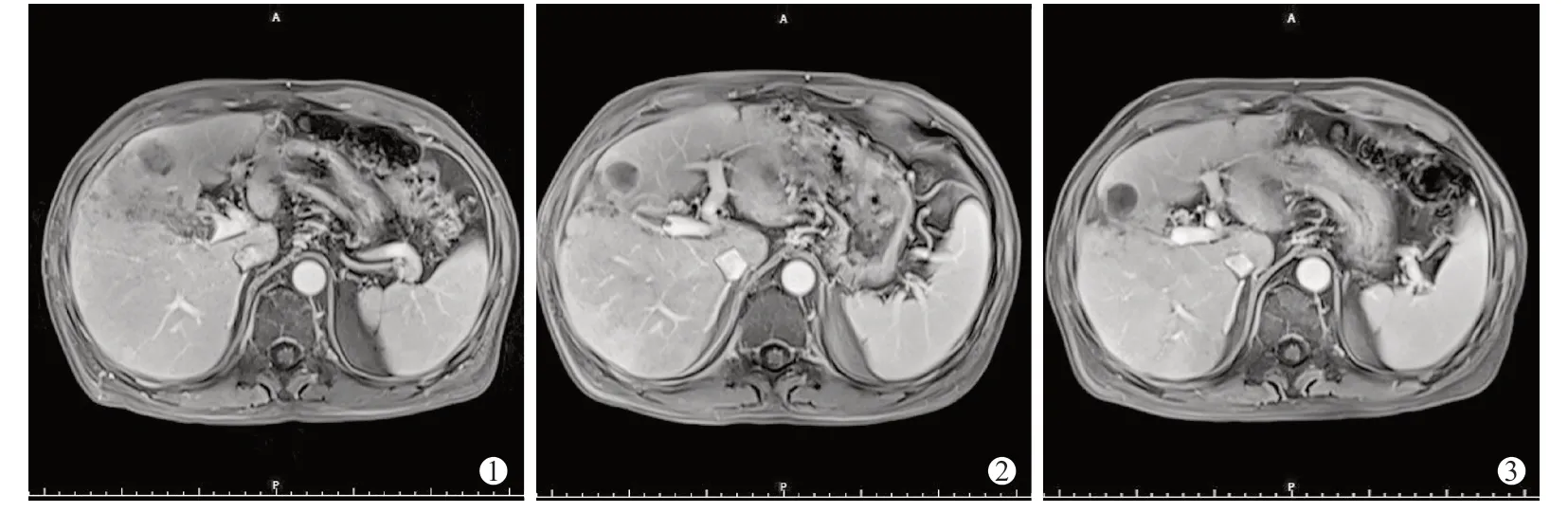
图2 门脉癌栓患者术前术后增强MRI 随访影像
3 讨论
PLC 是我国最常见的恶性肿瘤之一。TACE 技术发展至今已有近40 年历史,现已成为不能切除中晚期肝癌的一线治疗方法,但由于TACE 不是一个规范化治疗方案,目前对于最佳患者的选择、栓塞剂以及化疗药物的选择、治疗的时机以及次数国内外尚无统一标准[8]。
在栓塞材料中,传统的液体栓塞剂以碘化油最为经典,碘化油单独使用或联合明胶海绵颗粒是目前cTACE 最常用的栓塞材料。但碘化油栓塞时效相对较短,沉积后短期内易被血流冲刷,明胶海绵也具有可降解的特性,TACE 术后短期内肿瘤靶血管易再通、肿瘤易复发[9]。在载药微球出现之前,曾尝试使用微球(空白微球)联合碘化油行TACE 治疗中晚期肝癌并取得了较好的效果。徐彦哲等[10]一项meta 分析发现微球联合碘化油治疗肝癌可以显著提高疾病控制率,近期疗效优于单独使用碘化油。本研究应用的CalliSpheres 载药微球在空白微球的基础上可吸附多种化疗药物并在局部缓慢释放,能同时发挥永久性栓塞和局部化疗的双重作用,增加抗肿瘤效应的同时可减少全身不良反应[11-12]。徐文杰等[13]对60 例肝癌患者随机分组研究发现,应用CalliSpheres 载药微球联合碘化油行TACE 术与传统TACE 术(碘化油联合明胶海绵)近期疗效相当,但能明显减少术后不良反应发生率。
本研究的结果表明,使用CalliSpheres 载药微球联合碘化油对大肝癌行化疗栓塞,术后1、3 和6 个月的疾病缓解率分别为85.7%、78.6%、64.3%,疾病控制率分别为92.9%、92.9%、78.6%,与Wu 等[6]单用CalliSpheres 行DEB-TACE 得 出 的3、6 个 月 疾病缓解率83.3%、62.5%,疾病控制率91.7%、83.3%和Golfieri 等[14]单用DC-Beads 行DEB-TACE 得出的1、3 个月疾病缓解率89.9%、74.7%,疾病控制率93.3%、79.7%基本相仿。本研究中患者术后7 d、术后1 个月复查AFP 较术前都有不同程度下降,也证明了治疗的有效性。肝功能指标方面,患者术后7 d的ALT、AST 及TBIL 较术前有轻度升高,ALB 较术前有所下降,但在术后1 个月时都已基本恢复至术前基线水平,与Wu 等[6]报道基本一致。虽然大多数患者在术后出现了轻度栓塞后综合征,主要表现为轻度腹痛、低热、恶心、呕吐,但经对症处理后均在1 周内得到缓解,术后均未出现急性肝功能衰竭、胆囊及胃肠道穿孔、消化道大出血、肝脓肿、肝癌破裂出血、骨髓抑制等严重并发症,说明只要注意术中超选择插管以及避免误栓胆囊动脉,使用载药微球联合碘化油治疗大肝癌是安全的。
体积较大的肝癌组织往往血供丰富,供血动脉迂曲、增粗,且常有多支血管参与供血,若单用载药微球行DEB-TACE 治疗,往往需要不止一瓶载药微球才能达到栓塞终点;若单用碘化油行cTACE 治疗,术中碘化油的用量也较大。载药微球价格昂贵,特别是对于经济欠发达的西部地区患者而言,往往难以承受多瓶载药微球带来的经济负担;虽然碘化油价格相对便宜,但过量使用碘化油会产生威胁生命的严重不良事件[15]。本研究使用CalliSpheres载药微球联合碘化油治疗大肝癌,术中碘化油平均用量(12.21±4.17) mL,载药微球平均用量(0.86±0.16) g(均只使用1 瓶载药微球),两者联合使用可明显减少单独使用的剂量。有研究表明,肝脏肿瘤组织微血管直径约为7~400 μm,碘化油具有肝癌细胞的亲和性,能栓塞直径约为40~70 μm的肿瘤末梢动脉和血管床[16-17]。本研究选用的粒径100~300 μm 载药微球不易进入正常肝脏终末小动脉(内径为20~50 μm)及肝窦(宽为7~15 μm)内,可避免异位栓塞加重肝脏损害。本研究中先用碘化油栓塞,可较准确地判断肿瘤分布范围,发现一般影像检查难以发现的小病灶,后用载药微球逐级栓塞肿瘤血管,可弥补碘化油栓塞不彻底的缺点,同时发挥载药微球缓慢释放化疗药物的优点,明显延长化疗药物对肿瘤的作用时间。两者联合使用,能达到更加彻底、持久的化疗栓塞。且栓塞剂直径越小对PVTT 的栓塞效果更好[18-19]。本研究中3 例患者术前肿瘤侵犯门静脉分支,按程氏分型PVTT Ⅰ型2 例、Ⅱ型1 例,肝功能Child-Pugh A 级2 例,B级(7 分)1 例,术后有2 例出现轻度腹部疼痛,1 例发热(38.1℃),经对症治疗后3~5 d 症状消失,未出现肝功能衰竭等严重并发症。术后影像随访时可见门静脉癌栓内有部分碘油沉积,2 例患者术后3个月复查时见癌栓体积缩小,其中1 例术后6 个月复查时见癌栓消失,门静脉右支恢复通畅。说明载药微球联合碘化油对伴有门静脉癌栓的大肝癌治疗有效,碘化油能发挥其亲肿瘤的特点更易进入供血动脉细小的癌栓组织中,加上载药微球协同栓塞,可使栓塞更加彻底,从而延缓肿瘤进展,改善预后。由于本研究仅纳入了PVTT Ⅰ型及Ⅱ型患者,且Ⅱ型患者的门静脉右支并未完全阻塞,虽然术后并未发生严重肝功能损伤,但可能与肿瘤侵犯门静脉较轻、术前肝功能储备良好等有关,所以载药微球联合碘化油行TACE 治疗大肝癌合并门静脉癌栓的疗效及安全性尚需进一步大规模研究证实。
综上所述,CalliSpheres 载药微球联合碘化油治疗大肝癌有良好的近期疗效,安全可行,在达到与DEB-TACE 相似效果的同时能减少载药微球剂量,从而减轻患者经济负担,值得临床推广。本研究也存在一些不足之处:属于回顾性分析,且纳入病例较少、随访时间不长等。CalliSpheres 载药微球联合碘化油治疗大肝癌的远期疗效也尚待临床多中心、大样本的进一步研究。
