层状复合金属氧化物臭氧催化剂的制备及其对苯胺废水降解的动力学研究
2020-04-10张延青王长治齐元峰
张延青 郭 策 王长治 齐元峰,
(1.青岛理工大学 环境与市政工程学院,山东 青岛 266033; 2.浙江省环境保护科学设计研究院,浙江 杭州 310007)
0 引言
苯胺(Aniline,C6H7N),呈弱碱性无色或淡黄色的油状液体,被广泛应用于染料制作、医药制造、橡胶硫化生产、军事工业等方面[1].苯胺对环境和人体健康都能造成严重的危害,其可以通过皮肤、呼吸道和消化系统进入人体,长期接触苯胺可使人食欲下降、贫血、体重减轻、神经系统受到影响[2].苯胺排放到水体中,通常会扰乱水环境,造成严重的水体污染,甚至会造成水生动植物的死亡.由于苯胺具有很强的生物毒性并且可以在环境大量累积,同时对人体具有“致癌、致畸、致突变”的作用[3,4],越来越多的国家和地区已经对苯胺的释放量提出了严格的限制[5,6].因此,如何减少含苯胺的废水排放,减轻乃至消除苯胺废水对环境的污染,已广泛引起社会的关注.
层状复合金属氢氧化物 (Layered Double Hydroxide,LDH) 是一类具有层状结构合成类粘土材料[7,8],LDH一般由两种或两种以上的金属阳离子形成主体层板,由阴离子通过非共价键实现板层的结合,其化学组成通式[9-11]
(1)
其中M2+表示二价金属阳离子如Mg2+、Ni2+、Co2+、Zn2+、Cu2+等;M3+表示三价金属阳离子如Al3+、Cr3+、Fe3+、Sc3+等;An-表示可形成共价键的层间阴离子如CO32-、NO3-、Cl-、OH-、SO42-等;m为层间结合的水分子个数.当二价金属离子与三价金属离子摩尔比介于2-4之间(即x值在0.17-0.33之间)时能得到结构稳定的LDH[12].
在一定焙烧温度下,LDH内部的结合水及氢氧根会发生层内脱水的现象,从而进一步形成层状复合金属氧化物(Layered Double Oxide,LDO)[13].LDO是一种具有活性位分布均匀、晶粒小、比表面积大、稳定性较好的层状金属氧化物材料[14].近年来,其优异的催化活性在污水处理[15]领域受到极大的关注.
Gustavo等[16]采用共沉淀法制备LDH前驱体,后煅烧负载制备Nb-LDO催化剂,用以光催化氧化苯胺转化偶氮苯衍生物,转化率可达到98%;Sui等[17]采用共沉淀法制备Co/Mn/Al-LDH用以催化臭氧降解水中的硝基苯,发现Co/Mn/Al-LDH催化剂表现出较高的催化活性;Kaoutar等[18]采用共沉淀法制备镍基LDH用以催化臭氧降解染料废水中的甲基橙,发现反应1 h后,COD去除率可达到72%,比单纯臭氧氧化降解提高58%.
LDH以及在此基础上制备的LDO催化剂,在催化降解氧化含氮芳香烃体现了极强的催化活性,然而以LDO作为臭氧催化剂催化降解苯胺的报道并不多见;其次,在目前的报道中,采用共沉淀法制备LDH是一种简洁高效的方式,然而对于制备过程中使用正向/反向共沉淀法对比的研究报道比较罕见.因此,制备性能优异的LDO催化剂催化臭氧氧化苯胺废水,对减轻乃至消除苯胺废水对环境的影响很有意义.为此,本研究以Fe2+、Co2+、Mn2+作为二价金属阳离子来源,以Fe3+、Al3+为三价金属阳离子来源制备用于苯胺降解的LDO臭氧催化剂,考察制备原料的选择等因素对LDO臭氧催化剂催化性能的影响,以及对比通过正向共沉淀法和反向共沉淀法制备的催化剂催化性能的差异,并进一步对臭氧催化氧化苯胺的反应动力学进行分析.
1 实验
1.1 原料及仪器
实验过程中使用的药剂主要有:六水硝酸钴(Co(NO3)2·6H2O)、六水硝酸锰(Mn(NO3)2·6H2O)、九水硝酸铁(Fe(NO3)3·9H2O)、九水硝酸铝(Al(NO3)3·9H2O)、七水硫酸亚铁(FeSO4·7H2O)、氢氧化钠(NaOH)、无水碳酸钠(Na2CO3)、硝酸(HNO3)、苯胺(C6H7N)、碘化钾(KI),药剂均为分析纯,购买于上海麦克林生化科技有限公司.所用的氧气购自浙江长兴京兴燃气有限公司,纯度99.9%.
测试使用的仪器有:臭氧采用CF-10F型臭氧发生器(北京沃雪阳光科技有限公司,最大臭氧产量10 g/h);CODCr测试采用5B-3C型消解-紫外光分光光度计(北京连华永兴科技有限公司,测试范围 50-1500 mg/L,精度0.1 mg/L)进行测试:每次测试水样体积为2.5 mL,加入0.7 mL重铬酸钾(K2Cr2O7)溶液和4.8 mL H2SO4-Ag2SO4溶液,均匀混合后放置于165 ℃消解槽内反应10 min后测试溶液的吸光度转化为CODCr的浓度;总有机碳TOC在TOC-2000型总有机碳分析仪(上海元析仪器有限公司,测试范围 0-500 mg/L,精度0.01 mg/L)测试,反应温度800 ℃,载气量180 mL/min,根据所测试样吸收峰峰高,由校正曲线回归方程算得总碳(TC)和总无机碳(TIC),总有机碳(TOC)浓度=总碳(TC)-总无机碳(TIC);SEM测试采用场发射扫描电子显微镜(MIRA3,泰思肯(中国)有限公司)对LDO的形貌进行观察.
1.2 LDO臭氧催化剂的制备
LDO是以LDH前驱体煅烧制备而来,参照文献[17,19,20]制备条件,本次LDO臭氧催化剂的制备分为四个步骤:(1) 在初始pH=7的去离子水中,以一种二价金属离子(Co2+、Mn2+或Fe2+)和三价金属离子(Fe3+或Al3+)按照特定摩尔比例配制混合金属盐溶液A(Solution-A),并保持溶液A的阳离子摩尔浓度为0.6 mol/L;配置包含1 mol/L NaOH和0.1 mol/L Na2CO3的混合碱溶液B(Solution-B);(2) 分别采用正向共沉淀法[21]和反向共沉淀法制备LDH前驱体.LDH前驱体的正向共沉淀制备流程为:在特定温度的恒温水浴锅中,在Solution-A中缓慢滴加Solution-B并剧烈搅拌直至特定pH,停止搅拌陈化24 h;LDH前驱体的反向共沉淀制备流程为:在特定温度的恒温水浴锅中,在Solution-B中缓慢滴加Solution-A并剧烈搅拌,整个过程中采用NaOH溶液保持pH不变,随后停止搅拌并陈化24 h;(3) 将陈化后的LDH前驱体分离并用去离子水冲洗至pH=7,随后在105 ℃恒温干燥箱中干燥2 h;(4)最后将LDH前驱体在500 ℃氮气保护的马弗炉中煅烧2 h,冷却至室温后粉碎至100目.
1.3 苯胺废水及臭氧催化反应装置
苯胺模拟废水中苯胺浓度为400 mg/L,并采用1 mol/L的NaOH和1 mol/L的HNO3共同调节苯胺废水初始pH为8.0±0.1.配置好的苯胺废水放置于棕色瓶中保存.臭氧催化降解苯胺废水的反应装置为自行制作,具体组成如图1所示.
臭氧发生器以氧气罐存储的氧气作为臭氧来源,通过减压阀和气体流量计控制臭氧产量;封闭反应器(共3个)由1000 mL锥形瓶改造而成,通过硅胶管将臭氧与封闭式反应器内的碳化硅曝气头(孔径10 nm)连接以实现臭氧在废水中均匀扩散;用磁力搅拌器强化废水、催化剂和臭氧的混合;反应后的废气通过硅胶管道与吸收瓶相连接,吸收瓶中的吸收液为 2.0%浓度的KI溶液.
在催化臭氧氧化苯胺试验中,分别在3个反应器内加入400 mL苯胺模拟废水和4 g LDO臭氧催化剂(即催化剂添加量为1 g/L),调节单个反应器臭氧流量为25 mg/min.并同步启动磁力搅拌器使LDO催化剂处于均匀悬浮状态.设置反应时间为1 h,反应后测定废水CODCr和TOC去除率,每个样品取两次有效测试结果的平均值,有效测定结果判定方式为:若两次数据误差超过3%,则进行第三次测定并取平均值.
2 结果与讨论
2.1 LDH前驱体的最佳原料配比与制备条件选择
LDH作为LDO的前驱体,LDH的制备过程将直接影响LDO的性能.用于考察正向共沉淀制备LDH前驱体的原料选择和配比、终点pH与制备温度正交实验设计如表1所示,在此基础上制备的LDO催化臭氧降解苯胺废水的CODCr去除率作为相应的分析结果如图2所示.

表1 两次正向共沉淀法制备LDO催化剂1正交试验设计
注:1:LDO焙烧温度500 ℃,焙烧时间120 min,N2气氛;2:M2+=Fe2+、Co2+或Mn2+;正交实验1:M3+=Fe3+;正交实验2:M3+=Al3+.
从图2中可以看出,影响LDO催化剂催化臭氧去除苯胺废水CODCr的主要因素为LDH前驱体制备原料,以二价钴离子为制备原料的LDO催化剂去除效果明显好于其他两种金属离子.分析原因,LDH前驱体经过焙烧后得到LDO,不同金属氧化物催化剂对臭氧的催化分解活性差异很大,复合金属氧化物催化剂的催化分解活性主要由较高活性的金属氧化物所决定[22],并与复合金属氧化物的成分比例有关.其中金属氧化物对臭氧的催化分解活性[23]Co>Mn>Fe,以钴为原料制备LDO催化剂具有较高的臭氧催化活性,加快臭氧氧化的效率;同时Co/Al-LDO催化剂双金属之间的协同作用略优于其余LDO催化剂,促进了对臭氧的催化分解.
LDO制备过程中原料摩尔比例、制备温度和pH均对催化臭氧氧化苯胺废水CODCr的去除有一定的影响.当二价金属离子与三价金属离子的摩尔比例在2-4之间时,可以制备出结构比较完整的LDO催化剂[20,24,25];制备温度和pH影响LDO的结晶度和热稳定性[19,26-28],相对合适的温度和pH可以得到稳定的LDO结构.因此,铁基LDO催化剂最佳制备条件为:选用钴铁为原料,Co2+∶Fe3+摩尔比例3∶1,制备温度60 ℃,制备pH 10;铝基LDO催化剂最佳制备条件为:选用钴铝为原料,Co2+∶Al3+摩尔比例3∶1,制备温度60 ℃,制备pH 10.
2.2 正向沉淀和反向沉淀制备效果比对
从图3中可以看出,正向共沉淀法制备的Co/Fe-LDO催化剂CODCr去除率可达到65.72%,TOC去除率可达到38.22%;反向共沉淀法制备的Co/Fe-LDO催化剂CODCr去除率可达到66.93%,TOC去除率可达到38.78%;正向共沉淀法制备的Co/Al-LDO催化剂CODCr去除率可达到67.6%,TOC去除率可达到39.02%;反向共沉淀法制备的Co/Al-LDO催化剂CODCr去除率可达到69.3%,TOC去除率可达到39.92%.反向共沉淀法制备的LDO催化剂相较于正向共沉淀法制备的LDO催化剂,对催化臭氧氧化苯胺废水CODCr和TOC的去除效果更加明显.
在LDH前驱体制备过程中,存在如式(2)-(4)[29-31]沉淀反应过程
Al(OH)3⟺Al3++3OH-Ksp(Al(OH)3)=(Al3+)(OH-)3=1.3×10-33,
(2)
Fe(OH)3⟺Fe3++3OH-Ksp(Fe(OH)3)=(Fe3+)(OH-)3=4×10-38,
(3)
Co(OH)2⟺Co2++2OH-Ksp(Co(OH)2)=(Co2+)(OH-)2=1.6×10-15.
(4)
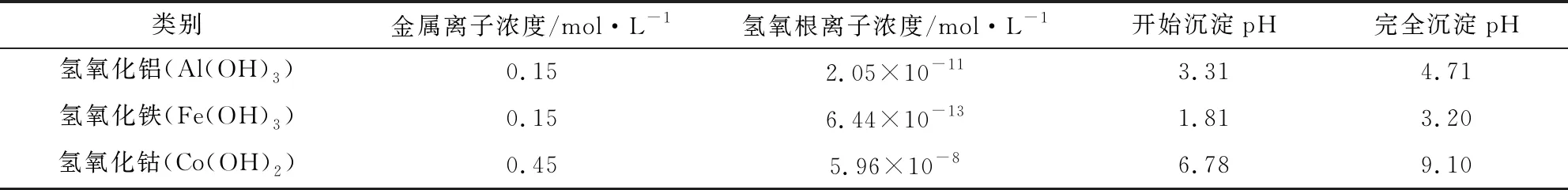
表2 催化剂制备过程沉淀物出现时溶液pH值
根据表2所示,对于Co/Fe-LDO臭氧催化剂,用正向共沉淀法制备时,随着碱混合液的滴加,溶液pH值升高,当pH>1.81时出现氢氧化铁(Fe(OH)3)沉淀,pH>3.2时溶液中Fe3+完全沉淀,而在pH>6.78时才开始出现氢氧化钴(Co(OH)2)沉淀,两种氢氧化物沉淀的形成有先后顺序,实际生成的Co/Fe-LDH和在此基础上制备的Co/Fe-LDO中二价金属离子与三价金属离子比例远大于3:1,层板状结构存在缺陷.而用反向共沉淀法制备时,溶液pH保持不变且远大于Co2+和Fe3+完全沉淀pH,钴铁复合金属氢氧化物同时生成,层板状结构完整且分布均匀.
同样,对于Co/Al-LDO臭氧催化剂,用正向共沉淀法制备时,随着碱混合液的滴加,溶液pH值升高,当pH>3.31时出现氢氧化铝(Al(OH)3)沉淀,pH>4.71时溶液中Al3+完全沉淀,而在pH>6.78时才开始出现氢氧化钴(Co(OH)2)沉淀,两种氢氧化物沉淀的形成有先后顺序,实际生成的Co/Al-LDH和在此基础上制备的Co/Al-LDO中二价金属离子与三价金属离子比例远大于3:1,层板状结构存在缺陷.而用反向共沉淀法制备时,溶液pH保持不变且远大于Co2+和Al3+完全沉淀pH,钴铝复合金属氢氧化物同时生成,层板状结构完整且分布均匀.
LDO催化剂的催化活性与其层状结构以及比表面积有关[32],用反向共沉淀法制备的LDO催化剂层状结构更加完整,分布更加均匀,比表面积较大,有利于与臭氧的接触,加强催化效果以及对污染物质的吸附作用为臭氧氧化反应提供更大的反应场所.
2.3 LDO催化臭氧氧化苯胺的反应动力学分析
根据n级反应动力学模型,关系方程
dα/dt=k(T)(1-α)n,
(5)
α=(C0-C/C0-Cn)×100%,
(6)
其中α是反应物浓度转化率,%;t是反应时间,min;k(T)是反应速率常数;n是反应级数;C0是初始浓
度,mg/L;C是实时浓度,mg/L;Cn是反应结束浓度,mg/L.
式(5)两边取对数得到式(7),线性拟合后斜率即为反应级数n,如图4所示.
ln(dα/dt)=lnk(T)+nln(1-α),
(7)
由图4可知,LDO催化剂催化臭氧氧化苯胺废水CODCr的降解反应均符合伪一级动力学模型,关系为
ln(C/C0)=kt,
(8)
其中C是实时浓度,mg/L;C0是初始浓度,mg/L;k是一级反应速率常数,min-1;t是反应时间,min.
图5(a) 不同LDO催化剂+臭氧对苯胺废水CODCr去除效果随时间变化图;(b) 正向Co/Fe-LDO催化剂+臭氧对苯胺废水CODCr去除反应速率图;(c) 反向Co/Fe-LDO催化剂+臭氧对苯胺废水CODCr去除反应速率图;(d) 正向Co/Al-LDO催化剂+臭氧对苯胺废水CODCr去除反应速率图;(e) 反向Co/Al-LDO催化剂+臭氧对苯胺废水CODCr去除反应速率图
如图5所示,ln(C/C0)与时间t之间呈线性关系,反应速率k可由斜率得出.结果表明,由反向共沉淀法制备的LDO催化剂的反应速率高于由正向共沉淀法制备的同类LDO催化剂.
利用化学反应速率方程(9)和阿伦尼乌兹方程[33](10)可推算该反应活化能E,结果如图6和表3所示.
k=ΔC/Δt,
(9)
k(T)=Aexp(-E/RT),
(10)
其中k是反应速率常数;ΔC是CODCr浓度变化量;Δt是时间变化量;A是Arrhenius指数前因子常数;E是反应活化能;R是摩尔气体常数(8.314 J·(K mol)-1);T是反应温度(293.15 K).
计算结果表明,在相同反应温度(293.15 K)下,由反向共沉淀法制备的LDO催化剂催化臭氧氧化苯胺废水反应所需活化能低于同类由正向共沉淀法制备的LDO催化剂.活化能越小,反应速率越快,更有利于臭氧氧化反应的进行.
2.4 催化剂微观结构比对
如文献[34]所述,LDO一般具有八面体对称性,其基本结构单元为八面体,金属离子位于中心,羟基离子位于八面体顶角,通过相邻分子共用边连接形成八面体配位层,这类结构可以为催化反应提供较大的比表面积和催化活性有利于增大与臭氧的接触面积,增强催化作用,也有利于将污染物质吸附到其表面.从图7中可以看出,四种样品均具有典型的LDO层状结构且表面粗糙.
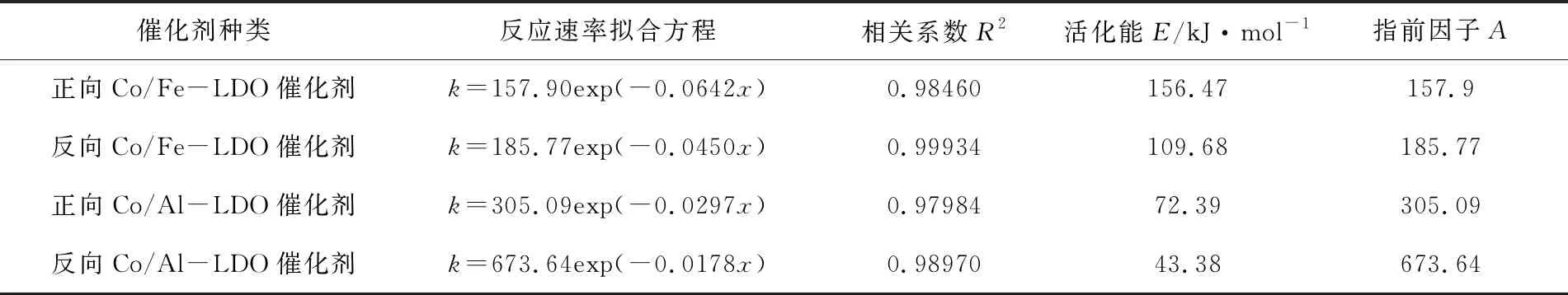
表3 不同LDO催化剂+臭氧氧化苯胺废水CODCr反应活化能
3 结论
采用正向/反向共沉淀方法制备用于模拟苯胺废水处理的两类LDO臭氧催化剂,重点考察原料对LDO催化臭氧的性能影响并进一步进行反应动力学分析.
LDO催化剂制备原料对催化效果的影响最大,选用二价钴离子为制备原料,在制备温度60 ℃,pH 10,二价金属离子与三价金属离子摩尔比例3:1时,可以得到催化效果最佳的Co/Fe-LDO催化剂和Co/Al-LDO催化剂.反向共沉淀法制备的Co/Fe-LDO和Co/Al-LDO催化剂比正向共沉淀法制备的两种材料对苯胺废水CODCr去除率提高1.21%和1.7%,TOC去除率提高0.56%和0.9%;LDO催化剂催化臭氧氧化苯胺废水反应符合伪一级反应动力学模型,反向共沉淀法制备的LDO催化剂催化臭氧氧化苯胺废水反应所需活化能低于同类由正向共沉淀法制备的LDO催化剂.四种催化剂样品均具有典型的LDO层状结构且表面粗糙,反向共沉淀法制备的催化剂比使用正向共沉淀法制备的催化剂层状结构更加清晰.
