纳米钯催化芳基卤化物与四苯基硼酸钠的水相高效偶联反应研究
2020-04-10张源民王天昀杜正银
胡 贝 张源民 王天昀 杜正银
(西北师范大学 化学化工学院,甘肃 兰州 730070)
作为有机合成的中间体,联苯类化合物在许多天然产物、医药合成和有机聚合物的制备等领域具有广泛的应用[1-3].合成联芳化合物离不开芳基化试剂.尽管近些年二芳基碘盐作为芳基化试剂在形成碳碳键、碳氮键方面有较多研究[4-6],但是过渡金属催化的芳基硼酸参与形成联芳化合物已被证实是最有效的芳基化试剂之一[7-9].与芳基硼酸相比,四苯基硼酸钠可以与4当量的亲电试剂反应.从经济和环境的角度来看,这是有机合成中的原子经济反应.尽管有这个明显优势,但使用四苯基硼酸钠构建C-C键的反应并不多[10,11].
通常Suzuki-Miyaura偶联法使用钯配合物作为催化剂,并且反应在高温下进行.然而,这些催化剂大多数是有毒的,价格昂贵并且所得产物经常被钯金属和配体污染.近些年来无配体钯盐及负载零价钯催化体系由于其在绿色催化方面的应用引起了化学家的广泛关注[7,12,14].
水作为溶剂具有低成本,易得和无毒等显著的优点.由于其高介电常数,水是传统热条件和微波辐射Suzuki-Miyaura交叉偶联反应非常有用的溶剂[15-17].低分子量的聚乙二醇(PEG)也是一种高效溶剂,可替代传统的挥发性有机溶剂用于化工分离、催化和有机合成中[18].聚乙二醇因其具有高极性、高沸点、低毒性和良好的环境相容性也已被用于Suzuki-Miyaura反应研究中[19-21].我们以工业来源丰富、价格低廉的氯化钯为钯源,在PEG400中制备了纳米钯,将其作为催化Heck反应[22]、Suzuki反应[23]和Stiller偶联反应[13]的高效催化体系,取得了很好的结果.研究表明,PEG能够将Pd(II)还原为Pd(0),并且其羟基被氧化成醛基.这使得在不使用还原剂的情况下可以很容易地在PEG中制备钯纳米颗粒.由于其特殊的分子结构,PEG还可充当稳定剂来稳定钯纳米颗粒.这里,我们以PdCl2-PEG400原位生成的纳米钯颗粒作为催化剂,研究了卤代芳烃与四苯基硼酸钠在水相中发生高原子利用率的交叉偶联生成联芳化合物的反应.
1 实验部分
1.1 试剂与表征
实验中所用的石油醚和乙酸乙酯为工业品,使用前需进行蒸馏纯化.其他所有试剂均为市售分析纯.
1H NMR光谱和13C NMR光谱在Mercury 400 plus Nuclear Magnetic Resonance光谱仪上测定,使用TMS作为内标,以氘代氯仿(CDCl3)作为溶剂,化学位移(δ)以ppm给出,偶合常数(J)以赫兹(Hz)给出.
1.2 Suzuki-Miyaura偶联反应
将芳基卤化物(1.0 mmol),Ph4BNa(0.25 mmol),K2CO3(3.0 mmol),PdCl2(0.01 mmol),PEG400(1.0 mL)和H2O(2.0 mL)的混合物加入到50 mL圆底烧瓶中.在50℃下搅拌反应,通过TLC判断直至原料完全消耗.停止搅拌,将反应混合物用盐酸酸化后倒入分液漏斗中,用乙醚(10 mL×4)萃取,将合并的有机层用无水MgSO4干燥.通过减压蒸发除去溶剂,得到粗产物,使用石油醚和乙酸乙酯作为洗脱剂,将粗产物通过硅胶柱色谱进一步纯化得到产物.产物均为已知化合物,经测定熔点、1H NMR和13C NMR表征,与文献保持一致.代表性化合物的表征数据如下:4-Carboxaldehydebipheny:white solid,mp:57-58oC;1H NMR (400 MHz,CDCl3):δ=10.06 (s,1H),7.95 (d,J=8.0 Hz,2H),7.75 (d,J=8.4 Hz,2H),7.64 (d,J=6.8 Hz,2H),7.50-7.42 (m,3H);13C NMR (100 MHz,CDCl3):δ=191.9,147.2,139.7,135.2,130.2,129.0,128.4,127.7,127.3.1,4-Diphenylbenzene:white solid,mp 213-214oC;1H NMR (400 MHz,CDCl3):δ=7.69-7.63 (m,9H),7.45 (t,J=7.6Hz,4H),7.38-7.34 (m,2H);13C NMR (100 MHz,CDCl3):δ=140.7,140.1,128.8,127.5,127.3,127.0.
2 结果和讨论
2.1 实验条件的探索与优化
为了探索一个良好的反应条件,我们使用溴苯和四苯基硼酸钠的反应作为模板反应进行反应条件的筛选.我们测试了不同的溶剂、碱、反应温度及催化剂的用量等对该偶联反应的影响.如下表1所示.从表1可以看出,首先,在室温下,PEG400:H2O=1:1(vol/vol),1.0mol%PdCl2存在下,使用K2CO3作为碱,1 mmol的溴苯与0.25 mmol的四苯基硼酸钠反应180 min后联苯的产率达到76%;当溶剂PEG400/H2O=1/2(vol/vol)时产率达到83%(表1,条目1和2).当水的量仅为微量时,反应几乎不能发生(表1,条目3).反应温度升至50 ℃,反应时间则缩短为45min,而目标产物的收率高达99%(表1,条目4).当反应在单独的PEG400中和纯水中进行时产物的收率都不高(表1,条目5和6).可见,水在该体系中是必须的,太多不利于卤代芳烃的形成均相反应,太少则四苯基硼酸钠的溶解受限,不利于反应.接下来我们对碱的种类进行了筛选,使用同样量的Na2CO3、NaOH、DMAP和K3PO4时发现产物收率都低于碳酸钾(表1,条目7-10).继续对K2CO3的用量进行优化,发现当其用量为2.5 mmol时产率降为98%(表1,条目11).最后对催化剂PdCl2的用量进行了考察,当PdCl2用量减为0.5 mol%时,产率降为94%(表1,条目12).通过上述实验,我们决定采用PEG400/H2O (1 mL/2 mL)、K2CO3(3.0 mmol)、PdCl2(1.0 mol%),50 ℃为该反应的最佳反应条件.
表1 反应条件的优化a
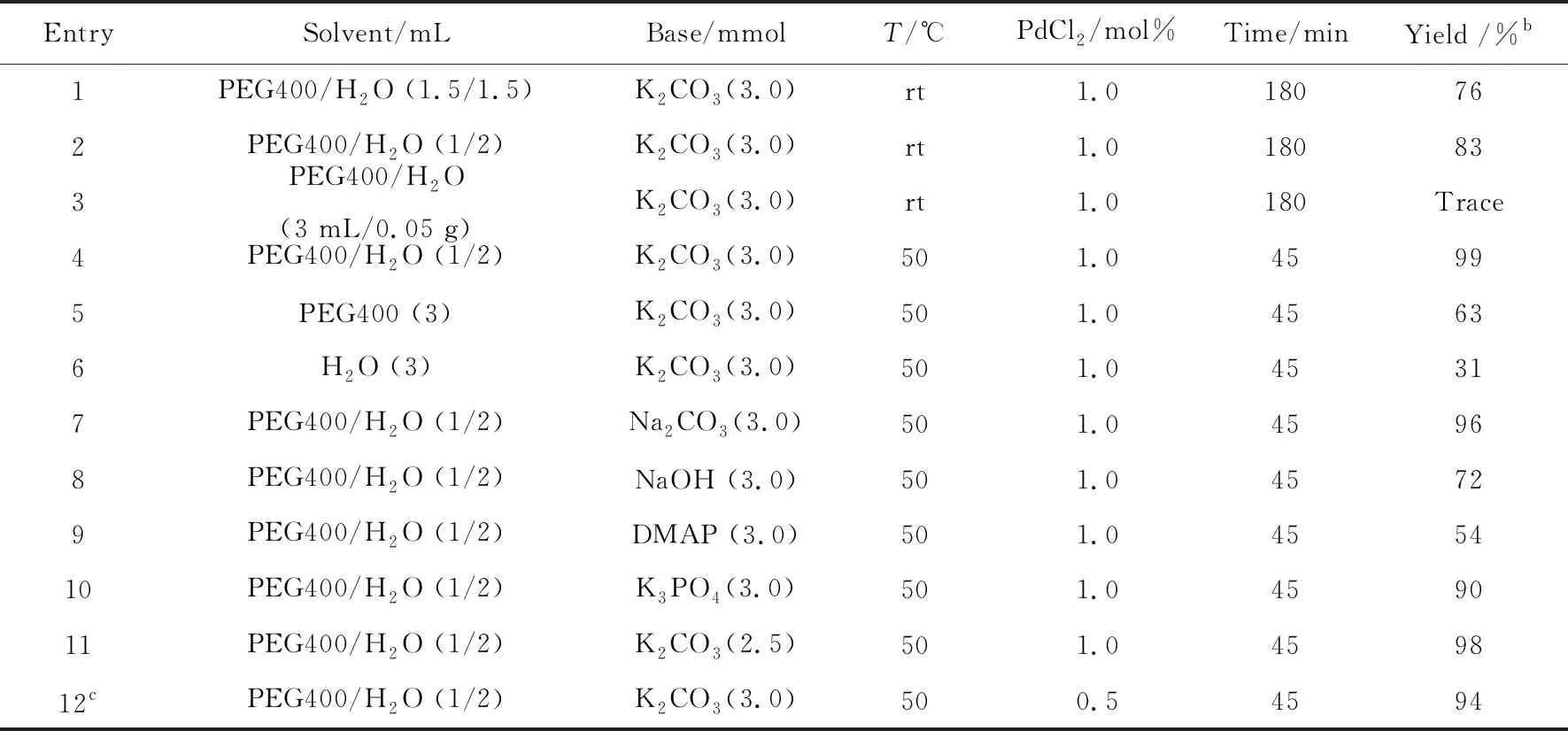
EntrySolvent/mLBase/mmolT/℃PdCl2 /mol%Time/minYield /%b1PEG400/H2O (1.5/1.5)K2CO3(3.0)rt1.0180762PEG400/H2O (1/2)K2CO3(3.0)rt1.0180833PEG400/H2O(3 mL/0.05 g)K2CO3(3.0)rt1.0180Trace4PEG400/H2O (1/2)K2CO3(3.0)501.045995PEG400 (3)K2CO3(3.0)501.045636H2O (3)K2CO3(3.0)501.045317PEG400/H2O (1/2)Na2CO3(3.0)501.045968PEG400/H2O (1/2)NaOH (3.0)501.045729PEG400/H2O (1/2)DMAP (3.0)501.0455410PEG400/H2O (1/2)K3PO4(3.0)501.0459011PEG400/H2O (1/2)K2CO3(2.5)501.0459812cPEG400/H2O (1/2)K2CO3(3.0)500.54594
注:a:反应条件:溴苯(1.0 mmol),四苯基硼酸钠(0.25 mmol),碱,PdCl2(0.01 mmol);b分离产率;c:氯化钯的用量为0.005 mmol.
表2 芳基溴化物与四苯基硼酸钠的交叉偶联反应a
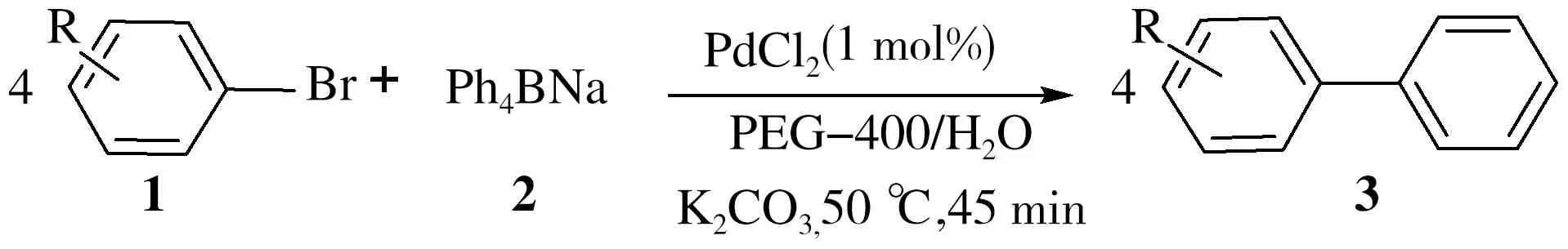

EntryRTime /minProductbYield/%1H459924-CHO609734-COCH3459844-Cl459653-Cl559464-CN459974-COOH459984-OCH3609194-OH6092102-OCH36076114-NH26087124-CH36090134-Ph4593144596156094
注:a:反应条件:1(1.0 mmol),2(0.25 mmol),PdCl2(1 mol%),K2CO3(3.0 mmol)和PEG400 / H2O (1 mL / 2 mL),50 ℃; b:所有产物均已测试熔点,并经过1H NMR和13C NMR表征.
在优化反应条件后,我们开始对芳基溴化物的适用范围进行了研究.实验结果如表2所示.根据条件优化结果我们知道,溴苯与四苯基硼酸钠反应生成联苯的收率为99%(表2,条目1).当使用含有吸电子基团如,醛基、乙酰基、氯原子、氰基、羧基的芳基溴化物与四苯基硼酸钠反应时产物的分离收率均能达到94%以上(表2,条目2-7).芳基溴化物的对位有给电子官能团如甲氧基、甲基、氨基的交叉偶联反应也能顺利进行,产物收率不低于87%,而2-位有取代基时因位阻原因收率稍低(表2,条目8-12).与吸电子取代基相比,含有供电子取代基的溴苯反应产物的收率略低.当以4-溴联苯和1-溴代萘作为反应底物时,1,4-三联苯和1-苯基萘的收率分别为93%和96%(表2,条目13和14).进一步的研究表明,1,3-二溴苯也能以94%的收率得到同时发生双苯基化的1,3-三联苯产物(表2,条目15).可见该反应对溴代芳烃具有很好的适用性,对各种官能团也具有良好的兼容性.
与相应的芳基溴化物的反应性相比,芳基碘化物与四苯基硼酸钠的交叉偶联反应也是非常高效的,如表3所示,产物收率比溴化物的反应略高(表3,条目1-4).然而当以氯苯作为反应底物时联苯的收率仅有31%(表3,条目5).这说明卤代芳烃的反应活性顺序是碘代苯>溴代苯>氯代苯.
表3 芳基碘化物与四苯基硼酸钠的交叉偶联反应[a]
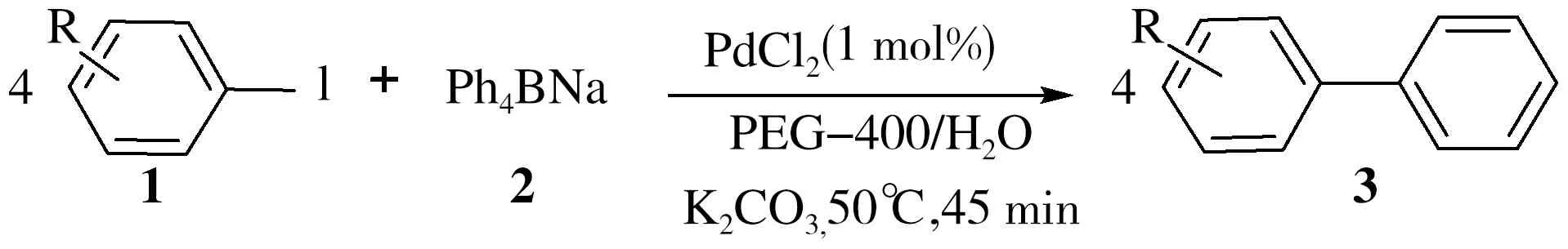

EntryRTime/minProductYield/%1H459924-OCH3459834-COOH459944-NH2459459031
注:a:反应条件:1(1.0 mmol),2(0.25 mmol),PdCl2(1 mol%),K2CO3(3.0 mmol)和PEG400/H2O (1 mL / 2 mL),50℃.
为了考察反应介质以及催化剂的可重复使用性,选择芳基溴与四苯基硼酸钠的偶联作为模型反应.初次实验结束后,将反应混合物用乙醚萃取,减压蒸馏除去PEG中的残余乙醚.反应介质和Pd催化剂体系可直接用于下一轮反应.表4总结了该催化剂体系循环利用的结果.可以看出,催化剂的活性在循环使用3次后有较明显的降低,反应时间从45 min延长至70 min,也能获得88%的产率.这可能是原位生成的纳米钯颗粒在循环使用过程中团聚导致催化活性降低[23].

表4 催化剂体系的循环使用a
注:a:反应条件:溴苯(1.0 mmol),Ph4BNa(0.25 mmol),PdCl2(1 mol%),K2CO3(3.0 mmol)和PEG400/H2O(1 mL/2 mL),50 ℃.
3 结论
我们以廉价易得的氯化钯为钯源,以聚乙二醇400和水作为反应介质,发展了一种原位生成的钯纳米颗粒作为催化剂,催化芳基卤化物与四苯基硼酸钠发生Suzuki-Miyaura交叉偶联反应生成联芳化合物的高效且经济的方法.该方法反应条件温和,反应时间短,有机基团原子利用率高,产物收率高,底物适用范围广,反应过程经济环保.
