双源能谱CT 虚拟平扫替代常规平扫评估食管癌的可行性研究
2020-04-09郑星星冯峰丁勇生李月玥李瑞
郑星星 冯峰 丁勇生 李月玥 李瑞
食管癌是全球第八大常见癌症, 也是全球癌症致死的第六大原因, 其在发展中国家的发病和死亡病例占了全球的80%以上[1]。CT 常规平扫(true noncontrast,TNC)和增强扫描是临床常用的食管癌影像检查方法,不仅可以清晰显示病灶解剖学细节,还有助于定位及评价病灶与周围结构的关系;但CT 常规检查需要多期扫描,增加了病人的辐射剂量,而且食管本身及周围器官对辐射有较高的敏感性,因此在充分发挥CT 检查技术优势和保证影像质量的同时,如何降低辐射剂量至关重要。 近年出现的双源CT利用碘物质分离技术可以将碘对比剂从CT 增强影像中去除,从而获得类似于TNC 的影像,即虚拟平扫(virtual non-contrast,VNC)影像[2]。采用VNC 可减少1 次TNC,从而降低病人辐射剂量。以往研究[3-4]多报道VNC 在肾癌和胃癌检查中的应用,而应用于食管癌的报道甚少。本研究通过比较双源能谱CT VNC与TNC 影像对食管癌影像质量的主观及客观评价差异,探讨VNC 替代TNC 评估食管癌的可行性。
1 资料与方法
1.1 一般资料 回顾性分析2019 年1—5 月南通大学附属肿瘤医院46 例食管鳞状细胞癌病人的临床及CT 影像资料,其中男33 例,女13 例,年龄50~88 岁,平均(67.2±8.2)岁。 所有病人均行TNC 及双能量双期(动脉期及静脉期)增强扫描。 病灶位于食管上段3 例,中段30 例,中上段2 例,中下段8 例,下段3 例。 纳入标准:①经胃镜或手术病理证实;②均为单发病灶;③无严重心脏、肝脏、肾脏功能衰竭及碘过敏史者。 排除标准: ①影像资料及临床数据缺失或不完整;②影像质量不佳,不能用于诊断。
1.2 设备与方法 采用Siemens Flash 双源CT(Somatom Definition)行胸部加上腹部TNC 及双能量双期增强扫描。 所有病人检查前禁食8~12 h,并于检查前10~15 min 饮水800~1 000 mL 以充盈上胃肠道。 检查取仰卧位, 扫描范围从肺尖至肾上腺上极。 扫描参数:TNC 管电压120 kV,管电流200 mA;动脉期及静脉期采用双能扫描模式:A 球管, 管电流/管电压210 mA/100 kV,B 球管162 mA/140 kV。矩阵512×512,FOV 300 mm×300 mm,层厚、层间距均为5 mm,螺距1.2,旋转时间0.5 s/r。 采用基于自动实时衰减的专用管电流调制软件 (CARE Dose 4D,Siemens)采集所有数据。用高压注射器经肘正中静脉团注对比剂碘海醇(含碘300 mg/mL,扬子江药业),剂量1.2 mL/kg 体质量,注射流率3.0 mL/s。注射对比剂后,以主动脉弓水平测量CT 值,监测阈值达到100 HU 后, 延迟6 s 后开始扫描触发动脉期,动脉期后25 s 扫描静脉期。 影像加权因子为0.5(即,按照100 kV 数据和140 kV 数据各占50%的比例,通过双源CT 自动计算后得到相当于120 kV 的融合影像)。
1.3 图像后处理 将所有双源CT 数据重建成层厚、层间距均为1 mm 的薄层图像,并传到后处理工作站(Siemens Syngo-via VB10),应用“VNC”程序进一步分析。 参照蓝等[5]的研究方法,选择动脉期的双能量数据集进行后处理。 首先将碘对比剂的融合比率调整到0,获得初始VNC 图像,设置与TNC 相同的窗位(300 HU)、窗宽(40 HU),然后将VNC 数据保存并导入3D 软件,重组出与TNC 层厚、层间距相同的最终VNC 影像。
1.4 影像分析 由2 名分别有2 年和15 年诊断经验的放射科医师采用双盲法独立对工作站后处理影像进行定性和定量分析, 若结果出现分歧则通过讨论达成一致。
1.4.1 定性分析 影像评价基于影像伪影的严重程度、解剖学细节清晰度及5 分等级标准[6]:5 分,解剖结构及细节清晰,没有明显的噪声,能明确评价;4 分,解剖结构和细节不太清晰, 噪声和伪影增加;3 分,大部分解剖结构清晰,细节不太清晰,噪声和伪影很明显,但基本能满足诊断要求;2 分,解剖结构不清晰,很难识别细节,噪声和伪影非常明显;1 分,解剖结构模糊,细节无法识别,噪声和伪影非常明显。≥3分的影像符合诊断要求。 由上述2 名观察者记录VNC 和TNC 影像上食管癌形态学特征, 包括病灶处的管壁增厚(食管管壁厚度>5 mm 为异常)、病灶与周围主要组织(气管及支气管、主动脉)的关系以及淋巴结有无肿大(淋巴结短径>10 mm 为肿大)。
1.4.2 定量分析 在TNC 和VNC 横断面影像中病变最大层面的实性部分上选取面积为0.3~1.0 cm2相同兴趣区,尽量避开钙化、坏死区域。 测量病变组织、同层面降主动脉、胸椎椎体后方肌肉、皮下脂肪及空气的平均CT 值、标准差(SD),测量3 次,取其平均值。 同时计算病灶信噪比(signal to noise ratio,SNR)及对比噪声比(contrast to noise ratio,CNR)。 计算公式为SNR=病灶CT 值/病灶SD,CNR=|病灶CT值-同层面椎后肌肉CT 值|/噪声(以前胸壁皮下脂肪SD 值作为噪声)。 在横断面影像上病灶最大层面测量最大管壁厚度,若该层面管壁均匀增厚导致管腔完全闭塞, 则以食管直径的一半作为最大管壁厚度[7],TNC 和VNC 中测量层面一致。
1.5 辐射剂量分析 常规CT 检查为三期扫描模式, 辐射剂量为TNC 与双期增强辐射剂量之和;双能量双期扫描模式则为双期增强扫描的辐射剂量之和。 记录2 种扫描模式的CT 剂量指数(CT dose index volume,CTDIvol)与 剂 量 长 度 乘 积(dose length product,DLP),均为设备自动生成。 计算有效剂量(effective dose,DE)=DLP×K(换算因子),K 值为0.014[8]。
1.6 统计学方法 采用SPSS 21.0 统计软件对数据进行分析。 符合正态分布的计量资料用均数±标准差(x±s)表示,2 组间比较采用配对样本t 检验;非正态分布的计量资料以中位数 (四分位间距)[M(P25,P75)]表示,2 组间比较采用Wilcoxon 秩和检验。计数资料以例表示,2 组间比较采用χ2检验。 采用Kappa检验分析2 名医师影像质量评分的一致性,κ<0.4表示一致性较差,0.4≤κ<0.75 表示一致性中等,κ≥0.75 表示一致性较好。 P<0.05 为差异有统计学意义。
2 结果
2.1 2 种影像上食管癌形态学特征的比较 2 种影像上所显示的病灶形态学特征的差异均无统计学意义(均P>0.05),除了两者所显示的肿瘤与气管、支气管间隙分布的病灶数略有不同外, 其余各特征均完全一致(表1,图1、2)。
2.2 影像质量主观评分比较及一致性分析 2 名观察者对食管癌TNC 和VNC 影像质量主观评分均为3 分以上, 一致性均较好 (TNC,κ=0.957;VNC,κ=0.964),见表2。 2 名观察者对TNC 影像的主观评分中位数为5(4,5)分,对VNC 影像的评分中位数为5(4,5)分,评分差异无统计学意义(Z=-1.737,P=0.082)。
2.3 2 种影像上病灶处管壁厚度、 不同部位CT 值及影像质量的比较 2 种影像上食管癌病灶处管壁厚度的差异无统计学意义(P>0.05)。 VNC 影像的降主动脉、皮下脂肪CT 值均高于TNC(P<0.05),2 种影像上食管癌病灶、 椎体后肌肉和空气的CT 值差 异无统计学意义(P>0.05)。 VNC 的SNR 高于TNC,而噪声低于TNC(均P<0.05),2 种扫描方式的CNR差异无统计学意义(P>0.05),见表3。
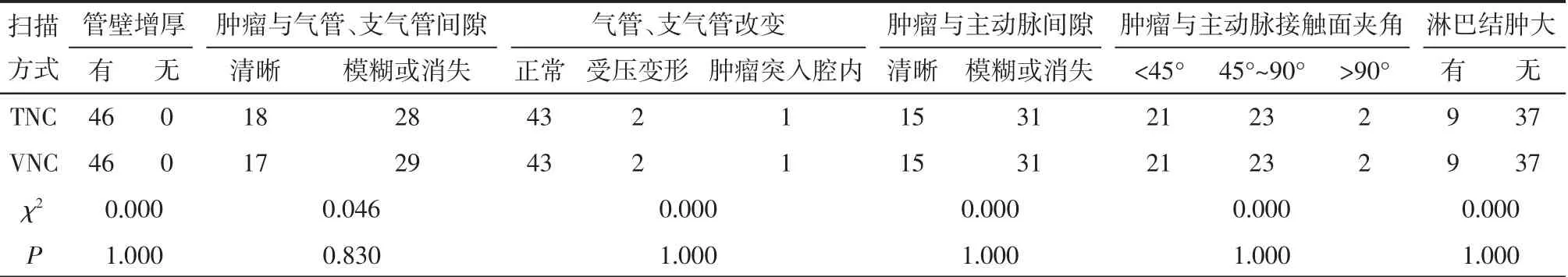
表1 TNC 与VNC 影像上食管癌的形态学特征比较n=46,例
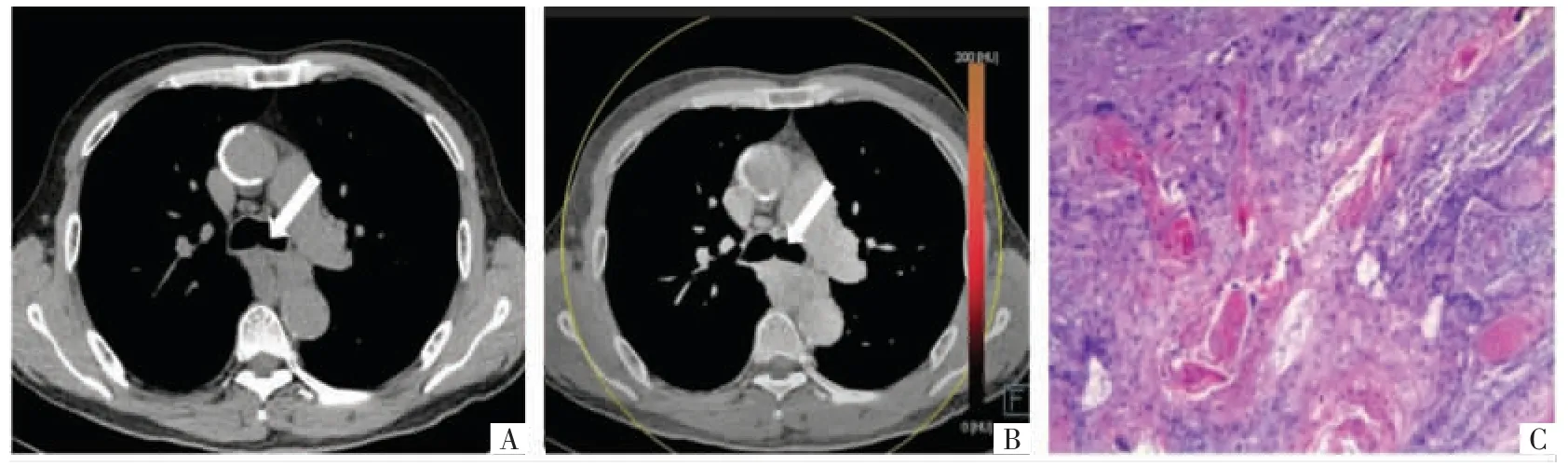
图1 病人男,75 岁,食管鳞癌。 A、B 图分别为TNC、VNC 影像,均显示食管中段不规则增厚,局部管腔变窄,周围脂肪间隙欠清(箭头),病灶接触胸主动脉夹角为60°。 A、B 图上病灶CT 值、噪声、SNR、CNR 分别为45.00 HU、20.50、2.68、0.59 和43.75 HU、12.95、2.73、0.48,主观评分均为4 分;C 图,镜下可见癌细胞分化良好,癌细胞较大,呈多角形或圆形,胞浆较多,核分裂象较少,诊断结果为高分化鳞状细胞癌,侵及食管外膜层(HE,×200)。

图2 病人男,73 岁,食管鳞癌。A、B 图分别为TNC、VNC 影像,均较好显示食管中段不规则增厚,局部管腔变窄,周围脂肪间隙欠清,纵隔内见肿大的淋巴结(箭头)。 A、B 图上病灶CT 值、噪声、SNR、CNR 分别为41.50 HU、12.50、2.39、1.24 和46.10 HU、9.65、2.67、0.79。 主观评分均为4 分。
2.4 2 种扫描方式辐射剂量的比较 双能量双期扫描的ED、CTDIvol、DLP 均低于常规三期扫描(均P<0.05),双能量双期扫描的辐射剂量减少了(3.46±0.87)mSv,见表4。

表2 2 名观察者对食管癌VNC 与TNC影像主观评分结果n=46
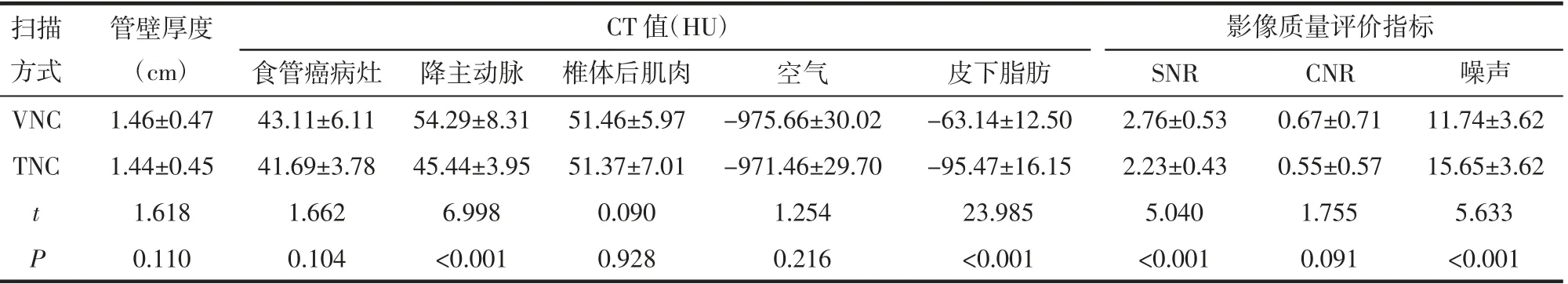
表3 VNC 与TNC 影像上病灶处管壁厚度、各部位CT 值和影像质量评价指标的比较n=46

表4 2 种扫描方式的辐射剂量比较n=46
3 讨论
双源CT 采用2 个X 线球管和2 个探测器采集图像, 改变了以往单一球管及探测器的图像采集方式, 能够快速扫描成像, 从而获得2 组不同能量数据,利用物质分离及基物质成像技术,从增强影像中分离并去除碘,可得到VNC 影像,这种扫描方式不仅可减少辐射剂量,还能提供与TNC 影像质量相当的虚拟影像[9-10]。
CT 对显示食管癌的管壁增厚、周围组织侵犯及淋巴结转移具有重要意义, 可为临床诊断和术前分期提供可靠依据。 本研究中双源CT VNC 与TNC 影像显示食管癌病灶处的管壁增厚、 病灶与周围主要组织(气管及支气管、主动脉)的关系及淋巴结有无肿大特征的差异无统计学意义, 而且2 名观察者对VNC 和TNC 影像质量的主观评分差异也无统计学意义,均在3 分以上,表明VNC 和TNC 均有良好的影像质量,能够达到影像诊断要求。 VNC 和TNC 影像质量对比分析在其他部位研究较多,Shi 等[11]对74 例胃癌病人的TNC 和VNC 影像质量评分, 分别为(4.93±0.30)分和(4.15±0.70)分,其差异无统计学意义,且VNC 影像评分均≥3 分。 Yun 等[12]比较76例颅内动脉瘤术后病人的常规CT 和双源CT 影像质量,结果显示2 名观察者对VNC 影像质量评分均在4 分以上。 与本研究扫描部位相同的一项研究[13]对50 例临床疑诊纵隔淋巴结病变的病人行胸部双能量CT 扫描,结果也显示VNC 与TNC 的影像质量无统计学差异,且均可满足临床诊断要求。由此表明VNC 技术在减少辐射剂量的同时不会影响主观影像质量。
本研究中VNC 与TNC 影像上食管癌病灶、椎体后肌肉及空气平均CT 值差异无统计学意义。 与本研究中相同物质(如肌肉)的CT 值分析也有相似报道,Chai 等[4]在TNC 与VNC 影像上测量95 例胃癌病人腰大肌CT 值,发现2 种扫描方式肌肉CT 值差异无统计学意义。 原因在于动脉期影像上对比剂主要集中在动脉血管中, 而组织和脏器毛细血管中的对比剂含量较少,因此VNC 影像上所得到的组织和脏器的CT 值更接近于TNC 影像[5]。而本研究中2种影像上降主动脉及皮下脂肪CT 值差异有统计学意义,Jamali 等[14]研究认为无论评价哪种组织,测量的CT 值可以存在差异, 但都有其允许范围, 一般为±15 HU。 本研究结果显示两种方式测量降主动脉CT 值差异<15 HU, 皮下脂肪CT 值差异>15 HU,这与Javadi 等[15]对123 例胰腺癌病人行腹部常规CT和双能量CT 检查的研究结果一致。 其原因为:①双能量射线可能存在交叉,造成物质分离及抑碘不足,导致极少部分碘仍然存在于VNC 影像中,且无法完全去除。 ②脂肪不属于物质分解算法的一部分。 对于食管癌病灶, 本研究结果显示VNC 测量病灶CT值及管壁厚度与TNC 差异无统计学意义。目前有关食管癌的类似研究少有报道, 有在其他部位应用的一些报道,Navin 等[9]利用VNC 技术测量23 例肾脏疾病病灶CT 值,结果也显示VNC 和TNC 影像病灶CT 值差异无统计学意义。 今后可以进一步收集病例,验证VNC 技术在测量食管癌管壁厚度和CT 值方面的可行性。
CT 对食管癌病灶显示的清晰程度可以通过影像的噪声、SNR 和CNR 进行分析。本研究中VNC 影像噪声小于TNC,与Kaufmann 等[16]评估63 例肾脏、胰腺、 肝脏病变病人VNC 与TNC 的影像噪声结果相符。 张等[17]比较35 例腮腺肿块病人VNC 和TNC的病灶CNR 及SNR, 结果显示VNC 的SNR 高于TNC,而CNR 差异无统计学意义,本研究结果与其一致。 尽管以上报道中的疾病与本研究中的不同,但均可能是由于VNC 影像的后处理算法中光滑处理导致背景噪声降低,病灶SNR 升高;此外,双源CT 设置较低的电压并运用CARE Dose 4D 技术能够提高SNR,从而提高病灶检出率[4,9]。
通过迭代或者解析重建算法构建最小辐射产生适当的影像质量极其困难。 双源CT 采用CARE Dose 4D 技术与VNC 技术结合获得类似TNC 影像,不仅减少了非增强相位,还有效减少了辐射剂量,因此降低有效辐射剂量是VNC 影像的另一个潜在优势。本研究采用VNC 行双期扫描比常规三期扫描的辐射剂量降低了(3.46±0.87)mSv。 同样是对胸部疾病的研究,刘等[18]对50 例疑似肺癌病人进行双源CT 双能量扫描, 结果显示应用VNC 技术的平均有效辐射剂量比常规三期扫描减少2.29 mSv。可见,采用VNC 技术双期扫描替代常规三期扫描检测食管癌,不仅可以减少一期常规平扫,还大幅度降低辐射剂量,并节约了扫描时间。
本研究尚存在一定局限性:①样本量较少,只评估了食管癌及部分兴趣区的CT 值, 未基于获得的数据对病灶特征及分化等进行详细评估, 有待于今后扩大样本量进一步完善; ②研究结果是采用双球管双能量能谱CT 扫描设备获得的, 能否适用于其他能谱CT 机型(如,单源瞬时kVp 切换能谱CT)需在今后工作中进一步研究。
总之,双能量CT 扫描VNC 技术应用于食管癌检查时, 其得到的影像与TNC 影像的质量相当,不仅能满足临床诊断要求,而且可以简化检查流程,降低辐射剂量,故其有望取代TNC 用于食管癌形态学评估。
