碳点基固相微萃取涂层测定水体中邻苯二甲酸酯
2020-04-07陈秀林田彤吴剑锋赵广超
陈秀林 田彤 吴剑锋 赵广超


摘 要:利用溶胶-凝胶法制备了纳米碳点基固相微萃取涂层,建立了固相微萃取-气相色谱法(SPME-GC)测定水体中四种邻苯二甲酸酯的方法,优化了方法条件。结果表明,在优化条件下,方法线性范围2.5~200 μg/L内线性良好(R2=0.990 3~0.998 1),检出限为0.83 ~1.81 μg/L(远低于国标0.09~2.70 mg/L),相对标准偏差1.4%~9.8%。在5和10 g/L加标浓度水平下,水样的加标回收率为82.2%~121.3%,相对标准偏差2.6%~9.7%。建立的方法满足实际水样的分析要求。
关 键 词:固相微萃取;纳米碳点;邻苯二甲酸酯;溶胶-凝胶
中图分类号:TE685.3+1 文献标识码: A 文章编号: 1671-0460(2020)03-0753-04
Determination of Phthalate Acid Ester in Water by
Carbon Nanodots-based SPME Coating
CHEN Xiu-lin1,2, TIAN Tong1, WU Jian-feng1, ZHAO Guang-chao1
(1. School of Environmental Science and Engineering, Anhui Normal University, Anhui Wuhu 241000, China;
2. Shanghai Chemical Monitoring Station for Environment Protection, Shanghai 201540, China)
Abstract: A carbon nanodots-based solid-phase microextraction(SPME) coating was prepared using a sol-gel technique. Coupled with gas chromatography (GC), an analytical method for the determination of phthalate acid ester (PAEs) in water was proposed. The experimental parameters were optimized. The results showed that the prepared coating extracted target analytes with good linearity in the wide concentration range from 2.5 μg/L to 200 μg/L,with the correlation coefficient (R2) of 0.990 3~0.998 1. The detection limit of proposed method was from 0.83 μg/L to 1.81 μg/L(which was far lower than the national standard of 0.09~2.70 mg/L) and the relative standard deviation (RSD) was between 1.4% and 9.8%. In the level of 5~10 μg/L, spiked recoveries for four PAEs in water samples were in the range from 82.2% to 121.3% with RSDs of 2.6%~9.7%. The proposed method can meet the requirement of the determination of PAEs in actual water samples.
Key words: solid phase micro-extraction; carbon nanodots; phthalate acid esters; sol-gel
邻苯二甲酸酯(PAEs)作为一类改善材料物理性能的增塑剂被广泛添加于塑料产品中,由于其没有与塑料之间形成相对稳定的化学键,受产品使用寿命影响,产品中PAEs可转移至环境中,造成环境污染[1]。有研究表明: PAEs作為一类环境激素,进入人体后扰乱内分泌系统,容易形成人类生殖和发育方面潜在危害[2]。2005年美国环境保护署(USEPA)将邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二辛酯(DNOP)等PAEs列入了优先控制污染物名单。我国相关部门也采取了相应行动,将DMP,DEP和 DNOP 等PAEs列入“中国环境优先控制污染物黑名单”[3], 并就食品安全、食品接触材料及制品中的PAEs的测定和迁移量的测定制定了国家标准[4]。
环境中PAEs存在的浓度普遍为痕量水平,现代分析测试仪器很难达到直接测定的灵敏度要求。一般仪器测定前都需要对样品进行富集、浓缩等前处理。固相微萃取法(SPME)是一种省时高效、简单方便与绿色环保的前处理技术[5],它与气相色谱仪联用被广泛应用于环境分析领域。已有文献报道了商业化SPME纤维被广泛应用于分析环境中PAEs[6,7]。这些方法有一定的优势,但市场上商业化纤维存在着如萃取范围有限、使用寿命较短、热稳定性不足、萃取效不高等问题[8]。为此,发展新的涂层材料以便扩展萃取对象、提高萃取性能是SPME研究方向之一[9]。
碳点材料作为继石墨烯、碳纳米管后的碳材料家族的新成员,具有尺寸更小,比表面积更大等特点,在环境分析领域具有良好应用前景[10]。本研究中使用碳点作为涂层材料,结合固相微萃取-气相色谱法(SPME-GC)对水体中4种PAEs进行了分析。该方法为环境水体中PAEs测定提供了新的选择。
1 实验部分
1.1 主要仪器与试剂
GC-2010气相色谱仪(Shimadzu公司);Hitachi S-4800扫描电子显微镜(Hitachi公司);8400s- FTIR傅里叶红外变换光谱(Shimadzu公司)。
四种PAEs混合标准溶液:邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二辛酯(DNOP)(上海百灵威科技有限公司)。实验均采用超纯水。
工作储备溶液配制:取四种PAEs混合标准溶液用丙酮配制成100 mg/L混标溶液,在4 ℃条件下保存,待用。
1.2 样品采集与处理
塑料杯水样:取超纯水50 mL用热水壶加热至沸腾,将沸水倒入一次性塑料杯中浸泡两小时,冷却后获得水样,保存于4 ℃冰箱中。
长江水样:取长江干流芜湖段滨江公园段水样250 mL, 用45 μm滤纸过滤水样中泥沙、大颗粒等不溶性杂质,装入清洁的玻璃瓶中,保存于4 ℃冰箱中。
1.3 GC-FID条件
GC条件:进样口温度250 ℃,无分流进样,色谱柱初始60 ℃,保持1 min;以20.0 ℃/min升温至220 ℃,保持1 min;以5.0 ℃/min升至280 ℃,保持5 min。FID检测温度300 ℃。载气为氮气(纯度>99.999%),柱流量1.51 mL/min,氢气(纯度>99.999%), 流量40.0 mL/min; 采取空气自动进气装置,流量400.0 mL/min。
1.4 SPME纤维制备
采用文献报道的方法[11],合成了納米碳点材料,烘干后待用。
取10 mL离心管加入2 mL无水乙醇,加入20 μL 10%的稀盐酸,于超声情况下缓慢加入200 μL钛酸正四丁酯,2 min后缓缓滴入25 μL超纯水,盖上管塞。10 min后,加入0.02 g碳点材料,磁力低速搅拌12 h,获得均匀的纳米碳点基凝胶溶液,置于4 ℃下保存待用。
取一根不锈钢丝(? 0.5 mm),抛光后用丙酮、2 mol/L NaOH溶液处理。将其处理后的一端1 cm插入纳米碳点基凝胶溶液,放置5 min,缓慢取出于80 ℃烘箱中烘干,获得SPME纤维。再与微量进样器组装成SPME装置,在260 ℃ 下将纤维老化1 h,待用。
1.5 顶空SPME过程
取10 mL水样,将SPME萃取头插入样品中,采用顶空模式下萃取目标分析物,萃取温度60 ℃、搅拌速率100 r/min、盐浓度为0%下萃取20 min。萃取结束后将萃取头缓慢拔出,立即插入GC进样口,热解吸5 min,进行GC-FID检测分析。每项进行三次平行实验。
2 结果与讨论
2.1 自制SPME涂层与碳点材料的表征
采用扫描电子显微镜对制备的SPME涂层进行了表征。图1(a)和图1(b)分别表示不同放大倍率下SPME涂层的SEM图,其中图1(b)清晰地显示许多球状颗粒团聚在一起,形成孔隙率较高的三维空间结构。图1(c)和(d)是没有纳米碳点存在时的SPME涂层的SEM图,图1(d)显示支撑体体表面形成了凝胶网状结构,但与碳点基涂层相比,显然没有密集的立体孔隙结构。碳点基材料作为更小尺寸的碳纳米材料,比表面积更大,故制备的碳点基SPME涂层更高的萃取效率。
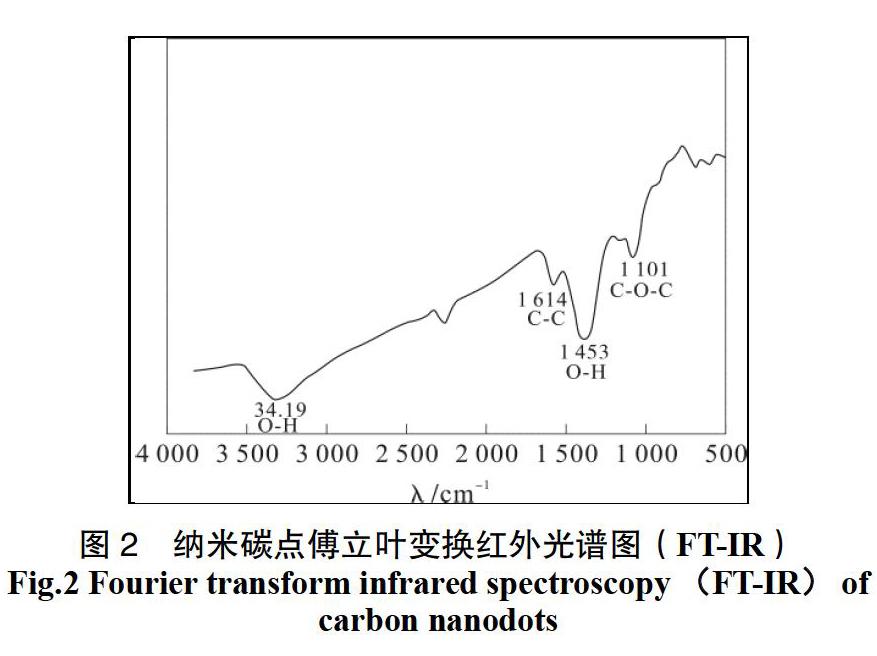
图2是制备的纳米碳点的傅立叶红外变换光谱(FT-IR)图,如图所示:制备的纳米碳点在3 419和1 483 cm-1处发生了明显伸缩振动,这代表了其表面有丰富的O-H官能团;1 614 cm-1处也发生了伸缩振动,这是由表面存在C=C骨架振动产生的;1 101 cm-1吸收峰处是由是由O-H或者C-O-C伸缩振动产生的。由上述的吸收峰可知,纳米碳点基表面具有大量O-H存在,它们容易与PAEs分子之间形成氢键;而C=C的存在,可以与PAEs分子形成电子云重叠,增加相互作用;C-O-C的存在可能有助于与PAEs分子间形成螯合结构,提高其萃取效果[12]。
2.2 萃取条件优化
SPME是一种预平衡技术,基于涂层及均一的样品基质之间分配平衡而建立。在这一过程中,萃取萃取温度、溶液的运动、萃取时间等因素都会影响萃取效果[13-15]。
另外,萃取物的解吸也是SPME过程中不可或缺的步骤,较低温度不利于目标分析物从涂层中解吸,而较高温度可能导致目标分析物中大分子发生裂解,影响分析准确性。本实验选择对萃取效果影响较大的萃取时间、萃取温度、搅拌速率和解析时间等条件参数进行了优化。通过正交试验,筛选出最佳条件。正交实验选择的实验参数条件列于表1中。
根据Design-Expert 8.0.6软件对实验的正交设计,进行条件优化实验,将各组合设计获得的峰面积对不同的PAEs的影响关系运用响应面分析方法(Responsed area analysis, RSA)进行分析得出不同组分的优化条件,经过软件系统评估选择对各组分萃取最优的实验参数条件。图3为软件处理优化实验过程中所制备的碳点基涂层对水样四种PAEs中典型的DNOP萃取效果的影响与条件评估。综合评估结果显示,涂层对目标分析物的萃取最佳条件为:萃取温度60 ℃;搅拌速率100 r/min;萃取时间20 min;离子强度8%。
2.3 检测方法的线性范围、相关系数、检出限和重现性等
在最优化条件参数下,使用制备的碳点基涂层对4种PAEs进行了SPME-GC分析, 实验结果见表2。
由表2可知,浓度在2.5~200μg/L范围内,4种不同PAEs具有良好线性关系,其相关系数(R2)在0.990 3~0.994 1之间;方法的检出限为0.83~1.81μg/L;单根纤维日内与日间相对标准偏差(RSD)为1.4%~6.7%;多根纤维间RSD为5.6%~9.8%。与文献报道的涂层相比较,本实验制备的涂层也具有一定的优势,如表3所示。
2.4 实际水样的测定及加标回收率
实际水样按1.5的步骤在最优化参数条件下进行SPME-GC检测分析。结果显示:沸水冲泡2 h后的塑料杯水样中未检测到四种PAEs;在长江水样中未检测到四种PAEs中的DMP和DNOP,但检测出DEP,其浓度为4.17 μg/L;检测出DBP的浓度为3.2 μg/L。使用5和10 μg/L两种浓度的混标溶液对水样分别进行加标实验(n=3),结果显示在塑料杯水样中PAEs加标回收率82.2%~121.3%,RSD为2.6%~9.7%。长江水样中PAEs加标回收率87.2%~117%,RSD为3.5%~9.5%。实验结果总结在表4中。
3 结论
制备的纳米碳点材料具有较大比表面积、孔隙率和吸附容量,适宜于制备固相微萃取涂层并能用于测定水体中邻苯二甲酸酯的测定。与文献相比,建立的测定方法在检测水体中PAEs时能满足食品检测、环境检测的要求。另外,制备的碳点基涂层还可用于检测环境中存在的其他痕量有机污染物样品(如TPHs、PCBs、双酚A、有机氯农药、荻氏剂、异荻氏剂、DDT、PAHs、以及SVOCs等),具有广阔的发展前景。
参考文献:
[1]张丽丽,陈焕文,李建强,等. 邻苯二甲酸酯类化合物检测方法研究进展[J]. 理化检验-化学分册,2011, 47(2):241-247.
[2]程爱华,王磊,张睿,等.水中微量邻苯二甲酸酯类物质实用分析方法的测定[J].环境工程,2007,25(3):77-79.
[3]周文敏,傅德黔,孙宗光.水中优先控制污染物黑名单[J].中国环境监测,1990, 6(4):1-3.
[4]國家标准局信息分类编码研究所. GB 31604.30-2016 CHN[S]. 北京:中国标准出版社,2016.
[5]Dandan Ge, Hian kee lee. Polypropylene membrane coated with carbon nanotubes functionalized with chitosan: Application in the microextraction of polychlorinated biphenyls and polybrominated diphenyl ethers from environmental water samples[J]. Journal of Chromatography A, 2015, 1408: 56-62.
[6]张泽明,张洪海,李建龙,等. 固相微萃取-气相色谱-质谱联用测定海水与沉积物中邻苯二甲酸酯类污染物[J]. 分析化学,2017, 45(3):348-356.
[7]陈海东,鲜啟鸣,邹惠仙,等. 固相微萃取气相色谱法(SPME-GC)测定水体中邻苯二甲酸酯[J].分析实验室,2006, 25(3):32-36.
[8]胡庆兰. 新型固相微萃取涂层测定土壤中的邻苯二甲酸酯[J]. 现代化工,2012,32(11):117-119.
[9]Agata Spietelum, Lukasz Marcinkowski, Miguel de la Guardia, et al. Recent developments and future trends in solid phase microextraction techniques towards green analytical chemistry[J]. Journal of Chromatography A, 2013, 1321:1-13.
[10]王林鹏,马玉洁,周学华,等. 碳点的制备与应用研究进展[J].材料工程,2015, 43(5):101-112.
[11]Haipeng Liu, Tao Ye, Chengde Mao. Fluorescent carbon nanoparticles derived from candle soot[J]. Angewandte Chemie, 2007, 46: 6473-6475.
[12]Mohammad Hossein Banitaba, Saied Saeed Hosseiny Davarani,etal. Solid-phase microextraction of phthalate esters from aqueous media by electrophoretically deposited TiO2 nanoparticles on a stainless steel fiber[J]. Journal of Chromatography A, 2013,1283:1-8.
[13]Saraji Mohammad, Mehrafza Narges. A simple approach for the preparation of simazine molecularly imprinted nanofibers via selfpolycondensation for selective solid-phase microextraction[J]. Analytica chimica acta, 2016, 936: 108-115.
[14]楊左军,张伟亚,王成云,等. 溶胶-凝胶富勒烯固相微萃取-气相色谱法测定塑料水浸泡液中多种邻苯二甲酸二酯[J].分析化学,2004, 32(5):637-6.
[15]邓伟,朱健美. 饮用水中的痕量邻苯二甲酸酯类有毒物质检测[J].当代化工,2018(12):2708-2711.
